
POLUAREA CU OXIZI DE SULF
GENERALITATI
1.1. DEZVOLTAREA INDUSTRIALA SI SURSELE DE POLUARE A MEDIULUI
Dezvoltarea accentuata a industriei din ultimele decenii a demonstrat relatia stransa existenta intre cresterea economica si modificarile ce se petrec in mediu.
Orice politica de dezvoltare care nu este ancorata intr-un context ecologic este sortita esecului. La inceputul dezvoltarii umane, mediul era protejat natural datorita pe de o parte posibilitatilor reduse ale omului de a transforma natura, iar pe de alta parte capacitatii mediului de a se autoregla. Pe masura industrializarii societatii umane activitatile generatoare de poluare au depasit capacitatea de autocuratare si autoreglare a factorilor de mediu, ajungandu-se sa se puna in pericol existenta vietii pe Terra.
Progresul tehnico-stiintific a afectat echilibrul om-natura prin accentuarea riscului real de epuizare a unor resurse naturale, modificarea calitatii aerului, solului, apei, sporirea volumului de deseuri si a diversitatii lor, realizarea unor tehnologii generatoare de materiale reziduale si toxice ce au constituit originea accidentelor tot mai frecvente, creand noi riscuri pentru sanatatea oamenilor si a mediului.
Compozitia atmosferei s-a schimbat ca urmare a activitatii omului, emisiile de noxe gazoase, pulberi si aerosoli conducand la grave probleme de mediu ca: poluarea urbana, ploile acide, modificarea climei.
In acest context este nevoie ca problemele privind poluarea atmosferei sa se trateze pe cat posibil in mod global.
Organismele din cadrul Organizatiei Natiunilor Unite studiaza poluarea atmosferica a oraselor, a zonelor industriale si rurale. Dupa mai multe statistici facute, concentratia dioxidului de sulf in atmosfera, in mai multe state dezvoltate, a scazut ca urmare a aplicarii diferitelor reglementari, dar exista zone unde emisiile au crescut.
S-au incheiat acorduri regionale sau mondiale referitoare la:
supravegherea si evaluarea poluarii atmosferica in orase, largirea retelei de supraveghere in tarile in curs de dezvoltare;
formularea unor strategii de supraveghere integrata a poluantilor pe termen lung;
elaborarea de noi metode de descriere a propagarii la mari distante a poluantilor, metode de supraveghere a depozitelor uscate si a oxidantilor fotochimici.
Pentru alegerea masurilor de combatere a poluarii atmosferei cu gaze nocive industriale (Tabel 1.1) trebuiesc cunoscute principalele procese generatoare de poluanti [1].
Tabel 1.1. Procese generatoare de poluanti.
|
Nr. crt. |
Agentul nociv |
Procesele tehnologice generatoare |
|
Dioxidul de sulf |
Arderea combustibililor, topitorii, turnatorii, industria chimica. |
|
|
Oxid de carbon |
Arderea incompleta, motoare de explozie. |
|
|
Amoniac |
Instalatii frigorifice, explozivi, lacuri, vopsele, ingrasaminte. |
|
|
Oxizi de azot |
Explozivi, ingrasaminte, curatare metale, combustii la temperaturi ridicate. |
|
|
Acid fluorhidric |
Gravare pe sticla, fabricarea ingrasamintelor. |
|
|
Dioxid de carbon |
Arderea combustibililor, procese de descompunere, activitate vulcanica. |
|
|
Fosgen |
Descompunerea termica a hidrocarburilor clorurate, produse farmaceutice. |
|
|
Acid cianhidric |
Furnale, coloranti. |
|
|
Hidrocarburi |
Gaze de esapament, prelucrarea combustibililor. |
|
|
Aldehide |
Descompunerea termica a grasimilor si a glicerinei. |
Principalele surse de poluare industriala sunt:
- Industria siderurgica si metalurgica.
Industria de prelucrare a minereurilor in vederea extragerii componentilor ferosi sau neferosi se bazeaza in special pe procedee de topire si innobilare la temperaturi inalte in urma carora rezulta cantitati extrem de mari de gaze nocive si pulberi.
- Industria petrochimica.
In rafinariile din industria petrochimica apar emisii de hidrocarburi, dioxid de sulf, hidrogen sulfurat, oxizi de carbon alaturi de alti componenti nocivi mai putin importanti. Pe perioada depozitarii produselor, in special a celor rafinate, datorita tensiunii de vapori ridicate sunt posibile emisii, cel mai frecvent de propan si butan.
- Industria materialelor de constructii.
Industria materialelor de constructii elimina mari cantitati de praf si mai putin gaze nocive.
- Industria chimica.
Procesele tehnologice ce se desfasoara in industria chimica conduc la poluarea atmosferei cu diverse substante: oxizi de sulf, hidrogen sulfurat, oxizi de azot, clor, etc.
- Industria miniera.
Ritmul ridicat de exploatare la minele deschise inseamna dislocarea unor cantitati mari de pamant si eliminarea de pulberi solide.
- Industria energetica si transporturile.
Industria energetica si transporturile, sub aspect cantitativ, se situeaza pe primul loc al surselor de emisii de gaze nocive datorita faptului ca toate industriile necesita cantitati mari de energie, iar obtinerea ei prin combustie este legata de generarea de cantitati imense de gaze reziduale (dioxid de sulf, oxizi de azot, oxizi de carbon), praf si fum.
1.2. EFECTELE POLUARII CU OXIZI DE SULF
Oxizii de sulf au actiune daunatoare atat asupra organismului uman si a regnului vegetal cat si asupra constructiilor din metal si piatra.
La om, acesti oxizi provoaca iritatii ale mucoaselor cailor respiratorii. Acestea apar la concentratii de 5 ppm [2].
Pagubele cele mai importante provocate de SO2 plantelor se petrec ziua, cand activitatea fotosintetica este maxima, actiunea fitotoxica a SO2 constand in distrugerea clorofilei [3]. Prin expunerea unor plante la o atmosfera artificiala de SO2 s-a constatat ca in urma absorbtiei unui gaz se elimina H2S, proces ce se desfasoara numai in prezenta luminii [4].
1.3. LEGISLATIA PRIVIND NORMELE DE EMISII DE NOXE
In Romania, Legea Protectiei Mediului nr. 137/1995 are ca obiectiv reglementarea protectiei mediului pe baza principiilor si elementelor strategice care conduc la dezvoltarea durabila a societatii [5].
Sectiunea a doua a acestei legi priveste protectia atmosferei.
Articolul 40 - Prin protectia atmosferei se urmareste prevenirea, limitarea deteriorarii si ameliorarea calitatii acesteia pentru a evita manifestarea unor efecte negative asupra mediului, sanatatii umane si a bunurilor materiale.
Articolul 41 - Autoritatea centrala pentru protectia mediului promoveaza politicile regionale si globale, fundamentand principiile si actiunile specifice, atat la nivel national cat si local, privind protectia atmosferei.
Politica nationala de protectie a atmosferei consta in principal in urmatoarele:
a) introducerea de tehnici si tehnologii adecvate pentru retinerea poluantilor la sursa;
b) gestionarea resursei de aer, in sensul reducerii emisiilor de poluanti pana la realizarea celor mai scazute niveluri si care sa nu depaseasca capacitatea de regenerare a atmosferei;
c) gestionarea resursei de aer, in sensul asigurarii calitatii corespunzatoare securitatii sanatatii umane;
d) modernizarea si perfectionarea sistemului national de monitorizare integrata a calitatii aerului.
Articolul 42 - Autoritatea centrala pentru protectia mediului, cu consultarea ministerelor competente, elaboreaza normele tehnice, standardele si regulamentele de aplicare privind:
a) calitatea aerului in functie de factorii poluanti din atmosfera;
b) emisiile de poluanti atmosferici pentru surse fixe si mobile, precum si conditiile de restrictie sau de interdictie pentru utilizare, inclusiv pentru substantele ce afecteaza stratul de ozon;
c) calitatea combustibililor si carburantilor precum si reglementarile privind vanzarea - cumpararea si transportul acestora;
d) supravegherea calitatii aerului, proceduri de prelevare si analiza, amplasarea punctelor si instrumentelor pentru probare si analiza, frecventa masuratorilor si altele.
2. ARDEREA COMBUSTIBILLILOR FOSILI. FORMAREA SO2 SI SO3
Combustibilii solizi care se mai numesc si "carbuni" contin ca elemente principale: carbon, oxigen, azot, sulf, elemente ce formeaza masa organica, alaturi de substante minerale si apa ce alcatuiesc masa anorganica.
Sulful total continut de carbuni este alcatuit din sulf organic, sulf piritic si sulf sulfatic. In timpul procesului de combustie se transforma in dioxid de sulf si in mai mica masura in trioxid de sulf.
Un mecanism simplificat pentru formarea acestor doi oxizi poate fi reprezentat prin ecuatiile:
S + O2 SO2 (2.1)
2SO2 + O2 SO3 (2.2)
Cantitatea relativa a fiecaruia din compusi nu depinde intr-o masura apreciabila de cantitatea de oxigen prezenta. Chiar in exces mare de aer, SO2 se formeaza intr-o cantitate mai mare. Cantitatea de SO3 format in procesele de ardere depinde de conditiile de reactie, in special de temperatura. Cel mai periculos din punct de vedere ecologic este SO3 responsabil de formare ploilor acide.
Continutul total de sulf din carbune variaza in limite largi pentru diferite zacaminte in functie de conditiile de formare ale acestora.
Carbunii romanesti au un continut mediu de sulf de 2-3%, variind de la 0,3 pentru antracitul de la Schila pana la 8% pentru huila de Cozia.
3. PROCEDEE DE REDUCERE A EMISIILOR DE SO2
Reducerea emisiilor de SO2 se realizeaza prin:
a) Prelucrarea materiilor prime ce contin sulf inainte de a fi introduse in procesul tehnologic;
b) Desulfizarea gazelor de ardere.
3.1. PRELUCRAREA COMBUSTIBILILOR PENTRU REDUCEREA CONTINUTLUI DE SULF
Procedeele de desulfurare a carbunilor se clasifica in:
Pretratarea chimica urmata de indepartarea mecanica a sulfului continut ca impuritate in pirita (sulful organic nu poate fi indepartat). Reducerea sulfului piritic se face in proportie de 90%.
Transformarea chimica a sulfului din carbune in compusi solubili sau volatili.
Desulfurarea prin desulfurare - lichefiere, urmata de solidificarea produsului si diferite procedee de gazeificare a carbunelui.
Pentru pacurile cu continut ridicat de sulf s-au utilizat diverse metode de indepartare a sulfului in vederea obtinerii emisiilor reduse de oxizi de sulf. Printre acestea se numara:
Aditivitatea pacurii, prin folosirea aditivilor de combustie care au rolul de a reactiona cu dioxidul de sulf din gazele de ardere si de a forma produse slab active sub raport coroziv.
Metoda petrochimica de a indeparta compusii cu sulf prin rafinare.
3.2. DESULFURAREA GAZELOR INDUSTRIALE
In vederea micsorarii nocivitatii gazelor emise, varianta cea mai studiata si aplicata este desulfurarea gazelor de ardere.
Retinerea dioxidului de sulf din gazele reziduale se poate realiza prin procedee conventionale ce au la baza procese ca: absorbtia, adsorbtia, oxidare catalitica, reducere catalitica si procedee neconventionale prin iradiere cu fascicul de electroni accelerati sau fascicul de electroni - microunde.
4. ASPECTE TEORETICE PRIVIND DESULFURAREA GAZELOR REZIDUALE
4.1. ASPECTE TEORETICE PRIVIND DESULFURAREA GAZELOR REZIDUALE PRIN ABSORBTIE, LA TEMPERATURA JOASA
Procedeele de desulfurare la temperatura joasa se caracterizeaza prin absorbtia oxizilor de sulf intr-o solutie alcalina pe baza de combinatii de calciu, magneziu, sodiu, amoniac, obtinandu-se ca produsi finali sulfatii respectivi.
Solubilitatea dioxidului de sulf in apa este mica, ea scazand cu cresterea temperaturii.
In timpul absorbtiei in apa are loc un proces de hidroliza, conform ecuatiei:
SO2 + H2O H+ + HSO-3 (4.1)
Pentru a creste gradul de absorbtie al SO2 in solutii apoase este necesara introducerea in sistemul de absorbtie a unei substante care sa indeparteze protonul (H+), sau sa lege anioniul bisulfitic (H SO3-). Pentru aceasta se folosesc solutiile unor substante cu caracter bazic.
Procesul de absorbtie a SO2 in solutii alcaline este un proces heterogen, in majoritatea cazurilor, reactia chimica are loc in faza lichida, iar cel putin unul din reactanti provine din faza gazoasa.
Reactia chimica si transferul de masa se influenteaza reciproc.
Prezenta reactiei chimice concomitent cu transferul de masa se poate cuantifica definind factorul de amplificare al transferului de masa si factorul de utilizare a fazei lichide, denumiti factori de limita.
Deoarece pentru cele trei modele clasice ale transferului de masa (modelul filmului, penetratiei si reinnoirii suprafetei), factorul de amplificare al transferului de masa are aceeasi valoare, pentru transferul de masa se alege modelul filmului. Prin teoria filmului, rezistenta la transferul de masa se considera concentrata in doua zone de dimensiuni relativ mici situate de o parte si de alta a interfetei, fenomenele complexe ce au loc in filmul de lichid avand la baza mecanismul difuzional.
4.1.2. MODELUL MATEMATIC AL ABSORBTIEI SO2 INTR-O SUSPENSIE DE Ca(OH)2
Interactiunea dintre transferul de masa si reactia chimica in termeni de factori limita a fost studiata in mai multe randuri. Astfel, Ramachandram si Sharma (1969) au pus bazele modelului filmului, remarcand ca in filmul de lichid se pot intalni doua cazuri:
dizolvarea solidului in filmul de lichid (nu este importanta);
dizolvarea solidului in filmul de lichid este importanta, viteza de absorbtie a gazelor in prezenta particulelor solide este mult mai mare decat in absenta acestora.
Uchida si colaboratorii (1975) au considerat cazul 2 ca unul teoretic si au aratat ca viteza de dizolvare a solidului este limitata de reactia dintre gazul absorbit si solidul dizolvat in filmul de lichid.
In cele ce urmeaza sunt prezentate doua modele [6] pentru procesul de absorbtie cu viteza finita de reactie intr-o suspensie. Procedeul este analizat pornind de la modelul filmului si este comparat cu datele experimentale.
Modelul I (este o extindere a modelului lui Ramachandran si Sharma) are urmatoarele premize:
procesul de absorbtie are loc in filmul de lichid si decurge dupa o reactie reversibila de ordinul II:
A(G) + nB(L) Produsi (4.2)
cele doua procese, transferul de masa si reactia chimica, au loc paralel;
reactia chimica este instantanee.
Modelul matematic este format din ecuatiile de difuzie ce au loc in filmul de lichid, cu conditiile limita respective:
ecuatia difuziunii prin filmul lichid al fazei gazoase:
![]()
ecuatia difuziunii prin filmul de lichid al speciei solide:
![]() (4.4)
(4.4)
conditie
limita: ![]()
![]()
![]() (4.5)
(4.5)
![]()
![]()
![]() (4.6)
(4.6)
Ecuatiile nu pot fi rezolvate analitic. Pentru rezolvare se adimenisioneaza:
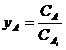 ;
; ![]() ;
; 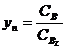 (4.7)
(4.7)
Se noteaza:
![]() (4.8)
(4.8)
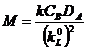 (4.9)
(4.9)
![]() (4.10)
(4.10)
![]() (4.11)
(4.11)
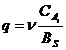 (4.12)
(4.12)
Se obtin ecuatiile:
![]() (4.13)
(4.13)
![]() (4.14)
(4.14)
Conditiile devin:
![]()
![]()
![]() (4.15)
(4.15)
![]()
![]()
![]() (4.16)
(4.16)
Rezultatele sunt exprimate prin folosirea factorului limita (de amplificare) definit de relatia:
![]() (4.17)
(4.17)
Modelul II (extinderea modelului Uchida si colaboratorii) este modelul reactiei cu doua planuri si are urmatoarele premise:
viteza de dizolvare a solidului este accelerata de reactia dintre gazul absorbit si solidul dizolvat in filmul de lichid;
reactia chimica este instantanee.
Modelul matematic este alcatuit din ecuatiile difuziei in filmul de lichid al reactantului gazos si solid:
![]() (4.18.)
(4.18.)
![]() (4.19.)
(4.19.)
Scrise in forma adimensionalizata:
![]()
![]()
![]() (4.21.)
(4.21.)
Comparativ
cu Modelul I, viteza de dezvoltare a lichidului care aste amplificata cu
factorul ![]() ce reprezinta
factorul limita pentru dezvoltarea solidului, iar in cazul reactiei
instantanee este maxim:
ce reprezinta
factorul limita pentru dezvoltarea solidului, iar in cazul reactiei
instantanee este maxim:
![]()
Rezultatele numerice ale celor doua metode sunt prezentate in figurile 4.1. respectiv 4.2.
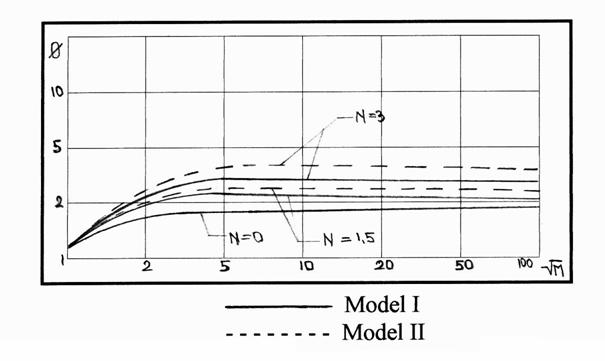
Fig. 4.1. Relatiile
intre factorii limita si modelul M pentru absorbtia gazului in
solutie continand particule solide (r=q=1).
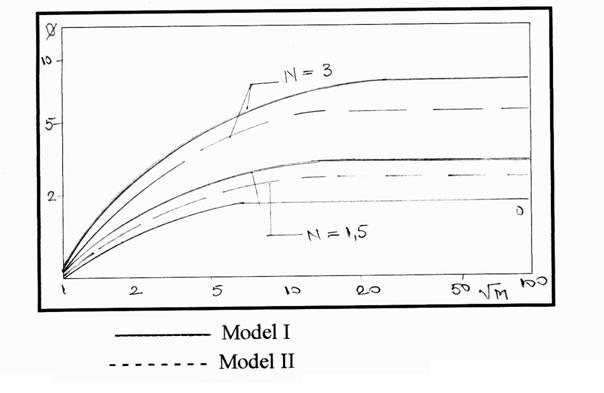
Fig. 4.2. Comparatie
intre factorii limita pentru absorbtia gazului in solutie
continand particule solide, cu factorul limita (de amplificare)
pentru absorbtia gazului in solutii ce contin particule solide
(r=q=1).
Figura 4.1. reprezinta relatia dintre factorul
limita de amplificare si modul Hatta, raport viteza reactie
chimica / viteza transfer masa, ca un parametru al lui N,
valorile parametrului N = 1,5; 3; 4,5 corespund concentratiei de solid W =
0,1; 0,2; 0,3 ![]() calculate dintru
exemplu dat de Uchida si colaboratorii, folosind particule cu diametru de
calculate dintru
exemplu dat de Uchida si colaboratorii, folosind particule cu diametru de ![]() cm.
cm.
Figura 4.2. reda comparatia dintre factorii limita pentru absorbtia gazului in solutie continand particule solide, cu factorul limita (de amplificare) pentru absorbtia gazului in solutii ce nu contin particule solide (r=q=1).
Rezulta ca
raportul intre viteza de absorbtie intr-o solutie continand
particule solide fine, ![]() , si viteza de absorbtie intr-o solutie
saturata ce nu contine particule solide
, si viteza de absorbtie intr-o solutie
saturata ce nu contine particule solide ![]() este echivalent cu
raportul factorilor limita in aceleasi conditii
este echivalent cu
raportul factorilor limita in aceleasi conditii ![]() .
.
|
Politica de confidentialitate |
| Copyright ©
2024 - Toate drepturile rezervate. Toate documentele au caracter informativ cu scop educational. |
Personaje din literatura |
| Baltagul caracterizarea personajelor |
| Caracterizare Alexandru Lapusneanul |
| Caracterizarea lui Gavilescu |
| Caracterizarea personajelor negative din basmul |
Tehnica si mecanica |
| Cuplaje - definitii. notatii. exemple. repere istorice. |
| Actionare macara |
| Reprezentarea si cotarea filetelor |
Geografie |
| Turismul pe terra |
| Vulcanii Și mediul |
| Padurile pe terra si industrializarea lemnului |
| Termeni si conditii |
| Contact |
| Creeaza si tu |