
Bazele azotate
In structura nucleotidelor si a polimerilor lor intra cinci baze azotate majore care le confera proprietati esentiale pe care le vom trece in revista in continuare. Acestui grup i se adauga bazele modificate enzimatic in structura acizilor nucleici, dupa sinteza acestora, si care reprezinta adesea, semnale chimice de protectie si control.
Diferitele baze din structura au origini diverse: intermediari metabolici, produsi de transformare chimica in conditii celulare, analogi de sinteza, etc.
Tipuri de baze azotate
Baze majore
Sunt derivati oxi- sau amino- ai pirimidinei si ai purinei (imidazolpirimidina) care formeaza cele doua familii de baze care intra in constitutia nucleotidelor naturale. In figura 1.2 sunt prezentate cele doua tipuri, in conformitate cu numerotarea conventionala normala, iar in tabelul 1 sunt trecute simbolurile acestora.
Numele utilizate curent nu sunt corelate cu denumirile sistemice folosite in chimia organica. Anumite denumiri evoca sursa unde bazele azotate au fost descoperite: guanina de la guano (excremente de pasare), timina de la evidentierea sa in timus de vaca. Pe de alta parte prin terminatia sa «-ozina», citozina intretine o anumita confuzie interferand cu denumirea unor nucleozide.
Baze pirimidinice: pirimidina; citozina (2-oxi-4-aminopirimidina); uracilul (2,4-dioxipirimidina); timina (5-metil-2,4-dioxipirimidina);
Baze purinice: purina (imidazolpirimidina); adenina (6-aminopurina); guanina (2-amino-6-oxipurina).
Figura
1. Bazele majore din structura acizilor nucleici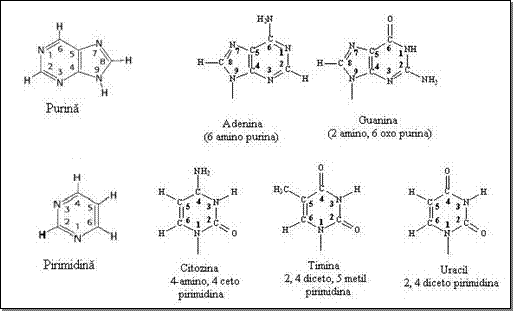
Nucleotidele din structura ADN si ARN nu contin decat patru baze azotate: trei dintre acestea sunt comune celor doua tipuri de acizi nucleici - cele doua purine si citozina si cate una este specifica pentru fiecare tip: baza pirimidinica timina este specifica pentru ADN si derivatul sau metilat, uracilul pentru ARN.
Baze modificate
In structura acizilor nucleici sunt prezente o serie de forme modificate sau substituite ale bazelor azotate. Situsurile de modificare sunt prezente la nivelul ciclului sau sunt exociclice. Pentru nomenclatura, in primul caz, este suficient indicarea numarului atomului, in timp ce in al doilea caz sunt necesare indicatii privind natura gruparii modificatoare si pozitia in ciclu a atomului pe care aceasta se grefeaza (Figura 1.3
ADN reprezinta un bun substrat pentru metilarea bazelor purinice in anumite regiuni ale moleculei (Figura 1.3). Rolul unora dintre aceste modificari este cunoscut. De exemplu, 5-metil-citozina din structura ADN de la plante si animale este un semnal negativ de reglare a expresiei genelor. Gruparea metil favorizeaza conformatia inactiva a ADN in forma condensata si impiedica fixarea factorilor de transcriptie, deci copierea informatiei in structura ARN;
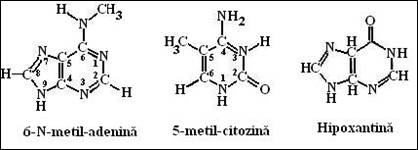
Figura 1.2. Baze modificate: N6-metil adenina (bacterii) 5-metil- citozina (plante, animale); hipoxantina.
Moleculele de citozina metilate din structura ADN bacterian au cel putin doua roluri:
i) constituie un sistem de distinctie si de protectie a ADN bacterian fata de ADN strain. Celula activeaza de fapt enzime de restrictie (endonucleaze) pentru a distruge ADN viral nemetilat, cel putin in cazul primei infectari. Acest sistem de aparare este cunoscut sub numele de restrictie-modificare;
ii) sunt elemente ale sistemului de corectare a eventualelor greseli de replicare.
Moleculele de ARN, si mai ales ARNt contin un numar variat de baze modificate derivate de la purina (hipoxantina derivata de la guanina) sau de la pirimidina.
Degradarea bazelor purinice implica reactii de deaminare daca nu sunt reciclate, bazele purinice sunt degradate la acid uric trecand prin formele deaminate hipoxantina si xantina. Acidul uric, foarte putin solubil, este produsul de excretie al acestor baze la primate (Figura 1.4
In aceeasi categorie cu produsii amintiti mai sus putem introduce alcaloizii vegetali, cu structura de metil-xantine, care au si utilizari farmacologice: cafeina (stimulant), teobromina si teofilina (stimulatori cardiaci, relaxanti ai musculaturii netede si vasodilatatorii)
Analogii sintetici sunt molecule utile, care intra in structura acizilor nucleici si pot avea utilizari diferite:
- a) in biologia moleculara: 5-bromo-uracilul este mutagen; de asemenea exista derivati fluorescenti care servesc drept reactivi de marcare pentru polinucleotide;
- b) in medicina ca agenti terapeutici: intra in competitie cu bazele naturale; se comporta ca antimetaboliti ai sintezei acizilor nucleici si pot avea astfel rol bacteriostatic; agenti antivirali; antimitotici. In figura 1.5 sunt prezentate cateva exemple: i) derivatii fluorurati, tiol si aza care sunt substante cu actiune antitumorala; ii) derivat ester al N9-metilguanina care este un agent antiviral eficace fata de herpesul genital (comercial aciclovir).
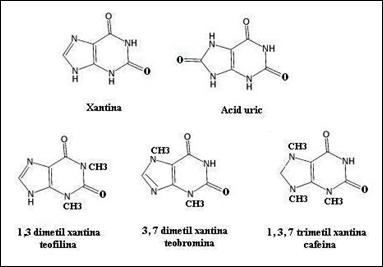
Figura 1. Produsii de degradare si alcaloizii vegetali derivati ai baze-lor purinice. (Xantina; acidul uric; 1,3-dimetil-xantina = teofilina; 3,7-dimetilxantina = teo-bromina; 1,3,7-trimetil
xantina = cafeina)
Proprietatile bazelor azotate
In urma examinarii structurilor din figura 1.2 se constata urmatoarele:
a) dublele legaturi creeaza sisteme conjugate cu consecinte structurale si fizice;
b) heterociclurile azotate sunt susceptibile de ionizare caracterul lor de baze slabe variind in functie de substituentii ciclurilor;
c) moleculele prezinta dualitate: gruparile functionale sunt purtate de nuclee heterociclice. Caracterul dual este la originea principalelor interactii principale din structura polinucleotidelor si determina functiile acestora.
d) reactivitatea acestor structuri faciliteaza diferite transformari chimice, in anumite conditii celulare.
Conjugarea dublelor legaturi
In structura heterociclurilor purinice si pirimidinice starea de rezonanta, care apare intre atomi, delocalizeaza electronii p ai dublelor legaturi. Consecintele sunt cele ale caracterului aromatic: i) stabilizarea puternica a moleculei; ii) structurile sunt aproape plane (pirimidinele sunt plane si purinele usor pliate); iii) moleculele exista sub diferite forme tautomere.
Tautomeria care apare la nivelul gruparilor ceto/enol si amino/imino si deplasarile de electroni din structura ciclurilor au drept consecinta existenta mai multor posibilitati structurale. Figura 1.6 prezinta cateva dintre formele tautomere ale diferitelor baze azotate. Prin tehnici de cristalografie si prin spectroscopie in infra-rosu s-a demonstrat ca la pH 7,0 sunt predominante formele ceto-amino.
Heterociclii cu azot si derivatii lor nucleozidici si nucleotidici prezinta spectre de absorbtie moleculara caracteristice in ultraviolet (UV). Absorbanta derivatilor purinici este mai importanta decat a celor pirimidinici. Existenta celor doua cicluri determina o condensare mai densa a sarcinilor deoarece acestea sunt mai dens conjugate. Aceste proprietati optice permit dozarea si controlul puritatii nucleotidelor si a acizilor nucleici. Raportul absorbantelor la lungimi de unda de 260 si 280 nm ne ofera informatii importante privind puritatea compusilor nucleotidici si eventuala lor contaminare cu proteinele. Aminoacizii triptofan, tirozina, fenilalanina, prezenti in proteine, confera acestora absorbanta la 280 nm.
Fluorescenta bazelor este o caracteristica care nu poate fi utilizata in aceste scopuri. Emisia fluorescenta se situeaza in regiunea spectrului UV intre 300 si 320 nm si este foarte scazuta: pentru purine sensibilitatea este de 400 de ori mai mica decat cea a triptofanului, si pentru pirimidine de 2500 de ori mai mica.
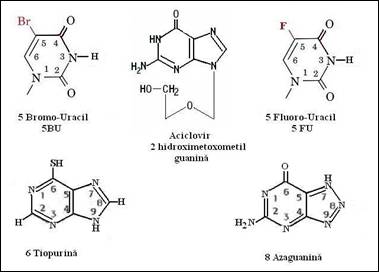
Figura 1.4. Cativa analogi sintetici ai bazelor din structura acizilor nucleici: 5-bromouracil, aciclovir (2-hidroxi-etoxometil guanina), 5-fluoro-uracilul; 6-tiopurina; 8-azaguanina;

Figura 1. Echilibre tautomere posibile la pH 7,0 intre formele lactam (la stanga) si lactim (la dreapta) ale bazelor pirimidinice si purinice (prezente sunt forma nucleozidica sau nucleotidica).
Ionizarea heterociclurilor azotate
Purinele, pirimidinele si nucleotidele derivate de la acestea sunt baze slabe ale caror molecule nu au sarcina ionica la pH 7,0. Pentru cele mai multe structuri comportamentul la titrare este complex deoarece poseda multiple situsuri potentiale donoare sau acceptoare de protoni cu localizare diferita in functie de forma tautomera implicata (ea insasi dependenta de pH).
Nuclee si grupari functionale
Faptul ca heterociclii substituiti sunt relativ hidrofobi are urmatoarele consecinte
i) solubilitatea scazuta in apa a bazelor acizilor nucleici (contrar structurilor pirimidinice si purinice din care deriva). La pH si temperatura fiziologica bazele purinice sunt aproape insolubile. La valori de pH acide sau bazice dizolvarea lor in mediu apos este favorizata de ionizare;
 ii) un efect de respingere al apei de
catre bazele ale caror planuri
tind sa se suprapuna.
Aceasta tendinta
reprezinta fenomenul de stivuire sau "stacking" care este
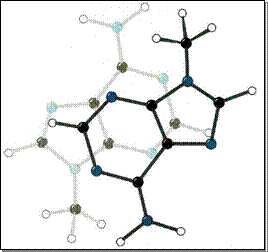
foarte mult studiat. In figura 1.7 este prezentat modelul de stivuire a
inelelor din cristalul de 9-metil-adenina. Suprapunerea partiala
a inelelor reprezinta o asociere tipica a bazelor in structuri
cristaline si in dubla elice a acizilor nucleici.
ii) un efect de respingere al apei de
catre bazele ale caror planuri
tind sa se suprapuna.
Aceasta tendinta
reprezinta fenomenul de stivuire sau "stacking" care este
foarte mult studiat. In figura 1.7 este prezentat modelul de stivuire a
inelelor din cristalul de 9-metil-adenina. Suprapunerea partiala
a inelelor reprezinta o asociere tipica a bazelor in structuri
cristaline si in dubla elice a acizilor nucleici.
Figura 1.6. Stivuirea bazelor in cristalul de 9-metil-adenina (dupa Biochemistry, Voet & Voet, 1995)
De mai bine de treizeci de ani s-au realizat studii numeroase de difractie cu raze X pe cristale ale diferitilor derivati ai bazelor si asupra comportamentului acestora in solutie (vascozitate, presiune osmotica, absorbanta, spectre RMN si IR). Acestea au dovedit ca heterociclurile au o puternica tendinta de a se suprapune plan peste plan, cu un decalaj caracteristic intre planuri.
In solutie, conditia cea mai interesanta pentru extrapolarea interactiilor celulare, apa are rolul determinant in formarea si stabilizarea acestor stivuiri. Repulsia apei prin efectul hidrofob al nucleelor reprezinta unul din motivele pentru care apare acest tip de organizare. Legaturile de hidrogen sunt total excluse. Stabilizarea se realizeaza prin forte Van der Waals si interactii dipol-dipol intre planuri. Apropierea dintre nuclee modifica distributia lor electronica si determina aparitia dipolilor in fiecare ciclu.
Cu toate acestea, trebuie sa remarcam ca originea fortelor care dirijeaza asocierea spontana, remarcabila, ramane inca subiect de controverse. Retinem ca fenomenul nu este asimilabil cu cel de repliere hidrofoba a proteinelor deoarece are un caracter contrar. Datele termodinamice demonstreaza ca acesta este controlat de entalpie in timp ce fenomenul caracteristic resturilor aromatice din proteine este controlat de entropie.
Faptul ca bazele se stivuiesc intr-o ordine preferentiala: pur-pur>pur-pir>pir-pir a fost demonstrat de valorile constantelor de disociere ale diferitelor combinatii de baze, in solutie, si de frecventa dimerizarii timinei prin fotoreactivare.
Aceasta prima modalitate de interactiune intre baze este un factor primordial de stabilizare a structurii spatiale a acizilor nucleici responsabila de efectul hipocrom al acizilor nucleici. Stivuirea bazelor are drept consecinta scaderea absorbtiei in UV a unui acid nucleic fata de o solutie echivalenta de nucleotide libere, urmata in acelasi timp de deplasarea spectrului cu cativa nm. Temperatura care, prin efectul sau de crestere a agitatiei moleculare este un factor de dezorganizare, inlatura hipocromicitatea (Figura 1.8). Efectul temperaturii asupra fortelor de stivuire poate fi urmarit comparativ in cazul unui polinucleotid si a unui dinucleotid (Figura 1.9
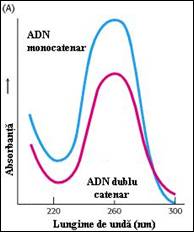
Figura 1. Absorbtia diferita in UV a moleculelor de ADN mono- si dublucatenare insotita de deplasarea spectrului de absortie
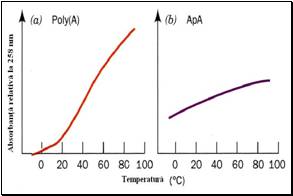
Figura 1. Variatia absorbtiei relative la 258 nm cu cresterea temperaturii:a) polimerul poli (A); b) dinucleotidul ApA (dupa Biochemistry,Voet&Voet,1995)
Capacitatea de a forma legaturi de hidrogen: grupele polare fixe, carbonil si amino, si atomii de azot ai ciclurilor sunt adecvate pentru stabilirea legaturilor de hidrogen intre baze, de tip O---H si N---H. Aceasta a doua modalitate de interactiune, coordonata de imperecherea necovalenta dintre baze, este un fenomen cheie pentru formarea structurii secundare a acizilor nucleici si pentru duplicarea, copierea si exprimarea materialului genetic. Formele tautomere, in care se gasesc partenerii bazelor, au o importanta foarte mare deoarece conditioneaza posibilitatea formarii acestor legaturi.
Transformarea chimica a bazelor
In celule, bazele din structura acizilor nucleici suporta alterari spontane sau sub efectul diferitilor agenti fizici sau chimici. Daca aceste modificari nu sunt reparate (ADN este singura molecula supravegheata si reparata de catre un sistem specific), ele pot sta la originea mutatiilor care determina aparitia diferitelor maladii (de ex. cancer).
Deaminare spontana lenta, cu oxidarea grupelor amino exociclice, modifica natura bazei. Tinand cont de structurile bazelor azotate din compozitia nucleotidelor putem evidentia urmatoarele transformari (Figura 1.10)
![]()
![]() citozina uracil; 5-metilcitozina timina;
citozina uracil; 5-metilcitozina timina;
![]()
![]() adenina hipoxantina; guanina xantina.
adenina hipoxantina; guanina xantina.
Intr-o celula de mamifer, frecventa deaminarilor spontane este de ordinul 100/zi pentru citozina, si de numai 1/zi pentru bazele purinice.
Radiatiile energetice altereaza mai mult sau mai putin profund bazele din structura acizilor nucleici: i) iradierea UV deschide dublele legaturi din structura a doua baze suprapuse si determina formarea de legaturi covalente C-C intre acestea. Dimerizarea pirimidinelor (timinelor), este un factor care estimeaza capacitatea de carcinogeneza a acestor radiatii; ii) radiatiile ionizante (X, g, etc.) deschid ciclurile si le rup;
Numerosi agenti chimici reactioneaza cu bazele: i) acidul azotos (HNO2) si compusi organici si minerali derivati de la acesta: nitrozamine, nitriti si nitrati ca si acidul sulfuros (HSO3-) au actiune de deaminare Figura 1.11 . In industria alimentara regasim acesti compusi in categoria conservantilor utilizati pentru a impiedica dezvoltarea bacteriilor. ii) mediul industrial este sursa de substante toxice alchilante care determina metilarea diferitelor baze (guanina este cea mai usor de metilat); iii) speciile reactive de oxigen - peroxizii, radicalii liberi, oxigenul "singlet" - sunt favorizate prin expunere la lumina si determina modificari oxidative la nivelul bazelor care obliga sistemele de reparare sa reactioneze.
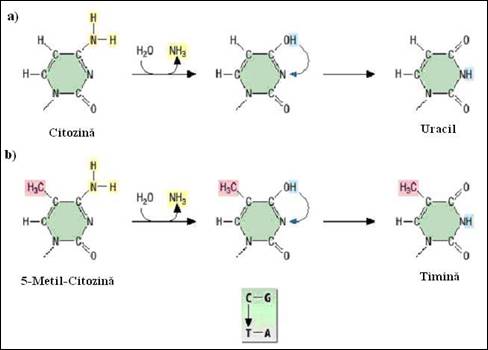
Figura 1.9. Reactii de dezaminare ale bazelor: a) citozina la uracil; b) 5-metil-citozina la timina
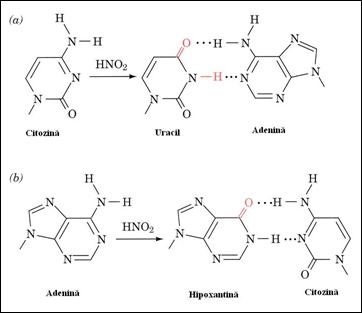
Figura 1. . Dezaminari provocate de acidul azotos si consecintele acestora
|
Politica de confidentialitate |
| Copyright ©
2024 - Toate drepturile rezervate. Toate documentele au caracter informativ cu scop educational. |
Personaje din literatura |
| Baltagul caracterizarea personajelor |
| Caracterizare Alexandru Lapusneanul |
| Caracterizarea lui Gavilescu |
| Caracterizarea personajelor negative din basmul |
Tehnica si mecanica |
| Cuplaje - definitii. notatii. exemple. repere istorice. |
| Actionare macara |
| Reprezentarea si cotarea filetelor |
Geografie |
| Turismul pe terra |
| Vulcanii Și mediul |
| Padurile pe terra si industrializarea lemnului |
| Termeni si conditii |
| Contact |
| Creeaza si tu |