
Generalitati:
In epoca contemporana de intensa dezvoltare industriala, cand consumul de metale si utilaje este in continua crestere apare ca deosebit de importanta, in special pentru cele feroase, preocuparea pentru protejarea acestora impotriva distrugerii prin coroziune.
Pierderile de metale si aliaje produse de coroziune reprezinta aproximativ o treime din productia mondiala. Chiar daca se considera ca o parte din metal se reintoarce in circuit prin retopire, totusi aceste pierderi totalizeaza in cazul fierului cel putin 10-15% din metalul obtinut prin topire.
Pagubele provocate de coroziune sunt legate nu numai de pierderile de metal, ci si de faptul ca utilajele, constructiile, piesele etc. distruse de coroziune au un cost mult mai mare decat al materialului din care sunt confectionate. Daca la acestea se adauga si chelutielile pentru repararea pagubelor provocate de coroziune, montarea aparaturii de inlocuire, utilizarea materialelor anticorozive scumpe, aplicarea metodelor de protectie anticoroziva, cat si faptul ca aproape in toate domeniile industriei se pune problema protectiei anticorozive, ne dam seama de importanta economica pe care o prezinta coroziunea.
Coroziunea metalelor si aliajelor se defineste ca fiind procesul de distrugere spontana a acestora, in urma interactiunilor chimice, electrochimice si biochimice cu mediul de existenta.
In practica fenomenele de coroziune sunt de obicei extrem de complexe si apar sub cele mai diferite forme, motiv pentru care, o clasificare riguroasa a tuturor acestor fenomene nu este posibila, intre diferite clase existand intrepatrunderi.
Dupa mecanismul de desfasurare se pot distinge doua tipuri de coroziune :
coroziunea chimica care se refera la procesele de distrugere a metalelor si aliajelor care se produc in gaze uscate, precum si in lichide fara conductibilitate electrica si in majoritatea substantelor organice ;
coroziunea electrochimica se refera la procesele de degradare a metalelor si aliajelor in solutii de electroliti, in prezenta umiditatii, fiind insotite de trecerea curentului electric prin metal.
Atat coroziunea chimica cat si cea electrochimica, fiind procese ce se desfasoara la interfata metal-gaz, fac parte din categoria reactiilor eterogene si se supun legilor generale ale cineticii acestor reactii.
Dupa aspectul distrugerii, coroziunea poate fi clasificata in : coroziune continua, cand intreaga suprafata metalica a fost cuprinsa de actiunea mediului agresiv; si caroziunea locala cand distrugerea se produce numai pe anumite portiuni ale suprafetei metalului sau aliajului.
Coroziunea chimica :
Coroziunea chimica a metalelor sau aliajelor se produce prin reactii ce se desfasoara la suprafata acestora in contact cu gaze uscate sau solutii de neelectroliti. Produsele care rezulta sub actiunea acestor medii raman, in general, la locul interactiunii metalului cu mediul coroziv, sub forma de pelicule de grosimi si compozitii diferite. Coroziunea chimica a metalelor este procesul care se desfasoara pe suprafata metalelor in contact cu gazele uscate sau cu solutiile de neelectroliti. In urma reactiilor dintre metal si mediul agresiv, pe suprafata metalului raman produsele coroziunii ce se numesc pelicule de coroziune. Aceste pelicule franeaza coroziunea rezultand o protectie mai mult sau mai putin pronuntata, dupa cum peliculele sunt mai izolatoare respectiv mai penetrabile. In cele mai multe cazuri peliculele nu sunt nici complet penetrabile nici complet izolatoare.
In functie de proprietatile lor fizico-chimice peliculele de corziune exercita o influenta importanta asupra desfasurarii ulterioare a procesului de coroziune, a cineticii acestuia, putandu-l frana intr-o masura mai mare sau mai mica.
Formarea peliculelor oxidice de coroziune :
Termenul de pelicula de coroziune este mai indicat decat cel de pelicula protectoare deoarece nu toate peliculele de coroziune sunt protectoare. Grosimea peliculelor de coroziune depinde in mare masura de temperatura mediului, de durata procesului si de agresivitatea mediului coroziv.
Grosimea peliculelor poate varia in limite foarte largi. Conventional sunt considerate pelicule subtiri cele invizibile cu grosimea sub 400Å, putand fi alcatuite chiar dintr-un strat monomolecular. In acest caz culoarea specifica a metalului nu este afectata. Peliculele medii au grosimea comparabila cu lungimile de unda ale undelor vizibile 400-5000Å. Sunt vizibile datorita fenomenului de interferenta a luminii si apar colorate putin diferit. Peliculele groase, mai mari de 5000Å, pot fi de ordinul micronilor sau chiar milimetrilor. Culoarea lor difera mult fata de culoarea metalului.
Grosimea peliculelor nu caracterizeaza suficient proprietatile anticorozive. Pentru a avea o actiune protectoare pelicula trebuie sa indeplineasca urmatoarele conditii:
Pelicula trebuie sa fie aderenta, compacta, continua (fara fisuri, pori).
In cazul peliculelor oxidice sunt continue acelea care au volum mai mare decat al metalului de baza:
![]() > 1;
> 1;
Daca volumul oxidului produs este mai mic decat volumul metalului generator rezulta
ca raportul este subunitar iar pelicula de oxid se fisureaza fiind
mai putin protectoare. Metalele
alcaline (Li, Na, K, Rb, Cs, Fr) si alcalino-pamantoase (Be, Mg, Ca,
Sr, Ba, Ra) au
raportul ![]() < 1, deci
formeaza pelicule discontinue, afanate, cu proprietati slab
protectoare. Pe alte metale ca Al, Ti, Zr, volumul oxidului format la
incalzire este putin mai mare ca al
metalului deci se pot forma pelicule continue de oxizi.
< 1, deci
formeaza pelicule discontinue, afanate, cu proprietati slab
protectoare. Pe alte metale ca Al, Ti, Zr, volumul oxidului format la
incalzire este putin mai mare ca al
metalului deci se pot forma pelicule continue de oxizi.
 Pelicula trebuie sa fie durabila in conditii de exploatare. O
influenta foarte mare asupra comportarii anticorozive a piesei o
au tensiunile interne ce apar in timpul cresterii
peliculelor de coroziune chiar la temperatura
Pelicula trebuie sa fie durabila in conditii de exploatare. O
influenta foarte mare asupra comportarii anticorozive a piesei o
au tensiunile interne ce apar in timpul cresterii
peliculelor de coroziune chiar la temperatura
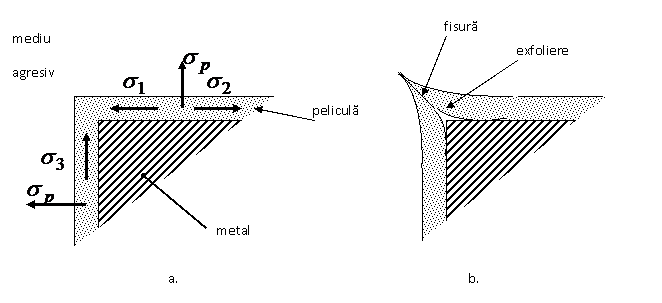
Fig. Influenta tensiunilor interne asupra peliculelor de oxizi
a.- cresterea peliculei si aparitia tensiunilor; b.- fisurarea si exfolierea.
La compunerea celor doua
eforturi de crestere a pelicule ![]() si
si ![]() are loc desprinderea (exfolierea) peliculei de
oxid. La muchii si colturi pelicula va prezenta fisuri si de
aceea nu va fi durabila in exploatare. Durabilitatea ei este
influentata de gradul de prelucrare a suprafetelor. O piesa
degrosata va favoriza mentinerea mediului agresiv o durata
indelungata de timp si aparitia rapida a fisurarilor
si exfolierilor, in timp ce o piesa rectificata sau
lustruita va avea o durabilitate mai mare. O piesa cu muchii si
colturi nete va avea o durabilitate mai mica.
are loc desprinderea (exfolierea) peliculei de
oxid. La muchii si colturi pelicula va prezenta fisuri si de
aceea nu va fi durabila in exploatare. Durabilitatea ei este
influentata de gradul de prelucrare a suprafetelor. O piesa
degrosata va favoriza mentinerea mediului agresiv o durata
indelungata de timp si aparitia rapida a fisurarilor
si exfolierilor, in timp ce o piesa rectificata sau
lustruita va avea o durabilitate mai mare. O piesa cu muchii si
colturi nete va avea o durabilitate mai mica.
Pelicula trebuie sa posede proprietati mecanice superioare adica sa reziste la diverse solicitari mecanice, la socuri si eforturi alternative ce apar in exploatare.
Diferenta dintre coeficientii de dilatare (liniara sau de volum) al peliculei si al metalului trebuie sa fie cat mai mica, astfel incat pelicula sa reziste la variatii cat mai mari de temperatura, fara sa se fisureze si exfolieze.
Peliculele prea subtiri nu protejeaza suficient de obicei, deoarece opun o rezistenta scazuta difuziei, in timp ce peliculele prea groase se pot fisura sub actiunea tensiunilor interne. Din punct de vedere al protectiei anticorozive, cele mai bune rezultate le dau peliculele de grosime intermediara.
Sub actiunea oxigenului din aer sau a altor medii care contin oxigen, metalele se acopera cu pelicule de oxizi a caror grosime depinde de temperatura si timpul de incalzire.
Mecanismul reactiilor de oxidare chimica
Considerentele anterioare legate de proprietatile, legile de crestere si structura peliculelor de coroziune n-au tinut seama de natura particulelor si de sensul in care difuzeaza acestea in timpul procesului.
In prezent, conform datelor experimentale, se admite ca in majoritatea cazurilor are loc deplasarea atomilor sau ionilor de Me+ si a electronilor e- prin pelicula spre exterior si numai in foarte mica masura, a oxidantului spre interior.
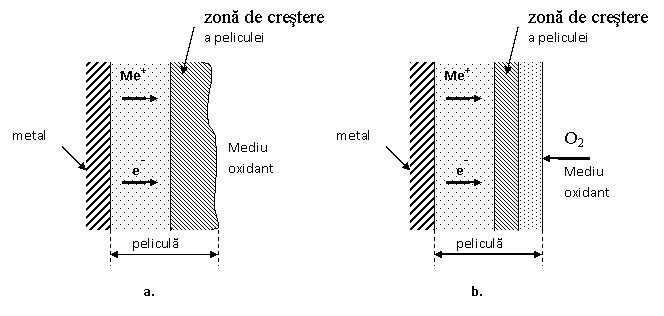
Fig .
In cazul a.(Fig -a) difuzeaza numai ionii metalici Me+ si electronii e- si este specific formarii compusilor oxid de cupru (CuO) sau sulfura de argint (Ag2S), cand pelicula creste exclusiv la suprafata.
In cazul b. difuzeaza de la metal spre mediu ionii metalici Me+ si electronii e- iar dinspre mediul oxidant difuzeaza agentul oxidant O2.
Din compararea dimensiunilor parametrilor retelei cristaline cu dimensiunile particulelor, rezulta ca prin pelicula difuzeaza de preferinta ionii de metal, avand diametrul mai mic decat atomii de metal si atomii de oxigen, cu diametrul mai mic decat al ionilor de oxigen O2
Unii compusi ca Al2O3, ZnO, CdO, AgCl, Ag2S, contin un exces de ioni metalici Me+ si electronii e- disponibili a se deplasa prin interstitiile retelei cristaline, deoarece au dimensiuni mici fata de parametrii retelei.
Alti compusi ca FeO, CaO, NiO, Cu2S( ) contin exces de ioni de O2 si goluri sau noduri catodice.
Teoria ionoelectronica a cresterii peliculelor de coroziune arata ca aceasta crestere a peliculei este rezultatul functionarii unei pile galvanice cu circuitele interior si exterior dispuse in interiorul aceleiasi faze (pelicula de coroziune).
Anodul pilei, constituit de suprafata de la interfata metal-pelicula, cedeaza ioni metalici Me+ si electronii e- iar catodul alcatuit din suprafata exterioara a peliculei si partial insasi masa peliculei accepta electronii e-. Aceasta teorie admite ca deplasarea ionilor in pelicula se produce nu atat sub influenta gradientului de concentratie, cat indeosebi ca urmare a migratiei ionilor in campul electric creat de diferenta dintre potentialul electric intern si cel extern.
Coroziunea metalelor in gaze
Influenta diferitilor factori asupra vitezei de coroziune in gaze
Dupa intensitatea actiunii lor corozive asupra metalului, factorii de coroziune se impart in doua categorii :
factori ce exercita o influenta puternica asupra vitezei de coroziune (durata, temperatura metalului, compozitia fazei metalice).
factori cu o influenta mai mica (viteza de deplasare a fazei gazoase, deformatiile metalului), incluziunile superficiale.
Din practica rezulta ca structura retelei cristaline si deformarile produse de prelucrarea metalelor exercita o influenta slaba asupra procesului de coroziune si numai in prima perioada.
Influenta compozitiei metalului este mult mai intensa. Carbonul si elementele insotitoare nu exercita o influenta prea semnificativa daca sunt in limitele admise. In schimb introducerea de Cr, Al, Si, duce la imbunatatirea proprietatilor refractare (maxim 30% Cr, 10% Al, 5% Si). Peste aceste procente, proprietatile refractare cresc dar scad proprietatile mecanice deoarece creste fragilitatea.
Influenta caracterului mediului gazos
In acest caz, viteza de coroziune depinde de compozitia chimica, viteza de deplasare si temperatura mediului. Influenta compozitiei mediului gazos asupra coroziunii depinde de natura celor doua faze, se manifesta din momentul aparitiei in mediul gazos a componentului agresiv si variaza foarte putin cu compozitia acestuia.
La schimbarea atmosfere obisnuite cu una de oxigen, viteza de coroziune a unei probe de fier (Fe) la 800 - 1000 oC, sau a unei probe de cupru (Cu) la 700 oC creste de aproximativ doua ori si nu de cinci ori cum ar urma sa creasca in cazul proportionalitatii directe, intre variatia vitezei de coroziune si presiunea partiala a oxigenului.
Coroziunea metalului se intensifica in aer la temperatura inalta, in prezenta unor impuritati date de gaze agresive ca vapori de apa, monoxid de carbon (CO), acid clorhidric (HCl) gazos.
Viteza de deplasare a gazului influenteaza coroziunea metalului numai in primele momente ale contactului fazelor. Dupa formarea peliculei viteza de coroziune este determinata de viteza de difuziune a particulelor prin pelicula. Deci viteza de coroziune nu mai depinde de aportul convectiv al gazului. La viteze deosebit de mari de curgere a gazului coroziunea se intensifica datorita distrugerii erozive a peliculei.
Din practica rezulta ca prin cresterea temperaturii, viteza de coroziune creste conform ecuatiei diferentiale a lui Arrhenius:
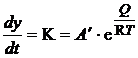
K =
![]() ,Q
= constante ce pot fi calculate pe baza
determinarii experimentale a vitezei de coroziune a vitezei K la cel
putin doua temperaturi diferite T1 si T2 .
Viteza de coroziune chimica variaza cu inversul
temperaturii
,Q
= constante ce pot fi calculate pe baza
determinarii experimentale a vitezei de coroziune a vitezei K la cel
putin doua temperaturi diferite T1 si T2 .
Viteza de coroziune chimica variaza cu inversul
temperaturii ![]() , fapt verificat de practica.
, fapt verificat de practica.
Coroziunea electrochimica a metalelor
Spre deosebire de cazul coroziunii chimice, suprafetele metalelor in contact cu solutiile bune conducatoare de electricitate, se corodeaza electrochimic. Solutiile si metalul sunt strabatute in acest caz de un curent electric propriu, generat de procesele electrochimice desfasurate la limita celor doua faze. Coroziunea electrochimica este atribuita adesea activitatii unor pile galvanice microscopice sau de dimensiuni mai mari ai caror anozi realizeaza distrugerea propriu-zisa pe anumite portiuni ale metalului, in timp ce restul suprafetei functioneaza catodic adica nu se distruge.
Suportul experimental al teoriei pilelor locale consta in influenta pronuntata pe care o exercita asupra vitezei de coroziune a metalelor tehnice, neomogenitatile de orice natura, incluziunile de impuritati metalice. De asemenea viteza de coroziune este influentata de eterogenitati de alta natura ca:
pelicule discontinue de coroziune;
portiuni cu tensiuni interne in metal;
compusi intermetalici.
Reactiile de coroziune electrochimica pot fi clasificate dupa trei tipuri de procese :
1. Coroziune cu degajare de H2 pe suprafata metalului
2Na + 2H2O 2NaOH + H2
Cd + H2SO4 CdSO4 + H2
Zn + 2NaOH Na2ZnO2 + H2
2. Coroziunea cu reducere de O2
2Fe + 2H2O + O2 2FeO2
3. Coroziune cu reducerea ionilor ferici la ioni ferosi
Fe + Fe2(SO4)3 3FeSO4
In realitate coroziunea se desfasoara pe suprafata metalului sub forma a doua reactii de electrod simultane de sens contrar si cu viteze egale adica legate intre ele prin transferul aceluiasi numar de electroni, reactii complet independente una fata de alta, numite reactii electrochimice conjugate. Viteza acestor reactii depinde in primul rand de potentialul de electrod.
Reactia anodica (reactia de ionizare sau de oxidare a metalului).
Aceasta reactie se poate scrie in forma generala, fara a tine seama de hidratarea ionilor astfel:
M Mz+ + ze -
In urma reactiei ionul metalic paraseste reteaua cristalina solida, trecand sub forma de ion hidratat in mediul lichid corosiv, lasand in faza solida cantitatea echivalenta de electroni.
Reactia catodica
O+ + ze - O
Aceasta reactie consta in reducerea unui agent oxidant capabil sa accepte un numar de z electroni rezultati prin ionizarea atomului de metal. Viteza procesului global al coroziunii, egala cu viteza procesului anodic si cu viteza procesului catodic poate fi exprimata numeric in g/m2h, metal trecut in solutie.
Coroziunea metalului omogen
Practic nu se intalnesc metale omogene datorita prezentei unei cantitati mici de impuritati sau defectelor de structura. Totusi coroziunea metalului omogen intereseaza deoarece furnizeaza elementele necesare pentru intelegerea proceselor mai complexe care se desfasoara pe suprafata structurilor eterogene.
Mecanismul coroziunii metalului pur se studiaza convenabil prin compararea comportarii in mediul acid a unui electrod reversibil de hidrogen si a unui electrod metalic cu potential electronegativ (amalgamul pur de zinc).
Electrodul reversibil de hidrogen se obtine prin saturarea cu hidrogen pur a unei placute de platina sau paladiu, prin scufundare intr-o solutie ce contine ioni de hidrogen (de obicei acid).
Pe electrodul de platina scufundat in solutia saturata in hidrogen a unui acid pot avea loc doua reactii simultane de sens contrar.
De tip A : 1/2H2 H+ + 1e - reactie anodica (de ionizare)
De tip B : H+ + 1e - 1/2H2 reactie catodica (de descarcare)
In conditii de echilibru aceste reactii decurg cu viteze egale:
i0 = ![]() = |
= | ![]() ; la
echilibru i = 0 si ji jrev T h
; la
echilibru i = 0 si ji jrev T h
In aceste conditii compozitia sistemului si potentialul nu variaza in timp. Spre deosebire de electrodul reversibil de hidrogen, pe suprafata amalgamului de zinc in contact cu solutia de hidrogen a unui acid mineral sunt posibile urmatoarele reactii elementare :
Zn Zn2+ + 2e - reactie anodica (se
desfasoara cu viteza ![]()
Zn2+ + 2e - Zn reactie catodica (se
desfasoara cu viteza ![]()
1/2H2 H+ + 1e - reactie anodica (se
desfasoara cu viteza ![]()
H+ + 1e - 1/2H2 reactie catodica (se
desfasoara cu viteza![]()
Cele patru reactii electrochimice pot lua parte la doua procese de schimb conform reactiilor:
I. Zn Zn2+ + 2e -
II. 1/2H2 H+ + 1e -
Cat timp metalul se dizolva de la sine cu degajare de hidrogen, viteza efectiva de dizolvare este:
i2 = ![]() -
- ![]()
adica diferenta densitatilor de curent a reactiei de ionizare I si a reactiei de descarcare II, va fi egala cu viteza de descarcare a hidrogenului :
i1 = ![]() -
- ![]()
Putem atunci spune ca:
i1 = i2 = is
unde is = curentul stationar de coroziune.
Potentialul ![]() pe care il ia electrodul in timpul dizolvarii sale cu viteza is se numeste
potential stationar. El mai este cunoscut in
literatura de specialitate si sub denumirile de potential mixt,
potential mediu, potential comun sau potential de compromis.
Reactiile anodice 2.2.5.5. si 2.2.5.7 pe de-o parte si reactiile
catodice 2.2.5.6 si 2.2.5.8 pe de alta parte se numesc reactii
electrochimice conjugate. Ele se desfasoara simultan si
independent una de alta si viteza uneia nu influenteaza viteza
celeilalte. Deci
la un potential stationar
pe care il ia electrodul in timpul dizolvarii sale cu viteza is se numeste
potential stationar. El mai este cunoscut in
literatura de specialitate si sub denumirile de potential mixt,
potential mediu, potential comun sau potential de compromis.
Reactiile anodice 2.2.5.5. si 2.2.5.7 pe de-o parte si reactiile
catodice 2.2.5.6 si 2.2.5.8 pe de alta parte se numesc reactii
electrochimice conjugate. Ele se desfasoara simultan si
independent una de alta si viteza uneia nu influenteaza viteza
celeilalte. Deci
la un potential stationar ![]() se poate scrie
ca:
se poate scrie
ca:
![]() +
+ ![]() =
= ![]() +
+ ![]()
In concluzie, suma vitezelor tuturor reactiilor catodice este egala cu suma vitezelor reactiilor anodice sau astfel spus numarul de electroni eliberati in cursul reactiilor anodice, este egal cu numarul de electroni asimilati in cursul reactiilor catodice.
Metalul pur scufundat
intr-o solutie acida sau in alt electrolit, cu conductibilitate mare
ia de la sine un potential stationar ![]() constant in timp,
acelasi pe intreaga suprafata metalica, la care oxidarea
metalului si reducerea oxidantului au loc cu aceeasi viteza egala cu is. Acestea sunt deci caracteristicile
principale ale starii stationare.
constant in timp,
acelasi pe intreaga suprafata metalica, la care oxidarea
metalului si reducerea oxidantului au loc cu aceeasi viteza egala cu is. Acestea sunt deci caracteristicile
principale ale starii stationare.
In conditiile
coroziunii metalelor tehnice, potentialul stationar variaza de
obicei in prima perioada a coroziunii tinzand apoi spre o valoare
Coroziunea metalului eterogen
Mecanismul coroziunii structurilor eterogene este mai complex decat cel al coroziunii metalului omogen. In principiu pe fiecare portiune omogena a unei suprafete eterogene se pot desfasura reactii de electrod in ambele sensuri. In acelasi, timp pe portiuni de natura diferita, pot avea loc reactii de electrod diferite. Coroziunea metalului eterogen se poate studia convenabil urmarind coroziunea in acizi a zincului impurificat cu cupru Fig. 2.2.6.1)

Fig.
Daca zincul ar fi pur potentialul
de coroziune stationar ![]() s-ar stabili la aceeasi valoare cuprinsa intre
s-ar stabili la aceeasi valoare cuprinsa intre ![]() si
si ![]() la care vitezele celor
doua reactii sunt egale. Pe zincul impurificat se stabileste
insa un potential
la care vitezele celor
doua reactii sunt egale. Pe zincul impurificat se stabileste
insa un potential ![]() . Din cauza reactiei de descarcare a ionilor de hidrogen pe cupru are loc deplasarea
potentialului
. Din cauza reactiei de descarcare a ionilor de hidrogen pe cupru are loc deplasarea
potentialului ![]() la
la ![]() la care viteza de
ionizare a zincului este egala cu suma vitezelor de descarcare a
ionilor de hidrogen pe cupru si zinc.
la care viteza de
ionizare a zincului este egala cu suma vitezelor de descarcare a
ionilor de hidrogen pe cupru si zinc.
Intrucat impuritatile de cupru
sunt in contact direct metalic cu masa de zinc, ele vor trebui sa ia acelasi potential, ceea ce este posibil
numai daca prin incluziunile de cupru va trece un curent catodic i![]() compensat de un curent anodic
compensat de un curent anodic ![]() de aceeasi marime pe suprafata zincului. Aceasta fractiune de curent i
de aceeasi marime pe suprafata zincului. Aceasta fractiune de curent i![]() ce trece de la
suprafata de zinc la cea de cupru se numeste curent local de
coroziune si se mai noteaza cu
ce trece de la
suprafata de zinc la cea de cupru se numeste curent local de
coroziune si se mai noteaza cu ![]()
ic = ![]() +
+ ![]()
In teoria clasica a coroziunii se admite ca distrugerea
metalului se datoreaza exclusiv curentului local i![]() iar zincul si cuprul
erau considerate electrozii unor elemente galvanice (pile locale scurtcircuitate ). Localizarea coroziunii are o
importanta practica deosebita insa mecanismul coroziunii nu se reduce
numai la functionarea simpla a unei pile locale, ci trebuie avut in
vedere intregul mecanism de formare a potentialului stationar.
Desfasurarea normala a celor doua reactii de electrod
nu necesita diferentierea suprafetei metalice care se corodeaza , in portiuni exclusiv anodice si
catodice. Pe suprafata omogena, ambele reactii se pot
produce cu aceeasi probabilitate in orice punct al suprafetei, cauza
coroziunii fiind micsorarea energiei libere a sistemului si nu
existenta unor pile galvanice locale. In cazul suprafetei eterogene
poate sa apara o localizare pronuntata a reactiilor de
electrod, daca incluziunile sunt astfel amplasate incat pe unele
portiuni se poate desfasura mai usor procesul catodic iar
pe altele procesul anodic. Gradul de diferentiere
al acestor procese depinde de gradul de eterogenitate al suprafetei,
insa in principiu, in limitele fiecarei portiuni omogene, se pot
desfasura ambele reactii electrochimice conjugate.
iar zincul si cuprul
erau considerate electrozii unor elemente galvanice (pile locale scurtcircuitate ). Localizarea coroziunii are o
importanta practica deosebita insa mecanismul coroziunii nu se reduce
numai la functionarea simpla a unei pile locale, ci trebuie avut in
vedere intregul mecanism de formare a potentialului stationar.
Desfasurarea normala a celor doua reactii de electrod
nu necesita diferentierea suprafetei metalice care se corodeaza , in portiuni exclusiv anodice si
catodice. Pe suprafata omogena, ambele reactii se pot
produce cu aceeasi probabilitate in orice punct al suprafetei, cauza
coroziunii fiind micsorarea energiei libere a sistemului si nu
existenta unor pile galvanice locale. In cazul suprafetei eterogene
poate sa apara o localizare pronuntata a reactiilor de
electrod, daca incluziunile sunt astfel amplasate incat pe unele
portiuni se poate desfasura mai usor procesul catodic iar
pe altele procesul anodic. Gradul de diferentiere
al acestor procese depinde de gradul de eterogenitate al suprafetei,
insa in principiu, in limitele fiecarei portiuni omogene, se pot
desfasura ambele reactii electrochimice conjugate.
Daca vitezele unora dintre procesele partiale sunt neglijabile poate rezulta practic localizarea totala a proceselor anodic si catodic, distrugandu-se prin coroziune locala doar portiunile ce functioneaza anodic (ex: coroziune intercristalina, coroziune punctiforma - pitting ). Repartizarea curentilor locali de coroziune pe suprafata metalului tehnic este atat de complexa incat un calcul exact al lor nu este posibil. Cu toate acestea studiul electrochimic al diversilor constituenti structurali ai metalului eterogen poate furniza date asupra polaritatii lor in timpul coroziunii.
Coroziunea a doua metale in contact
In conditii practice contactul a doua metale, chiar de inalta puritate, trebuie considerat ca un sistem in care sunt posibile cel putin patru reactii de electrod. Cele patru reactii posibile intr-un sistem de doua metale introduse in solutie corosiva sunt:
Ionizarea metalului M1: M1 M1z+ + ze -
Ionizarea metalului M2: M2 M2z+ + ze -
Degajarea hidrogenului pe metalul M1: 1/2H2 H+ + 1e -
Degajarea hidrogenului pe metalul M2: 1/2H2 H+ + 1e -
Daca metalele M1 si M2
nu s-ar afla in contact atunci M1 s-ar coroda cu viteza ia1 la potentialul ![]() iar M2 s-ar coroda cu viteza ia2 la potentialul
iar M2 s-ar coroda cu viteza ia2 la potentialul ![]() . Din cauza contactului metalic cele doua
potentiale stationare
. Din cauza contactului metalic cele doua
potentiale stationare ![]() si
si ![]() se egaleaza la
valoarea
se egaleaza la
valoarea ![]() la care viteza de
coroziune a metalului M2 scade cu Dia2 iar viteza de coroziune a metalului M1
creste cu Dia1. De
aici apare explicatia protectiei anticorosive prin metode
electrochimice.
la care viteza de
coroziune a metalului M2 scade cu Dia2 iar viteza de coroziune a metalului M1
creste cu Dia1. De
aici apare explicatia protectiei anticorosive prin metode
electrochimice.
Aceste metode sunt:
metoda anozilor sacrificati
protectia catodica folosind curenti exteriori
Metoda anozilor sacrificati
Daca in locul
metalului M1 s-ar fi luat un alt metal cu potential reversibil
mai electronegativ decat ![]() , potentialul
, potentialul ![]() al contactului ar fi
rezultat de asemenea mai negativ. In practica se alege
un metal M1 atat de electronegativ incat la contact acesta se
dizolva protejand partial sau integral metalul M2. Deci
metoda anodului sacrificat consta in fixarea pe obiectul protejat a unor
placi de Zn, Mg sau Al, cu potential puternic electronegativ.
al contactului ar fi
rezultat de asemenea mai negativ. In practica se alege
un metal M1 atat de electronegativ incat la contact acesta se
dizolva protejand partial sau integral metalul M2. Deci
metoda anodului sacrificat consta in fixarea pe obiectul protejat a unor
placi de Zn, Mg sau Al, cu potential puternic electronegativ.
Metoda protectiei catodice cu curenti exteriori
Aceasta consta in conectarea piesei de protejat la polul negativ al unei surse de curent la al carei pol pozitiv este legat un anod indiferent (otel, grafit, etc).
Coroziunea mai multor metale in contact
Coroziunea
mai multor metale in contact apare in cazul unor instalatii industriale ce au in componenta otel, bronzuri, alame,
Zn, Al, instalatii ce se afla in contact cu solutii de
electroliti. Akimov a denumit astfel de constructii sisteme de
polielectrozi, ce dau nastere unor macropile
galvanice de coroziune. In solutii suficient de bune conducatoare de
electricitate (polare), sistemele polimetalice pot fi considerate ca pile
polielectrodice scurtcircuitate. In acest caz se pune problema
determinarii unui potential de compromis, notat ![]() , al tuturor metalelor in contact, dupa care se
stabileste care metale lucreaza ca anozi si care
functioneaza drept catozi. Acele metale care au potentialul
reversibil mai electronegativ decat
, al tuturor metalelor in contact, dupa care se
stabileste care metale lucreaza ca anozi si care
functioneaza drept catozi. Acele metale care au potentialul
reversibil mai electronegativ decat ![]() vor functiona ca
anozi si se vor distruge, iar cele cu potential reversibil mai
electropozitiv decat
vor functiona ca
anozi si se vor distruge, iar cele cu potential reversibil mai
electropozitiv decat ![]() , functionand catodic, raman protejate.
, functionand catodic, raman protejate.
Influenta diferitilor factori asupra coroziunii electrochimice
Natura metalului
Coroziunea unui metal este posibila daca potentialul sau reversibil este mai negativ decat potentialul reversibil al unui agent oxidant in aceeasi solutie. Luand ca baza seria potentialelor standard de electrod, se poate considera ca in apa cu sau fara continut de saruri neutre tind sa se corodeze toate metalele care au potentiale reversibile mai negative decat -0,414 V si anume: metale alcaline, metale alcalino-pamantoase, Al, Ti, Zr, Cr, Zn, Fe. In practica insa numai metalele alcaline si alcalino-pamantoase descompun apa, celelalte trecand in stare pasiva in apa si chiar in unii acizi oxidanti. Rezulta ca nu exista un paralelism riguros intre locul metalelor in seria potentialelor standard si in sistemul periodic pe de-o parte si comportarea lor la coroziune pe de alta parte. Totusi exista o concordanta cu caracter general intre stabilitatea metalelor la coroziune si locul acestora in cele doua sisteme. Astfel metalele cu cele mai electronegative potentiale standard au si stabilitatea chimica cea mai mica, respectiv rezistenta la coroziune mica. Este vorba de Li, Na, K, Pb, Cs.
Rezistenta anticorosiva a metalelor in subgrupele din dreapta si in grupa a opta secundara a sistemului periodic, creste de sus in jos ca in subgrupele:
Cu Zn Fe
Ag Cd Rb
Au Hg Os
Metalele cu cea mai mare tendinta de pasivare se afla in randurile de jos, pare ale perioadelor mari, in grupele 4, 5, 6, 7, 8, secundare.
Structura si starea suprafetei metalului
Cele mai stabile aliaje la coroziune sunt cele de tip solutie solida deoarece acestea sunt constituenti omogeni (monofazic, Fa la temperatura ambianta). Diferiti constituenti cu structura eterogena (amestecuri mecanice, compusi chimici), intensifica procesul de coroziune pentru ca se afla in contact cu matricea si aliajul se comporta ca doua metale aflate in contact in acelasi mediu corosiv. Exceptie face, de exemplu, eutecticul Al-Si din siluminuri carte rezista bine la coroziune in apa de mare.
Cercetand comportarea anticorosiva a solutiilor solide, Tamann a stabilit o regula de mare importanta practica, numita regula limitei de rezistenta chimica sau regula n/8 (n este numar intreg ce ia valorile 1, 2, 4, . Conform acestei reguli rezistenta la coroziune a aliajelor tip solutie solida creste brusc cu variatia compozitiei, in momentul in care continutul elementului stabil fata de cel al elementului instabil intr-un mediu dat atinge fractiunea n/8
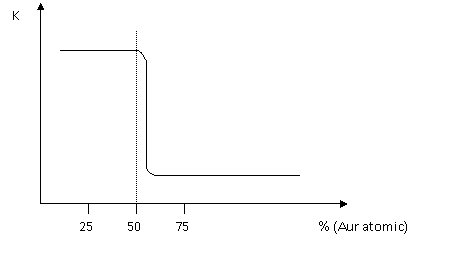
Fig.
Intr-o solutie de Cu-Au scufundata in acid azotic (HNO3) rezistenta la coroziune creste brusc la peste 50% Au atomic. Pana la 50% Au atomic solutia se corodeaza cu viteza de coroziune a cuprului. La o mica depasire a procentului de Au atomic, viteza de coroziune K scade pana la valori foarte mici. Deci creste rezistenta la coroziune si aliajul are comportarea aurului pur.
Explicatia consta in efectul de ecranare al metalului mai nobil, respectiv aurul din solutia solida, care nu se dizolva din primele momente ale coroziunii, ramanand la suprafata. Distantele interatomice ale metalului nobil sunt mai mici decat diametrul ionilor din mediul corosiv si astfel nu este permisa difuzia acestora spre metal.
Un alt fenomen caracteristic solutiilor solide este dizolvarea selectiva a unuia dintre componenti insotita de distrugerea aliajului.
In cazul alamelor scufundate in solutii acide sau apa de mare are loc un fenomen de dizolvare a zincului, mai exact de trecere a zincului in solutie astfel incat in metal ramane numai cuprul sub forma de pulbere fina. Consecinta procesului de dezincare este pierderea coeziunii aliajului si deci reducerea drastica a proprietatilor mecanice.
Marimea grauntilor cristalini
Aceasta influenteaza in mica masura coroziunea, insa viteza de coroziune creste cu gradul de dispersie a impuritatilor deci cu finetea structurii, cu conditia ca aceste impuritati sa functioneze catodic.
Comportarea aliajelor ce constau din doua faze diferite depinde de polaritatea celor doi constituenti. Daca metalul de baza functioneaza preponderent ca anod si nu are tendinta de pasivare iar componentul structural are rol de anod, rezulta intensificarea coroziunii in raport cu cea a metalului de baza in stare pura.
Tensiunile interne si deformatiile intensifica coroziunea in toate cazurile si adesea inrautatesc repartitia ei transformand-o dintr-o coroziune uniforma intr-o coroziune locala sau intercristalina.
Starea suprafetei metalului
Aceasta influenteaza asupra coroziunii electrochimice, deoarece o suprafata rugoasa este mai expusa la coroziune decat una neteda. Raportul dintre suprafata efectiva si cea teoretica este :
![]() = 6 pentru piese brut turnate ;
= 6 pentru piese brut turnate ; ![]() = 1,2 pentru piese rectificate, lustruite.
= 1,2 pentru piese rectificate, lustruite.
Influenta calitatii suprafetei se resimte mai ales in conditiile coroziunii atmosferice cand rolul principal in coroziune il are condensarea umezelii in capilarele fine ale asperitatilor superficiale.
Compozitia solutiei corosive
Principalele caracteristici ale solutiei care prezinta interes din punct de vedere al coroziunii sunt: aciditatea solutiei (pH-ul), continutul de oxigen, concentratia sarurilor in solutie, prezenta acceleratorilor sau inhibitorilor de coroziune.
- Influenta oxigenului din solutie - Oxigenul poate avea dublu rol si anume :
Un rol de accelerator de coroziune (accelerator catodic), adica rol de agent oxidant care se reduce relativ usor pe metale facand posibila si chiar accelerand coroziunea. La probele imersate in solutii corosive intensitatea coroziunii este mai mare la interfata lichid atmosfera. De asemenea agitarea mediului corosiv datorita curgerii libere sau fortate maresc aportul de oxigen in solutie si intensifica coroziunea.
Un al doilea rol este acela de inhibitor de coroziune (franarea procesului anodic) atunci cand concentratia lui in solutie este asa de mare incat creste stabilitatea peliculelor protectoare pasivante pe suprafata metalului.
Influenta concentratiei sarurilor in solutie
Concentratia sarurilor in solutie influenteaza diferit coroziunea:
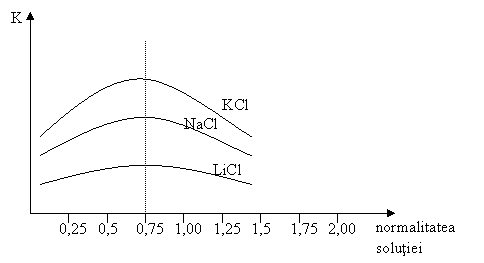
Fig.- Influenta continutului de sare din solutie asupra vitezei de coroziune a otelului moale scufundat la 35oC
La un
continut mic de sare viteza de coroziune creste cu concentratia
sarii, ca rezultat al cresterii continutului de anioni ![]() care activeaza procesul anodic. Efectul
contrar, de scadere a vitezei de coroziune inregistrat in domeniul
urmator (dupa 0,75) se datoreaza micsorarii
solubilitatii oxigenului cu cresterea concentratiei
sarii in apa.
care activeaza procesul anodic. Efectul
contrar, de scadere a vitezei de coroziune inregistrat in domeniul
urmator (dupa 0,75) se datoreaza micsorarii
solubilitatii oxigenului cu cresterea concentratiei
sarii in apa.
Influenta pH-ului este
importanta deoarece pe masura cresterii aciditatii
solutiei valorile potentialelor reversibile ![]() si
si ![]() devin din ce in ce mai pozitive si viteza
coroziunii creste.
devin din ce in ce mai pozitive si viteza
coroziunii creste.
Acizii cu functie oxidanta HNO3 H2SO4 concentrati exercita o actiune mai complexa asupra metalelor deoarece se formeaza cu o pelicula protectoare rezistenta la acid, care face imposibila studierea influentei directe a pH-ului asupra vitezei de coroziune. Variatia pH-ului solutiei are si o influenta indirecta asupra coroziunii, in functie de variatia solubilitatii si a proprietatilor protectoare ale produselor de coroziune cu pH-ul mediului. Din acest punct de vedere metalele tehnice se impart in doua grupe:
1. metale ale caror oxizi au proprietati amfotere : Al, Zn, Sn, Pb, care se corodeaza atat in acizi cat si in alcalii.
 2. metale
care dau oxizi solubili in acizi dar insolubili in alcalii : Fe, Ni, Cu, Cd,
Mg.
2. metale
care dau oxizi solubili in acizi dar insolubili in alcalii : Fe, Ni, Cu, Cd,
Mg.
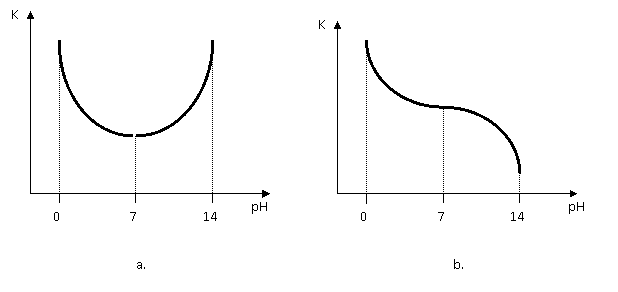
Fig..- Variatia vitezei de coroziune cu pH-ul.
a.- metale din prima categorie; b. - metale din a doua categorie
Prezenta acceleratorilor sau inhibitorilor de coroziune influenteaza direct viteza de coroziune chiar daca acestia sunt in cantitati mici sau foarte mici.
Importanta practica pentru coroziune prezinta inhibitorii de coroziune, insa trebuie cunoscute si proprietatile electrochimice ale acceleratorilor de coroziune.
Dupa procesul de electrod asupra caruia exercita actiunea principala, inhibitorii anorganici se impart in inhibitori anodici si catodici. Inhibitorii organici se folosesc in general la combaterea coroziunii in medii acide iar atunci cand au tensiunea de vapori suficient de mare se folosesc in calitate de inhibitori volatili.
Dintre inhibitorii anodici mai importanti sunt :
bicromatul de potasiu (K2O2Cr7) - 0,1 0,01% - reducerea coroziunii Fe si Al.
azotitul de sodiu (NaNO2) - conservarea sculelor instrumentelor si pieselor.
azotatul de sodiu (NaNO3) - pentru cazanele de abur.
Acesti inhibitori se folosesc in solutii de H2O neutra, putin activa anodic (fara anioni de Cl, Br, I), pentru ca altfel predomina viteza de reducere a lor fata de viteza actiunii pasivante. Unii inhibitori anorganici sunt considerati inhibitori anodici, deoarece formeaza cu ionii metalici trecuti in solutie produse de coroziune insolubile, care se depun pe metal sub forma unor pelicule protectoare aderente. Aceste produse (hidroxid de sodiu (NaOH), carbonat de sodiu (NaCO3), fosfat acid de sodiu (NaHPO4), silicat de sodiu (Na4Si)), realizeaza o ecranare a metalului si reduc suprafata de contact intre metal si mediul agresiv.
Inhibitorii catodici anorganici sulfitul de sodiu (Na2SO3) si hidrazina (NH2-NH2) micsoreaza sau chiar impiedica procesul catodic deoarece consuma oxigenul dizolvat in apa, trecand in produse inofensive.
Na2SO4 Na2SO3
NH2 - NH2 N2 +H2O
Actiunile inhibitoare ale carbonatului acid de calcar (Ca(CO3)2), sulfatului de zinc, clorurii de zinc(ZnCl2), pot fi atribuite alcalinizarii mediului ceea ce atrage dupa sine precipitarea carbonatului de calciu sau a dioxidului de zinc protectoare pentru metal. Astfel se explica agresivitatea mai redusa a apelor naturale (dure), bogate in carbonati fata de cea a apelor moi.
Coroziunea in mediul acid poate fi inhibata de sarurile unor metale electropozitive cu supratensiune relativ mare de hidrogen Ex: AsCl3, Bi2(So4)3). Dezlocuind aceste metale din solutia acida a sarurilor lor, ferul se acopera cu un strat fin de arseniu respectiv bismut, cu o supratensiune de hidrogen mai mare decat supratensiunea hidrogenului pe fer. Acceleratorii de coroziune intensifica distrugerea metalelor, atunci cand sunt adaugati intr-un mediu agresiv oarecare.
In practica sunt considerati drept acceleratori de coroziune, anionii de halogeni, agentii de complexare care, inglobeaza in timpul coroziunii ionii de metal proaspat formati, in complecsi solubili putin disociati, mentinand o concentratie redusa de ioni in solutie si deci viteze mai mari de ionizare a metalului decat in absenta lor.
Influenta temperaturii asupra coroziunii electrochimice
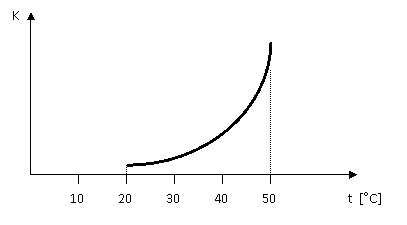
Fig.- Variatia vitezei de coroziune cu temperatura
In cazul solutiilor acide variatia de temperatura exercita o influenta puternica asupra coroziunii electrochimice, exprimata cantitativ de relatia lui Arrhenius.
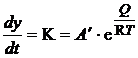
K =
![]() ,Q
= constante ce pot fi calculate pe baza
determinarii experimentale a vitezei de coroziune a vitezei K la cel
putin doua temperaturi diferite T1 si T2 .
,Q
= constante ce pot fi calculate pe baza
determinarii experimentale a vitezei de coroziune a vitezei K la cel
putin doua temperaturi diferite T1 si T2 .
Variatiile de temperatura pot influenta si indirect coroziunea de exemplu, prin intermediul influentei pe care o exercita asupra pH-ului solutiei. Astfel solutiile cu reactie neutra la rece dau reactie acida la cresterea temperaturii. De asemenea comportarea la coroziune a diverselor metale depinde in mare masura si de variatia proprietatilor peliculelor protectoare cu temperatura. De exemplu, pe zinc sub 50 oC se depune o pelicula aderenta sub forma de gel care este foarte protectoare; in schimb intre 50 oC si 95 oC se formeaza un produs cu aspect grauntos care rezista mai putin la coroziune.
Influenta presiunii solutiei asupra coroziunii
Sub actiunea presiunii apar tensiuni puternice in metal, se ingreuneaza imbinarea si etansarea detaliilor de constructie si totodata creste solubilitatea gazelor in solutie. Influenta cresterii presiunii se resimte mai intens in cazul in care oxidantul este un gaz dizolvat in solutie. Accelerarea coroziunii datorita cresterii presiunii se manifesta mai intens in cadrul proceselor ce se desfasoara la temperaturi inalte.
Influenta vitezei de curgere a solutiei
Intensificarea coroziunii ferului in medii neutre cu accelerarea curgerii la o viteza relativ mica se datoreaza intensificarii aportului de oxigen la suprafata metalica. In conditiile unui aport intens de oxigen coroziunea se poate atenua di cauza pasivarii treptate a ferului. La viteze mari jeturile de lichid tind sa smulga particulele din pelicula de protectie, iar metalul descoperit,venind in contact cu cantitati marite de oxidant se corodeaza mai intens.(Ex:corodarea tevilor de alama din condensatoare, corodarea rotoarelor,corodarea unor agitatori de suspensii ce contin particule dure). La viteze foarte mari de curgere in masa solutiei pot aparea bule, cu depresiuni puternice dand efecte de izbire si extragere cand se distrug nu numai peliculele ci si metalul insusi. Acest fenomen este cunoscut sub denumirea de cavitatie.
Influenta timpului asupra proceselor de coroziune
Evolutia coroziunii electrochimice in timp prezinta interes practic. Pe baza datelor experimentale pot fi construite doua tipuri de curbe:
a. - curbe pierdere de greutate - timp sau y = f (t)
b. - curbe
viteza de coroziune - timp sau ![]() = f (t)
= f (t)
I.
Pentru procesele in care conditiile
initiale de coroziune nu variaza in timp (Ex: compozitia
solutiei este
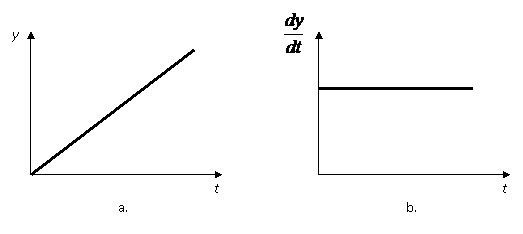
Fig.
II.
Pentru procesele in care coroziunea se atenueaza cu timpul din cauza formarii peliculelor din ce in ce mai protectoare.
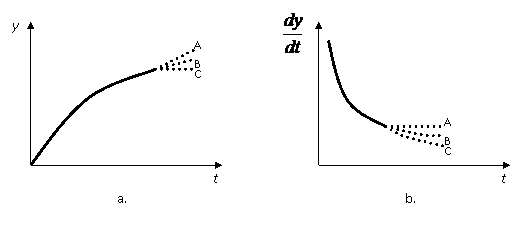
Fig.
In acest caz viteza de coroziune ![]() variaza dupa
o curba descendenta a carei portiune terminala devine
paralela cu abscisa (cazul B), o intersecteaza (cazul C) sau scade
lent (cazul A), dupa cum curba y = f (t) se termina intr-o
dreapta B, o orizontala C sau o portiune usor
ascendenta A.
variaza dupa
o curba descendenta a carei portiune terminala devine
paralela cu abscisa (cazul B), o intersecteaza (cazul C) sau scade
lent (cazul A), dupa cum curba y = f (t) se termina intr-o
dreapta B, o orizontala C sau o portiune usor
ascendenta A.
III.
Pentru coroziunea metalelor in acizi si a aluminiului in alcalii.
C D D C B B t b. a. y t![]()
![]()
![]()
![]()

![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
O
[
![]() Fig.
Fig.
In acest caz coroziunea se intensifica cu timpul fie din primul moment al contactului, fie dupa un anumit timp [OB], de la scufundarea probei in mediul coroziv. Intensificarea procesului poate fi datorata distrugerii peliculei protectoare sau cresterii temperaturii. Dupa un timp se stabileste un regim stationar C cand coroziunea este constanta in timp.
Pasivitatea metalelor
Pasivitatea reprezinta o stare de rezistenta mare la coroziune a metalelor si aliajelor, in conditiile in care, din punct de vedere termodinamic, aceste metale sunt active (deci se pot coroda), rezistenta provocata de micsorarea procesului anodic sub actiunea deplasarii in sens pozitiv a potentialului.
Ferul si numeroase alte metale tehnice se dizolva in HNO3 diluat iar viteza de dizolvare creste cu concentratia acidului. In cazul nparticular al ferului exista o concentratie critica a acidului la care viteza dizolvarii scade brusc si peste care coroziunea devine practic neglijabila desii nu inceteaza cu desavarsire.
Faraday a emis ipoteza ca starea pasiva a ferului se datoreaza formarii unor compusi intre atomii de metal de la suprafata si oxigen.
Starea pasiva a metalelor poate fi clasificata dupa metoda prin care a fost provocata sau dupa aspectul suprafetei rezultate in urma procesului, in urmatoarele categorii :
- Pasivitate mecanica - atunci cand prin scufundarea metalului in mediul corosiv, la suprafata lui se formeaza straturi groase de compusi chimici, ce au efect protector prin simpla izolare mecanica a fazelor. (Pb scufundat in H2SO4 formeaza la suprafata o pelicula de PbSO4).
- Pasiuvitatea chimica - atunci cand metalul scufundat in mediul coroziv se acopera cu un strat fin protector si invizibil (pasivarea ferului in HNO3 concentrat).
- Pasivitatea electrochimica (anodica) - atunci cand metalul trece in stare pasiva sub influenta curentului electric exterior
Aceasta clasificare a pasivitatii este conventionala deoarece in toate cazurile mecanismul de pasivare este electrochimic.
In stare activa, metalul simplu introdus in solutie si nelegat la un circuit electric exterior sau anodul metalic, trec in solutie cu formare de ioni hidratati cu conditia ca potentialul lor sa fie suficient deplasat in sens pozitiv de la valoarea potentialului reversibil. Daca potentialul stationar al unui asemenea metal simplu sau potentialul anodului unui circuit este si mai mult deplasat in sens pozitiv, sub actiunea unui factor oarecare, metalul poate ajunge in stare pasiva, cand trecerea ionilor metalici in solutie este impiedicata sau puternic franata de o asanumita bariera de oxigen (strat de compus Me-O2) aflat la suprafata metalului. In prezenta barierei protectoare de oxigen viteza de coroziune a mai multor metale se reduce de sute si mii de ori devenind neglijabila, desi din punct de vedere termodinamic metalul ramane activ.
Mecanismul pasivarii
Formarea peliculelor de pasivare atat la simpla scufundare a metalului in
solutia pasivanta, cat si la functionarea lor in calitate
de anozi este rezultatul unor procese electrochimice, deci starea
suprafetelor metalice si viteza proceselor ce se
desfasoara la suprafata sunt determinate de
potentialul de electrod. Pentru a intelege mecanismul pasivarii
trebuie sa se studieze curbele ![]() sau asanumitele curbe de
polarizatie.
sau asanumitele curbe de
polarizatie.
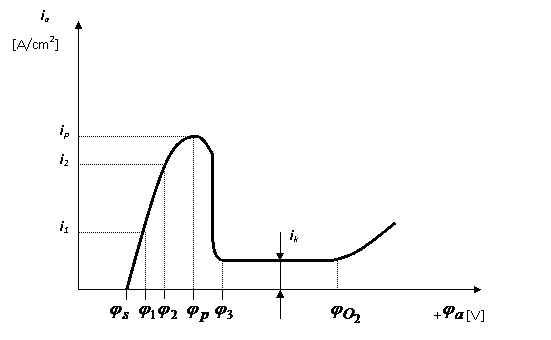
Fig. curba de polarizatie
![]() = potentialul electrodului cercetat;
= potentialul electrodului cercetat;
ia densitatea de curent rezultata in circuitul exterior
La scufundarea electrodului in
solutie, in absenta unui curent in circuitul exterior (ia = ,
se stabileste spontan potentialul stationar ![]()
![]() 0). In aceasta stare electrodul se corodeaza cu o viteza icor 0, care se poate determina pe baza pierderilor de masa. Deplasarea
potentialului in sens pozitiv duce la intensificarea dizolvarii
si la aparitia in circuitul exterior a unui curent a carui
valoare i1, i2, este data de ordonata punctelor
corespunzatoare potentialelor
0). In aceasta stare electrodul se corodeaza cu o viteza icor 0, care se poate determina pe baza pierderilor de masa. Deplasarea
potentialului in sens pozitiv duce la intensificarea dizolvarii
si la aparitia in circuitul exterior a unui curent a carui
valoare i1, i2, este data de ordonata punctelor
corespunzatoare potentialelor ![]()
![]()
Intensificarea dizolvarii sub
actiunea deplasarilor urmatoare de potential continua
pana cand electrodul atinge potentialul ![]() caruia ii corespunde curentul ip . La aceasta valoare o noua
deplasare a potentialului la
caruia ii corespunde curentul ip . La aceasta valoare o noua
deplasare a potentialului la ![]() are ca efect o scadere brusca a
curentului anodic, a vitezei de dizolvare pana la valoarea ik si trecerea metalului
in stare pasiva. Noua valoare a curentului ik poate fi de zeci de mii de
ori mai mica decat valoarea initiala a curentului icor .
are ca efect o scadere brusca a
curentului anodic, a vitezei de dizolvare pana la valoarea ik si trecerea metalului
in stare pasiva. Noua valoare a curentului ik poate fi de zeci de mii de
ori mai mica decat valoarea initiala a curentului icor . ![]() se numeste potential
critic de pasivare, iar ip se
numeste densitate critica de curent de pasivare. Deci la valori mai
mari ale lui
se numeste potential
critic de pasivare, iar ip se
numeste densitate critica de curent de pasivare. Deci la valori mai
mari ale lui ![]() curentul de coroziune scade la ik , de valori foarte mici diferite de 0, care
arata ca procesul de coroziune nu a incetat ramanand in
continuare posibil din punct de vedere termodinamic, insa are loc cu
viteze extrem de mici, practic neglijabile. Deci
la potentiale mai mari decat
curentul de coroziune scade la ik , de valori foarte mici diferite de 0, care
arata ca procesul de coroziune nu a incetat ramanand in
continuare posibil din punct de vedere termodinamic, insa are loc cu
viteze extrem de mici, practic neglijabile. Deci
la potentiale mai mari decat ![]() are loc desavarsirea
peliculei de pasivare, iar la valori mai mici decat
are loc desavarsirea
peliculei de pasivare, iar la valori mai mici decat ![]() metalul se afla in stare
activa.
metalul se afla in stare
activa.
Starea
pasiva se mentine pana la atingerea potentialului
reversibil ![]() la care incepe separarea gazului. Peste
potentialul
la care incepe separarea gazului. Peste
potentialul ![]() intensitatea curentului creste, dar
aceasta crestere nu mai poate fi folosita ca masura
directa a coroziunii, deoarece se datoreaza in mare masura
descarcarii ionilor hidroxil (OH).
intensitatea curentului creste, dar
aceasta crestere nu mai poate fi folosita ca masura
directa a coroziunii, deoarece se datoreaza in mare masura
descarcarii ionilor hidroxil (OH).
Cel mai usor se4 pasiveaza Cr, Mo, Al, Fe, Co, Ni, Ti, Ta, insa variind compozitia solutiei sau densitatea anodica de curent se pot crea conditii in care orice metal trece mai mult sau mai putin in stare de pasivitate.
Prin alierea unui metal mai greu pasivabil cu un component mai usor pasivabil, se pot obtine aliaje usor pasivabile cu structura, in general, de tip solutie solida (Ex: oteluri inoxidabile aliate cu Cr, fonte silicioase). Unele metale ca Al, Cr, Ti, Ta, se pasiveaza usor de la sine prin simplu contact cu oxigenul din aer si raman in stare pasiva atata timp cat pelicula superficiala nu este deteriorata sub actiunea unor factori externi.
Alte metale mai greu pasivabile trec in stare pasiva numai in contact cu medii puternic oxidante : acid azotic (HNO3), azotat de argint (AgNO3), clorat de potasiu (KClO3), bicromat de potasiu (K2Cr2O7), permanganat de potasiu (KMnO4).
Starea pasiva poate aparea brusc sau treptat. In ultimul caz metalul poate trece prin faze intermediare stabile. (Ex: Fe in HNO3 de o anumita concentratie se pasiveaza brusc in timp ce in solutii de cromati viteza de coroziune scade treptat).
Exista un numar de factori care impiedica aparitia pasivitatii sau distrug peliculele pasivante readucand metalele in stare activa. Pasivitatea dispare cand metalele vin in contact cu solutii care dizolva peliculele (Ex: solutii alcaline pe Al si Zn). De asemenea pasivitatea dispare si sub actiunea unor factori mecanici (eroziune, frecare, zgariere) daca viteza de restabilire a starii pasive in mediul dat este mai mica decat viteza de distrugere a peliculei.
Cercetarile experimentale privind pasivitatea metalelor nu au putut duce la o concluzie unica referitor la natura barierei de oxigen din cauza complexitatii fenomenului. De aceea in prezent exista doua teorii ale pasivitatii metalelor.
- teoria peliculei de faza
- teoria peliculei de adsorbtie
Teoria peliculei de faza sustine ca bariera de oxigen care determina starea pasiva a metalului este constituita dintr-o pelicula de faza din oxizi metalici. In prezent pelicula este considerata perfect continua iar compozitia oxidului rezistent in mediul acid si in mediul bazic este aceeasi. Se admite ca procesul electrochimic de dizolvare este inlocuit, in domeniul pasivitatii, prin dizolvarea chimica a peliculei de oxid cu formare de ioni ferici. De asemenea se admite ca pelicula este complet lipsita de pori deoarece, in caz contrar, viteza de dizolvare in pori ar depinde de potential .
Teoria peliculei de adsorbtie considera ca valenta atomilor de metal de la suprafata se satureaza prin formarea de legaturi chimice cu particulele care se pot adsorbi, ceea ce nu duce insa la distrugerea retelei metalice si la formarea unui compus stoechiometric cu retea proprie. Chiar daca acesti compusi s-ar forma cu timpul, ei au numai rolul de a constituii o bariera suplimentara de difuziune.
Conform acestor teorii metalele se impart in trei grupe:
Metale nobile ce nu formeaza pelicule de faza.
Metale din grupa ferului pe care autorii teoriei considera ca nu se formeaza pelicule de faza.
Metale ca Al, Ti, Ta, pe care se formeaza Pelicule groase vizibile de oxizi, lipsite de conductibilitate electronica.
Teoria peliculei de faza se refera numai la primele doua tipuri, aratand ca natura electrochimica a dizolvarii se pastreaza si in conditiile starii pasive in care se schimba numai cinetica procesului anodic.
In funtie de durata si de temperatura de incalzire a metalului, peliculele formate au diferite grosimi si proprietati de protectie prezentate in tabelul urmator :
|
Felul peliculei |
Grosimea peliculei [Å ] |
Proprietatile peliculei |
|
Pelicule subtiri |
Sub 400 |
Nu protejeaza din cauza rezistentei reduse pe care o opune difuziunii agentului corosiv |
|
Pelicule medii |
Prezinta proprietati de protectie a suprafetei metalice |
|
|
Pelicule groase |
Peste 5000 |
Protectie ineficienta deoarece se fisureaza sub actiunea tensiunilor interne |
O apreciere rapida a proprietatilor protectoare a peliculei de oxid rezultate in urma coroziunii este posibila cunoscand valoarea raportului dintre voluzmul oxidului format si volumul metalului distrus :
Vox =Mox /ρox ; Vm=An/ m Vox /Vm=Mox /ρox*ρm /An , in care:
Mox -este masa moleculara a oxidului;
ρox -greutatea specifica a oxidului;
A -masa atomica a metalului;
ρm -greutatea specifica a metalului;
n -coeficientul stoechiometric al metalului;
Daca acest raport este subunitar, adica Vox /Vm <1, stratul de oxid este discontinuu si permeabil, ca urmare, nu prezinta proprietatile protectoare. Astfel se comporta metalele alcaline si alcalino-pamantoase.
Pentru alte metale, ca: Ni, Cr, Cu, Sn, Zn,., raportul Vox /Vm >1; La suprafata acestora se formeaza pelicule care franeaza considerabil desfasurarea in continuare a procesului de oxidare, adica poseda proprietati protectoare.
Conditia Vox /Vm >1 nu asigura intotdeauna o protectie anticoroziva, deoarece in timpul formarii peliculelor, apar tensiuni care vor provoca fisurarea acestor pelicule.
In cazul Fe-ului oxidarea in atmosfera a acestuia cu formarea oxizilor de Fe (rugina) are loc in trepte.
In prima treapta de oxidare a Fe-ului, se formeaza FeO, oxidul feros, care este stabil numai in absenta oxigenului. Cand apare oxigenul atmosferic, oxidul feros se transforma in hidroxid de fier (Fe2O3H2O) sau FeO(OH), dintre care se cunosc 2 faze:
Faza 1 care corespunde unui exces mare de oxigen;
Faza 2 caracterizata prin o cantitate de oxigen, insuficienta, din care cauza, oxidarea evolueaza incet.
In functie de culoare se pot deosebi 3 feluri de rugina si anume:
Rugina alba Fe(OH)2 , care se formeaza dupa reactia:
Fe+2H2O→Fe(OH)2+H2
Acest tip de rugina trece rapid, prin oxidare, in rugina bruna, de aceea se observa foarte rar.
Rugina bruna, apare in urma reactiei:
4Fe(OH)2+O2→4FeO*OH+2H2O
Rugina neagra, este formata din oxid feros si feric; fiind denumita si magnetita din cauza proprietatilor sale magnetice si este considerata ca fiind forma cea mai stabila a oxidului de fier. Ea formeaza pe suprafata metalului un strat protector, cu structura omogena si aderenta. Reactia decurge astfel:
2FeO*OH+Fe(OH)2→Fe3O4+2H2O
Dr. H. Engell, de la Institutul Max Plank, descrie astfel ruginirea fierului la temperaturi inalte:
pana la 570˚C se formeaza pe metal fazele de oxidare, magnetita si hematita dintre care, magnetita reprezinta aproximativ 65-80% din grosimea stratului format.
De la 570˚C incepe sa apara FeO (vustita) care creste mult odata cu temperatura de oxidare;
La 700˚C stratul de tunder (oxid de laminare) se compune din 90% vustita.
Stratul de oxizi de laminare este alcatuit, de fapt, din mai multe straturi, dintre care, cel inferior, este format din FeO. Prezenta acestuia este cauza slabei aderente a oxizilor formati succesiv la suprafata metalica, deoarece sub influenta atmosferei, duce la hidroxid de fier, deci la rugina.
Coroziunea otelurilor la temperaturi inalte sub actiunea unor gaze oxigen, dioxid de carbon, hidrogen, apa, este insotita de reducerea continutului de carbon, ca urmare a descompunerii cementitei in straturile metalice din vecinatatea peliculei de oxid, dupa una din reactiile:
Fe3C+1/2O2↔3Fe+CO;
Fe3C+2H2↔3Fe+CH4 ;
Fe3C+ H2O↔Fe+CO+ H2;
Fe3C+CO2↔3Fe+2CO.
Din aceste reactii rezulta ca, marim concentratia in CO si CH4 in gaze echilibrele pot fi deplasate spre stanga. Pe acest principiu se aleg, in practica, atmosferele protectoare sub care se efectueaza tratamentele termice fara oxidare, carburarea sau decarburarea otelurilor.
Decarburarea duce la micsorarea rezistentei mecanice, coborarea limitei de oboseala.
Viteza de coroziune in gaze se micsoreaza prin crearea unei atmosfere inerte si mai ales prin alierea otelului cu diferite elemente se mareste stabilitatea otelului la temperaturi ridicate.
In ceea ce priveste coroziunea chimica a unui aliaj, in oxigen sau aer uscat, in principiu, depinde de afinitatea chimica a componentilor sai fata de oxigen, precum si de comportarea reciproca a oxizilor susceptibili de a se forma. De exemplu in cazul aliajului Fe-Cu, fierul are pentru oxigen o afinitate mult mai mare decat cuprul. Spre deosebire insa de fierul pur, oxidare se produce in adancime, provocand formare unui strat mixt de metal si oxid. Fierul oxidandu-se preferential, metalul ce ramane in stratul mixt se imbogateste in cupru si devin din acest motiv din ce in ce mai rezistent la coroziune. In cazul aliajului Ni-Cr, elementul de aditie este cromul, mult mai oxidabil in raport cu metalul de baza, nichelul. In urma coroziunii stratul superficial al aliajului va saracii in crom, dar va fi protejat ulterior de oxidul de corm, continuu si impermeabil.
|
Politica de confidentialitate |
| Copyright ©
2024 - Toate drepturile rezervate. Toate documentele au caracter informativ cu scop educational. |
Personaje din literatura |
| Baltagul caracterizarea personajelor |
| Caracterizare Alexandru Lapusneanul |
| Caracterizarea lui Gavilescu |
| Caracterizarea personajelor negative din basmul |
Tehnica si mecanica |
| Cuplaje - definitii. notatii. exemple. repere istorice. |
| Actionare macara |
| Reprezentarea si cotarea filetelor |
Geografie |
| Turismul pe terra |
| Vulcanii Și mediul |
| Padurile pe terra si industrializarea lemnului |
| Termeni si conditii |
| Contact |
| Creeaza si tu |