
INFLUENTA CHIMISMULUI APEI DIN CIRCUITUL SECUNDAR ASUPRA COROZIUNII OTELURILOR CARBON
Programul referitor la reglarea chimismului mediului apos din circuitul secundar reprezinta, una din modalitatile cele mai uzitate de imbunatatire a managementului circuitului secundar. In general, inca de la inceputurile reactoristicii nucleare a fost recunoscuta marea importanta a mentinerii corecte a chimismului apei din circuitele de racire ale CNE-urilor. Principalele motive pentru care trebuie respectat cu strictete chimismul apei atat din circuitul primar cat si secundar, au fost urmatoarele: integritatea materialelor; nivelele radiatiei din instalatii; gradul de ingrosare al depunerilor si siguranta in exploatare a centralei nucleare[13].
Optimizarea controlului chimic s-a facut pe baza experientei in operare, a testelor executate in laboratoare, a bazelor de date referitoare la coroziunea materialelor si la cantitatile de produsi eliberati si respectiv depusi ("crud") in regim de operare. Controlul chimic in centralele nucleare include cateva activitati esentiale si anume:
utilizarea unor substante chimice pentru contracararea efectelor nefaste ale produsilor de coroziune generati radiolitic, pentru ajustarea pH-ului la valoarea corespunzatoare la care materialele structurale vor avea viteza minima de coroziune si pentru a compensa variatiile de aciditate rezultate in circuitul secundar
minimizarea concentratiei impuritatilor chimice care pot cataliza degradarea materialelor, a acoperirilor protectoare de oxid si impurificarea agentului de racire.
In general, chimismul apei influenteaza puternic siguranta in functionare a circuitelor de racire din centralele nucleare in urmatoarele moduri:
prin afectarea potentiala a integritatii barierelor care contin radioactivitate, ca de exemplu teaca elementului combustibil si alte materiale din circuitul primar;
prin varierea campurilor de radiatie din afara miezului reactorului, care, la randul lor influenteaza dozele man/rem;
prin formarea unor depuneri care pot cauza micsorarea transferului termic si accelera procesele de coroziune localizata.
Un bun control al chimiei apei poate elimina total sau partial problemele susmentionate, imbunatatind, in consecinta, siguranta in exploatare a instalatiilor nucleare. Din cele aratate mai sus, rezulta ca respectarea stricta a chimismului fluidului care realizeaza transferul de caldura in circuitul secundar, este necesara pentru urmatoarele motive:
v minimizarea coroziunii componentelor aflate in contact cu apa de alimentare si respectiv cu aburul, inclusiv componentele apartinand Generatorului de Abur (GA) aflate pe partea de circuit secundar;
v minimizarea "murdaririi" sistemelor, in special a suprafetelor de transfer termic;
v minimizarea transportului prin circuit a speciilor chimice insolubile rezultate, in special, din procesele de coroziune;
v reducerea la minim a coroziunii materialelor din circuitul secundar in perioadele de revizie sau in decursul opririlor accidentale.
Ca urmare a investigarii chimiei apei si controlului coroziunii in instalatiile nucleare de catre expertii acreditati de Agentia Internationala pentru Energie Atomica (IAEA) de la Viena, au rezultat urmatoarele tematici prezentate sub forma rapoartelor DAWAC (Diagnostics for Water Chemistry and Corrosion Control in Nuclear Power Plants):
monitorarea continua a conditiilor in care se desfasoara procesele chimice, identificarea perturbarilor produse si/sau a tendintelor nefavorabile aparute in regimul chimic al apei, diagnoza cauzelor acestora si anumite recomandari pentru personalul operator;
identificarea si mentinerea sub control a perturbarilor aparute in operarea echipamentelor si gasirea cauzelor variatiilor produse in parametrii chimici ai apei;
crearea unui suport pentru rezolvarea problemelor operationale in ceea ce priveste mentinerea regimului chimic al apei in cadrul domeniului specificat;
prognozarea evolutiei regimului chimic al apei in vederea implementarii unor contramasuri care sa-l optimizeze.
In cadrul managementului chimiei apei in centralele nucleare, in figura 24[13] sunt prezentate sinoptic principalele directii enumerate mai sus.
Respectarea chimismului mediului in circuitele unei centrale nucleare se repercuteaza pozitiv asupra operarii acesteia, o importanta deosebita avand urmatoarele aspecte: imbunatatirea performantei centralei, o utilizare mai eficienta a combustibilului nuclear, o flexibilitate mai mare in operare si o siguranta mai mare in exploatare. Avand in vedere ca controlul coroziunii materialelor si variatia activitatii in circuite depinde de parametrii fizico-chimici ai agentului de racire, o problema foarte importanta o reprezinta monitorarea on-line a chimiei apei si coroziunii.
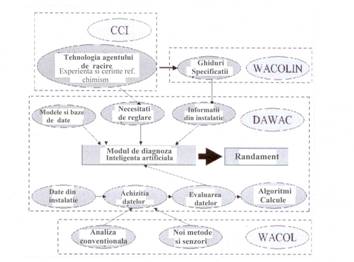
Fig.24[13] Principalele tematici acoperite de DAWAC
Legenda: DAWAC-Tehnologie de Procesare a Datelor si Diagnoza Chimiei Apei si Controlului Coroziunii in PHWR; CCI- interactia teaca element combustibil/agent de racire; WACOL - monitorarea on-line la temperatura inalta a chimiei apei si coroziunii; WACOLIN - investigatii ref.la controlul chimiei apei si la interactiile agentului de racire cu combustibilul si respectiv cu materialele circuitului primar si secundar expuse in reactoarele de putere racite cu apa.
Este recomandabil ca monitorarea chimismului mediului din CNE-uri sa se faca on-line in vederea obtinerii de informatii in decursul tuturor tipurilor de conditii de operare (stare stationara, tranzienti, perioadele de pornire si respectiv de oprire). Intr-un sens mai larg, aceste informatii obtinute in timp real vor conduce la o intelegere mai profunda a comportarii instalatiei in conditiile respective si la performante imbunatatite ale acesteia. Totodata, ele pot fi folosite pentru modelarea matematica a proceselor din instalatiile respective si pentru a mentine acele conditii care sa asigure o coroziune minima a materialelor din instalatie.
Sistemul de achizitie al datelor include datele referitoare la chimismul si radiochimia circuitului secundar, parametrii de operare ai acestuia, ca: temperatura, debitele masice si alte date operationale si termohidraulice precum si metodele, inclusiv senzorii conventionali, utilizati pentru colectarea lor. Modulul referitor la diagnoza - "inteligenta artificiala a chimismului" - este componentul-cheie al chimismului apei si al sistemului expert de control a coroziunii. Baza de cunoastere stocata in modulul de diagnoza va fi capabila sa prezinte prompt anomaliile chimismului, care pot afecta performantele la coroziune ale componentelor sau alti factori de performanta legati de chimismul instalatiei. Aceasta baza de date va furniza informatii despre cauzele posibile ale anomaliilor detectate si recomandari referitoare la contramasurile posibile.
Pentru a evalua starea instalatiei folosind datele de chimia apei, trebuie luate in considerare urmatoarele aspecte: asigurarea parametrilor fizico-chimici ai chimiei apei si concilierea lipsurilor aparute intre informatia necesara si rezultatele masuratorilor.
In centralele nucleare de putere tip PHWR, similare aceleia de la Cernavoda, care produc abur in scopul generarii electricitatii, circuitele de racire sunt construite preponderent din aliaje feroase. In decursul operarii, reactiile de coroziune in mediu apos la temperatura si presiune ridicata fac ca magnetita sau alti compusi ferici sau ferosi sa se acumuleze in aceste circuite, atat sub forma unor filme aderente pe suprafetele metalice cat si ca particule mobile (suspensii). Coroziunea materialelor din care este confectionat circuitul secundar al unei CNE poate fi minimizata, in general, prin selectarea judicioasa a materialelor si printr-un control riguros al chimismului agentului apos care vine in contact cu ele (Fig.25)[13, 35].
Experienta diferitelor centrale nucleare in operare a aratat ca chimia apei are un rol foarte important in mentinerea integritatii componentelor structurale, ceea ce implica necesitatea unui control chimic riguros al mediului apos din cele doua sisteme de transport a caldurii(Fig.26[36]).
|
|
Fig.25[13] Schema principalelor procese implicate in controlul chimismului apei |
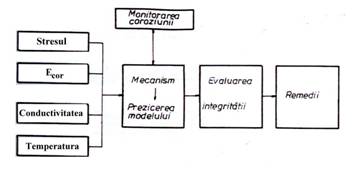
Fig.26[36] Reprezentarea schematica a influentei unor parametri ai chimismului mediului apos asupra monitorarii coroziunii
Principalele obiective ale mentinerii riguroase a chimismului agentului termic in sistemele de transfer ale caldurii (PHTS) sunt [12,36]:
micsorarea coroziunii componentelor si echipamentelor din sistem;
limitarea vitezei de formare a produsilor de coroziune radioactivi;
mentinerea unor viteze mici de coroziune ale componentelor ca si concentratii cat mai reduse de impuritati si produsi de fisiune;
minimizarea transportului activitatii printr-o indepartare eficienta a produsilor de coroziune radioactivi si a produsilor de fisiune solubili;
micsorarea murdaririi suprafetelor de transfer termic printr-un control strict al transportului si respectiv indepartarii produsilor de coroziune insolubili.
Standardizarea procedurilor de achizitie a datelor referitoare la chimismul apei trebuie sa contina obligatoriu urmatoarele date: locul si perioada de prelevare a probei, procedurile de prelevare si instrumentele analitice necesare pentru identificarea si determinarea cantitativa a componentilor chimici si radioactivi, procedurile de calibrare ale instrumentelor si frecventa cu care trebuie facute aceste calibrari, instruirea chimistilor care lucreaza in instalatia respectiva si alcatuirea unei documentatii complete. In acest context a fost elaborata o procedura standard de monitorare a documentelor referitoare la chimismul apei, care cuprinde urmatoarele doua capitole principale [35]:
a) standardizarea procedurilor de achizitie a datelor trebuie sa includa:
locatia, perioada si procedurile de prelevare a probelor;
instrumentele analitice utilizate si calibrarea lor;
documentatia referitoare la instruirea chimistilor si
monitorarea documentatiei.
b) trasabilitatea datelor referitoare la chimismul apei trebuie sa cuprinda:
proceduri standard preluate din documentatie si
monitorarea documentatiei.
Actualizarea specificatiilor referitoare la controlul chimismului apei fiind strans legata de imbunatatirile necesare in instalatiile respective, aceasta actualizare va fi facuta in urmatoarele situatii: ori de cate ori a avut loc un eveniment care a aratat caracterul inadecvat al unor specificatii ale chimismului apei sau in mod regulat, in vederea imbunatatirii permanente a controlului chimic al apei. Principalele motive care au stat la baza actualizarii specificatiilor chimice aplicabile unui eveniment specific, au fost: aparitia de noi procese de coroziune sau a unui nou tip de poluare identificat ca periculos si necesitatea de a optimiza si micsora dozele debit ale radiatiei, impactul ei asupra mediului, riscul de coroziune si degradarile asociate acesteia.
Aceste sisteme de procesare a datelor, diagnoza a chimismului apei si control al coroziunii necesita o aparatura sofisticata, care colecteaza datele din instalatii, referitoare la calitatea agentului de racire din circuite, operatie care este realizata folosind urmatoarele trei canale [35]:
Canalul 1 face monitorarea continua a datelor referitoare la chimismul apei din circuitul primar/secundar;
in Canalul 2 se executa revizia periodica a datelor referitoare la chimismul apei din circuitul primar/secundar folosind datele furnizate de Canalul 1, prelucrate cu programul "ANOMALY";
in Canalul 3 se executa revizia periodica a datelor referitoare la chimismul apei din circuitul primar/secundar folosind datele furnizate de Canalul 1, utilizand, de aceasta data un numar maxim posibil de proceduri de diagnoza.
Principalele date referitoare la chimismul apei din instalatiile PHWR sunt prezentate in tabelul 2[35].
In instalatiile nucleare de putere exista doua metode principale de control ale chimismului apei: prelevarea manuala a probelor, urmata de analiza lor in laborator si monitorarea continua, on-line, a parametrilor fizico-chimici ai apei.
Constatand ca exista anumite discrepante intre datele masurate referitoare la chimia apei si informatiile necesare pentru a stabili corelatiile corespunzatoare intre chimismul apei din instalatie si interactiile dintre materialele respective si apa de racire, s-a considerat util ca o parte din ele sa fie enumerate in tabelul 3[35].
Coroziunea otelurilor carbon in mediu apos la temperatura inalta se desfasoara, in general, conform modelului Potter-Mann, care implica formarea pe suprafetele care se corodeaza a unui strat duplex de produsi de coroziune[8]. Stratul interior este, in general, un oxid mai compact, fin-granulat care creste in directia metalului de baza, ocupand astfel volumul metalului care se corodeaza.
O parte din ionii de Fe2+ difuzeaza prin stratul interior spre interfata oxid/agent de racire, iar daca agentul de racire este deja saturat in ioni de Fe2+, acestia vor tinde sa suprasatureze stratul existent la limita fluidului, provocand precipitarea unui strat de oxid exterior. Magnetita din acest strat exterior este deobicei sub forma de cristale mai grosiere, octaedrice, avand dimensiunea de cativa microni.
Tabelul 2[35]. Principalele tipuri de interactii apa/materiale din PHWR
|
Factorii care influenteaza chimismul apei (date operationale) Factori macroscopici |
1) reducerea dozei debit |
2) integritatea combustibilului |
3) integritatea structurii |
|
pH [6,8-7,2]* * pH la temperatura inalta |
S pH-ul inalt coboara generarea de Co60& Co58 pe supr.combustibilului |
pH-ul inalt stabilizeaza coroziunea |
|
|
Conductivitate [<30mS/cm | |||
|
ECP (nedeterminat |
putine date | ||
Specii radioliticeH2[~2000ppb] O2 [<5ppbH2O2 [<1ppb] |
conc. H2 inalta mareste depunerea de Ni58(Co59) pe supr.combustibilului |
conc. H2 inalta promoveaza absorbtia H2 in Zr |
conc. H2 inalta promoveaza PWSCC |
|
efecte mici in cadrul domeniului |
efecte mici in cadrul domeniului |
efecte mici in cadrul domeniului |
|
|
efecte mici in cadrul domeniului |
efecte mici in cadrul domeniului |
efecte mici in cadrul domeniului |
|
Specii metaliceNi [cca.1ppb]Zn [< 50ppb]** injectie de Zn Li[0,7-2,2 ppm] B[0-2500ppm] |
S promoveaza depuneri groase si coroziunea Zy | ||
|
Zn modereaza depunerea Co60 pe tevi |
putine date |
Zn previne IGSCC |
|
|
putine date ref.efecte propriuzise |
S conc.inalta [Li] promoveaza coroziunea |
putine date ref.efecte propriuzise |
|
|
putine date ref.efecte propriuzise |
S conc.inalta [B] modereaza coroziunea |
putine date ref.efecte propriuzise |
|
RadioactivitateaCo60 FP [Bq/ml] |
S conc.inalta [Co58]cauzeaza doze debit inalte |
S defectele din combustibil cauzeaza [FP] inalte |
S dozele debit inalte obstructioneaza inspectiile & intretinerea |
Legenda: ECP-Potentialul electrochimic de coroziune; FP-produsi de fisiune radioactivi; PWSCC-SCC-ul circuitului primar; -efecte necunoscute ale factorilor respectivi; S-efect cuantificat si mecanism cunoscut; -efect cuantificat, dar mecanism necunoscut; -efectele unor factori cunoscuti, dar necuantificati; - efecte mici.
S-a constatat ca aparitia si propagarea coroziunii localizate in circuitul secundar a fost redusa de circa 10 ori pentru fiecare crestere cu o unitate a pH-ului apei de alimentare, valoarea optima situandu-se in domeniul (9,7
Tabelul 2 Discrepante aparute intre informatiile necesare
si datele existente de chimia apei
|
Informatia necesara pentru a intelege procesele din instalatie |
Datele de chimia apei determinate in instalatii |
Masuri luate pentru a realiza corelatia |
|
Conditii corozive [O2, H2 , H2O2] |
Conc. masurate de [O2, H2] |
Modele teoretice pentru radioliza apei Senzori de O2 la temp.inalta Senzori de ECP |
|
Chimismul apei din crevasa |
Chimismul apei din bloc |
Modele teoretice ale radiolizei apei in crevase Modele teoretice & empirice pentru concentratia de impuritati la varful fisurii |
|
Viteza de propagare a fisurii |
Viteza cresterii fisurii in conditii simulate |
Senzori la temp.inalta ai vitezei cresterii fisurii Modele teoretice & empirice ale vitezei de propagare a fisurii |
|
Specii metalice solubile si insolubile |
Conc.sol.saturate din liniile de prelevare a probelor |
Analiza solubilitatii & depunerii/eliberarii de-a lungul liniilor de prelevare a probelor Senzori de conductivitate la temperatura inalta |
|
pH-ul la temp.inalta |
pH-ul apei racite |
Evaluare teoretica Senzori ai pH-ului la temp.inalta |
|
Proprietatile filmelor de oxid de pe probele prelevate |
Caracterizarea filmului de oxid |
Modele de oxidare teoretica Senzori ai impedantei la temperatura inalta |
In figura 27[10] este ilustrat rolul important al mentinerii pH-ului in acest domeniu in vederea asigurarii unei coroziuni minime a materialelor structurale feroase din circuitul secundar. Avand in vedere faptul ca pentru reglarea pH-ului mediului apos din circuitul secundar pot fi folosite diverse amine, printr-o selectare inteligenta a acestora s-a ajuns ca acestea sa minimizeze nu numai viteza de coroziune a otelurilor carbon, ci sa reduca si coroziunea provocata de curgerea fluidului (Flow Assisted Corrosion)(FAC).
|
|
Fig.27[10] Solubilitatea magnetitei functie de temperatura la diferite pH-uri |
Desi initial, pentru reglarea pH-ului mediului apos din circuitul secundar, a fost folosit asa-numitul tratament cu amine volatile (morfolina si ciclohexilamina) (AVT), ulterior au fost cautate, verificate si atestate si alte amine organice, ca: etanolamina (ETA), dimetilamina (DMA), metil-fenil-amina(MPA), etc. In acest context, in figura 28[36] este prezentata grafic ponderea utilizarii diferitelor amine organice ca agenti de reglare ai pH-ului.
|
|
Fig.28[36] Ponderea utilizarii diverselor substante ca agenti de reglare ai pH-ului |
In ultima vreme, in SUA, in locul tratamentului AVT, a fost folosita numai morfolina la jumatate din unitatile PHWR, iar actualmente, in unele CNE-uri este utilizata monoetanolamina (MEA) in locul morfolinei, ca agent de reglare al pH-ului[36].
Degradarea prin coroziune a componentelor din otel carbon din circuitul secundar al unei CNE PHWR fiind o problema foarte costisitoare pentru industria nucleara, este necesara inspectarea frecventa a acestuia, urmata de reparatii si uneori chiar de inlocuirea completa a unor componente. Avand in vedere ca coroziunea generalizata a otelurilor carbon din acest circuit este actualmente destul de bine controlata, accentul s-a pus pe gasirea unui chimism cat mai adecvat al mediului apos din circuitul secundar, care sa aiba drept rezultat reducerea probabilitatii de producere a coroziunii localizate (IGA, SCC, pitting, coroziune in crevasa, etc), care fiind mai insidioasa, este mult mai periculoasa decat coroziunea generalizata.
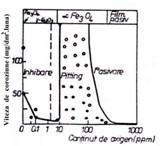
Fig.29[34] Evidentierea tipurilor de coroziune pe care le poate suferi
otelul carbon functie de concentratia de oxigen prezenta in mediul apos
Astfel, o dozare corecta a continutului de oxigen in mediul apos reduce drastic corozivitatea otelului carbon in apa la temperatura inalta (figura 29 [34]), prezenta unei mici cantitati de oxigen in mediu (< 10ppb) fiind asociata cu eliberarea unei cantitati minime de produsi de coroziune in mediu. Minimizarea vitezei de coroziune si a eliberarii de produsi de coroziune in mediu este datorata formarii unui film de oxid protector de magnetita pe suprafata aliajului. In prezenta unor nivele de oxigen mai inalte, magnetita se transforma treptat in hematita neprotectoare, viteza de coroziune devenind concomitent si ea mai inalta.
Deci, o modalitate de micsorare a coroziunii componentelor circuitului secundar consta in utilizarea unui program adecvat de reglare a chimismului mediului apos al acestuia. In consecinta, cercetarile recente in acest domeniu au fost axate, in special, pe intelegerea cauzelor si mecanismelor proceselor de coroziune, factorii decisivi in influentarea lor fiind in primul rand mentinerea unui pH adecvat si, in general, monitorarea riguroasa a tuturor parametrilor fizico-chimici ai mediului din circuitul secundar. Pe baza experientei in operare a circuitelor secundare apartinand unor centrale nucleare din SUA, s-a concluzionat ca procesul coroziv intergranular al unor componente din otel carbon prezente in circuitul secundar al Generatorului de Abur (GA) poate fi micsorat/ evitat prin utilizarea diverselor programe de tratare chimica a apei, inclusiv utilizarea unor amine noi, moderne, care au si proprietati de inhibitori de coroziune (Fig.30[36]).
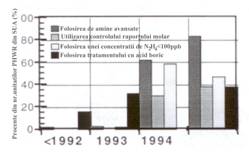
Fig.30[36] Variante de programe de tratare chimica a apei din circuitul secundar aplicabile in CNE-urile din SUA
Dupa cum se observa din fig.30[36], o practica de tratare chimica a apei, utilizata destul de frecvent in CNE-urile din SUA, este controlul raportului molar (MRC). Aceasta practica se bazeaza pe presupunerea ca pH-ul existent in crevase, care influenteaza initierea si cresterea fisurilor, poate fi modificat prin monitorarea raportului dintre concentratia anionilor acizilor tari si respectiv a cationilor bazelor tari, existent in agentul de racire. Ca atare, prima etapa in cadrul acestei metodologii este stabilirea unui chimism cat mai adecvat in crevase. Pentru a atinge acest obiectiv, trebuie luati in considerare toti parametrii care influenteaza coroziunea componentelor feroase din circuitul secundar si in special acei parametri care pot fi determinati practic. Aceasta practica a monitorarii raportului molar este utilizata in 50% din CNE-urile din SUA[36].
Actiunea de imbunatatire continua a calitatii apei de alimentare a circuitului secundar a avut uneori si efecte nedorite in sensul ca o crestere minora in nivelul unei impuritati a cauzat cresteri majore ale pH-ului in crevase. De aici rezulta ca o alta modalitate de reducere a coroziunii in crevasa este controlul echilibrului cation/anion, in vederea evitarii aparitiei unor medii caustice. Aceasta metoda - adoptata de majoritatea unitatilor CNE din SUA si Japonia - avand ca rezultat final reducerea admisiei de sodiu, va conduce implicit la diminuarea eliberarii impuritatilor [12].
Pornind de la premiza ca coroziunea aliajelor feroase este mai intensa in medii oxidante, caustice, neutre si acide si avand in vedere ca procesul de eliberare al impuritatilor din crevasa depinde puternic de valoarea potentialului in circuit deschis (ECP), care nu poate fi masurata direct, s-a mers pe varianta crearii unor conditii redox, care pot fi usor asigurate folosind substante reducatoare ca: hidrazina sau hidrogenul si/sau acolo unde este posibil, oxizi ai metalelor reducatoare, ca oxidul de cupru sau hematita. Tratamentul cu acid boric (BAT) a fost folosit initial pentru a evita aparitia coroziunii "denting" pe tuburile Generatorului de Abur (GA). Ulterior s-a observat ca acesta este benefic si pentru micsorarea probabilitatii de aparitie a coroziunii intergranulare si/sau SCC pe tuburile executate din oteluri carbon si aliaje feroase cu continut ridicat in nichel [36].
Migrarea produsilor de coroziune sub actiunea unui gradient de concentratie va avea loc pana in momentul in care se va stabili un echilibru intre valoarea momentana a concentratiei acestora si concentratia lor la echilibru. Cu alte cuvinte, concentratia la echilibru va fi stabilita cand va fi atinsa o valoare minima a concentratiei lor in circuit. Localizarea acestei valori minime pe curba solubilitatii compusului respectiv depinde de domeniul de temperatura pe care a avut loc procesul si de chimia locala a mediului. Concentratia unui element sau a unui compus intr-un punct al circuitului poate fi determinata folosind relatiile aferente vitezelor de dizolvare, de precipitare si respectiv de eliberare prin coroziune.
2.Rezultate experimentale proprii
2.1.Investigarea prin gravimetrie a caracteristicilor filmelor formate pe probele de otel carbon expuse in solutii aditivate cu diverse amine
Pentru a compara eficienta diverselor amine utilizate ca substante regulatoare de pH in mediul apos specific circuitului secundar, au fost executate autoclavizari la parametrii de operare, atat in mediul specific circuitului secundar - apa demineralizata tratata cu morfolina, ciclohexilamina si hidrat de hidrazina (AVT + N2H4) - cat si in urmatoarele alte variante de medii care asigura valori identice ale pH-ului:
apa demineralizata tratata cu ciclohexilamina si monoetanolamina (ETA) in locul morfolinei;
apa demineralizata tratata cu morfolina si trietanolamina (TEA) si respectiv
apa demineralizata tratata cu morfolina si trietilamina (TREA).
Tuturor acestor solutii li s-a adaugat concentratia corespunzatoare de hidrazina pentru a asigura o concentratie de oxigen sub 10ppb.
Pe baza evaluarilor gravimetrice ale probelor filmate dupa diferite perioade de autoclavizare si a efectuarii ulterioare a operatiilor de descalare pe aceste probe, au fost determinate urmatoarele caracteristici cinetice: pierderea in greutate datorata coroziunii, viteza globala de coroziune, cantitatea de produsi de coroziune total formati cu defalcarea ulterioara in produsi aderenti si respectiv eliberati, viteza de eliberare a produsilor de coroziune (sub forma de compusi) si respectiv viteza de eliberare a metalului propriu-zis in solutie. Avand in vedere ca in aceste conditii de mediu, probele sufera o coroziune generalizata, aceste caracteristici au fost reprezentate functie de timp, obtinandu-se astfel ecuatiile si curbele cinetice aferente coroziunii otelului carbon.
Pentru caracterizarea filmelor superficiale formate pe probe, au fost folosite urmatoarele metode: metalografia - pentru evidentierea uniformitatii si grosimii filmelor si metoda spectroscopiei impedantei electrochimice (EIS). In figura 31[39] sunt prezentate curbele corespunzatoare variatiei vitezei de eliberare a metalului in solutiile AVT clasice si respectiv in varianta modificata cu monoetanolamina [AVT]m, iar in figura 32[39] sunt prezentate curbele aferente variatiei vitezelor de coroziune ale probelor autoclavizate in aceleasi solutii.

Fig.31[39] Variatia vitezei de eliberare a metalului in solutiile tratate
cu AVT si respectiv in varianta modificata cu monoetanolamina
Din pozitionarea curbelor pe aceste grafice se observa ca viteza de coroziune minima si respectiv concentratiile cele mai mici de metal eliberate in solutie au fost gasite in solutiile al caror pH a fost reglat cu AVT.
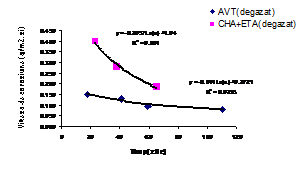
Fig.32[39]Variatia vitezelor de coroziune a probelor de otel carbon autoclavizate in solutiile tratate clasic cu AVT si respectiv in varianta modificata cu monoetanolamina [AVT]m
Utilizarea monoetanolaminei in locul morfolinei conduce la viteze de coroziune ceva mai mari, dar care - in valori absolute - nu reprezinta un pericol real pentru componentele din otel carbon. Deci, monoetanolamina poate fi utilizata ca aditiv pentru reglarea pH-ului impreuna cu ciclohexilamina, fara a afecta sensibil comportarea la coroziune a otelurilor carbon. Alte remarci care se desprind din examinarea pozitionarii curbelor cinetice trasate pe baza datelor gravimetrice, sunt urmatoarele[40]:
concentratia produsilor total formati pe probele autoclavizate in solutia care a continut monoetanolamina este mai mare decat concentratia acelora formati pe probele autoclavizate in solutia AVT, regula care se respecta si in cazul produsilor aderenti;
curbele aferente cantitatilor de produsi eliberati si respectiv vitezelor de eliberare a produsilor de coroziune fiind situate in partea inferioara a graficelor, corespund, unor valori foarte mici, in partea cea mai de jos fiind plasata curba aferenta autoclavizarilor executate in solutia AVT clasica. Vitezele de eliberare ale metalului in solutie variind foarte putin in cazul celor doua tipuri de autoclavizari, confirma faptul ca straturile de produsi de coroziune aderenti constituie o bariera relativ compacta si protectoare in calea accesului ionilor din solutie la metalul de baza.
In continuare, vor fi prezentate concluziile trase pe baza datelor gravimetrice obtinute in urma autoclavizarilor efectuate in solutia AVT clasica si in alte doua variante de solutii, in care, in locul ciclohexilaminei, au fost folosite trietanolamina (TEA) si trietilamina (TREA):
curbele aferente variatiei in timp a vitezelor de coroziune (figura 33[41]), a vitezei de eliberare a produsilor de coroziune si respectiv a concentratiei metalului eliberat in solutie, sunt functii puteri descrescatoare de forma: y = kx-n. Diferentele intre valorile constantelor si exponentilor din functiile putere si amplasarea comparativa a celor trei curbe pledeaza pentru ideea ca vitezele de coroziune si respectiv cele de eliberare ale produsilor de coroziune si ale metalului sunt mai mari in cazul probelor autoclavizate in solutia AVT, in timp ce in celelalte doua tipuri de solutii, au rezultat viteze mult mai mici, cele mai mici corespunzand probelor autoclavizate in solutia aditivata cu TEA.
curbele aferente variatiei in timp a cantitatii de produsi de coroziune total formati, aderenti si respectiv eliberati(figura 34[41]) sunt functii logaritmice de forma: y = k1ln(x) - k2. Amplasarea comparativa a celor trei curbe si implicit valorile constantelor si ale exponentilor pledeaza pentru ideea ca cele mai mari cantitati de produsi de coroziune total formati, aderenti si eliberati au luat nastere in urma autoclavizarilor executate in solutia AVT, iar cele mai mici - in urma autoclavizarilor executate in solutia aditivata cu TEA;
curbele pierderilor in greutate corespund unor functii puteri de forma: y = kxn si sunt pozitionate astfel: in partea superioara a figurii 35[41] este curba aferenta probelor filmate in solutia AVT, in timp ce in partea inferioara sunt plasate, practic suprapuse, curbele aferente otelurilor filmate in solutiile aditivate cu TREA si respectiv TEA.
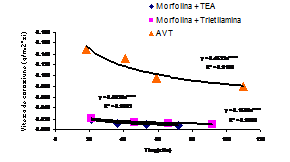
Fig.33[41]. Variatia vitezelor de coroziune ale probelor filmate in solutia clasica AVT si respectiv in solutiile aditivate cu TEA si TREA
Viteza de eliberare a metalului in solutie fiind corelata cu concentratia ionilor de fier gasiti in solutiile prelevate din autoclava dupa diferite perioade de autoclavizare, ea poate fi determinata printr-o metoda analitica oarecare (ex.spectrofotometrie sau spectrometrie de masa). In general, concentratiile ionilor de fier determinate in solutiile prelevate dupa diferite perioade de autoclavizare in cele trei tipuri de solutii dezoxigenate, fiind sub 50ppb, confirma rezultatele obtinute in urma prelucrarii datelor gravimetrice [38,41].
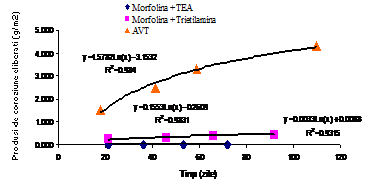
Fig.34[41] Variatia in timp a cantitatii de produsi de coroziune eliberati de probele filmate in solutia clasica AVT si in cele aditivate cu TEA si TREA

Fig.35[41] Variatia in timp a pierderilor in greutate aferente probelor
filmate in cele trei tipuri de solutii
Din cele aratate mai sus, reiese ca reglarea cu AVT a pH-ului solutiei in jurul valorii 9,7 minimizeaza drastic viteza de coroziune a otelului carbon, iar hidrazina consumand oxigenul conform reactiilor (1) si (2), reduce cu atat mai mult viteza de coroziune a otelurilor in solutiile respective, conform reactiilor de mai jos:
N2H4 + O2 --> N2 + 2 H2O (1)
N2H4 + 6 Fe2O3 --> 4 Fe3O4 + N2 + 2H2O (2)
De aceea, in centralele nucleare se practica o degazare intensa a agentului termic care circula prin instalatiile confectionate din otel carbon, fiind indicata folosirea ambelor tipuri de degazari: mecanica si chimica, aplicate consecutiv. Se stie ca in absenta oxigenului, aliajele feroase - cum este de exmplu otelul carbon - formeaza filme subtiri de Fe3O4 - magnetita, care se mai poate scrie FeO Fe2O3. Acest film, desi reprezinta el insusi un produs de coroziune, protejeaza substratul metalic de coroziunea ulterioara.
2.2. Investigarea filmelor de pe probele de otel carbon expuse in solutiile aditivate cu diverse amine folosind metoda impedantei
Rezultatele masuratorilor electrochimice de impedanta (EIS), sunt prezentate sub forma curbelor specifice - a unghiurilor de faza, Nyquist Bode - si a circuitelor echivalente interfetelor respective[39, 41].
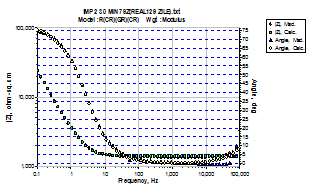
![]()
Fig.36[41] Curba Bode, a unghiului de faza si circuitul echivalent aferent unui otel carbon autoclavizat 130 zile in solutia AVT clasica, dezoxigenata
In urma examinarii prin metoda impedantei(EIS) a otelurilor carbon autoclavizate in solutia AVT clasica, dezoxigenata, o perioada de circa 130 zile, s-a constatat ca filmele lor superficiale sunt relativ uniforme ca grosime si putin poroase (fig.36[41]). Fitand rezultatele, a fost obtinuta o concordanta foarte buna intre curbele specifice masuratorilor de impedanta si fitarile teoretice, circuitul echivalent corespunzator acestor filme fiind R(CR)(QR)(CR).
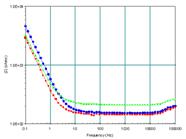
Examinand curbele Bode prezentate in fig.37a,b[41] aferente filmelor formate dupa diferite perioade de autoclavizare in solutia AVT degazata, probe mentinute in electrolit 0,5 si respectiv 24 ore anterior executarii masuratorilor de impedanta, s-a constatat o suprapunere aproape integrala a curbelor, in special in domeniul frecventelor medii si inalte; in domeniul frecventelor mici, ( 1Hz), s-a constat aparitia unei dispersii mici a curbelor, pe o decada a impedantei.
 a)
a)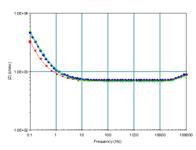 b)
b)
Fig.37a,b[41] Curbele Bode aferente unui otel carbon autoclavizat in solutia AVT degazata: 79, 110 si 129 zile (a - 0,5h; b- 24h in electrolit)
Aceasta suprapunere aproape integrala a curbelor EIS este confirmata si de circuitele echivalente corespunzatoare acestor curbe, care, pentru perioade mai scurte de autoclavizare, au fost de tipul: R(CR)(QR)(CR), pentru ca perioadei de 130 zile sa-i corespunda un alt circuit, un pic diferit si anume: R[(CR(QR))(CR)].
Examinand tipurile si valorile componentelor microcircuitelor echivalente corespunzatoare substratelor exterioare, constatam ca acestea au devenit din preponderent rezistive in preponderent capacitive pe masura cresterii perioadei de autoclavizare, caracteristica care sustine accentuarea caracterului protector al filmelor concomitent cu ingrosarea lor.
Curbele Bode corespunzatoare probelor testate perioade de timp mai scurte (sub 40 zile) si mentinute in electrolit 0,5 si respectiv 24 ore, reflecta existenta unei anumite porozitati a filmelor superficiale, fapt evidentiat de scaderea valorilor impedantei cu cresterea perioadei de mentinere a probelor filmate in electrolit.
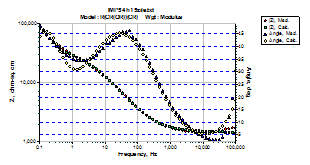
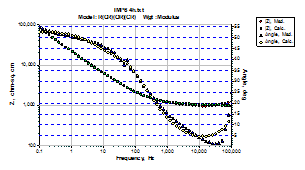
Examinand curbele specifice impedantei aferente probelor de otel carbon autoclavizate diferite perioade de timp in solutia degazata tip (AVT)m care a continut ciclohexilamina (CHA) si monoetanolamina (ETA) in locul morfolinei, s-a constatat ca in cazul otelului carbon autoclavizat 15 zile in solutia (AVT)m, curba unghiului de faza prezinta doua minime distincte, care, concomitent cu prelungirea perioadei de autoclavizare, s-au comasat intr-unul singur (fig.38a, b [39]).
Suprapunand curbele Bode aferente otelurilor carbon autoclavizate diferite perioade de timp in solutia continand monoetanolamina[AVT]m, se observa o dispersie mai mare a curbelor Bode in domeniul frecventelor mici si medii, care se estompeaza pe masura cresterii perioadelor de autoclavizare (fig.39[39]). Faptul ca toate circuitele echivalente aferente probelor autoclavizate diferite perioade de timp in solutia degazata continand monoetanolamina, au apartinut tipului R(CR)(QR)(CR), denota similitudinea caracteristicilor filmelor superficiale formate dupa diferite perioade de autoclavizare.
Comparand in figura 40a,b[39] curbele EIS aferente unor probe autoclavizate perioade identice in cele doua solutii degazate care au diferit printr-unul din componenti, se observa ca dupa 24 ore de mentinere in electrolit a probelor, filmul format in cea de-a doua solutie are o impedanta totala ceva mai mare decat omologul lui format pe proba autoclavizata in solutia clasica AVT.
 a)
a)
 b)
b)
Fig.38a,b[39] Curbele Bode si ale unghiurilor de faza aferente otelurilor autoclavizate in solutia degazata tip (AVT)m : a)-15 zile; b)- 65 zile
|
|
Fig.39[39] Curbele Bode aferente probelor autoclavizate in solutia dezoxigenata continand monoetanolamina : ● 15 zile; ♦ 38zile; ▲ 65 zile |
Aceasta amplasare a curbelor semnifica faptul ca filmele formate pe probele autoclavizate in aceasta solutie aditivata cu monoetanolamina au proprietati ceva mai protectoare fata de metalul de baza comparativ cu filmele formate in solutia clasica AVT dupa perioade identice de autoclavizare.
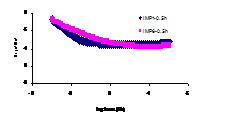 a)
a)
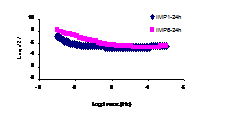 b)
b)
Fig.17a, b[39] Curbele Bode aferente probelor de otel carbon autoclavizate 70 zile in urmatoarele solutii: AVT clasic si [AVT]m
Referitor la caracteristicile filmelor formate in tipurile de solutii susmentionate, se remarca urmatoarele:
- curbele Bode corespunzatoare variatiei impedantei filmelor formate pe otelurile autoclavizate in solutia AVT clasica 25, 77 si 130 zile, inregistrate dupa 24h de mentinere in electrolit a probelor, sunt relativ apropiate, in special in domeniul frecventelor medii si inalte(fig.41[41]). Deplasarea paralela a curbelor Bode in domeniul frecventelor medii a fost atribuita unei porozitati relative a filmelor formate post-autoclavizare, porozitate datorata patrunderii unor ioni ai electrolitului in oxizii de fier relativ porosi [42];
- utilizarea trietilaminei in locul ciclohexilaminei pentru reglarea pH-ului mediului apos din autoclava la valoarea de 9,7, a condus la formarea unor filme compacte si relativ protectoare in cazul autoclavizarilor care au durat perioade mai lungi de 45 zile (fig.42[41]). Curbele specifice EIS si circuitele echivalente corespunzatoare indica o tranzitie de la tipul de circuit R(CR(QR)(QR)) - aferent filmului creat dupa 21 zile de autoclavizare - la tipul R(CR(QR)) - aferent filmului format dupa 72 zile de autoclavizare, pledand pentru ideea cresterii gradului de compactare al filmelor superficiale concomitent cu cresterea perioadei de autoclavizare;
- curbele Bode aferente filmelor formate pe probele autoclavizate in solutia al carei pH a fost reglat cu morfolina si trietanolamina, mentinute in electrolit 0,5h, sunt practic suprapuse, impedanta totala variind intre 103 si 1.104W.cm2 - (fig.43[41]), o slaba departajare a curbelor aparand doar intre curbele unghiurilor de faza si Nyquist.
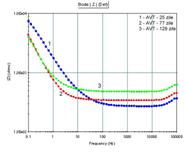
Fig.41[41] Curbele Bode aferente filmelor formate pe probele autoclavizate in solutie AVT urmatoarele perioade: 25 zile(1), 77 zile(2) si 129 zile (3)
(24h mentinere in electrolit)
Comparand caracteristicile filmelor formate dupa 20 zile de autoclavizare in cele trei tipuri de solutii, s-a constatat ca filmele cele mai protectoare s-au format pe probele de otel carbon expuse in solutiile continand trietanolamina si trietilamina (fig.44a, b[41]).
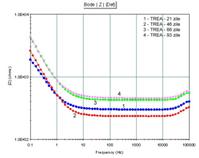
Fig.42[41] Curbele Bode aferente probelor autoclavizate in solutia continand trietilamina urmatoarele perioade: 21 zile (1), 46 zile (2), 66 zile(3) si
93 zile(4) (0,5h mentinere in electrolit)
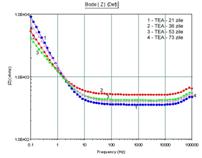
Fig.43[ Curbele Bode aferente otelurilor autoclavizate in solutia continand trietanolamina urmatoarele perioade de timp:
21 zile(1), 36 zile(2), 53 zile(3) si 73 zile(4) (0,5h in electrolit)
Mentinand 24 ore in electrolit probele autoclavizate circa 20 zile in cele trei tipuri de solutii, s-a remarcat faptul ca valoarea impedantei la frecvente mici a fost maxima in cazul filmelor formate pe probele autoclavizate in solutia continand AVT, in timp ce celelalte doua tipuri de filme create in solutiile continand TEA si TREA si-au pastrat practic neschimbate impedantele. Aceasta inversiune demonstreaza inca o data porozitatea mai accentuata a filmelor create in solutia AVT comparativ cu filmele create in celelalte tipuri de solutii, dupa o perioada scurta de autoclavizare.
|
|
|
|
Fig. 44a, b[41] Curbele Bode aferente filmelor formate pe otelul carbon autoclavizate 20 zile(a) si respectiv 70 zile(b) in solutiile continand AVT (1), trietanolamina(TEA)(2) si trietilamina(TREA)(3) (24h in electrolit) |
|
Examinand graficul din figura 44b, in care sunt suprapuse curbele Bode corespunzatoare filmelor formate pe probele autoclavizate 70 zile in cele trei tipuri de solutii, mentinute 24h in electrolit, constatam ca cele trei curbe Bode sunt relativ apropiate si paralele pe intreg domeniul de frecventa (10-3 105)Hz. Aceasta amplasare a lor pe grafic pledeaza pentru ideea formarii dupa o perioada mai indelungata de autoclavizare a unor filme compacte si aproape la fel de protectoare fata de metalul de baza in toate cele trei tipuri de solutii, concluzie sustinuta si de similitudinea circuitelor echivalente aferente lor.
2.3.Rezultatele investigarii prin SEM a filmelor formate pe probele de otel carbon autoclavizate in solutii continand diverse amine
Investigatiilor topografice efectuate prin microscopie electronica de baleiaj (SEM) le-au fost supuse doua tipuri de filme: cele formate pe probele de otel carbon autoclavizate perioade minime (cca.20 zile) si respectiv maxime de timp (cca.70 zile) in cele trei tipuri de solutii.
Astfel, filmele formate pe probele autoclavizate in solutia AVT atat 25zile cat si 77 zile, examinate la mariri mici (x500, x1500), se prezinta ca filme cristaline, duplex (figura 45a[41]), formate din cristale romboiedrice de diferite dimensiuni, intre care apar cristale mai mici, care incep sa formeze aglomerari sub forma de ciorchine (figura 45b). In spectrele acestor cristale obtinute prin analiza folosind electroni secundari (EDS) au fost identificate urmatoarele elemente pe suprafata filmului: Fe, Mn, O, Si (figura 46[41]).
Pe suprafata probei testate 21zile in solutia continand trietilamina (TREA), au fost identificate doua tipuri de zone: una mai inchisa la culoare, care contine cristale mai mari si mai rare si o alta care contine cristale mai mici si mai dese. Zona mai intunecata, examinata la o marire mai mare (x21400) releva prezenta unor cristale poligonale mai mari, relativ dispersate, printre care se disting in substratul inferior cristale mai mici.
In schimb, in zona mai alba, apare acelasi tip de cristale poligonale, avand, insa, marimi mai mici; printre acestea, apar aglomerate sub forma de ciorchine de cristale mai mici. Pe suprafata filmului format pe proba autoclavizata timp de 93 zile in solutia continand TREA, se observa aparitia unei dare relativ intunecate pe care exista foarte putine cristale, care difera net de restul suprafetei in care exista cristale foarte dese (figura 47a); in figura 47b este prezentat la o marire mai mare aspectul zonei in care au existat cristale putine; in spectrele acestor cristale au fost identificate urmatoarele elemente: Fe, Cu, Mn, O, C, Si, folosind analiza EDS.
Filmele superficiale formate pe probele de otel carbon autoclavizate 36 zile in solutia continand trietanolamina (TEA) se prezinta ca un invelis uniform de cristale partial suprapuse unele peste altele (figura 48a); o zona de pe acest film, examinata la marirea de 21400, este prezentata in figura 48b. Totodata, imaginile SEM pledeaza pentru faptul ca, simultan cu cresterea perioadei de autoclavizare, dimensiunea cristalelor s-a marit.
|
|
|
|
Fig.22a,b[41] Imagini SEM ale filmului format pe o proba autoclavizata 77 zile in solutie AVT la urmatoarele mariri: (a) (x1500) si (b)( x21400) |
|
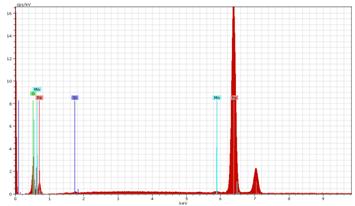
Fig.23[41] Spectrul EDS al filmului format pe o proba autoclavizata 77 zile
in solutie AVT(x15000)
|
|
|
|
Fig.24a,b[41] Imagini SEM ale filmului format pe o proba autoclavizata 93 de zile in solutie TREA la urmatoarele mariri: (a) (x500) si (b)( x1500) |
|
|
|
|
|
Fig.25a,b[41] Imagini SEM ale filmului de pe un otel autoclavizat 72 zile in solutia continand trietanolamina la urmatoarele mariri: (a) (x1500) si (b)( x21400) |
|
2.4.Rezultatele investigarii prin microscopie metalografica a filmelor formate pe probele de otel carbon expuse in solutii aditivate cu diverse amine
In vederea evidentierii grosimii si uniformitatii filmelor formate post-autoclavizare in diferite medii, acestea au fost examinate prin microscopie metalografica, marirea folosita, in general, fiind (x500). Examinand micrografiile acestor probe, am desprins urmatoarele concluzii:
Grosimea filmelor de pe otelurile carbon filmate in solutia AVT clasica a variat intre 1 si 5mm, pentru perioade mergand de la 25 la 129 zile (figura 26a,b,c). In cazul probelor expuse 25 zile in solutia AVT, se observa o neuniformitate a grosimii oxidului, care se ingroasa si devine ceva mai uniform prin expunerea ulterioara in solutia de autoclavizare.
|
|
Fig.26 a, b, c Micrografiile otelurilor filmate in AVT: 25(a), 77(b) si 129 zile(c) (x500) |
|
|
|
|
|
|
|
Fig.27a,b,c,d Micrografiile probelor expuse in solutia continand trietilamina (TREA): 21 zile(a), 46 zile(b), 66 zile(c) si 93 zile(d) (x500) |
|
|
|
|
|
|
|
|
Pe probele filmate perioade variind intre 21 si 93 zile in solutia continand trietilamina s-au obtinut filme de (1,2 ÷4,5)mm (figura 27a, b, c, d).
|
|
Fig.28a,b,c,d Micrografiile probelor expuse in solutia continand trietanolamina (TEA): 21 (a), 36 (b), 53 (c) si 72 zile(d) (x500) |
|
|
|
|
|
|
|
|
c) Probele filmate in solutia continand TEA
Grosimea filmelor formate pe probele autoclavizate in solutia continand trietanolamina (TEA), a variat intre 1,4 si 4mm, pentru perioade variind intre 21 si 72 zile(figura 28a,b,c,d). In cazul probelor autoclavizate maxim 40 zile in aceasta solutie, se observa formarea unor oxizi foarte subtiri, relativi neuniformi ca grosime, grosimea maxima a lor fiind de 2mm. In urma autoclavizarilor ulterioare, oxizii s-au ingrosat atingand pe majoritatea sectiunii cca.4mm. In general, oxizii formati in urma autoclavizarii in solutia continand TEA se prezinta mult mai uniformi ca grosime decat cei formati in solutia AVT si in cea continand TREA.
3. Influenta chimismului mediului asupra mecanismului coroziunii otelurilor carbon
In figura 29[51] este prezentat schematic oxidul format pe suprafetele feeder-ilor din otel carbon, in decursul exploatarii acestora intr-un mediu apos clasic tratat cu AVT.
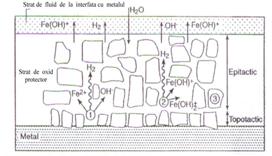
Fig.29[51] Reprezentarea schematica a oxidului format pe suprafetele din otel carbon mentinute intr-un fluid dezoxigenat tratat cu AVT
In antiteza, in figura 30[23], este prezentat schematic oxidul format pe suprafeele feeder-ilor in decursul exploatarii acestora intr-un mediu apos clasic, oxigenat, aditivat cu AVT.
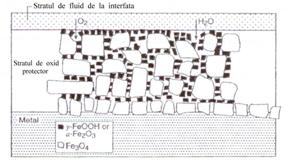
Fig.30[51] Reprezentarea schematica a oxidului format pe otelul carbon la interfata cu un mediu apos tratat cu AVT, cu continut inalt de oxigen
Aceasta comportare a probelor de otel carbon este explicabila pornind de la premiza ca aliajele feroase, cum este si otelul carbon, contin initial fier in stare elementara sau in starea de valenta "0". Odata ce coroziunea incepe, fierul incepe sa piarda electroni, oxidandu-se si dand in prima instanta ionul Fe+ sau Fe (I), care este foarte instabil. In consecinta, oxidarea continua, rezultand ionul Fe2+ sau Fe (II), care devine un component al produsilor de coroziune din apa. O parte din produsii reactiilor de coroziune sunt incorporati in filmele superficiale de oxizi, compuse deobicei din Fe3O4, iar o alta parte din produsii de coroziune sunt eliberati ca specii solubile. Aceste specii solubile sunt, probabil, hidroxizi ferosi sau alte specii chimice feroase, care pot fi usor coordinate cu ajutorul substantelor antiscala.
Cand produsii de coroziune "proaspeti"(proaspat eliberati) sunt expusi in conditii relativ oxidante, oxidarea lor are loc rapid, ionul Fe2+ fiind convertit la ionul feric sau Fe(III). Reducerea suspensiilor care contin Fe(III) la speciile solubile care contin Fe(II), are loc foarte lent in sistemele dezaerate, din cauza pH-ului inalt si a temperaturii existente. Deci, in cazul autoclavizarii probelor de otel carbon in solutia AVT dezoxigenata, probabilitatea de formare a ionilor Fe2+ prin reducerea ionilor Fe3+ este foarte redusa. In plus, avand in vedere ca ionii Fe2+ se oxideaza foarte rapid in apele cu pH inalt, care contin oxigen, prezenta lor in mediu constituie o indicatie a coroziunii active.
Datele cinetice, electrochimice si caracteristicile filmelor superficiale obtinute prin microscopie metalografica si SEM, aferente probelor autoclavizate in solutii avand pH-uri identice, aditivate cu morfolina si ciclohexilamina (AVT), trietilamina (TREA) si respectiv trietanolamina (TEA), au evidentiat faptul ca eficienta pasivarii a fost ceva mai mare in cazul folosirii trietanolaminei comparativ cu trietilamina. Explicatia diferentei de eficienta dintre cele doua amine folosite pentru reglarea pH-ului, care sunt in acelasi timp si inhibitori ai coroziunii otelurilor carbon in medii apoase, rezida in faptul ca TEA - avand in plus trei grupari hidrofile -OH cu caracter polar -, se adsoarbe mai usor pe suprafetele probelor acoperite cu oxi-hidroxizi si respectiv oxizi de fier. Ulterior, trietanolamina adsorbita deplaseaza mai usor decat trietilamina moleculele de apa de pe suprafata filmului exterior, formand diversi complecsi cu oxizii de fier superficiali. Acest proces conduce, in final, la diminuarea atacului coroziv al ionilor din solutie.
In general, intre amine si produsii de coroziune intermediari se formeaza legaturi de hidrogen, ca de exemplu compusul adsorbit [Fe(OH)ads].
Desi adsorbtia TEA si TREA datorata crearii unor legaturi de hidrogen cu [Fe(OH)ads] va aduce o mica contributie la inhibarea coroziunii, va rezulta, totusi, o aderenta net diferita a acestor doi inhibitori pe filmul superficial comparativ cu cea pe substratul metalic. Straturile de amine astfel create, suprapuse peste oxizi si legate de ei prin legaturi de hidrogen, vor conduce la cresterea gradului de compactare a filmelor superficiale, formand astfel un scut protector, eficient in calea atacului corodentilor din solutie asupra substratului metalic.
In lumina teoriei QSAR, un bun inhibitor tip amina trebuie sa contina:
- o molecula mare care sa fie solubila in apa;
- un numar cat mai mare de atomi donori de azot si
- cat mai multe grupari (>NH).
In figura 31 sunt prezentate doua mecanisme de adsorbtie ale aminelor: prin chemisorbtie pe suprafata metalului si prin intermediul formarii unor legaturi de hidrogen cu filmul superficial pasiv[14, 15]. Avand in vedere ca unele amine utilizate ca substante regulatoare ale pH-ului mediului apos din circuitul secundar se comporta si ca inhibitori ai coroziunii otelurilor carbon in mediile respective, in continuare vor fi prezentate cateva consideratii preluate din literatura referitoare la influenta si implicit mecanismul de actiune al acestor substante asupra coroziunii otelurilor carbon expuse in asemenea medii.
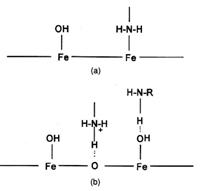
Fig.31[44] Ilustrarea mecanismelor de adsorbtie ale aminelor prin:
(a) chemisorbtie pe suprafata metalului si (b) legarea aminei prin punti de hidrogen de filmul superficial
Radovici[45] a clasificat inhibitorii in urmatoarele trei categorii functie de influenta temperaturii asupra eficientei lor, astfel:
a) inhibitori a caror eficienta (IE) scade cu cresterea temperaturii. In acest caz, concomitent cu cresterea temperaturii, valoarea energiei lor aparente de activare (Ea) in solutiile continand un inhibitor va deveni mai mare decat cea din solutia neinhibata;
b) inhibitori a caror eficienta nu variaza cu temperatura si implicit si energia lor de activare nu variaza cand se lucreaza la diferite temperaturi, in solutii neinhibate sau inhibate;
c) inhibitori a caror eficienta creste cu cresterea temperaturii; in cazul lor, concomitent cu cresterea temperaturii, valoarea energiei de activare (Ea) masurata in solutia inhibata va fi mai mica decat cea aferenta solutiei neinhibate.
Cresterea eficientei inhibitorilor cu marirea temperaturii este datorata unei interactii specifice intre fierul existent in filmul superficial si inhibitor. Valoarea mai coborata a energiei de activare a procesului care are loc in prezenta inhibitorului este atribuita chemisorbtiei, in timp ce in cazul opus, ea este atribuita adsorbtiei fizice.
Ivanov[46] a confirmat cele de mai sus, aratand ca cresterea eficientei inhibarii cu marirea temperaturii indica o schimbare in natura adsorbtiei; astfel, la temperaturi mai coborate, inhibitorii se adsorb fizic, in timp ce chemisorbtia este favorizata de cresterea temperaturii. Acelasi fenomen a fost explicat de alti cercetatori ca fiind datorat imbunatatirii calitatilor acoperirilor superficiale datorita participarii inhibitorului la formarea unui nou film superficial. Astfel, in cazul aparitiei unui alt grad de acoperire, difuzia prin filmul superficial care contine inhibitorul si produsii de coroziune devine etapa determinanta a vitezei dizolvarii metalului.
In general, existenta unei adsorbtii fizice necesita prezenta atat a unei suprafete metalice incarcata electric cat si a unor specii incarcate electric in solutie. Procesul de chemisorbtie implica o disproportionare a sarcinilor incarcate electric sau un transfer de sarcina de la moleculele inhibitorilor la suprafata metalului pentru a forma legaturi coordinative. Acest lucru este posibil in cazul unor suprafete incarcate atat pozitiv cat si negativ. Pentru aceasta este necesara prezenta unui metal de tranzitie avand orbitali liberi, ai caror electroni au energii mici si pe de alta parte a unui inhibitor avand electroni relativ slab legati sau heteroatomi avand o pereche de electroni liberi. Totusi, avand in vedere ca inhibitorii pe care i-am trecut in revista au fost, in general, baze organice, se poate presupune ca acestia se protoneaza in mediu acid, afectand, in special, atomul de azot din inelul imidazolic; in acest fel inhibitorii devin cationi aflati in echilibru cu forma moleculara initiala.
In cazul existentei unui strat de adsorbtie, eficienta inhibitorului depinde, pe de o parte, de taria fortelor de legatura cu suprafetele metalice si pe de alta parte de natura interactiilor existente in filmul superficial. In lumina celor aratate mai sus, functie de modalitatea de actiune asupra substratului metalic, inhibitorii de coroziune pot fi categorisiti astfel:
inhibitori care actioneaza printr-un mecanism electrochimic - utilizand in principal reactiile catodice sau anodice sau ambele tipuri -;
inhibitori care actioneaza prin formarea unor straturi de compusi superficiali, care vor constitui niste bariere intre mediul apos din circuitul respectiv si metalul de baza sau
inhibitori care combina cele doua mecanisme.
In plus, inhibitorii care poseda electroni p din abundenta si perechi de electroni neparticipanti - apartinand atomilor de N, O, X(halogen) - pot interactiona mai usor cu orbitalii "d" ai fierului, formand un film protector de magnetita.
Eficienta inhibitorilor, desi nu depinde explicit de perioada de timp in care actioneaza inhibitorul, ea depinde implicit de aceasta prin intermediul celor doua viteze de coroziune. Produsii de coroziune care iau nastere pe parcursul procesului de autoclavizare pot avea doua tipuri de efecte asupra vitezei de coroziune initiale, incetinind-o sau marind-o prin catalizarea altor procese de coroziune secundare.
Dupa cum se stie, inhibitorii de coroziune pot contine grupari functionale hidrofile si respectiv hidrofobe. In prezenta suprafetelor umede ale probelor, este foarte probabil ca ambele componente ale sistemului - oxidul superficial de pe proba si apa - sa atraga gruparile hidrofile. Diverse studii au aratat ca solutiile dispersabile de inhibitori, - tip emulsii stabile -, in care inhibitorul se afla intr-o concentratie mai mare sau cel putin egala cu concentratia micelara critica (CMC), sunt mai eficiente decat solutiile complet solubile in care concentratia inhibitorului este sub CMC[47].
Se mai stie, de asemenea, ca variatii in compozitia chimica a inhibitorilor pot atrage dupa ele mari schimbari in performantele acestora. De aceea, in consecinta, s-au efectuat multe studii care au avut ca obiect corelarea structurii moleculare a diferitilor inhibitori cu eficienta lor[45-47]. Cand inhibitorul de coroziune se afla in imediata vecinatate a suprafetei metalului, este important de determinat care grupari functionale se vor lega de metal, taria acestor legaturi, care grupari functionale contribuie la formarea filmelor superficiale si modul in care noile legaturi chimice pot afecta rezistenta acestui film.
Unii cercetatori au atribuit adsorbtia marita a cationilor organici atractiei electrostatice care apare intre anionii si cationii coadsorbiti . Izotermele de adsorbtie in forma de "S" corespunzatoare adsorbtiei combinate a cationilor si anionilor au fost interpretate ca o indicatie a predominarii fortelor Van der Waals si de atractie coulombiana in raport cu cele de repulsie coulombiana intre ioni avand aceeasi sarcina.
Hackerman a explicat variatia vitezei de coroziune (icor) si a capacitatii stratului dublu (Cdl) format in prezenta inhibitorilor prin efectul sinergetic al unei adsorbtii colective, care consta in contributia deplasarii potentialului superficial al electrodului si stabilizarea stratului de anioni adsorbiti de catre cationii organici [48]. Studiind o serie de inhibitori de coroziune care contineau atomi de azot, Hackerman a aratat importanta densitatii de electroni aferente atomilor din gruparile functionale, care constituie centrul de reactie hotarator[48]. Stiind ca, in general, electronii implicati in prima ionizare apartin primei perechi, potentialul de ionizare reprezinta in mod uzual o masura a densitatii de electroni de la atomul de azot. Astfel, Hackerman a aratat ca cu cat este mai coborat potentialul de ionizare, cu atat mai puternica este adsorbtia si implicit influenta inhibitorului asupra procesului respectiv.
Campul de forte care determina schimbarile energetice care se petrec cand un inhibitor se leaga de suprafata magnetitei (Fe3O4) formand un film bidimensional, va depinde de structura filmului superficial Fe3O4 - inhibitor, de interactiile dintre atomii de fier si atomii din molecula inhibitorului si de interactiile specifice dintre moleculele de inhibitor.
Utilizand mecanica cuantica, care a studiat aglomeratele la care participa moleculele de apa, substantele utilizate pentru reglarea pH-ului (NH3, diverse amine ca morfolina, ciclohexilamina,etc.), moleculele de inhibitori si fierul sau oxizii si oxi-hidroxizii de fier, au putut fi stabilite constantele specifice diferitelor forte si parametrii geometrici ai legaturilor chimice (lungimi normale ale legaturilor, unghiuri si forte de torsiune) adecvati interctiunilor dintre atomii de fier, oxigen si azot [49].
Imaginile SEM prezentate in aceasta lucrare pledeaza pentru veridicitatea explicatiei date de Ramachandran[49], conform careia, indiferent de mediul apos specific in care a avut loc autoclavizarea, suprafata probelor s-a acoperit cu filme exterioare de Fe3O4 de grosimi variabile. Conform lui Ramachandran, magnetita este formata dintr-un plan in care exista atomi de fier in starea de oxidare (+2), aflati la distanta de 5,935Å unul de altul. Fiecare ion Fe2+ are un ion O2- in vecinatatea lui, sub acest plan existand un alt substrat format din ioni Fe3+. Pe baza parametrilor de retea obtinuti prin difractie de raze X, el a stabilit ca atomii de oxigen din apa se afla la distanta de 2,08Å de ionii de Fe2+. Apa, avand molecule mici, multe molecule de H2O se pot atasa in locurile de pe suprafata in care exista ioni Fe2+. Apar, de asemenea, interactii de atractie intre ionii de H+ incarcati pozitiv din apa si ionii de O2- incarcati negativ din Fe3O4, interactii care implica comprimarea moleculelor de apa de pe suprafata probelor. Cu alte cuvinte, aceasta forta de atractie reprezinta un caz particular al fortelor electrostatice si al legaturilor de hidrogen. Din punct de vedere energetic, situatia cea mai favorabila este atunci cand trei molecule de apa se leaga de fiecare ion Fe2+ aflat pe suprafata Fe3O4 la distanta de 30,5 Å.
In cazul utilizarii inhibitorilor tip amina, distantele care se stabilesc intre atomii de N si respectiv de O din inhibitor si ionul de Fe2+ sunt egale respectiv cu 2,23Å si respectiv 2,36Å. Cand in prezenta probelor oxidate apare o substanta polara, aceasta va deplasa moleculele de apa de pe oxidul superficial. Variatia de energie care rezulta in urma deplasarii apei de pe suprafata Fe3O4 de catre diverse molecule de inhibitor s-a putut calcula tinand cont de conditiile de minimizare a energiei specifice fiecarei structuri [50].
Datele prezentate in aceasta lucrare reprezinta o pledoarie in sprijinul ideii ca chimismul mediului apos din circuitul secundar avand un impact deosebit de important asupra susceptibilitatii la coroziune a materialelor structurale din acest circuit si cu precadere asupra otelurilor carbon, este necesara respectarea lui cu strictete, iar atunci cand apar devieri de la normalitate, readucerea lui la parametrii normali
|
Politica de confidentialitate |
| Copyright ©
2024 - Toate drepturile rezervate. Toate documentele au caracter informativ cu scop educational. |
Personaje din literatura |
| Baltagul caracterizarea personajelor |
| Caracterizare Alexandru Lapusneanul |
| Caracterizarea lui Gavilescu |
| Caracterizarea personajelor negative din basmul |
Tehnica si mecanica |
| Cuplaje - definitii. notatii. exemple. repere istorice. |
| Actionare macara |
| Reprezentarea si cotarea filetelor |
Geografie |
| Turismul pe terra |
| Vulcanii Și mediul |
| Padurile pe terra si industrializarea lemnului |
| ACTINIDELE |
| TEHNOLOGIA ZAHARULUI |
| Metoda conductometrica |
| GAZE REALE |
| REGLEMENTARI IN DOMENIU - GAZE |
| Nucleotide - Mono si difosfat nucleozide |
| LEGATURI CHIMICE |
| Caracterele solventilor organici |
| Termeni si conditii |
| Contact |
| Creeaza si tu |