
Nucleotide
Tipuri de nucleotide
Sunt esteri fosfat ai nucleozidelor. Primele lor denumiri bazate pe numarul de grupari fosfat prezente in molecula (mono-, di-, trifosfati) au fost inlocuite printr-o nomenclatura care inlatura ambiguitatile. De fapt, in nucleotidele naturale:
a) fosforilarea priveste gruparea hidroxil legata la unul sau mai multi atomi de carbon din ciclul pentozei: nucleotidul este un nucleozid mono-, di- sau trifosfat;
b) gruparea fosfat poate ea insasi sa fie angajata: i) cu alte molecule de acid fosforic in condensari anhidridice; ii) cu un nucleotid cu structura de nucleozid di- sau trifosfat, deoarece aceasta combinatie si cea de mai inainte nu se exclud;
c) o alta grupare hidroxil, printr-o a doua legatura ester poate inchide molecula si determina formarea de nucleotide ciclice.
Acizii nucleici sunt polimeri de nucleozide monofosfat. Celelalte nucleotide intervin in biosinteza acestora si in alte tipuri de interactiuni de tipul acelora evocate mai sus. Nomenclatura si tipurile de nucleotide este prezentata in tabelul 1.3.
Mono- si difosfat nucleozide
Monofosfat nucleozide
Polifosforilarea C5' nu este o reactie foarte curenta. Acizii nucleici sunt polimeri de nucleozide 5'-fosfat. Existenta legaturii internucleotidice 3'OH-5'P poate fi dovedita prin eliberarea de nucleozide 3'-fosfat, in anumite etape ale hidrolizei lor. In figura 1.21. este prezentat mononucleotidul derivat de la adenozina, care are si o serie de alte implicatii metabolice.
Constantele de disociere acide (pKa) ale gruparilor fosforice fixe fac ca la temperatura si pH fiziologic gruparile sa contina doua sarcini negative: molecula este un acid (valoarea pKa a primei etape de ionizare este apropiata de 1,0) de unde si denumirea de acid pe care il atribuim acestor esteri-fosfati (Tabel 1.3
Solubilitatea lor in apa este variabila dar ramane redusa. Proprietatile optice de absorbtie sunt datorate bazelor prezente in structura si au fost trecute in revista in paragrafele anterioare.
Difosfat nucleozide
Aceste structuri sunt rare. Cele mai bine reprezentate sunt nucleotidele derivate de la adenina care sunt prezente in structura moleculelor de activare sau a coenzimelor (Tabel 1. 2). De exemplu adenozin 3', 5' -difosfat fixeaza o grupare sulfat printr-o legatura anhidridica, formata intre acidul sulfuric si fosfatul din pozitia 5'. Fosfoadenozil fosfosulfatul (PAPS) este implicat in reactiile de sulfatare a glicanilor si lipidelor (Figura 1.17); De asemenea, adenozin 3'-fosfat 5'-difosfat (exemplu de nucleotid diester mixt si anhidrida) formeaza o parte a moleculei coenzimei A, implicata in procesul de acetilare.
Polifosfat nucleozide
Difosfat nucleozidele rezulta din fixarea, prin legatura anhidridica acida, a celei de a doua molecule de acid fosforic, la nivelul esterului fosforic al carbonului C5'. Reluarea reactiei la nivelul acestui nucleozid difosfat (la nivelul celei de a doua molecule fosfat) conduce la obtinerea nucleozid trifosfatilor. Pentru exemplificare luam in discutie nucleotidul care contine adenina (Figura 1.22
Consecinta imediata a structurii este marea densitate de sarcini negative in conditii fiziologice: trei pentru difosfat si patru pentru trifosfat. Acestea ridica probleme pentru: i) echilibrul electric al celulei, concentratia de nucleotide libere fiind obligatoriu limitata; ii) fixarea acestor molecule la nivelul structurilor vii. Cationii divalenti de magneziu si mangan temporizeaza repulsiile electrostatice care pot sa apara (Figura 1.23
Acesti compusi au un inalt potential energetic. In conditii celulare, legaturile de tip anhidrida acida au o entalpie libera de hidroliza superioara legaturilor ester-fosfat (de ordinul a 30 kJ/mol). ATP este molecula selectionata evolutiv de catre organisme pentru a constitui rezerva temporara si sursa de energie utilizabila de catre materia vie (Figura 1.24), cu toate ca in cateva reactii metabolice intervin si CTP, GTP si TTP.
De hidroliza ATP depind: i) realizarea unor actiuni fizice cum sunt contractia musculara si transportul activ al ionilor si moleculelor; ii) reactiile chimice care sunt termodinamic imposibile fara cuplare energetica.
O diversitate mai mare de nucleotide sunt utilizate in vivo ca suport molecular de activare a grupelor sau moleculelor indispensabile intrarii acestora in reactiile metabolice. Activarea-fixarea se realizeaza prin consumarea unei legaturi anhidrida acida prezenta in structura unei molecule de nucleotid trifosfat:
a) etanolamina si colina sunt activate de catre CDP (Figura 1.25
b) glucidele sunt activate fie prin interventia: i) UTP si mai rar de GTP si CTP, pentru biosinteza glicanilor si a lanturilor glicozilate ale proteinelor; ii) ATP care reprezinta donorul de energie si de grupari fosfat pentru fosforilare.
Biosinteza polimerilor nucleozidici 5'-monofosfat (acizii nucleici) se realizeaza prin condensarea precursorilor trifosfat energia necesara formarii legaturii covalente fiind furnizata de hidroliza legaturii anhidridice. Este foarte clar ca celula trebuie sa intretina permanent o rezerva si sa echilibreze necesarul de NTP, asa cum procedeaza in cazul aminoacizilor necesari sintezei proteice.
Tabel 1. Nomenclatura si simbolurile diferitelor tipuri de nucleotide (sunt figurate numai ribonucleotidele, in afara de timina care serveste ca exemplu pentru deoxiribonucleotide).
|
Nucleotide* fosfat la nivelul a diferiti atomi de carbon (x', y': nr. atomilor de C ai pentozei) |
|||
|
Nume |
Simboluri |
||
|
Formula generala |
Nucleozid x', y'-bifosfat |
Nuc x', y' P2 |
|
|
Exemple |
adenozina 3'-5'-bifosfat |
Ado3', 5' P2 |
|
|
Nucleotide mono- si polifosfat (cu gruparea fosfat la nivelul aceluiasi atom de carbon) |
|||
|
Nume |
Simboluri |
||
|
Formula generala |
Nucleozid x'-fosfat* |
Nuc5'P |
NMP |
|
x'-difosfat |
Nuc5'PP |
NDP |
|
|
x'-trifosfat |
Nuc5'PPP |
NTP |
|
|
Aplicatii |
citidina 5'-fosfat |
Cyd5'P |
CMP |
|
5'-difosfat |
Cyd5'PP |
CDP |
|
|
5'-trifosfat |
Cyd5'PPP |
CTP |
|
|
uridina 5'-fosfat |
Urd5'P |
UP |
|
|
5'-difosfat |
Urd5'PP |
UDP |
|
|
5'-trifosfat |
Urd5'PPP |
UTP |
|
|
dtimina 5'-fosfat |
dThd5'P |
dTMP |
|
|
5'-difosfat |
dThd5'PP |
dTDP |
|
|
5'-trifosfat |
dThd5'PPP |
dTTP |
|
|
adenozina 5'-fosfat* |
Ado5'P |
AMP |
|
|
5'-difosfat |
Ado5'PP |
ADP |
|
|
5'-trifosfat |
Ado5PPP |
ATP |
|
|
guanozina 5'-fosfat |
Guo5'P |
GMP |
|
|
5'-difosfat |
Guo5'PP |
GDP |
|
|
5'-trifosfat |
Guo5'PPP |
GTP |
|
|
Nucleotide ciclice (punti fosfodiester intre Cx' si y' din pentoza) |
|||
|
Nume |
Simboluri |
||
|
Formula generala |
nucleozid x':y' -fosfat |
Nucx':y'P |
NMPc |
|
Aplicatii |
adenozina 3':5'-fosfat |
Ado3' :5'P |
AMPc |
|
guanozina 3':5'-fosfat |
Guo3':5'P |
GMPc |
|
caracterul acid al nucleozid monofosfatilor face ca ele sa fie denumite si:
acid 5'-citidilic (forma acida) sau 5'-citidilat (forma ionizata);
acid 5'-uridilic (5'-uridilat); acid 5'-timidilic (5'-dtimidilat);
acid 5'-adenilic (5'-adenilat); acid 5'-guanilic (5'-guanilat).
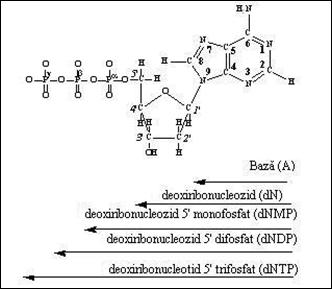
Figura 1.22. Structura nucleozid polifosfatului derivat de la adenina (ATP)
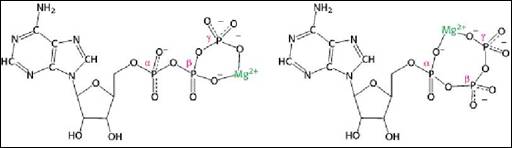
Figura 1.23. Complexe ATP Mg2+
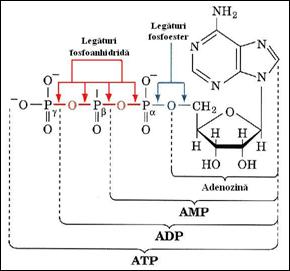
Figura 1.24. Structurile AMP, ADP si ATP cu marcarea legaturilor fosfoester si fosfoanhidrida
O serie de nucleotide sunt constituentii ai coenzimelor. Adenozin 5'-difosfatul intra in structura a doua coenzime implicate in reactii de oxido-reducere: nicotinamid adenin dinucleotid (NAD si omologul sau fosforilat NADP) si a flavin adenin dinucleotid (FAD) (Figura 1.26 Denumirea acestora are mai mult caracter istoric deoarece partea a doua a moleculei are structura ciclica dar nu reprezinta un nucleotid in adevaratul sens al cuvantului. Nucleotidul se leaga la restul moleculei prin intermediarul difosfatului sau. Cofactorii nu intervin in procesul catalitic ca in cazurile coenzimei A (Figura 1.27) si coenzimei B12 (Figura 1.18
Mediatori extracelulari nucleotidele extracelulare au fost recent recunoscute ca mediatori. Eliberate prin liza celulara sau prin exocitoza veziculelor membranare, acestea se fixeaza pe receptorii celulelor tinta, avand, in general, actiune activatoare. Familia ATP (ADP si AMP) este cea mai bine reprezentata pentru aceasta functie de comunicare celulara.
In tabelul 1.2 sunt prezentate coenzime si a intermediari metabolici care contin in molecula adenozina.
Nucleotide ciclice
In structura acestor derivati, un fosfat formeaza o punte fosfodiester intramoleculara care ciclizeaza molecula. Acesti compusi au fost selectionati pentru functiile lor in comunicare si semnalizare celulara fiind repartizati in compartimentul intracelular.
Mesagerii secundari conceptul de mesager secundar a fost impus odata cu descoperirea AMP ciclic (AMPc) in 1950 de catre Sutherland. Un mesager secundar este o molecula care asigura actiunea intracelulara a unui semnal extracelular. Acest semnal poate sa fie un hormon sau un alt mediator si constituie primul mesager care se fixeaza la suprafata celulara.
AMPc (Figura 1.28) este produs plecand de la ATP la nivelul fetei intracelulare a membranei plasmatice in urma fixarii moleculei semnal. Producerea AMPc este oprita, in momentul in care actiunea externa inceteaza, prin hidroliza uneia dintre legaturile ester, produsul 5'-AMP fiind reciclabil.
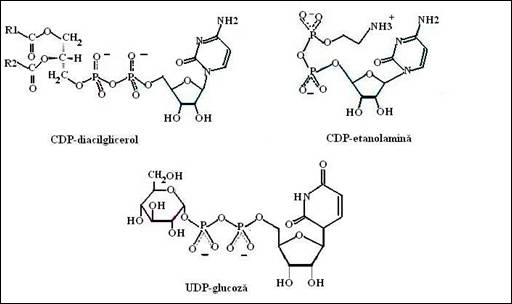
Figura 1.25. Exemple de intermediari metabolici activati: CDP-diacil glicerol, CDP-etanolamina, UDP-glucoza
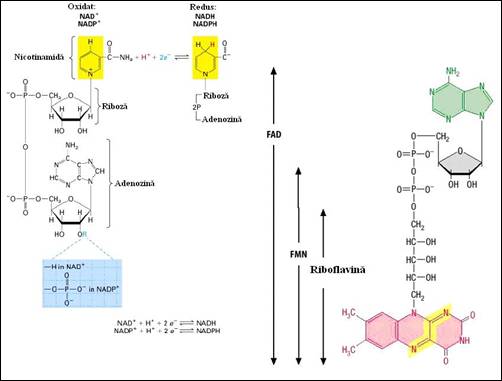
Figura 1. Structurile NAD(P)+ si FAD(H2)
Figura
1. 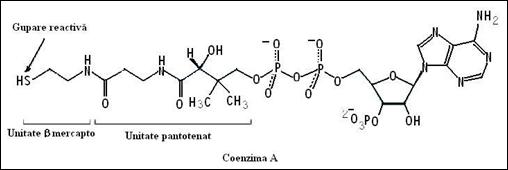 Structura Coenzimei A forma activa SH.
Structura Coenzimei A forma activa SH.
Analiza reactiilor la care participa AMPc ne face sa intelegem de ce aceasta molecula a fost aleasa evolutiv drept mesager secundar universal. GMP ciclic (GMPc) are o functie similara dar pentru un numar foarte scazut de cai de semnalizare (Figura 1.28
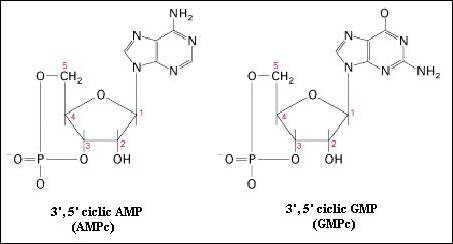
Figura 1.28. Nucleotide ciclice: AMPc si GMPc
Proprietatile nucleotidelor
Componentele celulare care contin fie baze purinice, fie pirimidinice pot fi usor detectate datorita absorbtiei puternice a luminii ultraviolete. Bazele purinice, nucleozidele si nucleotidele au absorbtii mai puternice decat pirimidinele si derivatii lor. Coeficientii de extinctie molara (o masura a absorbtiei luminii la lungimi de unda specifice) si lungimile de unda (lmax.) corespunzatoare acestora sunt prezentate in tabelul 1. 4. Lungimea de unda la care se inregistreaza absorbtie maxima variaza, in particular, cu baza din compozitia moleculei, dar in majoritatea cazurilor este apropiata de 260 nm. Spectrul UV pentru fiecare dintre aceste nucleozide sau derivati nucleotidici poate fi diferit in functie de pH. Absorbtiile UV puternice si diferentele datorate structurii specifice a bazelor, din structura, furnizeaza metode sensibile de dozare a acestor compusi atat din punct de vedere calitativ cat si cantitativ. De exemplu, deaminarea citozinei din structura nucleozidului sau nucleotidului la derivatii uracil corespunzatori determina a deplasare a lmax. de la 271 nm la 262 nm, care este usor de determinat. Datorita coeficientilor molari de extinctie mari ai bazelor purinice si pirimidinice in acizii nucleici, o solutie de ARN sau ADN de concentratie 1 mg/ml va avea o absorbanta la 260 nm de aproximativ 20 unitati, in timp ce o solutie proteica obisnuita cu concentratia de 1 mg/ml va avea la 280 nm o absorbanta de aproximativ o unitatea. In consecinta, acizii nucleici pot fi usor detectati si in concentratii foarte mici.
Legatura N-glicozidica, din structura nucleozidelor purinice si pirimidinice, este stabila in prezenta de baze. Totusi, stabilitatea acestei legaturi la hidroliza acida difera marcant. Legatura N-glicozidica din structura nucleozidelor si nucleotidelor purinice se hidrolizeaza usor in prezenta de acizi diluati si prin cresterea temperaturii (600C) conducand la purine libere si glucide sau glucide-fosforilate. Pe de alta parte, legatura N-glicozidica din nucleozidele derivate de la uracil, citozina si timina si din nucleotidele derivate de la acestea este foarte stabila la tratament acid. Pentru eliberarea pirimidinelor libere si completa distrugere a restului glucidic sunt necesare conditii drastice de hidroliza, cum ar fi acid percloric (60%) si temperatura de 1000C. Legatura N-glicozidica din structura nucleozidului derivat de la dihidrouracil este sensibila la tratament acid moderat.
Datorita gruparilor fosfat foarte polare, nucleotidele purinice si pirimidinice sunt mult mai stabile in solutii apoase decat nucleozidele si bazele libere din care deriva. In general, nucleozidele sunt mult mai solubile decat bazele purinice si pirimidinice libere.
Bazele purinice si pirimidinice, nucleozidele si nucleotidele derivate din acestea pot fi usor separate printr-o serie de tehnici. Aceste metode sunt: cromatografie pe hartie, cromatografie in strat subtire (Thin Layer Chromatography TLC), cromatografie de schimb ionic, electroforeza. Cele mai bune separari ale compusilor purinici si pirimidinici s-au realizat prin cromatografie lichida de inalta presiune in faza inversa (High Presure Liquid Chromatography HPLC). Prin aceasta tehnica pot fi separate cantitati de ordinul nano-molilor din aceste componente intr-o scurta perioada de timp. In figura 1.29 este prezentat profilul de separare prin HPLC al unui amestec format din baze, nucleozide si nucleotide. Dezvoltarea acestei tehnici prin introducerea coloanelor de inalta rezolutie permite o determinare rapida a nucleozidelor si nucleotidelor dintr-o numar mare si variat de celule in diferite stadii.
Tabel 1. Constante spectrofotometrice ale nucleozidelor purinice si pirimidinice
|
Nucleozidul |
Coeficientul molar de extinctie |
lmax la pH 7,0 |
|
Adenozina | ||
|
Guanozina | ||
|
Citidina | ||
|
Uridina | ||
|
Timidina |
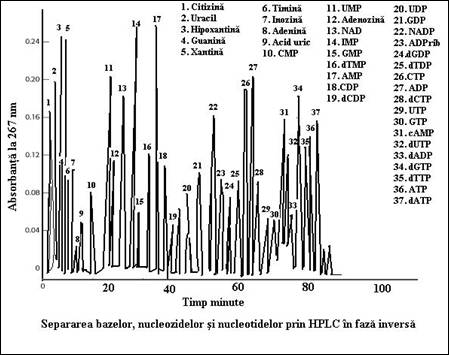
Figura 1.29. Separarea bazelor, nucleozidelor si nucleotidelor prin cromatografie lichida de inalta rezolutie (HPLC) in faza inversa: Coloana Alltina C18-NUC, 5 μm, 250 x 4,6 mm; faza mobila: gradient crescator de fosfat si descrescator de metanol; debit 1,5 ml/min; detector UV 267 nm
Functii metabolice ale nucleotidelor
Toate tipurile de celule (mamifere, bacterii, plante) contin o varietate foarte mare de nucleotide si de derivati ai acestora. Unele dintre aceste nucleotide se gasesc in cantitati importante in celule (de ordin mili-molar). Ratiunea existentei unui numar mare de nucleotide si de derivati ai acestora, in celula, este faptul ca acestea sunt implicate intr-un numar foarte mare de procese metabolice care asigura cresterea si functionarea normala.
Rol in metabolismul energetic: dupa cum am prezentat mai sus ATP reprezinta principala forma sub care energia este disponibila in celula. Cantitativ, ATP este generat in celule prin fosforilare oxidativa si fosforilare la nivel de substrat. ATP este folosit pentru a coordona reactiile metabolice, ca agent de fosforilare, fiind implicat si in procesele de contractie musculara, transport activ si mentinerea integritatii membranare. Ca agent de fosforilare, ATP serveste drept donor de fosfat pentru generarea altor nucleozide 5'-trifosfat (GTP, UTP si CTP).
Unitati monomere ale acizilor nucleici acizii nucleici, ADN si ARN, sunt compusi din unitati monomere, nucleotide. In reactiile de sinteza ale acizilor nucleici, nucleozidele 5'-trifosfat sunt substrate care participa la formarea legaturilor 3', 5'-fosfodiester cu eliberarea unei molecule de pirofosfat la fiecare condensare.
Mediatori fiziologici una dintre cele mai recent recunoscute functii ale nucleotidelor si ale derivatilor acestora este implicarea in procesul de mediere a unor procese metabolice cheie. In primul rand, trebuie luat in considerare rolul AMPc ca mesager secundar in controlul glicogenolizei si glicogenezei mediata de epinefrina si glucagon si in semnalizarea transmembranara prin intermediul proteinelor G. De asemenea a fost recunoscuta si importanta GMPc ca mediator celular. O serie de studii confirma rolul critic al concentratiei ADP in agregarea plachetelor in timpul coagularii sangelui. Adenozina provoaca dilatarea vaselor de sange coronariene si poate avea un rol important in reglarea fluxului de sange la nivelul coronarelor. GTP este necesar unor reactii cum este prelucrarea post-transcriptionala a ARNm (adaugarea capului), transmiterea semnalului catre proteinele G ("GTP binding protein"), si formarea microtubulilor.
Componente ale coenzimelor intra in structura NAD+, NADP+, FAD si CoA care sunt constituenti celulari foarte importanti cu rol critic in multe reactii metabolice.
Intermediari activati nucleotidele au si rolul de transportori ("carriers") ai intermediarilor "activati" intr-o serie de reactii metabolice. Compusul UDP-glucoza este un intermediar cheie in sinteza glicogenului si glicoproteinelor. Compusii GDP-manoza, GDP-fucoza, UDP-galactoza, si CMP-acid sialic sunt cu totii intermediari cheie in reactiile in care monomerii glucidici sunt transferati pentru sinteza glicoproteinelor. CTP este folosit pentru generarea CDP-colinei, CDP-etanolaminei si CDP-diacilglicerolilor, care sunt implicati in metabolismul fosfolipidelor. De asemenea, alti intermediari activati sunt S-adenozilmetionina (SAM) si 3'-fosfoadenozin 5'-fosfosulfat (PAPS). S-adenozilmetionina este un donor de grupari metil in reactiile responsabile de metilarea glucidelor si a bazelor din structura ARN si ADN si in formarea unor compusi cum sunt fosfatidilcolina, fosfatidiletanolamina, carnitina din lizina, etc. S-adenozilmetionina furnizeaza si grupari aminopropil pentru sinteza sperminei din ornitina. Intermediarul PAPS este folosit ca donor de grupari sulfat pentru sulfatarea biomoleculelor de tipul proteoglicanilor si sulfatidelor.
Efectori alosterici: o serie din etapele metabolice reglatoare sunt controlate prin intermediul concentratiilor intracelulare ale nucleotidelor.
In celule nucleotidele sunt distribuite diferit: principalele forme ale compusilor purinici si pirimidinici din celula sunt derivatii 5'-nucleotidici. In celulele normale ATP reprezinta nucleotidul cu concentratia cea mai mare. De retinut ca, in functie de tipul celular, concentratia nucleotidelor variaza foarte mult. De exemplu, in eritrocite adenin nucleotidele depasesc mult concentratia altor nucleotide, care sunt in concentratii abia detectabile. In celulele hepatice si in alte tesuturi se regaseste un spectru complex al mono-, di- si trifosfatilor care se regasesc cuplati in structurile UDP-glucoza, UDP-acid glucuronic, NAD+, NADH, etc. Prezenta bazelor libere, nucleozidelor sau nucleotidelor 2'- si 3'-fosfat, in fractia acida solubila din celule, este datorata reactiilor de degradare normala a nucleotidelor exogene si endogene. In acelasi mod se explica si prezenta bazelor minore rezultate din degradarea acizilor nucleici.
Concentratia ribonucleotidelor in celula este de ordin milimolar in timp ce concentratia deoxiribonucleotidelor este de ordin micromolar. De exemplu, concentratia ATP in celulele tumorii Erlich este de 3600 pmol/106 celule, in timp ce dATP este in concentratie de numai 4 pmol/106 celule. Totusi, nivelurile concentratiilor deoxiribonucleotidelor sunt subiectul unor fluctuatii majore in timpul ciclului celular, in contrast cu nivelul concentratiei ribonucleotidelor care ramane relativ constant.
In celulele normale, concentratia totala a nucleotidelor variaza intr-un domeniu ingust desi concentratia componentelor individuale poate sa varieze. De exemplu, concentratia totala a adenin-nucleotidelor (AMP, ADP si ATP) este constanta, desi pot exista variatii ale raportului ATP/AMP+ADP, dependente de starea energetica a celulelor. La baza "concentratiilor fixe" ale nucleotidelor sta faptul ca reactiile de biosinteza ale acestora reprezinta cai metabolice care presupun o reglare celulara foarte fina.
|
Politica de confidentialitate |
| Copyright ©
2024 - Toate drepturile rezervate. Toate documentele au caracter informativ cu scop educational. |
Personaje din literatura |
| Baltagul caracterizarea personajelor |
| Caracterizare Alexandru Lapusneanul |
| Caracterizarea lui Gavilescu |
| Caracterizarea personajelor negative din basmul |
Tehnica si mecanica |
| Cuplaje - definitii. notatii. exemple. repere istorice. |
| Actionare macara |
| Reprezentarea si cotarea filetelor |
Geografie |
| Turismul pe terra |
| Vulcanii Și mediul |
| Padurile pe terra si industrializarea lemnului |
| Termeni si conditii |
| Contact |
| Creeaza si tu |