
COLORANTI IN BIOCHIMIE, BIOLOGIE SI MEDICINA
1.Introducere
Este mai mult decat probabil ca toate cartile despre coloranti publicate in trecut incep cu utilizarea ca medicamente. Intr-adevar, anumiti coloranti au fost (si mai sunt inca) folositi ca agenti terapeutici. In realitate, totusi unii coloranti ca acestia sunt cazuri exceptionale. Cand privim intr-un context stiintific, acestia nu mai sunt uimitori. Este improbabil pentru un compus chimic, care este caracterizat mai inainte prin absorbtia totala a luminii in domeniul vizibil al spectrului sa aiba proprietati terapeutice mai interesante decat un compus necolorat. Acest punct de vedere este demonstrat foarte bine de istoria agentilor terapeutici sulfanilamidici. Prin testarea catorva mii de coloranti azo in 1930, G. Domage a gasit ca 2,4-diamino-azobenzen-4'-sulfonamida (probabil 16.1.) arata proprietati antibacteriene.
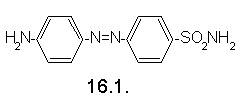
Investigatii detaliate, totusi, au aratat ca compusul biologic activ nu a fost colorantul insusi ci sulfonamida metabolizata, care este formata in tubul gastrointestinal prin reducere anaerobica a grupei azo.
Totusi, (in aceasta carte) noi mentionam numai putini coloranti cu proprietati terapeutice, nu intr-un capitol special, dar in acord cu structura lor cromogena, exemplu: derivati acridinici si fenoxazinici ca Acriflavina si Actinomicena D.
Antramicina Adiamicina 8.122 este un derivat antrachinonic si Protosilul este prezentat in context ca si coloranti azo degradabili microbiologic. Toxicitatea colorantilor, este de asemenea un efect farmacologic intr-un sens negativ. In 1980, totusi, cativa coloranti au devenit interesanti datorita culorii lor cand sunt administrati la un organism viu acesti coloranti au un efect terapeutic datorita absorbtiei luminii de catre acestia. Aceasta este baza terapiei fotodinamice impotriva cancerului.
O mare importanta o are utilizarea colorantilor in biochimie, biologie si medicina pentru identificarea vizuala (calitativa) sau cantitativa a structurilor morfologice (exemplu histologice). Aceste metode se bazeaza pe aplicarea colorantilor ca un instrument analitic pentru identificarea structurilor chimice si a reactiilor.
2. Colorarea biologica
Colorarea selectiva a structurilor biologice este necesara pentru caracterizarea lor microscopica.
Istoria tehnicii colorarii biologice se regaseste inca in secolul 18 si chiar in era colorantilor naturali.
Foarte curand dupa descoperirea colorantilor sintetici acesti coloranti au fost de asemenea aplicati in microscopie.
Cateva din aceste vechi metode sunt utilizate si azi.
Primul caz care s-a bazat numai pe pure observatii empirice si nu pe o reactie chimica a fost reactivul descoperit de Schiff in 1867, a putut detecta grupa aldehidica in materialul biologic.
Produsul colorat, de aditia SO2 la fucsina (al doilea colorant sintetic dupa Mauveina lui Perkin, descoperit de E. Verguin la Lyon in 1859) devine rosu in prezenta unei aldehide. Se formeaza un colorant trifenilmetanic N-alchilat asa cum se vede in schema urmatoare in urma reactiei cu formaldehida.
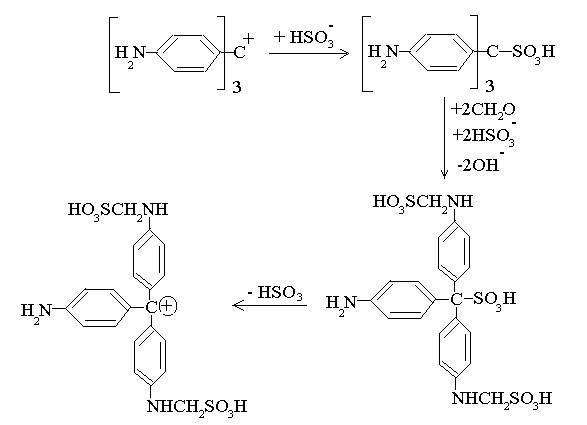
Este interesant ca aceasta reactie nu a fost inteleasa 100 de ani. Reactia, asa cum arata, a fost elucidata de Hörmann si colaboratorii in 1958.
Grupele aldehidice in materialele biologice reactioneaza probabil intr-o maniera similara.
Importanta este si reactia lui Feulgen pentru identificarea histochimica a acizilor dezoxiribonucleici (DNA) care sunt in nucleele celulelor.
Celalalt acid nucleic, acidul ribonucleic (RNA) este localizat in citoplasma celulelor, in principal in ribozomi.
Ambii acizi nucleici constau in unitati alternante de pentoza si fosfat cu o baza azotoasa, adenina, granina sau citozina (DNA si RNA), timina (DNA) sau aracilul (RNA) atasata la fiecare unitate de pentoza (R).
Aceste unitati de zaharide sunt dezoxiriboza si respectiv riboza.
Ciclurile dezoxiribozice ale DNA sunt deschise prin intermediul hidrolizei acide, urmata de expunerea hidrolizatului la actiunea bazei Schiff.
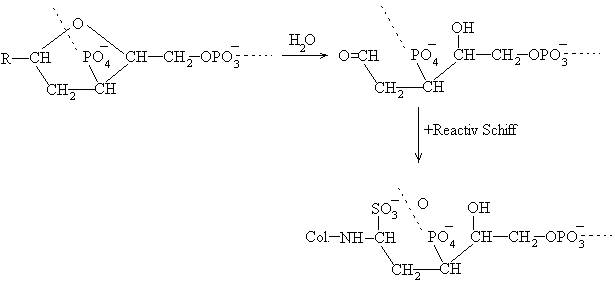
Reactivul Schiff poate fi considerat un colorant reactiv deoarece formeaza o legatura covalenta cu un substrat si a fost descoperit cu 80 de ani inaintea colorantilor reactivi.
O alta descoperire importanta a ultimului secol a fost observatia lui C. Gram in 1884 cu privire la colorantul Cristal Violet care colora ireversibil cateva bacterii, dar care poate fi indepartat prin spalare de catre alte bacterii.
Aceasta clasificare in bacterii Gram-pozitive si Gram-negative este folosita si astazi.
Horobin demonstreaza ca actul colorarii este bazat pe acea interactie colorant-substrat si pe cinetica sa ca in cazul colorarii textilelor.
Deoarece tesutul biologic consta din unitati morfologice diferite, mai importanta este colorarea selectiva.
Selectivitatea se bazeaza atat pe afinitatile diferite cat si pe vitezele diferite de difuziune ale colorantului in substrat.
In continuare sunt date cateva exemple caracteristice care sunt reprezentative pentru aspectele chimice:
a)Colorantii cationici coloreaza tesuturile care sunt bogate in cationi, ca de exemplu DNA si RNA.
Proteinele, totusi nu sunt colorate in conditii acide, dar la valori ridicate ale pH-ului ele sunt de asemenea anionice si pot fi colorate.
b)Pentru influenta interactiilor hidrofobice valorile π ale lui Hansh, care sunt folosite pentru estimarea balantei hidrofobic-hidrofilic a compusilor organici, sunt frecvent utilizate in histochimie.
Un exemplu este dat de Horobin pentru coloranti monocationici triarilmetanici de tipul fucsinei in care afinitatea este corelata bine cu suma valorilor π ale diverselor fragmente moleculare.
c)Agregarea colorant-colorant este importanta in colorarea biologica, ca si culoarea agregatelor diferita de cea a colorantilor monomeri.
In tehnica colorarii biologice aceasta se cheama metacsomazie.
Are loc mai usor in partile materialului care au o concentratie de ioni de semn contrar.
Agregarea poate fi de asemenea cauza schimbarilor de culoare in colorarea biologica fluorescenta.
Oranjul de acridina arata o fluorescenta galben-verzuie a DNA, dar rosie fluorescenta a RNA.
d)Foarte adesea colorarea selectiva nu este bazata pe afinitatile diferite semnificativ ci pe vitezele diferite ale difuziei.
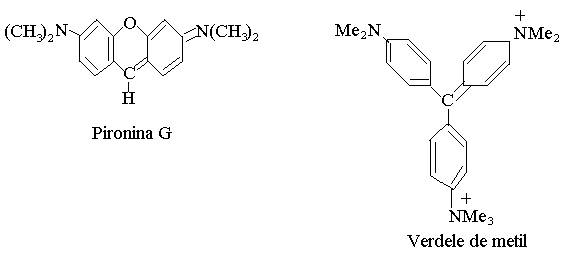
Un caz cunoscut este amestecul de pironina G si Metil Green.
Cationul relativ mare al Verdelui de metil (M = 408) coloreaza DNA, Pironina (M = 267) numai RNA.
Acesta este un efect cinetic.
Goldstein (1965) a aratat ca structurile continand proteine ribonucleare (RNA) au o porozitate mai scazuta decat structurile cromatine (DNA).
Diferenta dintre DNA si RNA este totusi data de efectele porozitatii.
e)Teoria legaturii colorant-fibra poate fi de asemenea aplicata la materialele biologice.
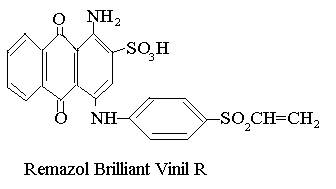
Un remarcabil studiu asupra influentei pH-ului este aplicat la colorantii reactivi vinilsulfonici in studiile histologice ale lui Salthouse si colaboratorii (1971). Colorantii reactivi sunt in particular folositi deoarece ei pot fi utilizati la marcarea amestecurilor de proteine.
Dupa separarea ulterioara, diferite fractiuni de proteine devin clar vizibile.
Un exemplu este utilizarea unui colorant reactiv intr-o etapa prestabilita pentru o proba cantitativa de proteine pe geluri poliacrilamidice. Astfel Datyner si Finnimore (1973) au gasit in colorantul reactiv cu o grupa -SO2CH=CH2 poate fi utilizat pentru acest scop.
f)Reactiile de colorare au fost folosite ca indicatori ai transferului enzimatic pentru un timp lung.
Mai recent mostrele enzimatice au fost facute de asemenea in regiunea UV a spectrului.
Colorimetria in domeniul vizibil este utilizata si in reactii redox si hidrolitice.
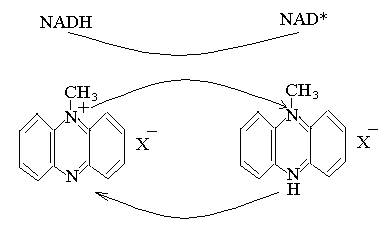
Multe dehidrogenari utilizeaza nicotinamide, adenine, dinucleotide (NAD*) sau fosfatul lor (NADP) ca coenzime.
Formele reduse ale acestor nicotinamide, coenzimele, sunt formate in aceste rectii de dehidrogenare (exemplu NADH).
In general ele pot transfera hidrogenul numai indirect la cei mai comuni coloranti.
Astfel sunt utilizati ca transmitori de hidrogen ionii de fenazinium (5-metilfenazinium-metasulfat de exemplu) sau fenoxazinele.
Acesti ioni reduc sarurile tetrazolice ca de exemplu 2,3,5-trifenil-tetrazolium clorura la formazom care este rosu-oranj in sistem.
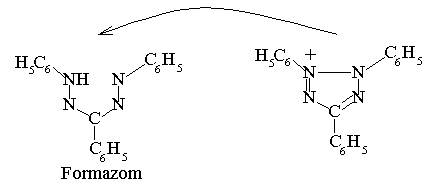
Structura sarurilor de tetrazoliu poate fi variata nu numai cu substituenti in nucleul fenilic, dar chiar si nucleele pot fi inlocuite in parte prin cicluri heterovasomatice.
Alternativ, compusii ditetrazolici pot fi utilizati prin atasarea a doua cicluri tetrazolice la o punte 4,4'-bifenilica.
In acest potentialul lor redox poate fi variat intre +50 si +460 mV obtinand o inalta specificitate.
Asa de exemplu 2,3,5-trifenil-terazolium clorura poate fi redusa de NAD*, dar nu de NADP pentru care sarurile tetrazolice cu cel mai scazut potential redox au nevoie de aditivi.
Reactiile redox cu H2O2 ca un intermediar generat de enzime pot fi vizualizate printr-o serie de reactii color.
Pentru acest scop sunt utilizate cuplante azo sau hidrozide heteroaromatice.
Ca un exemplu de identificare a reactiei hidrolitice este determinarea activitatii fosfatilor enzimelor care hidrolizeaza.
Se adauga la materialul biologic fosfatul unui naftol AS componenta de cuplare si o sare de diazoniu.
In prezenta fosfatoze, esterul fosfat al naftolului este hidrolizat si forma libera a naftolului cupleaza cu ionul de diazoniu formandu-se un colorant.
3. Colorarea fluorescenta
Colorantii fluorescenti si compusii care absorb in lumina vizibila dar emit lumina fluorescenta in spectrul vizibil au inlocuit colorantii conventionali pentru unele tehnici de colorare in ultimile doua decenii.
Aceasta se datoreste faptului ca metodele fluorescente asigura o mai mare sensibilitate in diferentierea de culoare a celulelor pline cu indicator.
Schimbarile potentialelor de membrana ale celulelor plantelor superioare sau animale pot fi masurate cu colorantii fluorescenti care sunt sensibili la schimbarile potentialului.
In particular, adecvati pentru aceasta aplicatie este colorantul cianinic cationic urmator:
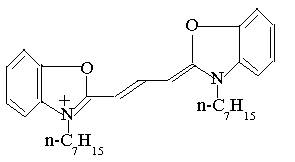
Descoperirea colorantilor reactivi pentru textile a influentat de asemenea tehnicile deoarece in unele cazuri formarea legaturii colorant-tesut are loc daca conditiile de aplicare, ca de exemplu pH-ul si temperatura sunt alese cu grija.
Astfel un colorant azodiclortriazinic a fost primul folosit in acest scop.
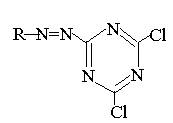
Colorantii Lucifer Yellow ca si Lucifer Yelow VS au inlocuit colorantii Procion Yelow MX 4R din cauza randamentului bun cuantic al fluorescentei mai mare.
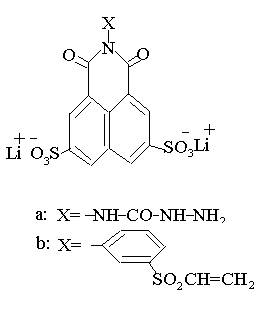
Datorita randamentului lor cuantic mare si non-toxicitatii ei pot fi aplicati pentru colorarea intracelulara a celulelor vii, de exemplu pentru functiile neurale ale celulei.
O alta noua metoda in neurologie este aplicarea colorantilor pentru monitorizarea activitatii neuronilor.
Este bine cunoscut astazi ca impulsurile nervilor sunt propagate ca schimburi in potentialul electric al membranelor celulei nervoase.
Experimental aceasta poate fi demonstrata si masurata cantitativ cu ajutorul microelectrozilor, o masura microelectrodica numai a potentialului si schimbarile sale in functie de timp intr-un neuron.
Din cauza numarului mare al celulelor legate intre ele si implicit in procese nervoase, solutiile multor probleme in neuropsihologie pot fi usurate daca se folosesc metode pentru monitorizarea activitatii neuronilor multipli sau individuali simultan.
O noua tehnica se bazeaza pe observatia ca o schimbare a potentialului in cealalta parte a membranei colorata cu cativa coloranti este insotita de schimbari in proprietatile sale optice, ca de exemplu absorbtia sau fluorescenta.
Cei mai sensibili sunt colorantii mezocianinici, cianinici, oxonoli si stirilici.
Exemplu colorantul mezocianinic urmator ajuta o absorbtie la lungime de unda mare (λmax=720nm)
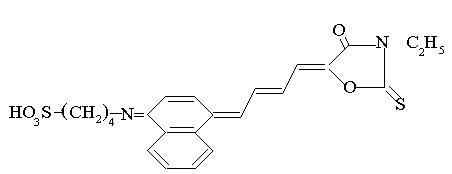
Colorantul urmator are o fluorescenta sensibila la potentialele electrice in neuroni (λmax=790nm).
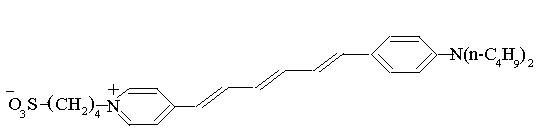
Este cunoscut ca electrocromismul-schimbarea proprietatilor optice ale cromoforului intr-un camp electric-cauzeaza schimbarile observate in neuroni.
Schimbarea rezulta probabil dintr-un potential dependent de agregarea colorantului, localizat pe membrana.
Colorarea fluorescenta este utilizata si in microscopia textilelor.
Coloranti pentru cromatografia de afinitate
Din punct de vedere istoric, colorantii au fost importanti pentru descoperirea si dezvoltarea primelor metode cromatografice.
Cu ajutorul compusilor colorati, coloana cromatografica a fost conceputa de Tvett la inceputul secolului XX.
Cromatografia de afinitate se bazeaza pe tehnologia colorantilor reactivi.
Ea este utilizata in laboratoarele ca au in studiu probleme biochimice si microbiologice.
In anul 1970 apar cele mai importante metode pentru purificarea enzimelor, in contrast cu alte metode, ele dand randamente ridicate in timp scurt.
Aceste tehnici au diverse avantaje prin utilizarea liganzilor naturali biospecifici ca de exemplu nucleotidele mobile si coenzimele.
Ele lucreaza cu chimicale comode care sunt biologic si chimic mai stabile decat liganzii naturali.
Capacitatea lor este in cele mai multe cazuri mai mare si au o scara mai mare de aplicatii.
Aceste metode sunt in general mai putin specifice.
Este bine cunoscut ca fiecare enzima are o afinitate biologica semnificativ de selectiva pentru alti compusi biologic activi sau pentru o grupa functionala a unui numar mare de compusi macromoleculari.
Asemenea compusi sunt numiti bioliganzi.
Daca un asemenea compus activ, selectiv, de marime relativ mica este imobilizat pe o coloana si un extract crud este trecut prin aceasta coloana, acea enzima care are o afinitate pentru bioligandul imobilizat va fi absorbita pe coloana ca un complex enzima-bioligand.
Alte enzime nu vor fi retinute. Dupa aceea, proteina retinuta poate fi eluata la o concentratie mare cu un bioligand solubil sau prin schimbarea conditiilor de eluare (solvent, pH, tarie ionica, temperatura).
Substraturile cu un colorant reactiv ca bioligand sintetic sunt obtinute de exemplu prin reactia colorantului antrachinon monoclortriazinic Cibacrom Blue F3 G-A si alti coloranti reactivi, cu o polizaharida.
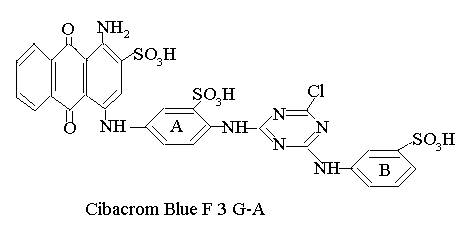
Drept polizaharide pentru imobilizarea colorantilor se utilizeaza dextrinele degradate (Sephadex) si derivatii de agaroza (Sepharose).
Separarea unei serii de proteine din lichidul celular prin cromatografia de afinitate cu colorantul Cibacrom Blue F 3 G-A este posibila datorita faptului ca prin eluarea diferitelor proteine, ele sunt retinute la diferite trepte dependent de afinitatea lor fata de bioligand.
Mici schimbari in structura acestor coloranti pot schimba semnificativ specificitatea.
Colorantul Cibacrom Brilliant Blue FRB-P care este un izomer al colorantului Blue F 3 G-A este capabil sa absoarba enzime fosfofructinaze.
Deoarece cele mai multe enzime nicotinamid-adenosin-dinucleotide (NAD+) si adenin-trifosfat (ATP) interactioneaza cu colorantul Cibacrom Blue F 3 G-A s-a presupus ca acest colorant poate fi strutural analog cu ATP.
Aceasta ipoteza devine improbabila dupa introducerea colorantului Procion Red H-E 3 B ca ligand in cromatografia de afinitate.
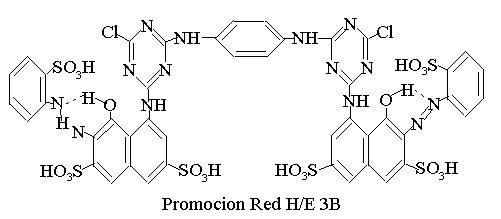
In ciuda acestei structuri complet diferite, acest colorant azoic reactiv bifunctional se comporta similar cu colorantul antrachinonic Blue F 3GA in ceea ce priveste interactia sa cu alte enzime.
Kopperschläger presupune ca interactia specifica a proteinelor cu colorantii reactivi imobilizati pe diferite suporturi se bazeaza printre alti factori, pe prezenta unui buzunar hidrofolic pe suprafata proteinei care este suficient de mare pentru interactia cu partile hidrofolice aromate ale colorantului.
Partea fenilamino-antrachinonica a colorantului Cibacrom Blue F 3 GA interactioneaza cu adenina, substituenta a dinucleotidei legand capatul dehidrogenazei si kinazei, asa cum arata analiza de raze X a complexului format intre alcool - dehidrogenaza si acest colorant.
Un caz interesant a fost gasit de Fish si colaboratori care au aratat ca nu numai enzimele dar si microorganismele pot fi atacate in vivo de picaturile de colorant reactiv Green A.
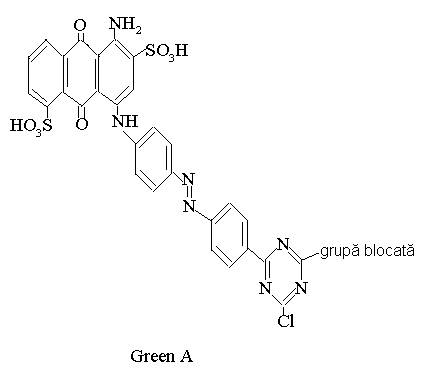
Numai partea fenil-amino-antrachinonica a colorantului Green A este implicata in legarea de tripanosani.
Low si colaboratorii au gasit ca picaturile continand un colorant omolog Cibracrom Blue F 3 G-A cu o punte de trei grupe metilenice intre ciclul A si grupa amino triazinica descompune o mostra comerciala a alcool hidrogenazei in doua componente active.
Spectrul de dicronism circular al colorantului Cibacrom Blue F 3 G-A in solutie in prezenta a doua dehidrogenaze a fost comparat cu spectrul calculat luand indolul ca parte a restului de triptofan al enzimei ca model pentru interactia colorant enzima.
Spectrul calculat al colorantului liber are benzi de absorbtie care sunt diferite cu 100-120 nm de spectrul experimental.
Informatii mai realiste despre interactia colorant:enzima se obtine din diferenta dintre spectrul colorantului Blue F3G-A de exemplu partea grafica a diferentei dintre spectrul vizibil al colorantului liber si interactionat. Un elegant exemplu al acestei tehnici a fost dat de Federici si colaboratorii (1985) care l-au utilizat la probe schimbate fin conformational in structura proteinei asociata cu conversia glutaminei sintetizata prin relaxarea, incordarea si oxidarea formelor disociate.
Cromatografia de afinitate cu Blue F 3 G-A a fost utilizata pentru purificarea si izolarea Orange II azoreductazei, o enzima care catalizeaza reductiv scindarea legaturii azo a Naftalen Orange G.
5.Aplicatii color-specifice ale colorantilor pentru scopuri terapeutice
Acest capitol este dedicat numai aplicatiilor terapeutice ale colorantilor pentru care absorbtia in lumina vizibila este esentiala pentru terapie.
In 1924 Policard a observat ca porfirinele se gasesc in concentratii mai mari in tumorile maligne decat in tesuturile normale. Asemenea porfirine sunt inofensive dar ele pot avea efect foarte toxic pentru celulele in care ele sunt concentrate daca sunt expuse la lumina.
In acest fel o tumoare poate fi distrusa prin aplicarea luminii daca contine o concentratie relativ mare de porfirine. Tesuturile normale vecine, totusi supravietuiesc pentru ca ele absorb putina porfirina. O noua terapie a cancerului, curenta, in dezvoltare, terapia fotocromica (PDT) [Astfel este denumita terapia fotoiradierii (PRT) sau fotochimioterapie (PCT)] se bazeaza pe distrugerea selectiva a tumorilor prin intermediul injectiei intravenoase a o serie de coloranti fototerapeutici, urmata de expunere la lumina rosie. Concentratia marita a acestor coloranti in tumorile maligne poate de asemenea fi folosita pentru detectia cancerului daca colorantii fluorescenti sunt injectati asa dupa cum s-a gasit in 1942 de Auler si Banzen si simultan de Figge.
Principiul PDT a fost aplicat in jurul anilor 1930 cand von Tappeiner si Jesianek au tratat o tumoare de piele prin aplicarea Eosinei si ulterior iradiere in lumina alba.
Figge si colaboratorii sugereaza utilizarea porfirinelor si metalporfirinelor pentru PDT a cancerului in 1948. In 1950 a fost utilizata hematoporfirina. La acest timp, totusi a fost dificil sa se determine puritatea hematoporfirinei si intr-adevar Schwatz si colaboratorii (1955) au avut cateva evidente in aceea ca fluorescenta observata pe iradierea tesuturilor maligne nu s-a datorat hematoporfirinei, dar la o impuritate a structurii necunoscute, numeste derivati hematoporfirinici.
PDT pentru tratamentul cancerului a fost real buna numai in jurul anilor 1970. Dupa aparitia pe piata a luminii laser si a fibrelor optice, aceste instrumente au permis doctorilor accesul direct la sursele de lumina exclusiv la tumorile maligne.
Daca apoi, fractiunile purificate ale hematoporfirinei au fost dezvoltate, si produsul Fotoporfirina II, obtinute de Quadra Logic Technologie Inc (QLT) din Vancouver (Canada) a fost testata pe cateva mii de persoane si cancere esofagiene. Este de asteptat sa fie recunoscuta in diverse tari in viitor. Testele clinice au gasit un produs secundar QLT, Lumin-G care este un derivat bemzoporfirinic, PDT cercetata si dezvoltata face un rapid progres. Statutul lucrarilor chimice, biologice si chimice este documentat in procedurile conferintei din San Diego, ce a avut loc in ianuarie 1990 si editata de Gamer (1990) si intr-un articol de sinteza de Sternberg si Dolfphin (1990).
In acest capitol noi vom discuta numai cateva aspecte relatate de chimia color si in acest scop a fost folosita chimia organica a colorantilor sau mai poate fi potential utilizata, in PDT si fotochimia celor mai multe mecanisme cunoscute ale fotodegradarii in celule.
Cercetarea pentru derivatii hematoporfirinei care sunt activi prin fotodegradare este totusi in progres. Spre exemplu, ~45% din compusii Photoporfirinei II au fost cunoscuti in 1989.
Etapa primara caracteristica a fotodestructiei este absorbtia unui foton de catre colorant (Col.) ce produce un singlet in stare excitata (Col*s). Colorantul poate apoi pierde aceasta energie direct in 5 cai:
a) prin dezactivare radianta producand energie termica;
b) prin fluorescenta de exemplu procesul care este esential la detectia cancerului;
c) prin reactia chimica cu substratul de exemplu cu componentele celulelor care formeaza radicali sau ioni radicali care sunt oxigenati de oxigenul molecular.Alternativ tranzitia la un triplet in stare excitata (Col*t) poate conduce la doua cai pentru colorant la pierderea energiei sale:
d) prin fosforescenta
e) prin reactia cu starea de baza a moleculei de oxigen (3O2) cu formarea oxigenului singlet (1O2), asa cum a fost investigat pentru multi coloranti in solutie.
Oxigenul singlet este un oxidant foarte rectiv care poate distruge componentele celulei.
In literatura PDT, mecanismele (c) si (e) sunt numite reactii de tipul I si tipul II. Concentratiile mari ale oxigenului favorizeaza tipul II si concentratiile mari ale substratului promoveaza tipul I. Pana acum starile triplet din timpul acestor procese fotosensibile au fost detectate experimental, dar nu starea de oxigen singlet, datorita reactivitatii sale mari. Totusi, el nu este cunoscut experimental asa cum sunt responsabile pentru fotodestructia in PDT. Dupa excitarea cu lumina rosie (630 nm pentru porfirine) energia este pierduta in producerea singlet/triplet a colorantului si totusi pierderea energiei in colorant nu este suficienta ca sa excite oxigenul. Astfel, in general numai starea singlet 1Δg este usor accesibila.
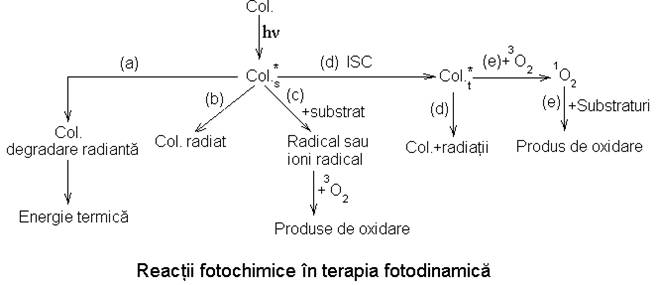
Asa cum s-a mentionat mai inainte, lumina rosie a fost utilizata aproape exclusiv pentru PDT pana acum. Lumina ultravioleta este nepotrivita deoarece penetreaza tesuturile si are potential pentru initiatori carcinogeni. Lumina rosie poate avea un avantaj asupra luminii vizibile in aceea ca ea furnizeaza un efect termic moderat [(a) in schema de mai sus.] Pe de alta parte Hpd si Fotoporfirina II absorb putin lumina la lungimi de unda >600 nm. Cercetari de a doua generatie cu procese la fotosensibilitate au fost concentrate in prima etapa asupra absorbantei fotosensibile de lungime de unda mare. Un numar mare de noi porfirine si diverse tetraazo-anulene au fost sintetizate de Schian si colaboratori (1990) si altii. Lucrarile sumarizate de Schian si colaboratori includ sisteme clasice de la clorofila, benzoclorine, purpurine si alte ciclic tetra-si pentapiroli, cu si fara un metal central. Compusii cu maxim de absorbtie pana la 752 nm au fost testati.
Deoarece actazo-anulenele spre exemplu ftalocianinele, de asemenea genereaza oxigen singlet in randamente cuantice semnificative, au fost investigate intensiv in aplicarea lor in PDT.
Tetrasulfoftalocianinele de zinc in stare monomera absorb la 677 nm de 48 de ori mai puternic decat un dimer al porfirinei. Randamentele mari in triplet si tripletul cu viata lunga sunt obtinute ca Zn2+, Al3+ si Ga3+ dar nu cu ionii metalici paramagnetici (Cu2+ etc.). Mai tarziu starea de triplet se stinge.
Complecsii naftalocianinelor cu siliconi au fost investigate de Firey si colaboratori (1988a), grupul lui von Lier (1990), Rodgers (1990) si altii. Un exemplu este urmatorul:
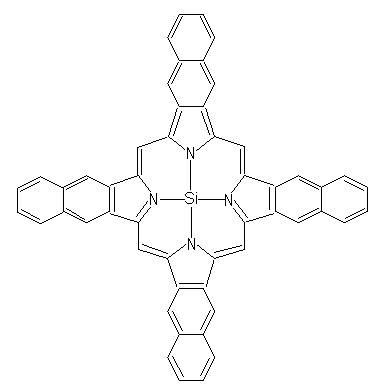
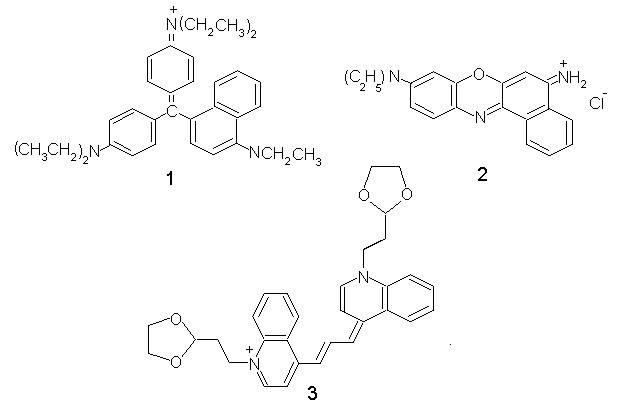
Toti fotosenzitorii in prealabil discutati sunt anioni sau neutri in conditii biologice. Colorantii cationici, totusi, de asemenea au efecte PDT. Investigatiile preclinice indica ca multi fotosensibilizatori anionici ataca vasele de sange si compusii cationici pot fi mai selectivi pentru celulele carcinoma si melanoma dar distruge mitoclondria. Cercetarile sunt acum in progres asupra terapiei multisenzitorilor unde sensibilizatorii ca Fotoporfirina II sau naftocianinele sunt administrate impreuna cu colorantii cationici ca de exemplu colorantul triarilmetanic Victoria Blue Bo (1), colorantul benzofenoxazinic Nile Blue A (2) si colorantul Kriptoaminic N,N'-bis(2-etil-1,3-dioxolan)-Kriptocianinic (EDKC) (3).
Un scurt rezumat pentru chimisti a fost publicat de Bergh (1986).
In ciuda rapidei dezvoltari in PDT, este totusi recomandat ca o introducere. Pentru un chimist colorist, este de asemenea fascinant citirea lucrarilor care au fost publicate in comun de chimisti (sinteza si selectia senzorilor potentiali), fizicieni,ingineri electricieni (echipament laser si fibre optice pentru aplicatii endoscopice) si doctori. Un exemplu este articolul lui Monnier si colaboratorii (1990) in care fotodetectia si PDT ai carcinomurilor de esofag si traheo-bronhice sunt discutate. Cel mai coprehensiv rezumat al tuturor aspectelor in cartea editata de Gamer (1990) mentionata deja.
|
Politica de confidentialitate |
| Copyright ©
2024 - Toate drepturile rezervate. Toate documentele au caracter informativ cu scop educational. |
Personaje din literatura |
| Baltagul caracterizarea personajelor |
| Caracterizare Alexandru Lapusneanul |
| Caracterizarea lui Gavilescu |
| Caracterizarea personajelor negative din basmul |
Tehnica si mecanica |
| Cuplaje - definitii. notatii. exemple. repere istorice. |
| Actionare macara |
| Reprezentarea si cotarea filetelor |
Geografie |
| Turismul pe terra |
| Vulcanii Și mediul |
| Padurile pe terra si industrializarea lemnului |
| Aparatul locomotor |
| Peptide |
| FARINGELE |
| Sistemul tegumentar |
| SISTEMUL MUSCULAR |
| Anatomia si fiziologia aparatului cardiovascular |
| MICROBIOLOGIA si Importanta microbiologiei |
| Aportul si eliminarea apei |
| Termeni si conditii |
| Contact |
| Creeaza si tu |