
FACULTATEA DE CHIMIE INDUSTRIALA SI INGINERIA MEDIULUI
PROIECT DE DIPLOMA
TEHNOLOGIA ACIDULUI GLUTAMIC
SA SE PROIECTEZE O INSTALATIE DE FABRICARE, IN FLUX CONTINUU PRIN PROCEDEU FERMENTATIV, A ACIDULUI GLUTAMIC DE PURITATE 95%, CU O CAPACITATE DE 54KG/SARJA
SCURT ISTORIC
In structura substantelor proteice au fost identificati frecvent 20 de aminoacizi denumiti din acest motiv aminoacizi naturali. Alaturi de ei pot sa apara si asa numitii 'aminoacizi ocazionali', care fie ca apar in cantitati mai mici, fie ca fac parte numai din compozitia unor anumite proteine, fie ca se gasesc sub forma libera in tesuturile animale si vegetale. Aminoacizii naturali sunt compusi organici cu functiuni mixte care contin gruparea functionala carboxil (-COOH) si gruparea functionala amino (-NH2). Dintre acesti aminoacizi, noua nu pot fi sintetizati de catre organismele animale, ei trebuie introdusi in organism o data cu hrana.[ 3 ]
Cele patru gusturi fundamentale sunt: acru, amar, dulce si sarat. Pe langa acestea gastronomia japoneza a adaugat 'umami', gustul de carne. Acesta este dat de monoglutamatul de sodiu, aroma artificiala comercializata uzual. Acidul L-glutamic a fost obtinut in anul 1866 de catre Ritthansen prin hidroliza glutenului, iar in 1890 Wolff realizeaza sinteza acidului D si L-glutamic din acid levulinic. Mai tarziu(1908), Ikeda obtine acid L-glutamic prin hidroliza la cald a unor alge(laminaria) si constata ca acestui acid i se datoreaza gustul placut al algei.[ 6 ]
Acidul glutamic, ca toti aminoacizii este o substanta amfotera, care dizolvata in apa, poate forma anioni si cationi alaturi de ioni de H+ si HO- eliberati simultan. Avand grupari aminice si carboxilice formeaza ioni bipolari prin neutralizare interna. Solubilitatea sa creste o data cu deplasarea pH-ului in mediu acid sau bazic. In mediu acid acidul glutamic este solubil in apa sub forma de clorhidrat, iar in mediu bazic sub forma de sare.[ 1 ] Denumirea sa provine de la glutenul cerealelor(graului), din care a fost extras prima data. Se gaseste in cantitati mai mari sau mai mici in diverse alte subproduse proteice :
9.5% in γ-globulina serica umana ;
12.2% in albumina serica bovina ;
20% in miozina ;
18.2% in α-cazeina ;
22% in zeina porumbului ;
peste 25% in glutenul graului
mari cantitati in proteinele de soia.[ 4 ]
PARTEA I : CONSIDERATII TEORETICE
I.1. Fisa tehnica a produsului
Denumire chimica :
- IUPAC: acid 2-aminopentadioic ;
- acid -aminoglutaric ;
Denumire comerciala : acid glutamic
Formula moleculara : C5H9NO4
![]() - forma
desfasurata : COOH-CH2-CH2-CH-COOH
- forma
desfasurata : COOH-CH2-CH2-CH-COOH
![]()
![]()
![]() NH2
NH2
Masa moleculara : M= 147,13g/mol;
Densitate: ρ= 1,4601g/cm3;
Punct de topire: pt= 225-227°C;
Constante de disociere : pKa : 2,16
4,15
9,58
PH-ul izoelectric: 3,22
Solubilitatea in apa: - in mediu acid este solubil in apa sub forma de clorhidrat ;
- in mediu bazic este solubil sub forma de sare ;
Solubilitatea in alcool etilic: - insolubil in alcool etilic absolut si in eter[ 2 ]
Aspect : produs solid, sub forma unei pulberi albe, cristaline cu gust acru si fara miros.[ 1 ]
I.2. Metode de obtinere
Exista patru procese pentru producerea aminoacizilor: extractia, sinteza chimica, fermentatia si cataliza enzimatica. Fermentatia si cataliza enzimatica folosesc toate celulele: bacterii, drojdii si celule active componente(enzime).
Cu toate ca acum este posibila sinteza tuturor aminoacizilor naturali prin metode microbiologice, procesele fermentative care utilizeaza specii modificate genetic de inalta performanta isi gasesc un larg domeniu de aplicatie industriala numai pentru sinteza acidului L-glutamic si L-lisinei.
Pentru obtinerea acidului L -glutamic se folosesc trei grupe de metode[ 6 ]:
extractia din surse naturale ;
sinteze chimice ;
biosinteza.
Se folosesc lesiile de la fabricile de zahar, deseurile de la fabricile de amidon din grau sau porumb si deseurile de origine animala( caseina ), care se supun hidrolizei in vederea eliberarii acidului glutamic si apoi separarea lui.
Hidroloza acida a proteinelor( caseina, gluten) se realizeaza prin fierbere indelungata cu acid sulfuric( H2SO4) sau clorhidric(HCl) urmata de neutralizare cu hidroxid de calciu Ca(OH)2 pentru indepartarea acidului sulfuric sub forma de sulfat, iar dupa filtrarea sulfatului se indeparteaza ionii de calciu cu acid oxalic. Solutia apoasa se concentreaza la vid, iar dupa racire cristalizeaza cristalizeaza acidul L-glutamic care se purifica prin recristalizari repetate.
Un alt procedeu de fabricare care foloseste ca materie prima deseurile de la fabricile de zahar prin hidroliza alcalina duce la obtinerea acestui aminoacid. Prin acest procedeu se fabrica in Franta, anual, peste 3000 tone.[ 1 ]
2.Sinteza chimica :
Pentru obtinerea prin sinteza a acidului L-glutamic se foloseste metoda care utilizeaza ca materie prima acrilonitrilul. Prin sinteza, plecand de la acrilonitril s-au obtinut in anul 1963, 4800tone/an, iar in 1970 12000tone/an.[ 1 ]
|
|
Schema de principiu a acestui procedeu este Figura 1.
Figura 1: Sinteza chimica a acidului glutamic
In metodele de sinteza rezulta intotdeauna un racemic.
Biosinteza
Procedeul de biosinteza foloseste ca surse de carbon: - glucoza
- zahar
- amidon
- hidrolizate de amidon
- surse de azot( uree sau saruri de amoniu)
- microelemente
Pe aceste medii se cultiva microorganismul Micrococcus glutamicus, principalul producator al acidului L-glutamic. Deasemenea s-au studiat si alte surse de carbon: acidul acetic, esteri organici si hidrocarburi alifatice, la care se adauga surse de azot si saruri minerale. Cele mai bune rezultate s-au obtinut la utilizarea n-parafinelor cu 12-17 atomi de carbon. S-a plecat de la acidul α-ceto-glutaric, intermediar an ciclul Krebs, produs prin conversia zaharului si s-a supus procesului de transaminare. Enzima care catalizeaza aceasta reactie este mult raspandita in tesuturile animale, vegetale si microorganisme.[ 5 ]
![]()
![]()
![]() COOH COOH
COOH COOH
![]()
![]()
![]() NH3 + C=O + NADPH + H+ CH-NH2 + NADP+ + H2O
NH3 + C=O + NADPH + H+ CH-NH2 + NADP+ + H2O
![]()
![]()
![]() CH2 CH2
CH2 CH2
![]()
![]() CH2 CH2
CH2 CH2
![]()
![]() COOH COOH
COOH COOH
acid α-cetoglutaric acid glutamic
Plecand de la mecanismul de biosinteza au fost propuse doua procedee:
intr-un singur stadiu, in care acidul glutamic este produs direct in biomasa de catre un singur tip de microorganisme;
in doua stadii, se obtine mai intai acidul α-cetoglutaric care este transformat in acid glutamic, fie cu ajutorul unui alt microorganism, fie prin metode enzimatice.[ 1 ]
I.3. Proprietati fizice
a-aminoacizii sunt substante de culoare alba, cristaline, sunt relativi stabili la caldura, in general descompunandu-se la 250-300°C. Aminoacizii sunt insolubili in solventi nepolari si de obicei nu sunt foarte solubili in cei polari; singurii aminoacizi care sunt solubili in alcool sunt hidroxiprolinele si prolinele. Solubilitatea in apa depinde de pH, ea fiind minima in punctul izoelectric. Solubilitatea minima in punctul izoelectric ajuta la purificarea si recristalizarea aminoacizilor. Desi unii aminoacizi au gust dulceag, nici unul din ei nu are 'glutame taste' (gustul glutamic) sau proprietatea specifica aromei asociata cu acidul glutamic.[ 17 ]
Stereochimie:
Cu exceptia glicerinei, toti aminoacizii naturali au o compozitie chirilica si ocupa 2 forme enantiomerice. Prefixele L si D redau configuratia absoluta, legata de α-carbon cu referire la forma stereochimica si relatia lor cu L si D glicerinaldehida. Determinarea polarimetrica a rotatiei specifice [ α ]tD poate fi folosita pentru a diferentia cei 2 enantiomeri si puritatea optica.
![]()
![]() COOH COOH
COOH COOH
![]()
![]()
![]()
![]()
![]() H2N H H NH2
H2N H H NH2
R R
L - aminoacid D - aminoacid
Acidul glutamic se prezinta sub forma unei pulberi albe, cristaline, un aminoacid care in conditii normale are gust acru. Conform datelor din literatura, principalele proprietati ale acidului glutamic sunt: - rotatia specifica in apa : [ α ]tD = 11.5;
- solubilitatea in apa( g/100ml apa): 0.864
Doua benzi IR sunt caracteristice aminoacizilor la 1560-1600 cm-1 (-COO) si
3070 cm-1(-NH3). Aceste benzi sunt 'probe' pentru a determina natura bipolara a unui aminoacid.
I.4. Proprietati chimice
Aparitia in microorganisme a acidului glutamic este o consecinta a degradarii oxidative a zaharurilor conform ciclului Krebs. Acidul α-cetoglutamic sub actiunea glutamat-dehidrogenazei si a ionilor NH4+ da acidul L(+)-amino-glutaric, acidul glutamic natural :
+ NH3
![]()
![]() HOOC-CH2-CH2-CO-COOH HOOC-CH2-CH2-CH(NH2)-COOH
HOOC-CH2-CH2-CO-COOH HOOC-CH2-CH2-CH(NH2)-COOH
- NH3
Acidul glutamic si glutamina sunt implicati in numeroase reactii catabolice, conducand la biosinteza unui numar mare de substante celulare. Acidul participa la reactii de transaminare a cetoacizilor, facand legatura cu metabolismul glucidelor prin acidul α-cetoglutaric, un intermediar al ciclului Krebs. Biosinteza acidului glutamic se petrece la majoritatea organismelor prin aminarea acidului α-cetoglutaric, sub actiunea L-glutamat dehidrogenazei localizata in citoplasma.
NH3 + Acid a-cetoglutaric+NADPH+H Acid glutamic +NADP+ + H20
Acidul glutamic dehidrogenat, prezent in drojdie si bacterii, in colaborare cu coenzima I (plante) sau coenzima II (drojdie), transforma L(+) acidul glutamic in a-cetoacid glutamic:
HOOC-(CH2)2 -CH(NH2)COOH HOOC(CH2)2COOH NH4
Glutamina este sintetizata din acidul glutamic, sub actiunea glutamin sintetazei. [5]
![]()
![]() NH3 + Acid glutamic + ATP Glutamina
+ ADP + H3PO4
NH3 + Acid glutamic + ATP Glutamina
+ ADP + H3PO4
Intermediar se formeaza acid g - glutamic fosforic:
|
|
|
|
In afara reactiei de transaminare, acidul glutamic si glutamina mai poate suferi si alte transformari. De exemplu biosinteza prolinei si hidroxipolinei pornesc de la acidul glutamic :
Transformarea acidului glutamic in prolina implica reducerea gruparii carboxil din pozitia g la o aldehida, urmata de formarea unei baze Schiff interne prin a carei reducere se obtin moleculele de prolina. In fond prolina se sintetizeaza din acid glutamic prin parcurgerea in sens invers a reactiei din calea metabolica degradativa, dar evident cu anumite diferente[ 3 ]. Sinteza microbiologica a aminoacizilor este o biosinteza ce utilizeaza intregul complex enzimatic al microorganismelor.
Cataliza enzimatica, dimpotriva utilizeaza enzime specifice sau sisteme enzimatice. Cataliza enzimatica este avantajoasa in cazurile in care L-aminoacizii pot fi produsi din precursori necostisitori cu specificitate mare intr-un proces cu operare continua. Hidroliza stereospecifica cu cataliza in prezenta acilazei a N-acetil -D, L-aminoacid este utilizata pentru a sintetiza alanina, valina, metionina, fenilalanina si triptofanul.
Enzima este reciclata fie prin legarea ei de catre un purtator si desfasurarea reactiei intr-o coloana [ 12 ] sau intr-un reducator inelar, implicand un filtru cu membrana pentru a retine enzima dizolvata in sistem [ 7 ].
Rezolutia enzimatica poate fi competitiva numai atunci cand este cuplata cu o racemizare eficienta, fie catalitica, fie enzimatica.
|
|
Conversia enzimatica a a-oxo-aminoacizilor la a-aminoacizi, de exemplu, folosind dehidrogenaze L-aminoacizi specifici, cofactori de regenerare sau folosind transaminaze, este destul de promitatoare, avand in vedere ca aceste sisteme enzimatice s-au dovedit a fi stabile in procese continue.
Acidul glutamic se poate obtine si din derivati ai acidului malonic; esterii acidului malonic pot fi alchilati. [ 14 ]
|
|
I.5. Utilizari
Folosit initial numai in industria alimentara drept aromatizant(in supele concentrate), acidul glutamic este astazi si un valoros medicament utilizat in tratamentul unor afectiuni ale sistemului nervos central. Acidul glutamic este necesar pentru dezvoltarea lactobacililor, amestecul acestui acid si 'asparagin' inlocuiesc amida nicotinei in dezvoltarea Bacteriei dysenteriae si celelalte organisme. Acidul glutamic are 10 celule diferentiale, acestea activeaza metoda de 'invatare' pentru sobolani, face parte din reactiile de transaminare. Este benefica in tratamentul 'petit mal' si atacuri nervoase. Sarea din acidul glutamic este unica, aroma din carne este perceptibila in 3000 parti higroscopice.[ 14 ]. Acidul glutamic este prezent intr-o mare varietate de alimente ca: peste, oua, carne si este responsabil pentru unul din cele 5 gusturi principale ale omului.
Productia acidului glutamic pentru comercializarea gluten monosodiului utilizeaza mai multe proteine hidrolizate, care sunt necesare pentru producerea altor aminoacizi individuali. Asadar este folosit in industria alimentara si farmaceutica sub forma de saruri de sodiu, pentru aromatizarea supelor concentrate, stimularea secretiei gastrice, ameliorarea activitatii sistemului nervos central si a ficatului cirotic.
II.1. Justificarea procesului tehnologic
Din cele trei metode de obtinere a acidului glutamic : extractia din surse naturale, sinteze chimice si biosinteza, prima se obtine la un randament scazut( se consuma 12 tone gluten din grau sau 18 tone gluten din soia pentru o tona acid, iar instalatiile mari utilizate fac ca acest procedeu sa fie scump, deci putin utilizat. In urma sintezelor chimice intotdeauna rezulta un racemic, iar separarea izomerilor ridica multe probleme tehnologice care au ca efect scumpirea produsului sintetizat, deci nici metoda ce utilizeaza ca materie prima acrilonitrilul nu este cea mai indicata.
Procedeul de biosinteza este cel mai utilizat, el permite obtinerea produsului la un pret de cost mult mai mic, comparativ cu celelalte metode. Asadar, el este cel mai rentabil. Productia acidului L-glutamic prin procedeul de biosinteza a crescut mereu, ajungand in anul 1966 sa reprezinte 84% din productia totala, iar in anul 1970 peste 88%. Odata cu cresterea acestei productii au scazut costurile acidului L-glutamic cu peste 60%.
Randamentele obtinute in prodesele de fermentatie directa variaza intre 24-54% fata de continutul de zahar, iar concentratia finala a acidului L- glutamic in biomasa e cuprinsa intre 5-80g/l, functie de compozitia mediului de cultura.[ 1 ]
II.2. Mecanismul biochimic al procesului
Procedeul cu cea mai mare pondere industriala de obtinere a acidului glutamic este biosinteza. Aparitia in microorganisme a acidului glutamic este o consecinta a degradarii oxidative a zaharurilor conform ciclului Krebs. Acidul α-cetoglutamic sub actiunea glutamat dehidrogenazei si a ionilor de amoniu da acidul L(+) α-amino-glutaric, adica acidul glutamic natural:
|
|
Acidul glutamic este un factor de transaminare. Sub actiunea glutamat transaminazelor actioneaza asupra cetoacizilor corespunzatori cu formarea cisteinei, glicinei, leucinei, tirozinei transformandu-se in acid cetoglutaric. Se acumuleaza in unele microorganisme prin legarea la acidul folic a 3 resturi glutamil( Corynebacterium) sau 7 resturi( drojdia de bere), probabil forma de depozitare a reactivului de transaminare. Procedeul de transaminare este reprezentat astfel :
|
|
Acidul glutamic este unul din cei mai importanti donori de grupe aminice in procesul de transaminare la nivel celular, favorizand aparitia altor aminoacizi.
II.3. Caracterizarea materiilor prime
Melasa [17]
Compozitia chimica a melasei variaza in functie de o serie de factori, printre care se mentioneaza calitatea sfeclei, procesul tehnologic aplicat in fabricile de zahar, etc.
Compozitia melaselor este urmatoarea (in %)
-polarizatie directa 43,2-54,00
-brix refractometric 1:1 75,5-86,40
-puritate aparenta 56,4-66,85
-umiditate 14,6-29,15
-zahar invertit 0,11-1,80
-CaO (cu sol sapun) 0,14-1,37
-cenusa sulfitica 7,60-12,33
-azot total 1,34-2,41
-S02 0,01-0,08
-pH 6,0-8,56
Caracteristicile termofizice sunt date in functie de temperatura astfel la: t=20°, r
Extractul de porumb (siropul de porumb)
Se obtine din apele de inmuiere a cerealelor (mai ales porumb) din procesul de obtinere a amidonului industrial si a fungilor de porumb, prin concentrare la cald, filtrare si sterilizare cu bioxid de sulf. Este o sursa foarte echilibrata de C,N,S, saruri minerale.
Utilizarea sa a produs o spectaculoasa marire de randament in biosinteza penicilinei (1943) si s-a impus apoi in intreaga industrie de biosinteza, ca ingredient principal al mediilor de cultura. Este un lichid vascos, brun, cu un continut de cca 4% azot aminic, corespunde unei cantitati de 40-
42% proteine, formata din 25% alanina, arginina si acid glutamic, fiecare cu cate 8%, leucina 6%, fenil-alanina 2%, prolina 5%, izoleucina, valina si treonina cate 3,5% metionina si cistina cate 1%.
Mai contine 15-30% acid lactic, 3% fosfor, 1% calciu si 15% potasiu, vitaminele B2, B6, PP, biotina, pantotenat, gume polizaharidice. [ 6 ]
. Micrococcus glutamicus
Practic toate microorganismele produc acid glutamic, dar putine in cantitati suficient de mari si in conditii selective. Mai productive sunt Brevibacterium amynophylum, diverse varietati de Micrococcus glutamicus si Carynebacteryum glutamicum, dar si Esteria Coli, Bacillus subtilis, etc.
Cultivarea Micrococcus glutamicus pe un mediu de glucoza 10% necesita o concentratie optima de biotina de 2,53%
Marirea si reducerea acestei concentratii face ca raportul intre cantitatea de aminoacizi continuti intra si extra celular sa varieze de la 12 la 0,3.
Pe medii naturale sarace in biotina cantitatea de aminoacizi trecuti in mediu este si de 200 de ori mai mare decat cele bogate in aceasta vitamina.
Componentele naturale si vegetale ale mediilor de cultura contin mari cantitati de biotina. Se impune folosirea unui mediu de cultura sintetic si folosirea inhibatorului natural al biotinei-alcoolul palmitic. [4]
. Ureea [17]
Formula moleculara : CH4 N2 O;
Formula structurala :
|
|
Masa moleculara relativa: 60,05
Aspect : cristale fine
Culoare : alba
Umiditate, %max: 0,2
Acid sulfuric[***17]
Formula moleculara: H2SO4
Masa moleculara: 98,08
Puritate: 96%
Aspect: lichid uleios, limpede sau opalescent
Culoare : conform STAS 9482-74
Densitate : 1,835 g/cm3
Acid clorhidric[***17]
Formula moleculara : HCl
Masa moleculara relativa : 36,5
Puritate : 32%
Aspect : lichid transparent
Culoare : incolor, galben-verzui
. Saruri minerale [17]
Experinetele privitoare la utilizarea ionilor anorganici in multiplicarea bacteriilor s-au facut prin cantarirea cantitatii de biomasa rezultata in mediu, din care un ion este absent.
|
Nr. crt. |
Denumire |
Conc % |
M g/mol |
d g/cm |
Punct de topire |
Punct de fierbere |
Caracteristici generale |
|
1. |
| ||||||
|
KH2 P04 |
solubil in apa, insolubil in alcool |
||||||
|
3. |
(NH4)2 S04 |
se prezinta sub forma de cristale de culoare alb-galbuie pana la portocaliu; u=0,6% |
|||||
|
ZnCl |
Carbunele activ este folosit ca material de umplutura pentru a retine mai usor catalizatorul de filtrare.
Se obtine din mangal sau turba prin tratarea la cald cu vapori de apa sau rumegus de lemn prin impregnare cu ZnCl2 sau H2 P04 si calcinare ulterioara.
|
|
II.4. Schema fluxului tehnologic
II.5. Descrierea procesului tehnologic
Procesul tehnologic de obtinere a acidului glutamic concentrat cuprinde urmatoarele etape: pregatirea si sterilizarea mediului de cultura, fermentatie, acidulare-coagulare, purificare-filtrare, concetrare, acidulare-cristalizare, centrifugare si uscare.
Pregatirea si sterilizarea mediului de cultura
In reactorul din pozitia 1 se introduc cu ajutorul unei palnii 615 kg melasa diluata 10%o si 100 de kg extract de porumb, se sterilizeaza, dupa care sunt trimise cu ajutorul unei pompe in fermentatorul din pozitia 7 unde de altfel sunt aduse si celelalte materii prime (fosfat mono si dipotasic de puritate 99%, sulfat de amoniu 99%, clorura de zinc 98%) si uree 89%) aflate in vasele de masura din pozitiile 2, 3, 4 si 5.
Mediul de cultura trebuie sa asigure sursa de carbon (glucoza) atat in faza de crestere a masei celulare cat si in faza de elaborare a acidului 1-glutamic. Deasemenea folosind ureea ca sursa de azot si ca agent de corectare pH-ului se obtin randamente mari in acid glutamic.
Fermentatia
Fermentatia in inoculator dureaza 18-24 de ore, iar in intermediar 12-16 ore.
Fermentatia in fermentatorul de regim se realizeaza la un pH=7,5-8,5; t=29-31° C cu o intensa aerare si agitare; la sfarsitul procesului continutul de zahar este de 0,8-0,9%.
Acidulare-coagulare
Dupa terminarea fermentatiei, biomasa se aciduleaza cu acid sulfuric 96%, la pH 6,5, dupa care se incalzeste la 70-75° C timp de o ora.
In tot timpul incalzirii este absolut necesar ca pH-ul sa fie mai mic decat 7 pentru a evita degradarea acidului 1-glutamic.
Purificare-filtrare
Dupa terminarea coagularii biomasei i se adauga 3 kg de carbune activ, apoi se raceste la 50-55° C si este trimisa cu ajutorul unei pompe centrifuge (8) la un filtru presa (9).
Are loc apoi concentrarea la vid urmata de cristalizare.
■ Concentrare
Filtratul de biomasa purificat este colectat in rezervorul din pozitia 10. De aici este trimis cu ajutorul unei pompe in rezervorul (11), unde se corecteaza pH-ul la 6,5 si se concentreaza sub vid la 50-55° C, pana ce densitatea ajunge la 1.20 g/cm3 .
■ Acidulare-cristalizare
Solutia obtinuta la concentrare este trimisa in cristalizorul (12), unde se aciduleaza cu HCl 32% pana la punctul izoelectric al acidului glutamic, dupa care se raceste lent pana la 10-12° C pentru cristalizare.
■ Centrifugare
Masa cristalina obtinuta se filtreaza pe centrifuga din pozitia (13), dupa care este trimisa in vasul de purificare din pozitia 14 (se dizolva in apa, se adauga o solutie de NaOH pana la pH 6,5 si carbune activ), dupa care se incalzeste la 70° C si se filtreaza pe filtrul presa (9).
Solutia purificata rezultata la filtrare se trimite in cristalizatorul din pozitia (20), se aciduleaza pana la pH 3,2 (punctul izoelectric al acidului 1-glutamic) si se raceste la 10-12° C timp de 24 de ore.
Cristalele de acid glutamic pur se separa prin centrifugare (pozitia 21) si se spala cu apa rece pentru indepartarea totala a ionilor de clor.
Uscare
Dupa ce cristalele de acid glutamic au fost spalate cu apa rece, se usuca in uscatorul din pozitia 22. Uscarea se face cu aer a carui temperatura la intrare in uscator este cuprinsa intre 100-105° C.
1.Pregatirea si sterilizarea mediului de cultura (randament 100%)
MATERIALE INTRATE
|
Nr. crt. |
Denumire material |
Conc |
Cantitatea(kg) tehnic pur |
Nr. kmoli |
Volum (l) |
Observatii M(kg/kmol);d(kg/m3) |
|
|
I. |
Melasa diluata |
10% |
615 |
615 |
0,1 |
600 |
d=l,025 |
|
Extract de porumb |
- |
100 |
100 |
161,89 |
d=0,6176 |
||
|
3. |
Fosfat dipotasic |
99 |
1,5 |
1,49 |
0,0086 |
- |
M=173 |
|
4. |
Fosfat monopotasic |
M=136 |
|||||
|
Sulfat de amoniu |
M=132 |
||||||
|
Clorura de zinc |
98 |
7 |
6,86 |
0,0504 |
M=136 |
||
|
7. |
Uree |
89 |
5,6 |
4,98 |
0,083 |
M=60 |
|
|
TOTAL |
734,1 | ||||||
MATERIALE IESITE
|
Nr. crt. |
Denumire material |
Conc % |
Cantitatea(kg) tehnic pur |
Nr. kmoli |
Volum (l) |
Observatii M(kg/kmol);d(kg/m3) |
|
|
1. |
Masa sterilizata |
- |
734,1 |
800 | |||
|
TOTAL | |||||||
2.Fermentatia (randament 60%)
MATERIALE INTRATE
|
Nr. crt. |
Denumire material |
Conc % |
Cantitatea(kg) tehnic pur |
Nr. kmoli |
Volum (l) |
Observatii M(kg/kmol);d(kg/m3) |
|
|
Masa sterilizata | |||||||
|
Suspensie de spori (MG.) |
- |
1,5 |
1,5 |
- |
1,39 |
d=l,08 |
|
|
Uree |
M=60 |
||||||
|
TOTAL | |||||||
MATERIALE IESITE
|
Nr. crt. |
Denumire material |
Conc % |
Cantitatea(kg) tehnic pur |
Nr. kmoli |
Volum (l) |
Observatii M(kg/kmol);d(kg/m3) |
|
|
1. |
Biomasa |
- |
- |
- |
- |
- |
|
|
a)acid glutamic |
- |
- |
55 |
0,37 |
- |
M=147 |
|
|
b)zaharuri nereactionate |
- |
- |
40 |
- |
- |
- |
|
|
c)apa |
- |
- |
553,5 |
30,75 |
553,5 |
M=18 |
|
|
d)biomasa epuizata | |||||||
|
e)impuritati chimice |
16,22 | ||||||
|
TOTAL | |||||||
3.Acidulare-coagulare (randament 100%)
MATERIALE INTRATE
|
Nr. crt. |
Denumire material |
Conc % |
Cantitatea(kg) tehnic pur |
Nr. kmoli |
Volum (l) |
Observatii M(kg/kmol);d(kg/m3) |
|
|
1. |
Biomasa |
- |
- |
- |
- |
- |
|
|
2. |
Acid sulfuric |
96% |
1,8 |
1,72 |
0,01 |
0,98 |
d=l,835 M=98 |
|
Total | |||||||
MATERIALE IESITE
|
Nr. crt. |
Denumire material |
Conc % |
Cantitatea(kg) tehnic pur |
Nr. kmoli |
Volum (l) |
Observatii M(kg/kmol);d(kg/m3) |
|
|
1. |
Biomasa acidulata | ||||||
|
Total | |||||||
4.Purlficare-filtrare (randament 99%)
MATERIALE INTRATE
|
Nr. crt. |
Denumire material |
Conc % |
Cantitatea(kg) tehnic pur |
Nr. kmoli |
Volum (l) |
Observatii M(kg/kmol); d(kg/m3) |
|
|
1. |
Biomasa acidulata |
- | |||||
|
2. |
Carbune |
- |
3 | ||||
|
Total | |||||||
MATERIALE IESITE
|
Nr. crt. |
Denumire material |
Conc % |
Cantitatea(kg) tehnic pur |
Nr. kmoli |
Volum (l) |
Observatii M(kg/kmol);d(kg/m3) |
|
|
1. |
Filtrat biomasa purificata |
495,14 | |||||
|
a)acid glutamic |
53,9 |
M=147 |
|||||
|
b)zaharuri nereactionate | |||||||
|
c)apa |
M=18 |
||||||
|
d)impuritati | |||||||
|
Reziduu |
386,66 | ||||||
|
a)rest de acid glutamic |
1,1 | ||||||
|
b)rest de zahar nereactionat |
0,8 | ||||||
|
c)carbune si biomasa epuizata |
232,0 | ||||||
|
TOTAL |
881,80 | ||||||
5..Concentrare (randamente 100%)
MATERIALE INTRATE
|
Nr. crt. |
Denumire material |
Conc % |
Cantitatea(kg) tehnic pur |
Nr. kmoli |
Volum (l) |
Observatii M(kg/kmol);d(kg/m3) |
|
|
1. |
Filtrare biomasa |
- |
- |
420 | |||
|
a)acid glutamic |
53,9 |
0,366 |
M=147 |
||||
|
b)zaharuri nereactionate |
Mglu=180 |
||||||
|
c)apa |
M=18 |
||||||
|
d)impuritati |
3,2 | ||||||
|
TOTAL | |||||||
MATERIALE IESITE
|
Nr. crt. |
Denumire material |
Conc % |
Cantitatea(kg) tehnic pur |
Nr. kmoli |
Volum (l) |
Observatii M(kg/kmol);d(kg/m3) |
|
|
1. |
Acid glutamic conc. |
215,6 |
M=147 |
||||
|
a)acid glutamic |
25 |
53,9 |
0,36 | ||||
|
b)zaharuri nereactionate | |||||||
|
c)apa |
M=18 |
||||||
|
d)impuritati | |||||||
|
Vapori de apa | |||||||
|
TOTAL | |||||||
6.Acidulare-cristalizare (randament 100%)
MATERIALE INTRATE
|
Nr. crt. |
Denumire material |
Conc |
Cantitatea(kg) tehnic pur |
Nr. kmoli |
Volum (l) |
Observatii M(kg/kmol);d(kg/m3) |
|
|
1. |
Concentratie acid glutamic |
25 |
215,6 |
53,9 |
0,41 |
M=131 |
|
|
2. |
Acid clorhidric conc. |
32 |
1,66 |
0,53 |
0,014 |
1,4 |
d=l,19 M=36,45 |
|
TOTAL | |||||||
MATERIALE IESITE
|
Nr. crt. |
Denumire material |
Conc % |
Cantitatea(kg) tehnic pur |
Nr. kmoli |
Volum (l) |
Observatii M(kg/kmol);d(kg/m3) |
|
|
Suspensie de acid glutamic | |||||||
|
a)acid glutamic |
M=131 u=20 |
||||||
|
b)impuritati | |||||||
|
c)alte componente | |||||||
|
d)apa | |||||||
|
TOTAL | |||||||
7.Centrifugare (randament 95%)
MATERIALE INTRATE
|
Nr. crt. |
Denumire material |
Conc |
Cantitatea(kg) tehnic pur |
Nr. kmoli |
Volum (l) |
Observatii M(kg/kmol);d(kg/m3) |
|
|
Suspensie de acid glutamic | |||||||
|
a)acid glutamic |
80 |
67,4 |
53,9 |
0,41 | |||
|
b)impuritati | |||||||
|
c)alte componente |
39,73 | ||||||
|
d)apa | |||||||
|
TOTAL | |||||||
MATERIALE IESITE
|
Nr. crt. |
Denumire material |
Conc % |
Cantitatea(kg) tehnic pur |
Nr. kmoli |
Volum (l) |
Observatii M(kg/kmol);d(kg/m3) |
|
|
1. |
Acid glutamic |
80 |
67,4 |
51,2 |
0,41 |
u=20 |
|
|
Lichid de centrifugare | |||||||
|
TOTAL | |||||||
8.Uscare (randament 100%)
MATERIALE INTRATE
|
Nr. crt. |
Denumire material |
Conc |
Cantitatea(kg) tehnic pur |
Nr. kmoli |
Volum (l) |
Observatii M(kg/kmol);d(kg/m3) |
|
|
1. |
Acid glutamic |
80 |
67,4 |
51,2 |
0,41 |
M 147 |
|
|
TOTAL |
67,4 | ||||||
MATERIALE IESITE
|
Nr. crt. |
Denumire material |
Conc % |
Cantitatea(kg) tehnic pur |
Nr. kmoli |
Volum (l) |
Observatii M(kg/kmol); d(kg/m3) |
|
|
Acid glutamic |
M 147 |
||||||
|
Vapori de apa |
- |
13,5 | |||||
|
|
TOTAL |
67,4 | |||||
II.6.1.Randamentul total al procesului
|
Nr.crt. |
Faza procesului |
Randament pe faze |
|
Pregatirea si sterilizarea mediului de cultura |
h |
|
|
Fermentatie |
h |
|
|
Acidulare-coagulare |
h |
|
|
Purificare-filtrare |
h |
|
|
Concentrare |
h |
|
|
Acidulare-cristalizare |
h |
|
|
Centrifugare |
h = 95% |
|
|
Uscare |
h |
Randamentul total al procesului este:
h h h h h h h h h =100 x 60 x 100 x 99 x 100 x 100 x 95 x 100=5,6
h
II.6.2.Capacitatea totala a instalatiei
Se determina numarul de zile lucratoare dintr-un an, cu ajutorul relatiei:
z=zc -(znl+zsl, +zr), unde:
z - numarul de zile lucratoare
zc - numarul de zile calendaristice, zc =365 zile
znl - numarul de zile nelucratoare, znl =104 zile
zsl - numarul de sarbatori legale, zsl = 7 zile
zr- numarul de zile programate reparatiilor, zr=15 zile
z=365-( 104+7+15)=239 zile
Se considera ca se lucreaza in trei schimburi, a 8 ore fiecare. Se calculeaza numarul de sarje produse intr-un an.
Nan - numar sarje/an
Tsarja - timpul de realizare a unei sarje
24(h) - durata unei zile lucratoare (h)
Nan = 24·239/25=229,44 sarje/an
Capacitatea instalatiei: C=Nan ·Msarja, unde:
C = capacitatea instalatiei ; MSarja =masa unei sarje
C=229,44 ·53,9=12366,8kg/an
|
|
II.6.3. Graficul timpului de lucru
Utilajul principal este un reactor cu amestecator IMPELER-Rlp
Caracteristici:
|
Tipul volum util |
Nr desen |
Presiune nominala, Kgf/cm2 |
Volum 1 |
Suprafata de shimb caloric m2 |
Cleme de strangere |
Electromotor kw; rot/min |
Reductor |
Robinet de golire Dn |
Greutate kg |
Spatiu de manevrare mm |
||
|
vas |
mantaa |
vas |
manta |
m2 |
Dn | |||||||
|
Rlp 800 |
1177- |
4 |
6 |
1000 |
100 |
3,60 |
52xM24 |
4: 1500 |
RSV2; 4,5kw; l:25 |
80/50 |
2040 |
1150 |
|
Tip/volum util, 1 |
d1 |
d2 |
H |
h1 |
h2 |
h3 |
h4 |
h5 |
h6 |
h7 |
h8 |
c |
m |
n1 |
n2 |
n3 |
L1 |
L2 |
L3 |
|
Rlp800 |
1000 |
1100 |
3670 |
1700 |
1150 |
525 |
260 |
1080 |
450 |
590 |
- |
75 |
656 |
400 |
350 |
290 |
1568 |
800 |
900 |
|
Tip/volum util, 1 |
R1 |
R2 |
R3 |
R4 |
R5 |
R6 |
R7 |
R8 |
R9 |
|
Rlp 800 |
250/80 |
150 |
2x80 |
80 |
3x50 |
80 |
2x40 |
40 |
40 |
Temperatura maxima in vas este de 150° C, iar in manta 165° C
Relatia de calcul care sta la baza calculului bilantului termic este:
Σ Qintrat= Σ Qiesit
1. Bilantul termic al reactorului chimic, expresie a conservarii energiei poate fi enuntat astfel:
Q1 + Q2 +Q3 = Q4 + Q5 + Q6, unde :
Q1 =cantitatea de caldura adusa in spatiul de reactie cu materiile prime sau reactantii respectivi.
Se calculeaza dupa relatia: Q1 = Σmi-cpi·ti = Σni··cpi·ti
Q2 =efectul termic al proceselor fizice si chimice.
Se calculeaza dupa relatia: Q2 = ni·∆Hri+Qprocese fizice
Q3 =cantitatea de caldura care trebuie schimbata cu agentul termic
Q3 =Qag
Q4 = cantitatea de caldura scoasa din spatiul de reactie cu produsii de reactie
Se calculeaza dupa relatia: Q4 = mf··cpf··tf= mf··Hf
Q5 = cantitatea de caldura necesara modificarii temperaturii aparatului
Se calculeaza conform relatiei: Q5 =map·cpap··∆tap unde :
map =greutatea aparatului (kg)
cpap =caldura specifica otelului (kj/kg °C)
∆tap =diferenta de temperatura (° C)
Q6 = suma pierderilor de caldura catre mediul ambiant prin suprafata laterala a aparatului si procesele fizice pentru care schimbul termic se manifesta in exterior.
Se calculeaza dupa relatia: Q6 = Qp +Qpf
Q6=(5÷10)Qag
2. Bilantul termic pentru etapa de concentrare :
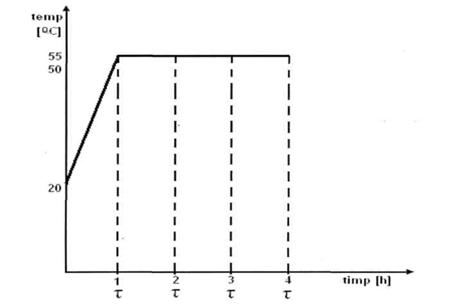
Bilantul termic se calculeaza pentru doua faze: pentru incalzire( 55°C) si pentru evaporarea apei( t=cst)
I. Bilantul termic pentru etapa I (incalzire) la 55° C este
QI1+ QI2 + QI3= QI4+ QI5+ QI6
Caldurile specifice se dau in tabele, pentru un numar mare de produse chimice. Sunt insa compusi organici la care nu se cunosc caldurile specifice. Calculul caldurilor specifice la substantele cu structura mai complexa se face in functie de caldurile atomice.
Se pot determina capacitatile calorice ale solidelor si lichidelor cu relatia Kopp :
Cp= Σni··ci (J/mol sau cal/mol·grd) unde:
ci =caldura atomica a elementului i, in J/atom-g·grd sau cal/atom-g·grd
ni=numarul atomilor de acelasi fel din molecula
QI1 = Σmi-cpi·ti
QI1= mAG · cAG ·ti + mGLU · cGLU -t1 + mapa·capa·t1
Notatii : AG-acid glutamic
GLU- glucoza
mAG=53,9 kg
cAG=5·1,8+9·2,3+4·4,0+1·2,7=48,4 J/mol·grd=48,4/0,147=329,25 J/kg·grd
|
|
mGLU=39,2 kg
cGLU=6·1.8+12·2,3+6·4,0=62,4/0,18=346,66 J/kg·grd
mapa=398,84 kg
capa=4190 J/kg·grd
QI1=53,9·329,25·20+39,2·346, 66·20+398·4190·20=34049,504 KJ
QI2=0
QI3=QIag
QI4=mag·cag·t2+mGLU·cGLU·t2+mapa·capa·t2
QI4=53,9·329,25·55+39,2·346,66·55+119,3· 4190·55=29216,144 KJ
QI5=mapa·cpapa·∆t=2040·0,50·35=35700 KJ
QI6=0,1·QI3
QI3=(QI4+QI5-QI -QI2)/0,9=34296,26 KJ
QI6=3429,62 KJ
qI=(QI3/t)=9,52 KJ/s
II. Bilantul termic pentru etapa II (evaporare a apei) este
QII1+ QII2 + QII3= QII4+ QII5+ QII6
QII1=QI4=29216,144 KJ
QII2=279,54·1086,2=303636,34 KJ
QII4= mag·cag·t2+mvap apa·rvap
QII4=215,6·329,25·55+279,54·2368,2·103=665910,87 KJ
QII5=0
QII3=( QII4+ QII5- QII1- QII2)/0,9=370064,87 KJ
QII6=0,1· QII3=37006,487 KJ
qII=(QII3/t)= 37006,487/(3·3600)=34,26 KJ/s
Comparand valorile fluxurilor pentru cele doua etape, se observa ca fluxul termic pentru etapa II este mai mare => dimensionarea reactorului se face pentru etapa de evaporare (la t = cst)
Potrivit datelor de dimensionare tehnologica[ 15 ], reactorul (de concentrare) dispune de o suprafata de schimb termic de 3,60 m2. Suprafata care se calculeaza din dimensionarea termica trebuie sa fie cel mult egala cu cea prevazuta tehnologic.
Suprafata de schimb termic se va calcula cu formula:
q= K·A·∆tmed, unde:
q=flux termic [W]
K=coeficient total de transmitere al caldurii [W/m2 ·K]
A-aria suprafetei de transfer de caldura [m2 ]
∆tmed =diferenta medie de temperatura intre agentul cald si agentul rece [K] q=34,26 KJ/s=34260 W
Calculul diferentei medii de temperatura:
abur 100° C ► 100° C (condens)
solutie 50° C ► 50° C
(masa de reactie)
![]() ∆tmed=(100+55)/2=77,5°C
∆tmed=(100+55)/2=77,5°C
Coeficientul total de transmitere al caldurii[ 15 ], K, se calculeaza cu formula:
|
|
abur - coeficient de transfer termic partial al aburului [W/m2 ·K]
sol - coeficient de transfer termic partial al solutiei [W/m·K]
Σr - rezistenta termica a peretului, inclusiv a depunerilor [m2·K/W]
~ Se admite abur =11600 W/m2 K
Calculul coeficientului partial de transfer termic in manta: sol In absenta datelor experimentale, amestecul de reactie se asimileaza cu apa.
Se calculeaza criteriul Grassoff si criteriul Prandtl si apoi, produsul lor.
Gr=(g·l3)/ν2·β·∆t, unde: g-acceleratia gravitationala [m/s2]; g=9,81m/s2
ν-vascozitatea cinematica [m2/s]; ν=η/ρ; ηapa=1000 Pa·s
|
|
ηapa=998 kg/m2[n1]
Pr(55˚C)=2,9; Prp(50˚C)=3,7
|
|
Gr·Pr=2,9·2,573=7,46·109. Deci se aplica urmatoarea formula:
Nu=255,53
λ(55sC)=32,4·10-2 W/m·K
sol=Nu· /Hm=255,53·32,4·10-2/0,525=157,69 W/m2·K
Nu-criteriul Nusselt
λ-coeficient de conductivitate termica a lichidului [W/m·K]
|
|
ol =grosimea peretelui; OL mm; e= grosimea peretelui; e = 1 mm
OL =conductivitatea termica a otelului; OL [W/m·K]
λe= conductivitatea termica a emailului; λe = 1,018 [W/m·K] r1=depuneri de lichid organic; r1=l/5800 [m2·K/W]
r2=depuneri din apa de racire; r2=l/5815 [m2·K/W]
r=0,04/46,5+0,001/1,018+1/5800+1/5815=1,412·10-3 [m2·K/W]
K= 1/(1/11600)+1,412·10-3+)1/157,69)=127,5
A=q/(K·∆tmed)=34260/(127,55·77,5)=3,46m2 < 23,60m2 (IUG Fagaras)
Aceasta conditie fiind verificata, dimensionarea reactorului corespunde cu cea prezentata conform IUC Fagaras.[ 20 ]
II.10.Automatizarea instalatiei
1.Aparate de masura si control
Introducerea elementelor de automatizare asigura :
-obiectivatea controlului si comenzii proceselor tehnologice ;
-centralizarea comenzii grupelor de agregate sau a unor linii tehnologice intregi, practic fara limitarea distantei ;
-realizarea cu precizie a procesului tehnologic cu indici calitativi si cantitativi optimi ;
-comanda proceselor de orice viteza de desfasurare a acestora si pentru orice valoare a parametrilor procesului;
-siguranta si securitatea functionarii agregatelor, maxima a conditiilor de munca; schimbarea formei acestora si, ca atare, ridicarea productivitatii muncii si micsorarea pretului de cost al productiei; [11]
Instalatiile de automatizare se impart in urmatoarele grupe:
-instalatiile de semnalizare automata, a caror sarcina consta in a avertiza personalul asupra starii de functionare. Dupa destinatie, semnalizarea poate fi: de avertizare, de control, de avarie, si de comanda;
-instalatii de blocare si protectie automata sunt sisteme cu selectare sau elemente de comunicatie statica;
-instalatii de control automat care au drept scop principal sa emita, de obicei la un centru unic, date asupra procesului controlat si sa pregateasca aceste date fie pentru perceperea directa catre om, fie pentru a fi introdusa in dispozitie de calcul; [9]
-instalatii de comanda automada destinate conectarii, deconectarii si modificarii regimului de functionare a diferitelor mecanisme sau elemente de executie ale masinilor si aparatelor;
-instalatii de dispecerat a caror sarcina ese de a mentine o anumita stare a procesului sau de a imprima acestei stari o anumita lege de variatie;
-automatizarea complexa cuprinde instalatii de reglare automata in care conducerea se face dupa un parametru tehnico-economic, folosind in acest scop calculatoare electronice si dispozitive de calcul.
In majoritatea cazurilor, fiecare instalatie automata reprezinta o combinare de elemente separate, unite functional.
Cele mai importante elemente specifice ale sistemelor automate sunt:
-traductoarele - elemente primare care formeaza organele de sesizare ce reactioneaza la modificarea starii obiectului controlat sau comandat (acestea sunt traductoarele de temperatura, presiune, nivel, debit, cantitate, densitate, compozitie, etc.)
-elemente de prelucrare a informatiilor, in care se inglobeaza indicatoarele, inregistratoarele, regulatoarele, amplificatoarele, stabilizatoarele, regulatoarele de calcul, etc.
-elemente de executie, care sunt elemente finale ale sistemelor automate, ventile de reglare, etc.
Aparatele de masura si control (AMC) sunt in principiu instalatii de automatizare care se impart in funtie de utilizarea lor :
AMC-urile existente in cadrul unei linii de prelucrare a acidului glutamic, cat si in laborator vor fi descrise mai jos. Astfel in cadrul instalatiei se folosesc urmatoarele aparate si dispozitive:
-dispozitiv de reglare a densitatii sau a concentratiei, care se va masura continuu;
-dispozitiv de control al nivelului - regleaza debitul de iesire la pompa de concentrat;
-statie centrala de reducere a aerului destinata alimentarii cu aer a instrumentelor de control;
-sistem de inregistrare de date: pentru inregistrarea celor mai importante date ale instalatiei, ca de exemplu presiunea aerului, densitatea vacuumului;
-ftinguri necesare: supape de reglaj fin pentru alimentare, supape pentru inchidere, supape de siguranta, robinete de aerisire, instrumente necesare de masura (debitmetre, manometru, termometru);
-tablouri de comanda (confectionate din otel Cr-Ni);
Procesul de automatizare se realizeaza printr-un complex de dispozitive care au diferite scopuri:
-instalatii de control automat al procesului de productie pentru masurarea diferitilor parametri fizici cum ar fi: temperatura, presiunea, tensiunea electrica, nivelul si debitul lichidelor, etc. [1]
-instalatie de protectie automata care functioneaza prin scoaterea partiala sau totala din functie a obiectivului proiectat, cand parametrul controlat depaseste o anumita limita. Aceste instalatii sunt prevazute in unele cazuri si cu semnal sonor (sirena);
-instalatii de comanda automata care asigura mentinerea regimului de lucru si functionare a masinilor, utilajelor intr-un interval de timp determinat.
Aparatura lucreaza in sistem unificat 2-10 mA in locurile in care se folosesc ca traductoare aparate din sistemul unificat. Conducerea procesului tehnologic se realizeaza de la tabloul de comanda situat in camera de comanda. [13]
Masurarea si reglarea automata a temperaturii
Schema reglarii automate a temperaturii este urmatoarea:
|
|
Reglarea temperaturii se face cu un regulator proportional (de tip P).
Blocul operator este alcatuit din elementul de comparatie si amplificatorul operational. Elementul de masurare (EH) este un termomentru pentru masurarea temperaturii solutiei la intrarea in evaporator, aceasta este in legatura cu blocul de reglare automata. Tot legat de regulator este si elementul de executie, in acest caz un ventil (V), de pe conducta de alimentare cu abur a unui schimbator. Parametrul care trebuie mentinut constant este temperatura de fierbere. Atata timp cat temperatura se mentine constanta, regulatorul nu va actiona si V va ramane in aceeasi pozitie. Daca temperatura este mai mica, acest semnal ajunge in elementul de comparatie al regulatorului, unde se compara temperatura masurata cu referinta.
Cu cat diferenta intre temperatura masurata si cea prescrisa este mai mare, cu atat regulatorul va actiona mai mult asupra ventilului de pe conducta de alimentare cu abur, pe care il va deschide.
Ca urmare a acestui fapt, debitul de alimentare cu abur creste, creste viteza aburului, coeficientul de transfer de caldura este imbunatatit si in final, temperatura solutiei va urca la valoarea prescrisa. Daca, insa, temperatura devine mai mare decat cea prescrisa, regulatorul va actiona asupra ventilului in sensul inchiderii lui. Rezulta ca temperatura va cobori.
|
Nr. crt. |
Pozitia in schema |
Denumire utilaj |
Materialul de constructie |
Nr. bucati |
Caracteristici |
|
Fermentator |
Otel Cr Ni |
Capacitate 1000 kg Agitator paleta |
|||
|
Filtru-presa |
Otel Cr Ni |
Dimensiunea placi 40x40 cm Tensionare filtru-av filetat Capacitate: lOOOkg/h |
|||
|
Cristalizor |
Otel Cr Ni |
Volum vas: 600 1 |
|||
|
Rezervor |
Otel Cr Ni |
Rezervor prevazut cu robinet de dozare si stuturi de alimentare, Capacitate: 700 1 |
|||
|
Pompa centrifuga |
Otel Cr Ni |
P=l,5 kW, capacitate de descarcare; 25 ml coloana apa Capacitate: 1000 kg |
|||
|
Centrifuga |
Otel Cr Ni |
Capacitate: 300 kg |
|||
|
Uscator |
Otel |
Capacitate: 100 kg |
|||
|
Vase de masura |
Otel Cr Ni |
Vas prevazut cu robinet de dozare Capacitate: 100 1 |
|||
|
9. |
16 |
Evaporator |
Otel CrNi |
1 |
Capacitate: 800 1 |
|
10. |
17; 19 |
Raci tor |
Otel CrNi |
1 |
Capacitate: 300 kg |
|
11. |
15 |
Preincalzitor |
Otel CrNi |
1 |
Capacitate: 900 kg |
|
12. |
18 |
Separator faze |
Otel CrNi |
Capacitate: 500 kg |
II.12.Aspecte tehnico-economice
Elemente de management si marketing
-Elemente de management-
Pretul productiei industriale este indicatorul care reflecta toate cheltuielile efectuate cu ocazia realizarii productiei, la care se adauga cheltuielile de desfacere si profitul brut. Se calculeaza cu relatia:
Pp=Mp+(-Mr)+S+CAS+CIFU+CGS+CGI+CD+Pr, unde:
Pp-pretul de productie
Mp-costul materiei prime si a materialelor
Mr-costul materialelor recuperate
S-salarii
CAS-contributii asupra salariului
CIFU-cheltuieli cu intretinerea si functionarea utilajelor
CGS-cheltuieli generale pe sectie
CGI-cheltuieli generale pe intreprindere
CD-cheltuieli de desfacere
Pr-profit brut
CAS-somaj, pensii, sanatate
CIFU-cheltuielile fixe(reparatii curente, capitale, intretinere, obiecte de inventar, combustibil si energie, cota parte din amortizari)
CGS-cheltuielile fixe, care nu se modifica cu volumul productiei pentru un interval de timp dat: salariile personalului indirect productiv, din birourile sectiilor, ale personalului de intretinere, iluminat, incalzit, cota parte din amortismentele, etc.
-CGI-din acelasi gen ca si cele ale sectiilor, dar la nivel de unitate
-CD-cheltuieli ocazionale de pregatirea livrarii produselor
-Pr-profilul reprezinta surplusul obtinut de o societate comerciala atunci cand venitul total obtinut depaseste cheltuielile necesare fabricarii produsului. Profitul este cota parte din pretul de productie ce asigura fondurile necesare pentru dezvoltarea productiei, pentru stimularea activitatii salariatilor.
Cresterea profitului se poate realiza prin cresterea volumului productiei industriale, reducerea costurilor sau modificarea preturilor de livrare. In pretul de productie intra profitul brut. Profitul impozabil se obtine scazand din profitul brut cheltuielile de protocol, reclama si publicitate.
Pr Imp = Pr brut - (C prp-Csu)
Impozitul pe profit (IP) se calculeaza ca fiind 38% din profitul impozabil
IP=0,38· Pr Imp
Profitul net se calculeaza ca diferenta intre profitul impozabil si impozitul pe profit. Impozitul pe dividende este de 10% din profitul net: ID=0,1·PN
Dividendele firmei se calculeaza ca diferenta dintre profitul net si impozitul pe dividende: D=PN-ID
Se obtine adaugand TVA-ul la pretul de productie: Pl=Pp+TVA1 ; TVA = 22%·Pp-TVA1 ; TVA=22%·Mp
Se obtine inmultind profitul de livrare cu cantitatea de productie obtinuta pe an (Q).
CA=Pl·Q
Cost complet (pret de cost) = Mp+(-Mr)+S+CAS+CIFU+CGS+CGI+CD
Exista un indicator identic care exprima volumul de munca cu care se realizeaza bunurile materiale, deci un indicator de eficienta a muncii. Serveste la compararea in diferite perioade a efortului uman investit in realizarea bunurilor materiale in general.
Se exprima in 2 forme:
a)Productivitatea fizica
Wf =Pt/Nmp, Pf - productia fizica
Nmp - numarul mediu de personal
b)Productivitatea valorica
WVPI=VPI/ Nmp VPI -valoarea productiei industriale (sau cifra de
afaceri CA)
Indicatori de eficienta a investitiei
Investitia specifica(i) se exprima sub forma unui raport intre efortul si efectul economic rezultat de pe urma acestui efort:
i=I/VPI, in care: I-valoarea totala a investitiei
VPI-valoarea productiei industriale
Durata de recuperare a investitiei (t)
Durata de recuperare (t) se calculeaza raportand valoarea totala a investitiei (I) la dividendele firmei (D):
t=I/D;
Eficienta fondurilor fixe (EFf)
a)Eficienta folosirii fondurilor fixe fata de VPI
EFf =VPI /Ff; Ff - fonduri
fixe
b)Eficienta folosirii fondurilor fixe raportata la profitul brut EFf =Profit brut/Ff
Legatura dintre suma cheltuielilor de productie si cantitatea de produse ce trebuie realizata pentru ca prin vanzarea sa sa se acopere toate cheltuielile, se evidentieaza cu ajutorul punctului critic, numit prag de rentabilitate.
-Elemente de marketing-
Prezentarea generala a firmei
-Volumul afacerilor si structura productiei (obiect de activitate)
-Puncte tari ale firmei (seriozitate si profesionalismul angajatilor, produse de calitate superioara, materii prime de buna calitate, pret corespunzator, etc.)
-Puncte slabe ale firmei (capacitate de productie mica, care nu satisface integral cererea pietei).
2.Piata de desfacere
Definirea si delimitarea segmentelor de piata presupune cunoasterea dimensiunilor pietei, acestea facandu-se cu ajutorul unor indicatori globali cum sunt: capacitatea, potetialul ei si consumul aparut :
Capacitatea pietei (Cp)
reprezinta probabilitatea pietei de a absorbi un
produs, lucrare sau serviciu, fara a tine cont de pretul
acestuia.
Cp=Nc·i, unde: Nc - numarul de consumatori
i - intensitatea medie de consum
. Potentialul pietei (Ppt)
Reprezinta volumul maxim al vanzarilor ce poate fi obtinut de toate firmele dintr-o industrie, de-a lungul unei perioade de timp, la un anumit nivel al efortului de marketing si in anumite conditii de mediu.
Ppt=Nci ·Pcp unde: Pcp - putere medie de cumparare la un pret anume
Potentialul pietei este intotdeauna mai scazut decat capacitatea pietei, intrucat cuprinde consumatori care doresc sa posede produsul comercializat, insa nu sunt dispusi sa-1 achizitioneze la pretul dorit de producator.
Volumul pietei - include la un moment dat pe o anumita piata, respectiv a ofertelor acceptate la un pret determinat.
Vp=q·p q=totalitatea marfurilor de un anumit tip vandute pe o piata
P=pretul marfurilor vandute
II.13. Controlul procesului tehnologic
Grafic de analize
|
Nr. crt. |
Denumire proces |
Parametrul controlat |
Frecventa controlului |
Valoarea prescrisa |
Metode de control |
Executant |
|
Pregatirea si sterilizarea mediului de cultura |
operator laborator |
|||||
|
Fermentatie |
pH-ul, temp Se face analiza biomasei |
6h |
29-31°C |
termometric |
operator laborator |
|
|
3. |
Acidulare-coagulare coagulare |
temp; pH |
30 min. |
6,5 |
cf STAS |
operator |
|
Puri ficare- fi ltrare |
temp |
30 min. |
termometru hartie indic. |
operator |
||
|
5. |
Concentrare |
pH; temp |
30 min. |
6,5 50-55°C |
cf STAS |
operator |
|
6. |
Acidulare cristalizare |
temp pH |
30 min |
10-12°C 3,2 |
termometrie |
operator |
|
Centrifugare |
30 min. |
cf. STAS |
operator laborator |
|||
|
8. |
Uscare |
temp.usc. umidit. finala |
30 min. |
100° C |
cf. STAS |
operator laborator |
Ape reziduale, deseuri, materiale refolosibile
Din procesul de obtinere a acidului glutamic prin biosinteza rezulta la faza de filtrare un reziduu ce contine: restul de acid glutamic, restul de zaharuri nereactionate(carbune, biomasa epuizata, apa). Deasemenea, in urma proceselor de centrifugare si concentrare, se elimina vapori de apa, ca si la uscare.
II.15. Norme de tehnica securitatii muncii[***18]
Protectia muncii personalului care deserveste o instalatie se asigura prin stabilirea cauzelor potentiale de pericol si luarea de masuri care sa le evite. Factorii cu rol in accidentare sunt de natura mecanica, electrica, termica si chimica. Sursele electrice de accidentare sunt: reteaua electrica, aparatele nelegate la pamant, contacte imperfecte in transmiterea curentului electric, conductori neizolati, etc. Sursele termice sunt: scapari de abur supraincalzit, apa fierbinte, suprafata fierbinte a evaporatoarelor, etc.
Sursele chimice sunt: acidul sulfuric si acidul clorhidric.
Pentru asigurarea unei exploatari in conditii de securitate a muncii, se iau urmatoarele masuri:
1. In toate incaperile sectiei locurile de munca, trecerile scarilor, grupurile sociale, spatiile de depozitare, produse, semifabricate si materiale, laboratorul sectiei vor fi mentinute intr-o stare perfecta de curatenie si ordine. Acestea trebuie corespunzator iluminate si dotate cu material pentru efectuarea si mentinerea curateniei.
2. Este oprita depozitarea in sectie a materialelor si a obiectelor care depasesc necesarul fabricii, a materialelor inflamabile si a materialelor care nu sunt folosite in procesul tehnologic.
Orice instalatie electrica defecta se va scoate din functiune si se va pune la dispozitia electricianului sef pentru reparatie.
4. Echipa de intretinere electrica este obligata sa verifice zilnic instalatiile electrice eliminand conductorii cu izolatii defecte, controland conectarea la pamant a aparaturii electrice si continuitatea conductorului de nul.
5. Manipulantii de motoare electrice trebuie sa aiba in vedere urmatoarele:
-sa nu fie cu imbracamintea, mainile si incaltamintea uda
-sa manevreze motoarele de pe covorul izolant.
6. Utilizarea lampilor portabile cu tensiune peste 12V este interzisa
7. Indepartarea dispozitivelor de protectie in timpul functionarii utilajelor este strict interzisa.
8. In timpul repararii utilajelor: fermentatoare, evaporatoare, etc. se vor lua urmatoarele masuri de securitate:
-scoaterea sigurantelor electrice;
-blindarea tuturor ventilelor si flanselor pentru a impiedica ajungerea in contact cu lichide fierbinti, corozive, abur, gaze toxice.
9. Este interzisa repararea utilajelor si anexelor in conditiile prezentei lichidelor corozive: acid, abur, soda, lichide fierbinti, solventi care prezinta pericolul de ardere prin stropire, incendiere sau explozie. Toate acestea se vor face dupa golirea utilajelor care trebuie supuse reparatiei, spalarea lor cu apa si suflarea cu abur pentru a antrena substantele daunatoare.
10. Este interzisa strangerea suruburilor la flansele de legatura ale conductelor aflate sub presiune, precum si strangerea presetupelor in timpul functionarii pompelor.
Norme de prevenirea si stingerea incendiilor (P.S.I.) [***19]
Art.22 - Activitatea de prevenire si stingere a incendiilor, fiind o componenta a functiunii de productie, face parte integranta din activitatea economica sau social-culturala desfasurata de unitati. La activitatea de prevenire si stingere a incendiilor este obligat sa participe intreg personalul incadrat in munca, aceasta constituind o sarcina de serviciu.
Art.23 - In toate unitatile este obligatorie organizarea si desfasurarea unei activitati permanente de P.S.I. care se realizeaza pe baza prevederilor actelor normative ce reglementeaza aceasta activitate.
Art.24 - Raspunderea pentru organizarea si desfasurarea activitatii de P.S.I. in unitati revine potrivit competentei ce o au, conducatorilor de unitati, conducatorilor sectoarelor de activitate si conducatorilor locurilor de munca.
Art.25 - Organizarea activitatii de prevenire si stingere a incendiilor intr-o unitate presupune :
a)constituirea comisiei tehnice de P.S.I., stabilirea obligatiilor ce revin membrilor acesteia si a modului de lucru, intocmirea planului de aparare impotriva incendiilor.
b)constituirea, incadrarea cu personal si dotare cu material si mijloace a formatiei civile, de pompieri; intocmirea programului de instruire a formatiei si stabilirea atributiilor ce revin membrilor acesteia.
c)stabilirea atributiilor si raspunderilor privind P.S.I., ce revin personalului incadrat in munca serviciilor si compartimentelor functionale precum si altor organisme constituite in unitati.
d)organizarea si prevenirea stingerii incendiilor la locurile de munca si a evacuarii personalului si bunurilor in caz de incendiu.
Pentru prevenirea incendiilor se vor evita focurile deschise; fumatul este permis doar in locurile special amenajate; se vor verifica prizele, instalatia electrica, intrerupatoarele, pentru a nu exista contacte imperfecte care, in caz de sarcina, duc la incalziri locale si pericol de aprindere; utilajele vor fi legate la pamant; se va asigura functionarea corecta a dispozitivelor de semnalizare a avariilor si de blocare a instalatiei in caz de avarii; se va dota sectia cu scule pentru stingerea incendiilor cu (nisip, exctinctoare cu spuma, guri de hidrant).
Bibliografie
Dr. Ing. Corneliu Oniscu, 'Tehnologia Produselor de biosinteza',Ed. Tehnica, Bucuresti,1978
D. Nenitescu, Viorica Ioan,'Manualul Inginerului Chimist',Vol.I, Ed. Tehnica, Bucuresti, 1951
Alfa Xenia Lupea, Prof. Dr. Aurel Ardelean, 'Elemente de Biochimie', Ed. Politehnica, Timisoara, 2002
C. Daescu, 'Produse de Bio si Semi-sinteza', editia a II-a adaugita, Editura Politehnica, Timisoara, 2006
Camelia Soldea, Alexandru Chichirau, 'Elemente de Biochimie', Universitatea Tehnica 'Gheorghe Asachi', Iasi-1999
C. Daescu, 'Industria medicamentelor', Ed Uni-Press, Bucuresti 1999
Wandrey C., 'Advances in Biochemical Engineering', vol 12, Springer Verlag, New York,1979
Valeriu Rugina,'Din secretele proceselor fermentative', Ed. Tehnica, Bucuresti, 1992
Urban, Scwartzenberg, 'Ullmann's Enciclopedia of Chemical Technology', 6th Ed. Electronic realease,1998
Gh. Lupusor, E. Merica, C. Gorea, V. Bucea-Gorduza,'Ingineria sintezei intermediarilor aromatici.Baze teoretice',vol. I, Ed. Tehnica, Bucuresti, 1977
Marinoiu V., Paraschiv N., 'Automatizarea proceselor chimice', Ed. Tehnica, Bucuresti,1992
J. Chibata, 'Imobilized Enzymes', Kodanska-Halsted Press, Tokyo-New York, 1978
Delia Perju, M. Suta, M. Geanta, C. Rusnac, 'Automatizari si optimizari in industria chimica', Lucrari de laborator, Ed. Mirton, Timisoara 1995
Kirk, Othmer, D. F. , 'Enciclopedia of chemical technology, the Intersciens encyclopedia', Inc., New York, 1947
Holman, T. Ralph, 'Progress in the Chemistry of Fatts and other Lipids', vol II, Ed. Pergamon Press LTD., London, 1954
Pavlov K. F., Romankov P., 'Procese si aparate in tehnologia chimica', Ed. Tehnica, Bucuresti,1981
C. Daescu, I. Macarie, I. Boc,' Indrumar de proiect',Timisoara, 1983
***Colectia standardelor de stat,1997-1998, Catalog de produse
***Norme de protectia muncii, Ministerul Industriei Alimentare, Bucuresti, 1989
***Norme de prevenire si stingere a incendiilor,Ministerul Agriculturii, Bucuresti, 1987
Catalog IUC Fagaras, Ministerul Industriei Chimice, IPAC, 1973
|
|
|
|
Reactor cu manta si agitator
|
|
Bilantul termic pentru etapa de concentrare
|
|

 Proiect de diploma
Proiect de diploma

METODA SPECTROFOTOMETRICA DE DETERMINARE A CONTINUTULUI DE CREATINA /CREATININA DIN DIFERITE PRODUSE CONCENTRATE SOLIDE
III.1. PREZENTAREA PROBLEMEI
III.1.1. INTRODUCERE
Creatina e un acid carboxilic ce contine in molecula un rest de guanidina. Se gaseste in mod natural in tesutul muscular al vertebratelor unde serveste ca supliment energetic celulei musculare( formula (I) [ 1, 6, 10 ]
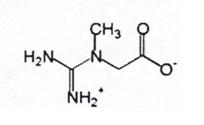
( I )
Formula moleculara: C4H9N3O2
Masa moleculara: 131,13 g/mol
Punct de topire: 303°C
Denumire chimica: Acid 2-(carbamimidoil-metil-amino) acetic
Sinonime: - acid α-metilguanidinoacetic
- creatina
- N- amidinosarcozina
Creatina a fost identificata in 1832 cand Michael Eugéne Chevreul a descoperit-o ca si componenta a muschilor scheletici denumind-o ulterior creatina, dupa denumirea din limba greaca pentru carne kreas.
Ulterior, in 1847 germanul Justus von Liebig a incercat sa promoveze pentru comercializare un extract de carne ce ar putea ajuta organismul uman sa desfasoare eforturi fizice suplimentare. " INGREDIENTUL SECRET" al extractului de carne al lui Liebig era creatina.
III.1.2. ROLUL CREATINEI
Aproape 95% din creatina totala a corpului nostru se gaseste in tesutul muscular. Aici creatina alimenteaza "masina moleculara generatoare de forta". Cea mai mare parte din necesarul zilnic de creatina este obtinut din carne si peste, iar suplimentarea dozei zilnice cu saruri sintetice de creatina creste performanta fizica. Astfel in cazul vegeta-rienilor care in mod normal poseda nivele mult mai scazute de creatina in organism, imbogatirea dietei cu creatina duce la un raspuns fiziologic mult mai prompt in conditii de efort. Creatina joaca un rol important si la nivelul sistemului nervos unde furnizeaza energia necesara atat functionarii corespunzatoare a acestuia cat si recuperarii dupa afectiuni si traume. Orice situatie care duce la scaderea severa a nivelurilor celulare de creatina duce inevitabil la tulburari musculare si neurodegenerative. Datorita importantei sale fiziologice in multe afectiuni ce implica sistemul muscular si nervos este testat clinic efectul suplimentarii cu creatina a dietei.
Practic, creatina a revolutionat industria suplimentelor nutritive. Niciodata, inainte, un supliment nutritional nu a fost receptat atat de bine de lumea stiintifica si sportiva.
Ultimele doua decenii au produs nenumarate studii care au demonstrat efectul net ergogen al suplimentelor cu creatina.[ 10,12 ]
III.1.2.1. PROCESAREA DE ENERGIE ADITIONALA IN TESUTUL MUSCULAR
Creatina imbunatateste performanta fizica actionand la diferite nivele fiziologice incepand de la celula si extinzandu-se apoi la diferite reactii anabolice. Desi atributele
sistemice ale creatinei au ramas ultimele de clarificat pentru efectele sale, sunt probabil cele mai importante pentru sanatate si performanta atletica.
Oricum datorita cercetarilor stiintifice continue, mecanismele de actiune si raspunsurile hormonale vor fi in curand clarificate. In prezent cel mai bine lamurit mecanism de actiune al creatinei este cel al cresterii nivelelor energetice la nivel celular in momentele de mare consum energetic. [ 7, 8, 9 ]
O explicatie biologica foarte simpla e urmatoarea: organismul nostru contine un compus foarte bogat in energie, adenozintrifosfatul (ATP), din care organismul poate obtine energia necesara foarte rapid. Organismele vii poseda si alte surse energetice: carbohidratii si grasimile, dar transformarea lor in energie utilizabila ia mai mult timp.
Cand organismul e implicat intr-o activitate foarte intensa, tesutul muscular necesita o sursa rapida de energie pe care si-o procura din acest ATP. Reactia chimica prin care ATP este descompus cu generare de energie produce adenozindifosfatul (ADP) si fosfatul anorganic:
ATP → ADP + Pi + 7.5 kcal (1)
Din pacate nu dispunem de o rezerva nelimitata de ATP. Practic, muschii contin doar atat ATP cat sa reziste la o excitatie maxima timp de 10 - 15 secunde, intrucat ADP-ul rezultat nu mai poate servi la producerea de energie.
In acest moment intervine creatina, mai exact creatinfosfatul. Majoritatea creatinei stocata in muschiul viu este legata de numeroasele resturi fosforice existente sub forma de creatinfosfat.(II)
![]()
![]()
![]()
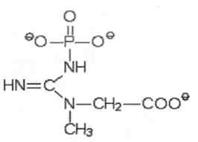
![]() Acesta este capabil sa
reactioneze cu ADP-ul existent transformand acest compus "inutil" in
"supersursa de energie" ATP. Un nivel ridicat de ATP inseamna mai mult
"combustibil muscular".[ 7, 10 ]
Acesta este capabil sa
reactioneze cu ADP-ul existent transformand acest compus "inutil" in
"supersursa de energie" ATP. Un nivel ridicat de ATP inseamna mai mult
"combustibil muscular".[ 7, 10 ]
III.1.2.2. CRESTEREA VOLUMULUI MUSCHILOR
Este o consecinta a cresterii nivelului lichidului in celulele musculare. S-a dovedit abilitatea creatinei de a "atrage apa" in celulele musculare crescand dimensiunea muschilor. Nu este clar insa in ce masura acesta este un efect poztiv.[ 10 ]
III.1.2.3. ROL DE TAMPON PENTRU "AGLOMERAREA" ACIDULUI LACTIC
Cercetari recente au aratat cum creatina poate ajuta la tamponarea acidului lactic format in cantitati mari in tesutul muscular in perioade de efort.
Stiintific procesul este foarte complicat. Simplificat creatina se leaga de un ion de hidrogen contribuind astfel la "intarzierea" aglomerarii acidului lactic, dar lucrurile nu sunt pe deplin lamurite.[ 10 ]
III.1.2.4. INFLUENTA ASUPRA SINTEZEI DE PROTEINE
Exista date care arata cum creatina influenteaza trecerea organismului intr-o stare anabolica propice sintezei de proteine. Datorita acesteia tesutul muscular castiga in dimensiune.[ 10 ]
III.1.3. NECESITATEA SUPLIMENTARII DIETEI CU CREATINA
In mod normal cantitatea medie de creatina stocata in organismul unui adult este de 120 g. In absenta perioadelor de efort intens aceasta cantitate ar trebui sa fie suficienta. Folosirea suplimentelor cu creatina ofera un plus de energie intrucat permit desfasurarea ciclului energetic al ATP pe o perioada mai mare de timp. Studiile au aratat ca tesutul muscular uman poate stoca maxim 5 g de creatina /kg, in conditiile in care continutul normal mediu ar fi intre 3,5 - 4 g/kg. Deci, suplimentarea cu creatina in sensul obtinerii unui rezultat optim trebuie sa asigure cresterea de la 3,5 la 5 g creatina/kg. Excesul de creatina este transformat in compusul rezidual creatinina, care este excretat.[ 2, 10 ]
III.1.4. METABOLISMUL CREATINEI
III.1.4.1. BIOSINTEZA
In corpul uman creatina e sintetizata preponderent in ficat utilizand fragmente provenind de la 3 aminoacizi diferiti: arginina, glicina, metionina. 95% din creatina astfel sintetizata este stocata in muschii scheletici, restul in creier, inima si tesuturi. Biosinteza creatinei este prezentata pe scurt in Schema 1 si detaliat in Schema 2.[ 1, 2, 11 ]
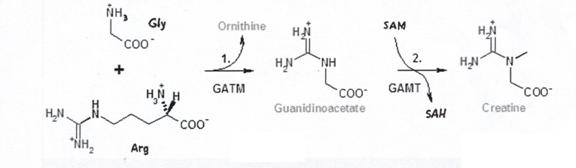
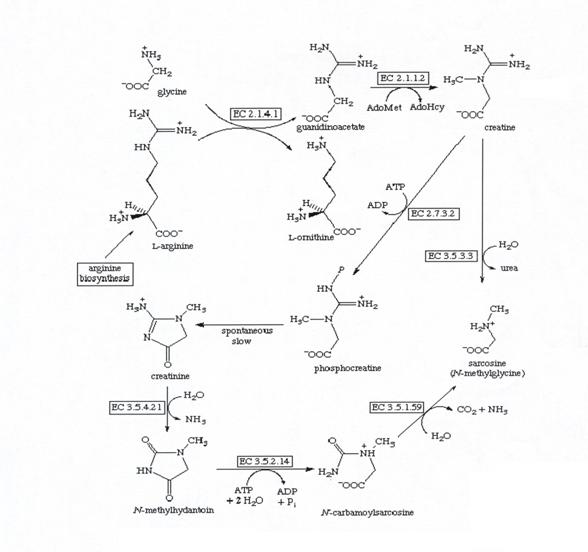 Schema.1.: Biosinteza creatinei
Schema.1.: Biosinteza creatinei
Schema .2.: Etapele detaliate ale biosintezei creatinei
Metilarea guanidoacetatului se produce folosind ca donor de grupare metil-S-adenozil-metionina. La randul sau guanidoacetatul se formeaza in rinichi din aminoacizii: arginina si glicina. Reactiile sunt catalizate enzimatic.
Creatina nu este excretata ca atare. In schimb defosforilarea spontana neenzimatica a fosfocreatinei produce printr-o reactie ireversibila creatina.
In vitro echilibrul reactiei reversibile neenzimatice de ciclizare a creatinei la creatinina e dependenta de pH si de temperatura. El este deplasat spre creatina la valori mari de pH si temperaturi scazute si spre creatinina la temperaturi ridicate in solutii acide. In ambele sensuri reactia este monomoleculara. Astfel plecand de la o solutie de creatina pura la pH = 7.2 si 38 °C intre 1 si 1.3 % din creatina este transformata zilnic in creatinina. Studiile in vitro asupra stabilitatii fosfocreatinei au aratat ca acest compus fosforic bogat in energie este sensibil in conditii acide si produce prin hidroliza fosfat anorganic si creatinina sau creatina in functie de temperatura si pH.
Situatia in vivo este totalmente alta, conversia creatina-creatinina fiind un proces ireversibil.[ 8, 10 ]
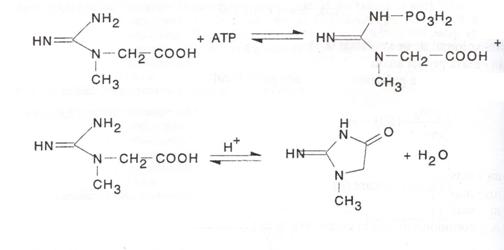 Fiecare individ sanatos clinic excreta o cantitate
importanta de creatina considerata normala( Schema 3):
Fiecare individ sanatos clinic excreta o cantitate
importanta de creatina considerata normala( Schema 3):
ADP (2)
(3)
Schema 3: Echilibrul creatina-creatinfosfat-creatinina
Valoarea acesteia in urina reflecta deasemenea proportia de masa musculara activa. Organismul feminin excreta intre 15-22 mg/kg, cel masculin intre 20-26 mg/kg. Deoarece in mod normal creatinina este excretata foarte rapid, orice crestere a nivelului sau in
sange indica o proasta functionare a rinichilor. Desi creatina nu este excretata in urina, copiii si femeile o fac in anumite situatii. In cazul femeilor proportia de creatina excretata creste mai ales dupa sarcina.
Nivelul creatinei urinare este mare la pacientii suferinzi de diabet, hipertiroidism, febra, cei malnutriti, sau pur si simplu s-au infometat, toate acestea reflectand degradari ale tesutului muscular.[ 7, 9 ]
III.1.5. INTREBUINTARI
Exceptand clasicele suplimente nutritive ce contin creatina utilizate in alimentatia persoanelor care trec prin perioade de efort intens, suplimentarea dietei cu creatina este cercetata ca o posibila terapie a unor afectiuni musculare, neuromusculare si neurologice. Astfel studii stiintifice au indicat cum creatina poate fi benefica in tratamentul afectiunilor neuromusculare intr-o masura mai mare decat tratamentul clasic. In industria alimentara creatina, compus solubil in apa se regaseste in carne si produse derivate de carne cum ar fi diferitele extracte, supe si sosuri concentrate. De aceea determinarea ei cantitativa este folosita pentru identificarea prezentei extractelor de carne in aceste produse. Pe de alta parte alimentele nu contin fosfocreatina deoarece aceasta este degradata pe parcursul transformarilor metalice care au loc in tesutul muscular viu post-sacrificare.[ 10 ]
III.2. DETERMINARI EXPERIMENTALE
III.2.1. CONSIDERATII GENERALE
In principal in partea experimentala s-a urmarit identificarea prezentei extractelor de carne in diferite produse concentrate solide prin determinarea cantitativa a creatininei despre care se stie ca este dovada adaosului extractelor de carne in aceste produse.
Obtinerea si utilizarea extractelor de carne are o istorie de peste 150 de ani. In acceptiunea moderna extractul de carne (de uz industrial) este definit ca un concentrat solubil in apa de constituenti ai carnii lipsit de grasime si proteine.[ 2, 3, 4 ]
Prima obtinere a extractului de carne i se atribuie lui Liebig in 1847. In prezent la scara industriala extractele de carne sunt obtinute prin extractia carnii maruntite cu apa fierbinte ( 90°C ) in contracurent, urmata de indepartarea grasimilor si filtrari succesive.
Solutia initiala are un continut mediu de substanta solida de 1.5 - 5% si este concentrata la vid pana la un continut de 45 - 65% materie solida.
Extractul final trebuie sa atinga un continut de 80 - 83% materie solida realizat printr-o evaporare la presiunea atmosferica la o temperatura de aproximativ 65°C. In prezent cea mai mare importanta economica o au extractele de carne obtinute prin procesarea apei folosita la prepararea conservelor. Randamentul raportat la carnea proaspata este de doar 4%.[ 2 ]
Compozitia medie a unui extract de carne uzual este prezentata in Tabelul 1.
|
Constituentul |
Continut ( % greut. ) |
|
Materie organica 1. aminoacizi, peptide 2. alti compusi cu azot creatinina totala amoniac uree 3. compusi liberi de azot lipide totale 4. pigmenti Minerale clorura de sodiu Continut de apa |
> 1.5 |
Tabelul 1: Compozitia extractului de carne uzual
PH-ul mediu al unei solutii apoase 10% a unui astfel de extract este aproximativ 5.5. In industria alimentara in scopul adaugarii la pulberi pentru supe sau alte tipuri de pudre sau concentrate solide( sosuri, cuburi cu diferite arome, etc), extractul de carne sub forma unei paste foarte groase este omogenizat impreuna cu ceilalti constituenti ai produsului respectiv si apoi uscat prin vid sau prin pulverizare.
In vederea determinarilor experimentale si pentru aprecierea cantitativa a extractului de carne adaugat se ia in considerare o valoare medie a continutului de creatina/ creatinina de 7.2%.
III.2.2. DETERMINAREA SPECTROFOTOMETRICA A CONTINUTULUI DE CREATININA
III.2.2.1. PRINCIPIUL METODEI
Metoda spectrofotometrica de determinare a continutului de creatina/creatinina este in prezent general acceptata si utilizata in laboratoarele de profil.[ 5 ]. Metoda se bazeaza pe obtinerea extractului apos din proba de analizat. Prin precipitare cu acid tricloracetic, urmata de centrifugare, extractul astfel obtinut este eliberat de constituentii nedoriti ce pot deranja ulterior. Prin tratarea extractului purificat si concentrat cu acid clorhidric (HCl) creatina ciclizeaza la creatinina.[ 3, 4 ]
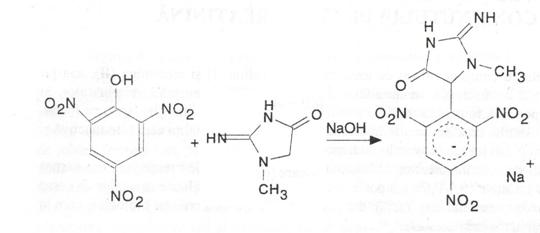 Simultan insa se mai pot forma si alti produsi din
descompunerea glucidelor (acid levulinic, hidroximetilfurfurol etc) ce pot
deranja ulterior determinarea spectrofoto-metrica. Ei sunt
indepartati in doua etape: absorbtie
pe o coloana de alumina activata (daca este cazul
urmata de o purificare suplimentara pe o rasina
schimbatoare de ioni), extractie
cu eter. In filtratul final, creatinina astfel izolata formeaza
cu acidul picric in mediu alcalin un complex colorat in galben (reactia
Jaffe), cu un maxim caracteristic de absorbtie in VIZ la lungimea de
unda λ=510 nm.[ 3, 4, 5 ]
Simultan insa se mai pot forma si alti produsi din
descompunerea glucidelor (acid levulinic, hidroximetilfurfurol etc) ce pot
deranja ulterior determinarea spectrofoto-metrica. Ei sunt
indepartati in doua etape: absorbtie
pe o coloana de alumina activata (daca este cazul
urmata de o purificare suplimentara pe o rasina
schimbatoare de ioni), extractie
cu eter. In filtratul final, creatinina astfel izolata formeaza
cu acidul picric in mediu alcalin un complex colorat in galben (reactia
Jaffe), cu un maxim caracteristic de absorbtie in VIZ la lungimea de
unda λ=510 nm.[ 3, 4, 5 ]
Reactia Jaffe:
(4)
In final continutul de creatinina al probei si respectiv al extractului de carne se determina folosind o curba de etalonare obtinuta cu creatina etalon.
III.2.2.2. REACTIVI
Reactivii utilizati sunt:
creatinina, minim 99.2%;
acid tricloracetic, solutie 20%;
acid clorhidric, solutie 18%;
alumina activata, calcinata la 700°C timp de 4 ore;
eter etilic; p.a.;
acid picric, solutie 1.2%;
hidroxid de sodiu, solutie 10%;
solutie etalon de creatinina (100 mg/l) care se obtine astfel: 0.1 g creatinina cantarita la balanta analitica se introduce intr-un balon cotat de 100 ml si se aduce la semn cu apa distilata. Din aceasta solutie se pipeteaza 10 ml intr-un balon cotat de 100 ml si se aduce la semn cu apa distilata obtinandu-se solutia etalon de creatinina.
III.2.2.3. MOD DE LUCRU [ 5 ]
III.2.2.3.1. TRASAREA CURBEI DE ETALONARE
In mai multe baloane cotate de 100 ml se pipeteaza cate 0, 1, 2, 3, 4,, 10 ml solutie etalon de creatinina. In fiecare balon se pipeteaza cate 10 ml solutie acid picric si 1 ml solutie hidroxid de sodiu (NaOH). Se agita baloanele energic, se lasa in repaus 20 de minute la temperatura mediului. Se aduc baloanele la semn cu apa distilata, se mai lasa in repaus 20 minute si se determina extinctia probelor la 510 nm fata de
martor (balonul ce nu contine solutie de creatinina). Rezultatele obtinute sunt prezentate in tabelul .2:
|
Nr. proba |
Solutie etalon (ml) |
Acid picric sol. 1.2%(ml) |
Hidroxid de sodiu sol. 10%(ml) |
Concentratia probei (mg/proba) |
Extinctia E510 (nm) |
Tabelul 2. Valorile pentru trasarea curbei de etalonare a creatininei:
Se reprezinta grafic extinctia functie de continutul de creatina a probelor E= f(conc) si se obtine curba de etalonare si caracteristicile acesteia: ecuatia dreptei si coeficientul de corelare.( Graficul 1 )
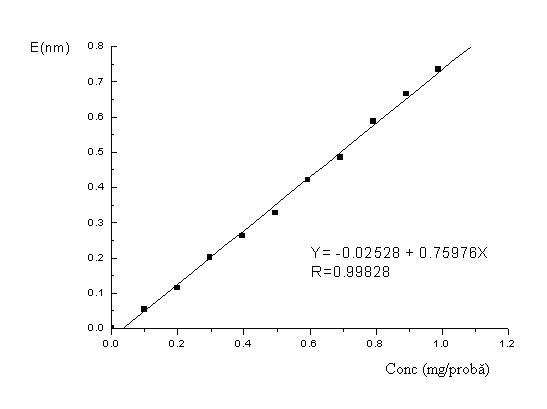
Graficul 1: Curba de etalonare pentru creatinina:
III.2.2.3.2. DETERMINAREA CONTINUTULUI DE CREATININA AL PROBELOR ANALIZATE
MOD DE LUCRU:
Se cantaresc la balanta analitica intre 0.25 - 10g proba bine omogenizata. Se solubilizeaza cu 50ml apa distilata, calda si se lasa la extras timp de 4 ore la temperatura de 60°C in baie de apa cu agitare ocazionala. Solutia apoasa calda se trateaza cu 10ml solutie acid tricloracetic. Se agita energic si dupa racire se centrifugheaza timp de 10 minute la 3000 rotatii/minut, dupa care se filtreaza printr-un filtru cutat intr-un balon cotat de 100ml. Rezidul de la centrifugare se spala de cateva ori cu volume mici de apa distilata, care se trec si ele pe filtru. In final, solutia din balon se aduce la semn cu apa distilata. Se pipeteaza 20ml filtrat intr-o capsula de portelan impreuna cu 5ml solutie acid clorhidric si se evapora lent pana la sec pe baia de apa. Reziduul format este reluat dupa racire cu 20ml apa distilata. Solutia obtinuta este trecuta pe o coloana cromatografica (dimensiuni 20*10mm) ce contine 8g alumina, apoi este filtrata si captata intr-un balon cotat de 50ml.
Daca dupa trecerea pe alumina filtratul ramane galbui, este necesara purificarea sa suplimentara pe rasina schimbatoare de ioni Amberlit IR 120 astfel 25ml filtrat obtinut pe coloana cu alumina se trece pe rasina schimbatoare de ioni, care apoi este eluata cu 150ml apa distilata. Creatinina se va capta in 150ml amoniac (NH3) solutie 10% in aproximativ 40 minute de eluare, iar eluatul incolor se introduce intr-o capsula de portelan si se aduce la sec pe baia de apa (in acest caz nu se mai parcurge faza de extractie cu eter). In continuare coloana cu alumina este eluata cu apa distilata, iar eluatele sunt adaugate in balonul cotat pana la semn. Se pipeteaza 25ml din acesta solutie intr-o capsula de portelan, se adauga 4 picaturi solutie HCl si se concentreaza pe o baie
de apa la un volum cat mai mic. Solutia acida se spala de pe pereti cu cateva picaturi apa distilata si se trece intr-o micropalnie de separare unde se spala de 4 ori cu cate 5ml eter
etilic. Faza apoasa separata este trecuta intr-o capsula de portelan si se aduce la sec. Rezidul rezultat se trece cantitativ cu 5 ml apa distilata intr-un balon cotat de 50 ml si se adauga 5ml solutie acid picric si 0.5ml solutie hidroxid de sodiu(NaOH). Se agita bine si se lasa in repaus 20 minute la 20°C, dupa care se aduce la semn cu apa distilata. Se mai lasa in repaus timp de 20 minute dupa care se determina extinctia probei la 510nm fata de martor (preparat identic dar fara proba).
Continutul de creatinina K in mg/100g proba se calculeaza astfel:
K (mg/100g proba) = a . 250/E
unde
a - cantitatea de creatinina aflata din dreapta de etalonare (µg/ml);
E - masa probei catarite (g);
250 - factor de corectie rezultat din cumularea dilutiilor, transformarea µg in g si raportarea la 100g proba.
Experimental am efectuat un set de 10 determinari pe diferite probe: concentrate sub forma de cuburi cu diferite arome si de provenienta diferita si supe concentrate. Modul de preparare al probelor si de exprimare al rezultatelor a fost de fiecare data acelasi. In continuare este exemplificat cazul cubului concentrat de gaina de la firma Maggi:
III.2.2.3.2.1. MOD DE LUCRU
Am cantarit la balanta analitica o cantitate de mp= 5.4378g cub concentrat de gaina, am omogenizat-o cu 50ml apa distilata incalzita. Am solubilizat proba si am pus-o la extras pe baia de apa la o temperatura constanta de 60°C. Solutia are o coloratie in galben deschis, cu aspect tulbure. Am agitat ocazional. Dupa patru ore am adaugat 10ml acid tricloracetic si am racit solutia.
La adaugarea acestuia solutia isi pastreaza coloratia, dar se formeaza un precipitat galben. Se centrifugheaza (in 6 eprubete echilibrate una fata de cealalta) la 3000 de rotatii pe minut timp de 10 minute. In urma acestui proces precipitatul de un galben intens s-a depus la baza eprubetelor, iar solutia a ramas aproape limpede. Am filtrat solutia intr-un balon cotat adaugand si apele de spalare ale rezidului de centrifugare. Am adus balonul cotat de 100ml la semn cu apa distilata. Solutia este limpede de culoare slab galbui. Din aceasta am pipetat 20ml filtrat si impreuna cu 5ml solutie HCl 18% l-am introdus intr-o capsula de portelan. Se evapora lent la sec pe baia de apa si se obtine un reziduu maroniu ce contine cristale ce se lasa la racit. Reziduul este reluat cu 20ml apa distilata, iar solutia este trecuta pe o coloana cromatografica ce contine 8g alumina activata si este captusita cu vata de sticla. Deasupra instalatiei se monteaza o palnie de separare pentru picurarea probei si apoi a apei distillate. Solutia se capteaza intr-un balon cotat de 50ml si este limpede.
Din solutia de mai sus se pipeteaza 25ml intr-o capsula de portelan, se adauga 4 picaturi solutie HCl 18% si se concentreaza pe baia de apa la un volum cat mai mic. Solutia se spala de pe pereti cu cateva picaturi apa distilata si se trece intr-o micropalnie de separare unde se spala in portiuni de 4 ori cu cate 5 ml eter etilic sub agitare energica. Aceasta etapa se face pentru a elimina eventualele parti grase (lecitina etc). Faza apoasa separata este trecuta intr-o capsula de portelan si se aduce la sec. Reziduul rezultat se trece cantitativ cu 5ml apa distilata intr-un balon cotat de 50ml si se adauga 5 ml solutie acid picric si 0.5ml solutie NaOH. Se obtine o solutie limpede de o coloratie portocalie. Se agita bine si se lasa in repaus 20 minute la 20°C, dupa care aducem la semn cu apa distilata. Se mai lasa in repaus timp de 20 minute, dupa care se determina extinctia probei la 510nm fata de martor, obtinut astfel: intr-un balon cotat de 50ml am pipetat 20ml apa distilata, 5ml acid picric si 0.5ml solutie NaOH. Se agita si se lasa in repaus 20 minute, dupa care se aduce la semn cu apa distilata.
III.2.2.3.2.2. REZULTATE EXPERIMENTALE
S-au obtinut urmatoarele date experimentale: Emartor = ─ 0.0197
Eproba = 0.0676
Epf = 0.0873
III.2.2.3.2.3. CALCULUL CONTINUTULUI DE CREATININA AL PROBEI
Epf = 0.0873
Y= ─0.02528+0.75976.X
Din curba de etalonare obtinem continutul de creatinina ca fiind: X=0.1482 mg/proba, iar valoarea exprimata in µg/ml proba: a=1.482 µg creatinina/ml. Din formula de calcul obtinem continutul procentual in proba analizata: K=68.134 mg creatinina/100g proba.
Tinand seama de continutul mediu de creatinina al unui extract uzual de carne de 7.2% acceptat la inceputul prezentarii determinarilor experimentale se poate determina un continut mediu procentual (c) al extractelor de carne in probele analizate. Astfel am obtinut o valoare de c=0.95% extract in cubul concentrat.
Valorile extinctiilor obtinute la 510nm pentru cele 10 determinari sunt prezentate in Tabelul.3, iar continutul de creatinina in Tabelul 4.
|
Nr. proba |
Tipul probei |
Cantitate cantarita (g) |
E510 (nm) |
|
1. |
Maggi, cub gaina |
5.4378 |
0.0873 |
|
2. |
Knorr, cub vita |
5.8174 |
0.0512 |
|
3. |
Korr, cub costita afumata |
6.6117 |
0.0098 |
|
4. |
Maggi, cub pui |
6.3251 |
0.1196 |
|
5. |
Maggi, cub legume |
5.5002 |
0.1775 |
|
6. |
Knorr, ciorba de burta |
7.4298 |
0.1250 |
|
7. |
Gallina Blanca, cub pui |
5.4183 |
0.0624 |
|
8. |
Knorr, cub gaina |
5.4251 |
0.0892 |
|
9. |
Knorr, cub legume | ||
|
Maggi, Apetit, granule |
Tabelul 3: Prelucrarea probelor si valorile obtinute din curba de etalonare
(Eproba la λ=510nm)
|
Nr. proba |
Tipul probei |
Continut de creatinina |
Cont.de extract de carne al probelor (c,%) |
||
|
Val. cf. dreptei de etalonare (X, mg/proba) |
Val. exprimata in (a, µg/ml proba) |
Cont. procentual in proba analizata (K, mg/100g proba) |
|||
|
1. |
Maggi, cub gaina |
0.1482 |
1.482 |
68.134 |
0.9463 |
|
2. |
Knorr, cub vita |
0.1007 |
1.007 |
43.275 |
0.6010 |
|
3. |
Knorr, cub costita afumata |
0.0462 |
0.462 |
17.469 |
0.2426 |
|
4. |
Maggi, cub pui |
0.1907 |
1.907 |
75.374 |
1.0468 |
|
5. |
Maggi, cub legume |
0.2669 |
2.669 |
121.310 |
1.6849 |
|
6. |
Knorr, ciorba de burta |
0.1978 |
1.978 |
66.560 |
0.9244 |
|
7. |
Gallina Blanca, cub pui |
0.1154 |
1.154 |
53.245 |
0.7395 |
|
8. |
Knorr, cub gaina |
0.1482 |
1.482 |
68.294 |
0.9485 |
|
9. |
Knorr, cub legume | ||||
|
Maggi, Apetit, granule | |||||
Tabelul 4 Determinarea continutului de creatinina si extract de carne din probele analizate
III.3. CONCLUZII
Scopul lucrarilor experimentale a fost identificarea prezentei extractelor de carne in diferite produse concentrate solide comercializate pe piata. Metoda folosita a presupus izolarea si determinarea cantitativa a creatininei ca dovada a prezentei adaosului de extract de carne in astfel de produse. In vederea, determinarii cantitative a creatininei s-a apelat la metoda spectrofotometrica general acceptata in prezent, utilizata in laboratoarele de analiza, mentionata si descrisa in standardele de specialitate.
Metoda presupune obtinerea unui extract apos al probei de analizat care este eliberat de constituentii nedoriti prin tratare cu acid tricloracetic si centrifugare. In extractul purificat in mediul de HCl creatina prezenta ciclizeaza la creatinina.
Celelalte substante insotitoare ce ar putea deranja determinarea au fost indepartate prin purificarea extractului prin trecerea sa pe o coloana cu alumina activata, urmata de extractii repetate cu eter etilic. Creatinina existenta in extractul final purificat formeaza cu acidul picric in mediu alcalin complexul stabil de culoare galbena cu un maxim caracteristic de absorbtie la lungimea de unda 510nm pe a carui determinare se bazeaza dozarea finala a continutului de creatinina a probelor.
Lucrarile experimentale au presupus doua etape:
trasarea curbei de etalonare folosind creatinina-substanta etalon;
prelucrarea probelor in vederea determinarii continutului de creatinina, respectiv a continutului procentual de extract de carne in probe. In acest scop s-a luat in considerare o valoare medie a continutului de creatina/creatinina in extractele uzuale de carne de 7.2%.
In partea experimentala a fost prezentat in detaliu modul de trasare a curbei de etalonare cu prezentarea ecuatiei algebrice si caracteristicilor acesteia, precum si etapele parcurse impreuna cu calculul final pentru una din probele analizate. Rezultatele obtinute pentru toate cele 10 probe au fost apoi prezentate in tabelele 3 si 4.
Din examinarea lor se pot desprinde urmatoarele concluzii:
1. Pentru concentratele tip cuburi cu aroma de pui, respectiv gaina, continutul procentual in extract de carne are valori apropiate pentru toate formele din care s-au efectuat probe:
Maggi, cub gaina ~ 0.95%
Maggi, cub pui ~ 1.05%
Gallina Blanca, cub pui ~ 0.74%
Knorr, cub gaina ~ 0.95%
2. In cazul concentratelor tip cub de alta provenienta, continutul procentual in extract de carne, este mult mai scazut. Astfel pentru cuburile cu aroma de vita de la Knorr el este de ~ 0.6%, iar pentru cuburile cu aroma de costita afumata de la Knorr este de ~ 0.24% (probabil ca in acest caz gustul final se datoreaza in cea mai mare masura adaosurilor de compusi cu aroma de fum).
3. Pentru cuburile concentrate de legume, in cazul celui provenit de la firma Maggi s-a inregistrat un continut procentual ridicat al extractului de carne( ~ 1.68%), dar care este posibil sa se datoreze si altor constituenti pe care purificarile pe coloane nu i-au putut indeparta. A fost singura proba care, chiar si dupa trecerile pe coloane si-a mentinut nuanta galbuie.
4. Prezenta extractului de carne a fost determinata si in concentratul tip granule Apetit de la firma Maggi, in concordanta de fapt cu mentiunile de pe ambalaj in ceeea ce priveste ingredientii.
Desi, majoritatea firmelor nu dau in cifre continutul procentual in extract de carne al acestui tip de produse, cifra datelor generale in ceea ce priveste tehnologia lor de obtinere, valoarea medie este in jur de 1%, ceea ce confirma datele obtinute experimental.
BIBLIOGRAFIE
Alfa Xenia Lupea, " Biochimie", Ed. Politehnica Timisoara, 2003, ISBN 973-625-101-2
H.D.Belitz, W. Crroscle, " Food Chemistry", Ed. 2, Springer Verlag New York, Berlin, Heidelberg, London, Paris, 1987
Alfa Xenia Lupea, M.Padure, D. Ardelean, "Chimia si Controlul alimentar de origine animala", Ed. Politehnica Timisoara, 2000, ISBN 973-9389-90-2
R. Matissek, F. M. Schnepel, G. Steiner, "Lebeusmittelanalitik", Ed. 2, Springer Verlag New York, Berlin, Heidelberg, London, Paris, 1992
*** Official Methods of Analysis of AOAC
International, 16th ed., edited by Patricia
*** Willey Encyclopedia of Food Science and Technology, 2nd ed., edited by F. J. Francis, John Willey & Sons, 1999
M. Wyss, R. Kaddurah-Daouk, "Creatine and Creatinine Metabolism", Physiological Reviews, 80, p.1107-1213, 2000
V. C. Myers, M. S. Fiue, "The Metabolism of Creatine and Creatinine", J. of Biological Chemistry, 4, 1915, p. 377-381
E. Bozler, "The Role of Phosphocreatine and Adenosine-Triphosphate" in Muscular Contractin, The Journal of General Phisiology, febr. 1953, p. 63-70
https://www.absolute-creatine.com
https://en.wikipedia.org/wiki/Creatine
https://en.wikipedia.org/wiki/Creatinine
|
Politica de confidentialitate |
| Copyright ©
2024 - Toate drepturile rezervate. Toate documentele au caracter informativ cu scop educational. |
Personaje din literatura |
| Baltagul caracterizarea personajelor |
| Caracterizare Alexandru Lapusneanul |
| Caracterizarea lui Gavilescu |
| Caracterizarea personajelor negative din basmul |
Tehnica si mecanica |
| Cuplaje - definitii. notatii. exemple. repere istorice. |
| Actionare macara |
| Reprezentarea si cotarea filetelor |
Geografie |
| Turismul pe terra |
| Vulcanii Și mediul |
| Padurile pe terra si industrializarea lemnului |
| Termeni si conditii |
| Contact |
| Creeaza si tu |