
In cadrul acestui capitol au fost analizate doua creme si o solutie bifazica de curatare a tenului din gama Avene si anume: crema tratament pentru ten acneeic (C I), crema tratament atiiritanta hidratanta (C II), lotiune matifianta purifianta (C III), urmarind calitatea acestora. Toate cremele sunt din categoria cremelor dermato-cosmetice .
Cremele au fost pastrate in recipiente adecvate, bine inchise, la temperatura camerei.
Au fost efectuate urmatoarele determinari:
Calculele si rezultatele determinarilor efectuate sunt redate in continuare:
Circa 1 g proba se preseaza intre doua placi de sticla de 10 x 25 cm, pana cand se obtine un strat uniform de circa 0,5 mm. Stratul de proba se examineaza apoi prin transparenta la lumina.
Proba se intinde in strat subtire pe o placa de sticla, dupa care se percepe mirosul organoleptic.
Se intinde o cantitate de proba in strat subtire pe o hartie alba, velina si se compara culoarea cu a mostrei etalon, pregatita in mod identic cu proba de analizat.
Aspectul, mirosul si culoarea sunt prezentate in tabelul numarul 12.
Tabelul nr.12. Caracteristicile organoleptice ale cremelor cosmetice.
|
Formula |
Aspect |
Miros |
Culoare |
|
C I |
Omogena, se intinde cu usurinta |
Specific |
Galbena |
|
C II |
Omogena, consistenta , se intinde cu usurinta |
Specific |
Alba |
|
CIII |
Solutie bifazica |
Specific |
Alba |
Culoarea galbena a cremei CI (crema tratament antiacneic) este data de prezenta pigmentului Red33, care este un colorant azoic.Mai este cunoscut sub denumirea de Acid Red 33 sau Simply Red 33 .
Solubilitatea poate fi exprimata prin specificarea volumului de solvent (in mL) necesar pentru a dizolva 1 g substanta solida, la temperaturi de 20±2°C.
Verificarea solubilitatii nu este necesara sa se efectueze cu toti solventii prevazuti in monografie, cel putin doi solventi diferiti. Daca se constata prezenta unor impuritati insolubile, se verifica solubilitatea si in ceilalti solventi prevazuti.
Cand se prevede solubilitatea in solutii de acizi sau in solutii de baze nu se precizeaza volumul din solutia respectiva, deoarece dizolvarea are loc ca urmare a unei reactii.
La grasimi, ceruri si parafine, solubilitatea se determina prin agitarea acestora, pana la dizolvarea sau topirea acestora, adaugarea solventului, agitare pana la racire si verificarea solubilitatii dupa ce solutia s-a tinut la 20±2°C timp de 2 h. Cand in amestec are loc o degajare de caldura, verificarea solubilitatii substantelor respective se efectueaza dupa 2 h de la dizolvare, timp in care amestecul este tinut la 20±2°C.
Caand se folosesc solventi volatili, determinarile se efectueaza in flacoane cu dop rodat.
Masa substantelor luate in lucru pentru determinarea solubilitatii se calculeaza astfel incat sa rezulte, de obicei 10-20 mL solutie.
Substanta se considera dizolvata cand solutia examinata cu ochiul liber nu mai prezinta particule in suspensie. Nu se iau in considerare urmele de impuritati mecanice daca solutia, fara a fi filtrata, corespunde etalonului de transparenta si daca dupa un repaus de 1 h, aceste impuritati nu formeaza un reziduu vizibil.
Solubilitatea. Solventii in care se dizolva cremele cosmetice sunt prezentate in tabelul numarul.13
Tabelul nr.1Solubilitatea
|
Solventul |
C I |
C II |
C III |
|
Alcool metilic |
Total solubila |
Insolubila |
Insolubila |
|
CCl4 |
Insolubil |
Insolubila |
Insolubila |
|
Apa calda |
Total solubila |
Partial solubila |
Insolubila |
|
Benzen |
Insolubila |
Insolubila |
Insolubila |
|
Eter de petrol |
Insolubila |
Insolubila |
Insolubila |
|
HCl[35%] |
Total solubil |
Insolubila |
Partial Solubila |
a.Metoda prin colorare
Emulsii de tip ulei in apa
Reactivi
Albastru de metil, solutie 1%.
Mod de lucru
Pe o sticla de ceas sau pe o placa de sticla, se intinde un strat de proba cu grosimea de circa 1 mm. In cateva locuri ale stratului de proba, se adauga cu pipeta cate o picatura de solutie de albastru de metil. Dupa 1015 minute se examineaza suprafata probei.
Daca reactivul a difuzat in stratul de proba si s-au format pete de culoare albastra, emulsia este de tipul ulei in apa.
Emulsii de tip apa in ulei
Reactivi
-sudan III, solutie 1% in ulei de floarea soarelui.
Mod de lucru
Se procedeaza conform modului de lucru al emulsiilor de tip ulei in apa, cu deosebirea ca in loc de solutie de albastru de metil se adauga o picatura de solutie sudan III.
Daca reactivul a difuzat in stratul de proba si s-au format pete de culoare rosie, emulsia este de tip apa in ulei.
b. Metoda dilutiei
Cremele nu se pot dilua decat in faza lor continua. Ca atare, daca crema se dilueaza in apa, inseamna ca faza ei continua e apoasa, deci tipul de crema este U/A. Daca crema se dilueaza in ulei, faza continua este uleioasa, crema este deci de tipul A/U.
c. Metoda conductivitati
In cadrul acestei metode se introduc doi electrozi in masa cremei si daca permite trecerea curentului inseamna ca masa curentului o formeaza apa, deci tipul emulsiei este U/A. Daca crema nu permite trecerea curentului electric intre cei doi electrozi, emulsia are faza continua de ulei, de tip A/U. De obicei in circuit se introduce o lampa cu neon sau un galvanometru. In cazul emulsiei de tip U/A, lampa se aprinde: daca lampa cu ulei se aprinde cu intermitenta, sau numai dupa un anumit timp de la trecerea curentului electric este o emulsie dubla sau o emulsie A/U.
Aparatura
-termostat care asigura mentinerea temperaturii la 4 si la 40°C.
Mod de lucru
Intr-o fiola de cantarire se introduce circa 5g de proba, se acopera cu capacul si se tine in termostat timp de 8h la temperatura de 4°C. Se scoate fiola din termostat, se examineaza proba, se acopera cu capacul si se reintroduce in termostat la temperatura de 40°C, timp de 8h, dupa care se examineaza din nou.
Proba se considera stabila daca fazele nu se separa.
In urma determinarii stabilitatii la 4 si la 40 °C am observat ca toate cremele au fost stabile de la temperatura de 4 °C
Aparatura
-pH-metru sau hartie de pH, dupa caz.
Reactivi
-apa distilata:
-parafina
Pregatirea extractului apos
In cazul cremelor semigrase:
Se introduce circa 1g proba intr-un pahar de laborator, se adauga 99cm3 apa, se fierbe timp de 5 minute si se filtreaza prin hartie de filtru cu porozitate medie.
In cazul cremelor grase:
Intr-un pahar de laborator se amesteca circa 2g de proba cu 30cm3 apa si 5g parafina. Amestecul se incalzeste pe baie de apa timp de 30min, amestecand din cand in cand. Apoi se raceste, se indeparteaza turta de parafina si solutia se filtreaza prin hartie de filtru cu porozitate medie.
Determinarea ph-ului se face pe extractul apos obtinut cu hartie indicator de pH sau cu pH-metrul Consort C535
Tipul de emulsie si pH-ul determinat sunt prezentate in tabelul numarul 14
Tabelul nr.14. Tipul de emulsie si pH-ul
|
Formula |
Tipul de emulsie |
pH-ul cu pH metru |
pH-ul cu hartia de pH |
|
C I |
U/A | ||
|
C II |
U/A | ||
|
C III |
U/A |
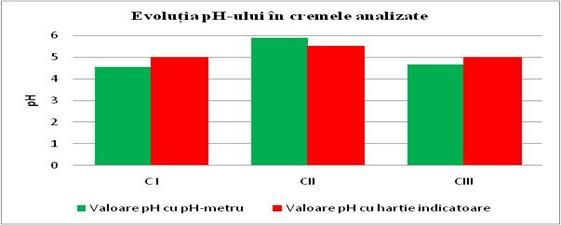
Toate cremele prezinta tipul de emulsie U/A, iar pH-ul variaza, C II avand pH-ul cel mai mare, iar CI cel mai mic.Valoarea mai mica a pH-ului la CI este data de continutul de acid glicolic cunoscut si ca acid hidroxiacetic (AHA) .Concentratia de acid glicolic din CI este de 6%. Daca ne luam dupa valoarea data de pH-metru ,valoare mult mai precisa decat cea data de hartia de pH cea mai apropiata valoare de pH-ul tenului o are C II.
Prin punct de topire se intelege temperatura la care o substanta se topeste complet. Daca substanta se topeste cu descompunere, se considera punct de topire sau punct de descompunere temperatura la care substanta isi schimba aspectul (se brunifica sau apar bule de gaz).
Determinarea punctului de topire la grasimi, ceara, rasini si produse asemanatoare
Tehnica de lucru
Un tub de sticla deschis la ambele capete, cu lungimea de 10 cm, cu diametru interior de 2 mm si cu grosimea peretelui de 0.5 mm se introduce prin presare si prin rotire, in masa solida ca atare (la untul de cacao) sau in masa solida topita, astfel incat sa se obtina un strat compact cu inaltimea de aproximativ 10 mm. Tubul astfel umplut se tine timp de 24 h la gheata sau la o temperatura sub 15 °C, apoi se ataseaza la un termometru cu ajutorul unui inel de cauciuc, astfel incat substanta din tub sa se gaseasca la acelasi nivel cu partea mijlocie a rezervorului cu mercur al termometrului. Se foloseste un termometru pana la 100°C, cu diviziuni din 0.5°C. Termometru cu tubul fixat se introduce intr-un balon Kjedahl de 250 mL, care contine apa, astfel incat tubul sa fie scufundat sub nivelul apei, pe o portiune de aproximativ 40 mm. Apa se incalzeste, in prealabil la o temperatura cu aproximativ 5°C sub punctul de topire presupus.Dupa introducerea tubului, incalzirea se continua, astfel incat sa se ridice cu 1°C/minut.
Se considera punct de topire temperatura la care substanta se deplaseaza catre partea superioara a tubului.
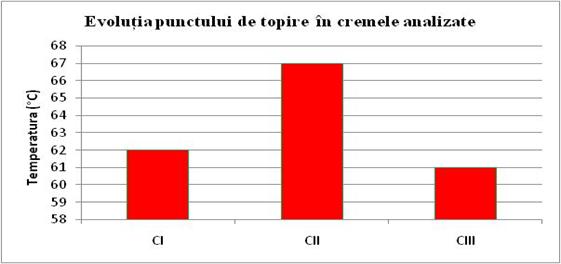
Temperaturile de topire determinate sunt prezentate in tabelul 15
Tabelul nr .15.Temperatura de topire
|
Formula |
Temperatura (0C) |
|
CI | |
|
CII | |
|
CIII |
In urma determinarilor reiese ca CIII are punctul de topire cel mai mic , iar CII cel mai mare .Pentru a mentine stabilitatea produselor , se recomanda depozitarea acestora la temperatura scazuta si ferite de lumina.
Mod de lucru
Intr-o fiola de cantarire cu circa 5g nisip calcinat, adusa in prealabil la masa constanta prin incalzire in etuva la 105 ± 5°C, se cantareste cantitatea de proba indicata in standardul de produs.
Fiola cu proba se introduce in etuva la 105 ± 5° si se usuca pana la masa constanta.
Calcul: continutul de apa si substante volatile se exprima in procente si se calculeaza cu formula:

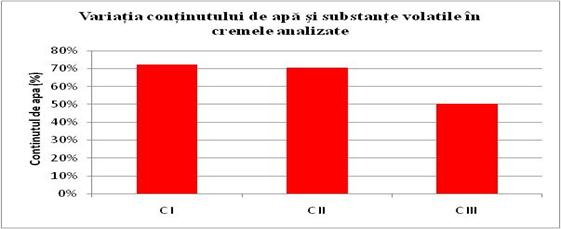
C I = 2910-2870 x 100 / 0.18 = 72.22%
C II = 3360-3100 x 100 / 0.37 =70.27%
C III = 61.740-61.140 x 100 / 1.21 = 50%
Continutul de apa si substante volatile determinate sunt prezentate in tabelul numarul 15.
Tabelul nr.16. Continutul de apa si substante volatile
|
Formula |
Continutul de apa si substante volatile |
|
C I | |
|
C II | |
|
C III |
Deoarece continutul de apa trebuie sa fie cat mai mare, indiferent de tipul de crema, crema cea mai hidratanta este C I.Procentul cel mai mic s-a inregistrat la CIII.Aceste rezultate sunt plauzibile , avand in vedere ca pe etichetele produselor CI si CII primul ingredient mentionat este apa termala .Procentul scazut inregistrat la CIII , se datoreaza faptului ca proba este o lotiune matifianta purifianta bifazica ,din care a fost indepartata faza apoasa , prin extractie, si ulterior s-a determinat continutul de apa si substante volatile.
Continutul de substante grase se poate determina prin doua metode:
-metoda I,
-metoda II.
Metoda I
Principiul metodei
Proba se incalzeste cu acid clorhidric sau sulfuric pentru separarea fazelor, iar substantele grase se extrag cu parafina si se dozeaza gravimetric.
Reactivi
-acid clorhidric 30%, sau acid sulfuric 30%,
-alcool etilic 96%vol.,
-metiloranj, solutie 0.1%,
-parafina.
Mod de lucru
In cazul emulsiilor si al cremelor cu continut de substante grase totale peste 45% se cantareste circa 5g de proba si se introduce intr-un pahar de laborator de 250cm Se adauga 30cm3 apa si 20cm3 acid clorhidric sau sulfuric.
Amestecul se incalzeste pe baie de apa la fierbere pentru separarea neta a fazelor.
Daca fazele nu se separa, se ia o noua cantitate de proba peste care se adauga doar 50 cm3 acid clorhidric sau sulfuric.
Se incalzeste pe baie de apa pana la separarea neta a continutului paharului, in doua straturi.
In cazul cremelor si emulsiilor cu continut de substante grase totale de max. 45% se cantareste circa 5g proba si se introduce intr-un vas conic de 250cm
Se adauga 50cm3 alcool etilic si 20cm3 acid clorhidric sau sulfuric. Amestecul se incalzeste pe baie de apa la fierbere, cu refrigerant ascendent, pana la separarea neta a fazelor, apoi se trece cantitativ intr-un pahar de laborator de 250 cm3, spaland vasul cu 25 cm3 apa fierbinte si 50cm3 alcool etilic.
Se adauga doua sau trei picaturi de solutie de metiloranj.
In cazul in care stratul apos nu se coloreaza in rosu, se adauga 2-3 cm3 acid clorhidric sau sulfuric si se fierbe din nou, pe baie de apa.
Operatiile se repeta in continuare ca mai sus, pana cand se obtine o coloratie rosie persistenta a stratului apos.
Se adauga 10 g parafina, cantarite cu precizie de 0,0002 g si amestecul se incalzeste pe baie de apa, agitand din cand in cand cu o bagheta, pana la topirea completa a parafinei si separarea neta a continutului paharului in doua straturi.
Paharul se lasa sa se raceasca cu bagheta in interior. Dupa racire turta de parafina se desprinde cu ajutorul baghetei, se scoate si se spala cu apa pana la reactie neutra.
Turta de parafina se usuca pe o hartie de filtru, apoi se aseaza intr-un pahar de laborator, adus la masa constanta prin uscare in etuva la 105 ± 5°C.
Paharul cu turta de parafina se introduce in etuva la 105 ± 5°C si se usuca pana la masa constanta.
 Calcul: continutul de substante
grase totale se exprima in procente si se calculeaza cu formula:
Calcul: continutul de substante
grase totale se exprima in procente si se calculeaza cu formula:
Metoda II
Principiul metodei
Proba se incalzeste cu acid clorhidric sau sulfuric pentru separarea fazelor, iar substantele grase se extrag cu eter de petrol si se dozeaza gravimetric.
Reactivi
-acid clorhidric 20%, sau acid sulfuric 20%,
-eter de petrol,
-metiloranj, solutie 0.1%,
-sulfat de sodiu, anhidru.
Mod de lucru
Se cantaresc 2-3 g de proba, se introduc intr-un pahar de laborator de 200 cm3 , se adauga 20cm3, acid clorhidric sau sulfuric si doua sau trei picaturi de solutie de metiloranj pe baie de apa la fierbere pana la separarea neta a fazelor.
Continutul paharului se trece cantitativ intr-o palnie de separare, spaland paharul cu 3050 cm3 eter de petrol care se adauga tot in palnia de separare. Se adauga 3050 cm3 apa, se agita pentru extractia glicerinei in apa si se lasa sa se separe straturile.
Solutia apoasa se trece intr-o palnie de separare, iar solutia eterica se supune la extractii repetate cu apa, pana la reactie neutra (dispare culoarea rosie)
Solutiile apoase unite in aceeasi palnie de separare se spala cu 3050 cm3 eter de petrol, iar dupa separarea straturilor se unesc solutiile eterice din cele doua palnii.
Solutiile astfel obtinute se filtreaza printr-o hartie de filtru cu porozitate medie, tratata, trecand intai solutia eterica si spaland hartia de filtru cu eter de petrol, apoi solutia apoasa care se prinde separat.
Solutia eterica se filtreaza apoi peste sulfat de sodiu anhidru prin hartie de filtru cu porozitate mare, intr-un balon uscat in etuva la 105 ± 5°C si cantarit. Filtru se spala cu eter de petrol, care se prinde in acelasi balon.
Eterul de petrol se distila incalzind balonul pe baie de apa, iar reziduul se usuca in etuva la 105 ± 5°C timp de 30 minute, apoi se cantareste.
Calcul
Continutul de substante grase totale se exprima in procente si se calculeaza cu formula:
Substantele grase totale = m /m1 x 100
m1- masa rezidului dupa uscare, in grame
m -masa probei luate pentru determinare, in grame
CI=1/2.13x100=46 %
CII=1/1.82x100=55%
CIII=1/91x100=52%
Tabelul nr.17. Continutul de substante grase totale
|
Formula |
Continutul de substante grase totale |
|
C I | |
|
C II | |
|
C III |
Cel mai mare continut de substante grase il are formula CII , iar cel mai mic procent il inregistreaza formula CI.Avand in vedere ca formula CII este o crema hidratanta, aceasta valoare este justificata .Continutul ridicat de substante grase totale din formula CII este dat de prezenta trigliceridelor de acid caprilic sau capric care au rolul de a completa deficitul de lipide din cimentul intercelular ,gresand pielea si evita pierderea de apa .
Prin indice de aciditate se intelege numarul de mg de KOH necesar pentru neutralizarea acizilor grasi liberi continuti in 1 g de proba de analizat.
Valoarea acestui indice ajuta la aprecierea calitatii grasimilor, prin determinarea acizilor grasi liberi ce apar ca rezultat al hidrolizei partiale in prezenta microorganismelor, cat si al transformarilor degradative din procesul rancezirii.
Tehnica de lucru
Se cantaresc la balanta 5 g proba de analizat, daca nu se prevede altfel. Se dizolva in 50 ml amestec, format din volume egale de alcool si eter, neutralizat in prealabil cu fenolftaleina si se tireaza cu KOH 0.1 n in apa pana la coloratie roz.
Indice de aciditate se calculeaza conform formulei:
IA=5.61xV/m
In care :
IA = indice de aciditate
V = volumul de KOH 0.1 n in apa folosit la titrare (in mL) :
M = masa probei luate in lucru (g) ;
5.61 = numarul de mg de KOH corespunzatoare la 1 mL KOH 0.1 n in apa.
Daca in timpul titrarii apare o tulbureala se mai adauga amestec de alcool-eter pana la redizolvare.
Pentru determinarea factorului de corectie al KOH 0.1 n am folosit trei pahare Erlenmayer in care am pus pentru fiecare dupa cum urmeaza:
-5 mL solutie etalon H2C2O4 0.1n ;
-indicator rosu de metil ;
-si am titrat cu KOH 0.1 n de la rosu pana la obtinerea culorii galben, obtinand urmatoarele rezultate :
F = V1 / V2,
unde, V1 = volumul solutiei etalon 5 mL ;
V2 = volumul folosit la titrare.
F1 = 5 mL / 5.2 = 0.9615
F2 = 5 mL / 5.1 =0.9803
F3 = 5 mL / 5.2 = 0.9615
F = F1 + F2 + F3 / 3=0.9615 +0.9803 +0.9615=0.9677
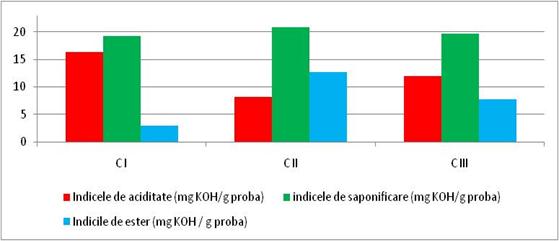
IA(C I ) = 5.6 x 3x 0.9677 / 1 = 16.25mg KOH/g proba
IA(C II ) = 5.6 x 1.5 x 0.9677 / 1 = 8.12 mg KOH/g proba
IA(C III ) = 5.6 x 2.2 x 0.9677 / 1 = 11.92 mg KOH/g proba
Tabelul nr.18 Indicele de aciditate
|
Formula |
Indicele de aciditate mg KOH/g proba |
|
C I | |
|
C II | |
|
C III |
Conform indicelui de aciditate, adica a volumului de KOH necesar neutralizarii continutului de acizi grasi din proba, s-a obtinut cel mai mic indice de aciditate la C II si C III iar cea mai mare la C I.Valorile sunt plauzibile , avand in vedere ca produsele sunt destinate tratamentului antiacneic , iar pe etichete nu se regasec acizii grasi.
Principiul metodei
Substantele grase din proba se saponifica cu hidroxidul de potasiu in exces. Excesul de hidroxid de potasiu se titreaza cu acid clorhidric.
Reactivi
-acid clorhidric 0.5 n;
-benzen sau xilen;
-fenolftaleina, solutie 1% m alcool etilic 70% volum;
-hidroxid de potasiu, solutie 0.5 n in alcool etilic 90% volum.
Mod de lucru
Se cantaresc 5g de proba si, impreuna cu turta de parafina obtinuta in cazul determinarii continutului de substante grase totale, se introduce intr-un vas conic de 250cm3 prevazut cu refrigerent ascentdent si se adauga 250cm3 benzen sau xilen si 25cm3 solutie de hidroxid de potasiu. Se fierbe pe baie de apa, cu reflux, timp de minimum 2h.
Dupa fierbere, solutia se titreaza imediat fara a se raci, cu acid clorhidric, in prezenta a trei sau patru picaturi de solutie de fenolftaleina, pana la decolorarea solutiei.
In paralel se efectueaza o proba de control al reactivilor, trecand prin toate fazele analizei aceiasi reactivi ca la proba de analizat, luati in aceeasi cantitati.
Calcul: indicele de saponificare se exprima in miligrame de hidroxid de potasiu pe gram de produs si se calculeaza cu formula:
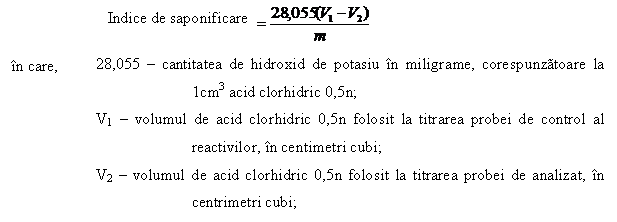
Pentru determinarea factorului de corectie al HCl 0.5 n, am folosit trei pahare Erlenmayer in care am pus pentru fiecare dupa cum urmeaza:
-10 mL solutie etalon de borax (Na2B4O7 x 10 H2O) 0.5 n
-2-3 picaturi indicator rosu de metil ;
-si am titrat cu HCl 0.5 n de la culoarea galben la rosu, obtinand urmatoarele rezultate :
F = V1 / V2,
unde, V1 = volumul solutiei etalon 10 mL ;
V2 = volumul folosit la titrare.
F1 = 10 mL / 10.2 = 0.9803
F2 = 10 mL / 10.2 =0.9803
F3 = 10 mL / 10.3 = 0.9708
F = F1 + F2 + F3 / 3=0.9803 +0.9803 +0.9708=0.9771
Is(C I ) = 28.055 x (4.2 - 0.7) x 0.9771 /5 = 19.18 mg KOH/g proba
Is(C II ) = 28.055 x (4.5- 0.7) x 0.9771 / 5= 20.83 mg KOH/g proba
Is(C III ) = 28.055 x (4.3- 0.7) x 0.9771 /5= 19.7 mg KOH/g proba
Tabelul nr.19. Indice de saponificare
|
Formula |
Indicele de saponificare mg KOH/g proba |
|
C I | |
|
C II | |
|
C III |
Indicele de saponificare , adica volumul de KOH necesar neutralizarii acizilor grasi rezultati la saponificarea probei de analizat, este cea mai mica la C I, iar cea mai mare la C II.Rezultatele sunt in concordanta cu valorile indicelui de aciditate .
Prin indice de ester se intelege numarul de miligrame de KOH necesar pentru neutralizarea acizilor grasi rezultati din saponificarea a 1 gram de proba de analizat.
Indice de ester se calculeaza conform formulei:
IE = IS - IA
In care:
IE = indice de ester
IS = indice de saponificare;
IA = indice de aciditate
IE(C I ) = 19.18 mg/g - 16.26 mg/g = 2.92 mg KOH/g proba
IE(C II ) = 20.83 mg/g - 8.12 mg/g = 12.71 mg KOH/g proba
IE(C III ) = 19.7 mg/g - 11.92 mg/g = 7.78 mg KOH/g proba
Tabelul nr.20. Indice de ester
|
Formula |
Indicele de ester mg KOH/g proba |
|
C I | |
|
C II | |
|
C III |
Indicele de ester adica numarul de miligrame de KOH necesar pentru neutralizarea acizilor grasi rezultati din saponificarea a 1 gram de proba de analizat a avut valoarea cea mai mare la formula CII si cea mai mica in formula CI.
Gradul de nesaturare a unei grasimi se apreciaza prin indicele de iod. Indicele de iod este o valoare care reprezinta cantitatea de iod exprimata in grame, ce se aditioneaza la 100g proba de analizat.
Tehnica de lucru
Se cantareste 1 g de proba, se dizolva in 4 ml cloroform si se adauga 5 ml solutie alcoolica de iod 0.1 n intr-un flacon cu dop rodat de 300 mL. Flaconul se inchide si se tine la intuneric timp de 30 minute, agitand din cand in cand. Se adauga 3 mL KI, 2 mL apa si se titreaza cu tiosulfat de sodiu 0.1n pana la coloratie galben-deschis. Se adauga 0.4 mL amidon si se continua titrarea, agitand puternic pana la decolorare.
In paralel se efectueaza determinarea cu o proba martor.
Indicele de iod se calculeaza conform formulei:
II = (V1-V2) x 0.01269 x 100 / m
In care:
II = indice de iod
V1 = volumul de tiosulfat de sodiu 0.1 n folosit la titrarea probei luate martor (mL);
V2 = volumul de tiosulfat de sodiu 0.1 n folosit la titrarea probei luate in lucru (mL);
m = masa probei luate in lucru (g);
0.01269 = numarul de g de iod corespunzator la 1 mL tiosulfat de sodiu 0.1n.
Pentru determinarea factorului de corectie al Na2S2O3 0.1 n am folosit trei pahare Erlenmayer in care am pus pentru fiecare dupa cum urmeaza:
-5 mL solutie etalon K2Cr2O7 0.1 n ;
-5 mL H2SO4 1 :1 ;
-o spatula de KI, le-am tinut la intuneric timp de 15 minute si apoi am titrat cu Na2S2O3 0.1 n pana la culoarea galben-pai, obtinand urmatoarele rezultate :
F = V1 / V2,
unde, V1 = volumul solutiei etalon 5 mL ;
V2 = volumul folosit la titrare.
F1 = 10 mL / 9.8 = 1.020
F2 = 10 mL / 9.8 =1.020
F3 = 10 mL / 9.9 = 1.0101
F = F1 + F2 + F3 / 3=1.020 + 1.020 + 1.0101=1.016
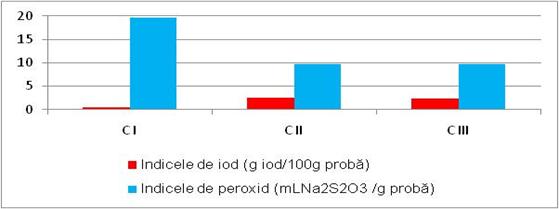
II(C I ) = (4-0) x 0.01269g /mL x 100 x 1.016/ 1 g=0.51 g iod/100g proba
II(C II ) = (4-1.8) x 0.01269g /mL x 100 x 1.016/ 1 g=2.6 g iod/100g proba
IIC III ) = (5.3-4) x 0.01269g /mL x 100 x 1.016/ 1 g=2.44 g iod/100g proba
Tabelul nr.21. Indicele de iod
|
Formula |
Indicele de iod g iod/100g proba |
|
C I | |
|
C II | |
|
C III |
Indicele de iod obtinut la cele trei creme, adica continutul in hidrocarburi nesturate, este cel mai mic la C I si cel mai mare la CII.Cantitatea de iod , este destul de mica indicand faptul ca nu exista concentratii ridcate de hidrocarburi nesaturate , iar probele analizate au fost proaspete.
Principiul metodei
Indicele de peroxid reprezinta continutul de peroxid si alte substante oxidante dintr-o anumita cantitate de produs, care, in conditiile metodei descrise in acest standard, oxideaza iodura de potasiu punand in libertate iodul.
Proba se dizolva intr-un amestec de acid si cloroform, se adauga iodura de potasiu, apoi se titreaza iodul pus in libertate, cu tiosulfat de sodiu in prezenta de amidon.
Reactivi
-acid acetic glacial;
-amidon, solutie 1%, proaspat preparata;
-cloroform;
-iodura de potasiu;
-tiosulfat de sodiu, solutie 0.01 n.
Mod de lucru
Se cantaresc circa 5g proba si se dizolva intr-un amestec din 18cm3 acid acetic si 12cm3 cloroform, intr-un vas conic cu dop slefuit. Se adauga o solutie proaspata preparata dintr-un gram de iodura de potasiu si 1cm3 apa si se agita puternic. Dupa 1min, se adauga 30cm3 apa si 2cm3 solutie de amidon si se tritreaza cu solutie de tiosulfat de sodiu.
In paralel se efectueaza o proba de control al reactivilor, trecand prin toate fazele analizei aceeasi reactivi ca la proba de analizat, luati in aceleasi cantitati.
Calcul: indicele de peroxid se exprima in miliechivalenti de peroxid pe kg de produs si se calculeaza cu formula:
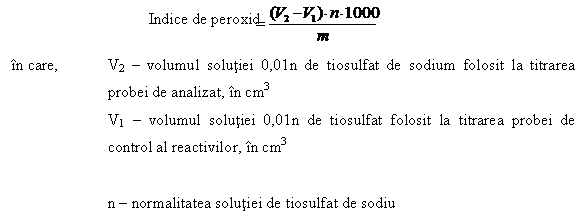 Pentru determinarea factorului de
corectie al Na2S2O3 0.1 n am folosit trei
pahare Erlenmayer in care am pus pentru fiecare dupa cum
urmeaza :
Pentru determinarea factorului de
corectie al Na2S2O3 0.1 n am folosit trei
pahare Erlenmayer in care am pus pentru fiecare dupa cum
urmeaza :
-5 mL solutie etalon K2Cr2O7 0.01n ;
-5 mL H2SO4 1 :1 ;
-o spatula de KI, le-am tinut la intuneric timp de 15 minute si apoi am titrat cu Na2S2O3 0.1 n pana la culoarea galben-pai, obtinand urmatoarele rezultate :
F = V1 / V2,
unde, V1 = volumul solutiei etalon 10 mL ;
V2 = volumul folosit la titrare.
F1 = 10 mL / 10.2 = 0.9803
F2 = 10 mL / 10.2 =0.9803
F3 = 10 mL / 10.3 = 0.9708
F = F1 + F2 + F3 / 3=0.9803 + 0.9803 + 0.9708=0.9771
Ip(C I ) = (6 - 4) x 0.1 x 1000 x 0.9771 / 1 g = 19.54 mL Na2S2O3 /g proba
Ip(C II ) = (5 - 4) x 0.1 x 1000 x 0.9771 / 1 g = 9.7 mL Na2S2O3 /g proba
IpC III ) = (4 - 3) x 0.1 x 1000 x 0.9771 / 1 g =9.771 mL Na2S2O3 /g proba
Tabelul nr.22.Indice de peroxid
|
Formula |
Indicele de peroxid mLNa2S2O3 /g proba |
|
C I | |
|
C II | |
|
C III |
Indice de peroxid s-a obtinut in cantitate mai mare la C I si mai mica la C III , ceea ce inseamna ca cea mai buna este C I, datorita efectului antibacterian si kerolitic al peroxizilor, aspect confirmat si de continutul de 0.1 % de retinaldehida de pe eticheta produsului .
Testele bacteriologice urmaresc decelarea microorganismelor patogene pe suprafata supusa prin insamantari pe medii de cultura speciale sau prin tehnici de colorare complexe. Schliesser T (1985) a folosit microorganisme de referinta, care sunt aprobate si acum pentru a fi utilizate in scopul caracterizarii capacitatii bactericide a unor substante cat si pentru controlul curent al eficientei decontaminarii de necesitate. Aceste test-organisme sunt : Staphilococcus aureus, Streptococcus faecium, Pseudomonas aeruginosa, Proteus mirabilis, Mycobacterium avium, Candida albicans, oochisti de Eimeria tenella oua neembrionate de Ascaris suum.[20]
Aparatura si materiale
-Termostat reglabil la 25±1°C;
-Termostat reglabil la 37±1°C;
-Baie de apa pentru topirea mediilor;
-Anse sterile;
-Cutii Petri cu diametrul de 10 cm steile;
-Eprubete de 16 X 160 mm sterile;
-Lupa 3X;
-Pipete cu diferite capacitatti, sterile;
-Spatule sterile;
-Tuburi de fermentatie sterile.
Diluanti
Solutie fiziologica sterilizata ;
Medii de cultura
Geloza Plate Count;
Geloza Sabouraud cu antibiotice;
Bulion lactozat;
Mediu Levine ;
Mediu hiperclorurat Chapman lichid;
Mediu hiperclorurat Chapman solid;
Testul numarului total de germeni mezofili aerobi (N.T.G.M.A) si a numarului total de micromiceti (N.T.M.) se executa dupa protocolul indicat de Directia de Sanatate Publica - din cadrul Ministerului Sanatatii .
Recoltarea probelor se face folosind tampoane sterilizate, tinute in eprubete, care inainte de folosire se umezesc prin introducerea in fiecare eprubeta a cate 1 cm3 solutie fiziologica sterilizata. Se recolteaza minimum 10 de probe de 1g fiecare : cate 5 probe din partea interioara, si cate 5 probe de pe peretii laterali. Recoltarea se face prin stergerea unei suprafete de 1cm2 din punctele alese, apoi tamponul se introduce in eprubeta, care se individualizeaza prin numere. Paralel pe un caiet se consemneaza locul recoltarii, corespunzator fiecarui numar.
Insamantarea probelor se executa prin stergerea tamponului pe suprafata gelozei Plate Count repartizata in placi Petri pentru determinarea NTGMA, apoi pe suprafata gelozei Sabouraud cu antibiotice (cloramfenicol) pentru micromiceti. Pe o placa Petri se pot insamanta 6 probe, dupa delimitarea a 6 zone triunghiulare, inscriind cu un creion dermatograf numarul probei pe sectorul insamantat. Incubatia se face timp de 24- 36 ore la 37oC pentru NTGMA si 4-5- zile la temperatura de 25- 30oC pentru micromiceti. Dupa incubatie se numara coloniile corespunzatoare fiecarei probe [20].
Rezultatele pentru proba analizata se apreciaza astfel:
Pentru NTGMA:
corespunzatoare: - absenta coloniilor
- 1- 50 colonii
necorespunzatoare: - peste 50 colonii
- colonii numeroase
Pentru NTM:
corespunzatoare: - absenta coloniilor
- 1- 10 colonii
necorespunzatoare: - peste 10 colonii
- colonii numeroase
Tabelul nr.23 Numarul total de germeni mezofili aerobi ,si numarul total de micromiceti
|
Formula |
Numarul total de germeni mezofili aerobi |
Numarul total de micromiceti (NTM) |
|
C I |
mai putin de 10 colonii viabile/ 1 g produs |
mai putin de 10 colonii viabile/ 1 g produs |
|
C II |
mai putin de 10 colonii viabile/ 1 g produs |
mai putin de 10 colonii viabile/ 1 g produs |
|
C III |
mai putin de 10 colonii viabile/ 1 g produs |
mai putin de 10 colonii viabile/ g produs |
Identificarea microorganismului Escherichia Coli
In vederea recoltarii probelor, se pregatesc tampoane de sanitatie (Ts).
Tamponul se face din vata sau tifon rasucit pe o tija de aluminiu, introdus in eprubeta de 180/ 18.Pe aceasta tija se confectioneaza un dop din vata hidrofuga.
Se iau in lucru 5 probe de 1g, si se introduc in eprubetele care contin 10 cm3 de bulion lactozat .
Eprubetele se prevad cu tuburi de fermentatie si se termostatreaza la 37°C timp de 48 h, dupa care se examineaza observandu-se producerea de gaz. Probele se insamanteaza prin inundare pe mediu Levine repartizat in placi Petri. Excesul de lichid se aspira cu pipeta Pasteur, iar placile se incubeaza 48 ore la 37oC.
Rezultatul este negativ daca pe daca pe mediul Levine nu se dezvolta colonii de Escherichia coli (violet inchis cu reflexe metalice aurii - verzui)[9].
Tab.24. Rezulatate analize continut de Escherichia Coli
|
Formula |
Microrganismul Escherichia coli |
|
C I |
Negativ |
|
C II |
Negativ |
|
C III |
Negativ |
Identificarea Staphylococului auriu
Se insamanteaza 1g proba cu ajutorul anse sterile pe hiperclorurat Chapman lichid. Proba insamantata se termostateaza 24 h la 37°C. A doua zi din mediul hiperclorurat Chapman lichid, proba se insamanteaza cu pe mediul hiperclorurat Chapman solid. Cutiile Petri se introduc in termostat la 37°C timp de 24-48 h apoi se examineaza cultura obtinuta.
Aparitia pe mediul hiperclorurat Chapman solid a unor colonii galbene care vireaza mediul, indica prezenta staphylococului auriu.[20]
Tab.25. Rezulatate analizelor continutului de
Staphylococului auriu
|
Formula |
Microrganismul Staphylococului auriu |
|
C I |
Negativ |
|
C II |
Negativ |
|
C III |
Negativ |
Spectrometria de masa cu plasma cuplata inductiv-ICP-MS
Metoda ICP -MS are un domeniu larg de aplicare, aria acestuia incluzand: mediul, geologia, semiconductorii, analize clinice, chimice si metalurgice. Cu ICP-MS se fac determinari rapide a urmelor de elemente din materialele analizate.[17]
Componentele interne ale aparatului ICP-MS tip Agilent 7500CE
Aparatul ICP-MS are in structura sa urmatoarele componente:
Sistemul de introducere a probelor ;
Nebulizor;
Camera de pulverizare ;
Sursa de plasma cuplata inductiv;
Interfata;
Lentilele ionice;
ORS - Sistem cu celula de reactie;
Analizorul ;
Detectorul;
Sistemul de vid;
Generatorul de RF;
Soft-ul de operare (ChemStation);
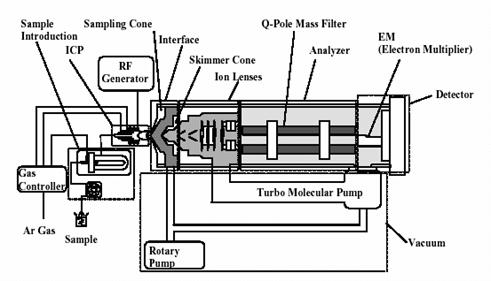
Fig. 9. Schema ICP-MS
Tabelul nr.26.Caracteristici tehnice ale aparatului ICP-MS
|
nume: agilent seria 7500ce - icp-ms |
||
|
ICP |
Nebulizor Camera de pulverizare Torta Interfata Sase controlere de debit Frecventa Putere RF Lentile ionice |
Concentric Cuart (control termoelectric) Din cuart, tip Fassel Din nichel sau platina Pentru: plasma, gaz auxiliar, gaz de adaos, gazul purtator si gazele pt.ORS 27.12 MHz max. 1600 W Extractie/Omega/ORS |
|
MS |
Filtru de masa Frecventa Domeniu de mase Detector |
Filtru de masa quadrupolar Aproximativ 3 MHz 2 - 260 amu Multiplicator electronic |
|
SISTEMUL DE VID |
Pompa |
Pompa rotativa Pompa turbomoleculara |
|
DIMENSIUNI |
1100x600x650, aproximaiv 175 kg. |
|
Principiul metodei
Solutia probei de analizat este pompata printr-un sistem de injectie unde este dispersata intr-un curent de gaz, formand un aerosol foarte fin ce ajunge in interiorul unei plasme de argon cu temperatura foarte mare. Aici se produce ionizarea atomilor, obtinindu-se un nor de sarcini pozitive. Ionii probei sunt extrasi din plasma si introdusi intr-un sistem vidat unde se gasesc analizorul quadrupolic si filtrul de masa. Analizorul poate scana domeniul de masa foarte rapid, si astfel analiza multi-elementalapoate fi executata.
Ionii sunt focalizati in interiorul analizorului unde sunt separati functie de raportul masa/sarcina. Concentratia corespunzatoare ionilor separati este masurataa intr-un detector multiplicator electronic. Numarul de impulsuri obtinute pentru fiecare ion este comparat si interpolat cu o curba de calibrare, obtinandu-se concentratia pentru fiecare element din proba.
Cu ajutorul aparatului ICP-MS se pot executa analize
Semicantitative (SQ)
Cand se executa o analiza semicantitativa se obtin informatii despre concentratiile tuturor elementelor care pot fi prezente in proba de analizat, fara a fi necesara o calibrare externa. Precizia unei analize semicantitative este de + 30%. Inainte de a executa o analiza SQ este recomandat sa se prepare si sa se analizeze un standard de calibrare pentru a seta factorii de raspuns ai elementelor, necesari in calculul concentratiilor.
Se utilizeaza o proba continand concentratii cunoscute din trei sau patru elemente ca standard de calibrare. Daca matricea probei necunoscute este cunoscuta, standardul de calibrare potrivit poate fi matricea, pentru imbunatatirea acuratetii analizei si apropierea de analiza cantitativa.
Cantitative(Q)
O analiza cantitativa permite determinarea concentratiilor elementelor de interes din proba de analizat, utilizand curbele de calibrare pentru acele elemente.
Pentru a putea executa o analiza cantitativa trebuie mai intai sa se obtina cate o curba de calibrare pentru fiecare element ce urmeaza a fi determinat in proba de analizat.
Programul ChemStation poate apoi calcula automat concentratiile elementelor din proba, pe baza acelor curbe de calibrare.[18]
Rezultate
Continutul de Ti
CI
Metoda utilizata:ICPCHEM1METHODSMET_M30B.M ;
Calibrare : ICPCHEM1CALIBMET_M30B.C ;
V=100 ml ; m=0.2603g ;
Dilutia :384.2=(100.0/2.603 E-01)*1.000
CII
Metoda utilizata:ICPCHEM1METHODSMET_M30B.M ;
Calibrare : ICPCHEM1CALIBMET_M30B.C ;
V=100 ml ; m=0.2580g ;
Dilutia :387.6=(100.0/2.580 E-01)*1.000
CIII
Metoda utilizata:ICPCHEM1METHODSMET_M30B.M ;
Calibrare : ICPCHEM1CALIBMET_M30B.C ;
V=100 ml ; m=0.2530g ;
Dilutia :395.3=(100.0/2.530 E-01)*1.000
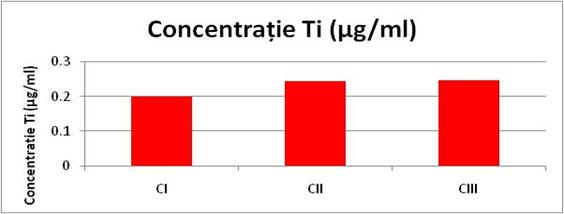
Tab.27. Continutul de Ti din cremele dermato-cosmetice
|
Formula |
Conc Ti(µg/ml) |
RDS(%) |
|
CI | ||
|
CII | ||
|
CIII |
*RDS=Deviatia standard relativa ;
Continutul de Ti din cele trei creme cosmetice este relativ apropiat.
Continutul de Cd , Pb,Hg;
CI
Metoda utilizata:ICPCHEM1DATAIMET_M31A.M ;
Calibrare : ICPCHEM1CALIBMET_M31A.C ;
V=100 ml ; m=0.2603g ;
Dilutia :384.2=(100.0/2.603 E-01)*1.000
CII
Metoda utilizata:ICPCHEM1DATAIMET_M31A.M ;
Calibrare : ICPCHEM1CALIBMET_M31A.C ;
V=100 ml ; m=0.2580g ;
Dilutia :387.6=(100.0/2.580 E-01)*1.000
CIII
Metoda utilizata:ICPCHEM1DATAIMET_M31A.M ;
Calibrare : ICPCHEM1CALIBMET_M31A.C ;
V=100 ml ; m=0.2530g ;
Dilutia :395.3=(100.0/2.530 E-01)*1.000
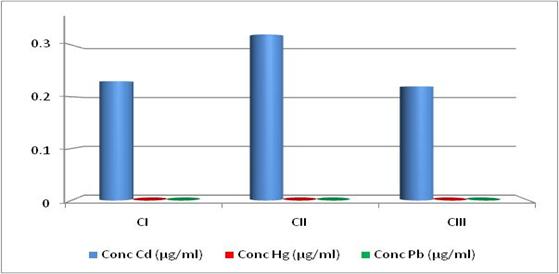
Tab.28.Continutul de Cd,Pb si Hg din cremele dermato-cosmetice
|
Formula |
Conc Cd(µg/ml) |
Conc Hg(µg/ml) |
Conc Pb(µg/ml) |
Conc Ti(µg/ml) |
|
CI | ||||
|
CII | ||||
|
CIII |
٭RDS=deviatia standard relativa
concluzii
In urma analizei ICP-MS a celor trei creme dermatocosmetice rezulta ca nu prezinta urme de Hg si PB , iar continutul de Cd a fost mai mare la CII iar CI si CIII au concentratii relativ egale . Continutul de Cd se situeaza in intervalele mentionate in studii de specialitate de 0.3-1.8µg/ml in creme cosmetice .[22]
In partea experimentala am analizat 3 tipuri de crema din gama Avenè, si anume : crema tratament pentru ten acneeic (C I), crema tratament atiiritanta hidratanta (C II), lotiune matifianta purifianta (C III), urmarind calitatea acestora. Toate cremele sunt din categoria cremelor dermato-cosmetice.Cremele au fost achizitionate din magazinele de profil .
In urma analizelor organoleptice ale celor trei creme s-a observat ca au un aspect omogen si miros specific .Crema tratament pentru ten acneeic (CI) a avut o culoare galbena , iar CII si CIII au avut culoare alba.
Cremele studiate difera din punct de vedere al solubiltatii si anume : C I este solubila in alcool metilic , HCl si insolubila in benzen si CCl4 .C II este doar partial solubila in apa calda si insolubila in CCl4, benzen si in HCl. C III e partial solubila in HCl si insolubila in CCl4, benzen, eter de petrol si in alcool metilic .
Aceste creme prezinta toate tipul de emulsie U/A, iar pH-ul variaza :C I si CIII au valori apropiate 4.54 respectiv 4.67, iar CII are valoarea cea mai apropiata de pH-ul pielii ,fiind de 5.84.
In urma verificarii stabilitatii celor trei creme s-a observat ca sunt stabile de la 4°C pana la temperaturi cuprinse in intervalul 40-60 °C.Temperaturile de topire pentru cele trei creme au fost : pentru CI 620C, pentru CII 670C respectiv pentru CIII 610C.
Deoarece continutul de apa trebuie sa fie cat mai mare, crema care corespunde cel mai bine este C I, in timp ce procentul cel mai mic s-a inregistrat la CIII.
La determinarea continutului de substante grase totale, procentul cel mai mare s-a obtinut la C II, iar cel mai mic la C I, lucru plauzibil avand in vedere ca este tratament antiacneic
Conform indicelui de aciditate, adica a volumului de KOH necesar neutralizarii continutului de acizi grasi liberi din proba, s-a obtinut cel mai mic indice de aciditate la C II si mai mare la C I aspect confirmat si de concentratia de acid glicolic de 6% mentionata pe prospectul produsului
Indicele de saponificare , adica volumul de KOH necesar neutralizarii acizilor grasi rezultati la saponificarea probei de analizat, este cea mai mica la C I, iar cea mai mare la C II.Rezultatele sunt in concordanta cu valorile indicelui de aciditate.
Indicele de iod obtinut la cele trei creme, adica continutul in hidrocarburi nesaturate, este mai mic la C I, si mai ridicat la CII si CIII ceea ce indica o stabilitate mai mare la oxidare si polimerizare pentru C I. Continutul de Ti din cele trei creme cosmetice este relativ apropiat .
In urma analizei ICP-MS a celor trei creme dermatocosmetice rezulta ca nu prezinta urme de Hg si PB , iar continutul de Cd a fost mai mare la CII , iar CI si CIII au concentratii relativ egale .
Toate cremele contin parabeni , aspect mentionat si pe etichetele acestora.cantitatea sau concentratia acestora nu este mentionata , dar conform Directivei Europene 76/768 limita admisa este de 0.4-0.8% .
Indicele de peroxid s-a obtinut in cantitate mare la C I, urmata de C II si C III.
In urma analizelor efectuate pentru determinarea incarcaturii microbiene s-a observat ca cele trei creme sunt lipsite de germeni patogeni aerobi si micromiceti , Staphylococ auriu sau Escherichia Coli.
Prin folosirea regulata a acestor creme se va vedea in timp o imbunatatire considerabila a tenului cu probleme devenind mai neted, mai luminos si plin de vitalitate.
M. Niederer , R. Bollhalder, Ch. Hohl-Determination of fragrance allergens in cosmetics by size-exclusion chromatography followed by gas chromatography-mass spectrometry, Journal of Chromatography A, pag 109-116,1 september 2006;
H. Masmoudi , Y. Le Dr´eau, P. Piccerelle, J. Kistera- The evaluation of cosmetic and pharmaceutical emulsions aging process using classical techniques and a new method: FTIR, International Journal of Pharmaceutics,pag 117-131,18 december 2004;
M. Padilla , M. Palma , C.G. Barroso- Determination of phenolics in cosmetic creams and similar emulsions, Journal of Chromatography A,pag 83-88,2005;
Adriana M. Maia, Andr´e Rolim Baby, Wilson J. Yasaka , Eunice Suenaga ,
Telma M. Kaneko , Maria Val´eria R. Velasco- Validation of HPLC stability-indicating method for Vitamin C in semisolid pharmaceutical/cosmetic preparations with glutathione and sodium metabisulfite, as antioxidants,Talanta,vol 71, pag 639-643,
C. Villa , R. Gambaro, E. Mariani, S. Dorato- High-performance liquid chromatographic method for the simultaneous determination of 24 fragranceallergens to study scented products, Journal of Pharmaceutical and Biomedical Analysis 44 ,pag 755-762,2007;
Maw-Rong Lee , Chueh-Yu Lin, Zu-Guang Li , Tzu-Feng Tsai- Simultaneous analysis of antioxidants and preservatives in cosmetics by supercritical fluid extraction combined with liquid chromatography-mass spectrometry Journal of Chromatography A, vol 1120,pag 244-251,2006;
Thais Guaratini, Mirela D. Gianeti, Patr´ıcia M.B.G.M. Campos- Stability of cosmetic formulations containing esters of Vitamins E and A:Chemical and physical aspects- International Journal of Pharmaceutics,vol 327,pag 12-16,2006;
Alberto Chisvert, Judit Sisternes, Ángel Balaguer, Amparo Salvador- A gas chromatography-mass spectrometric method to determine skin-whitening agents in cosmetic products-Talanta ,vol 81, pag 530-536,2010;
K. Verma, N. Agrawal, R.B. Misra, M. Farooq, R.K. Hans Phototoxicity assessment of drugs and cosmetic products using E. coli Toxicology in Vitro pag 249-253,2008;
M Thyagarejan-Parabens:Vital ingredients for Cosmetic Formulation,IDMA Bulletin Chemical Weekly,pag 189-190,2008;
Marleen Pauwels, Vera Rogiers-Safety evaluation of cosmetics in the EU Reality and challenges for the toxicologist, Toxicology Letters,pag 7-17,2004;
Gerhard J. Nohynek , Eric Antignac , Thomas Re, Herve Toutain Safety assessment of personal care products/cosmetics and their ingredients, Toxicology and Applied Pharmacology,pag 239-259,2010;
Mônica Manela-Azulay, Ediléia Bagatin-Cosmeceuticals vitamins, Clinics in Dermatology,pag 469-474,2009;
Wei Jin, Yong-Jian Yang, Wei-Yu Wang, Jian-Nong Ye-Simultaneous Determination of Antibiotics in Anti-Acne Cosmetics by Rapid LCwith DAD, Shanghai Institute for Food and Drug Control,2009;
Jens J. Thiele , Swarna Ekanayake-Mudiyanselage-Vitamin E in human skin: Organ-specific physiology and considerations for its use in dermatology, Molecular Aspects of Medicine ,pag 646-667,2007
Cristina Borulescu,Maria Giurginica,Ioana Demetrescu-Evaluarea unor antioxidanti naturali si de sinteza utilizati in produsele dermato-cosmetice cu efect antiimbatranire-Revista de Chimie ,nr 1,2007;
Horea Iustin Nascu, Lorentz Jantaschi-Chimie analitica si instrumentala , Ed.Academic Pres & AcademicDirect, 2006;
Determinarea cantitatii de metale prin metoda ICP-MS-metoda interna
[19] Tratamente cosmetice aplicate tipului de ten;www.scritube.com ;
Determinarea numarului total de germeni mezofili aerobi (N.T.G.M.A) si a numarului total de micromiceti (N.T.M.)-metoda interna;
[21] Tratamente dermato-cosmetice -prezent si viitor ;www.dermadoctor.ro
Nnorom I.C., IGWE, J.C. and Oji-Nnrom C Trace metal contents of facial cosmetics commonly used in Nigeria, Journal of Biotechnology ,Vol 4 , pag 1133-1138, October, 2005;
|
Politica de confidentialitate |
| Copyright ©
2026 - Toate drepturile rezervate. Toate documentele au caracter informativ cu scop educational. |
Personaje din literatura |
| Baltagul caracterizarea personajelor |
| Caracterizare Alexandru Lapusneanul |
| Caracterizarea lui Gavilescu |
| Caracterizarea personajelor negative din basmul |
Tehnica si mecanica |
| Cuplaje - definitii. notatii. exemple. repere istorice. |
| Actionare macara |
| Reprezentarea si cotarea filetelor |
Geografie |
| Turismul pe terra |
| Vulcanii Și mediul |
| Padurile pe terra si industrializarea lemnului |
| Termeni si conditii |
| Contact |
| Creeaza si tu |