Boala Crohn
INTRODUCERE
Boala Crohn este o afectiune inflamatorie intestinala (face parte din familia bolilor inflamatorii intestinale - BII), care determina inflamatia si ulceratia tractului digestiv. Poate afecta orice portiune a tubului digestiv, insa are predilectie pentru partea terminala a intestinului subtire (ileon) si intestinul gros (colon). Boala Crohn afecteaza straturile profunde ale tubului digestiv, cauzand ulceratii la acest nivel.
Boala Crohn este deseori intalnita la mai multi membrii ai aceleasi familii (transmitere genetica). Nu se cunoaste exact de ce unele persoane devolta boala, insa exista studii medicale de specialitate care au dovedit existenta anumitor factori declansatori (triggeri), ce pot declansa boala prin diferite mecanisme imune. S-a dovedit faptul ca boala poate fi declansata de aparitia unui raspuns imun anormal impotriva bacteriilor intestinale saprofite (care se gasesc in mod normal la nivelul intestinului gros) sau prin mecanisme imune complexe secundare unor infectii cu diferite bacterii sau virusi (Mycobacterii tuberculoase, Yersinia enterolitica, E.coli, B. fragilis). Se stie, de asemenea, ca factorii de mediu au un rol important in aparita bolii. Fumatorii au un risc crescut de a dezvolta boala.
Datorita faptului ca boala Crohn are o componenta imuna, exista o afectare si a altor organe, precum ochii (tulburari vizuale), articulatiile (dureri articulare), rash cutanat (eruptii cutanate) sau ficatul (inflamatia tesutului si cailor biliare). Exista mai multe afectiuni cu simptome asemanatoare bolii Crohn, cele mai des intalnite in clinica
medicala fiind diverticulita si abcesele intestinale.
Diagnosticul bolii Crohn se pune pe baza endoscopiei dar si prin intermediul altor investigatii imagistice( radiografia,CT, RMN ) precum si pe baza unor investigatii de laborator(proteina C reactiva, lactoferina fecala, calprotectina fecala, anticorpi). In uma examenului histopatologic s-a observat prezenta mai multor citokine rezponsabile de inflamatia intestinala sau de manifestarile clinice ale bolii. Astfel IL-12, IL-21 IL-6, TGFB,IL-23, NFkB, IL-10, TNF- au fost descoperite in mucoasa pacientilor cu boli inflamatorii intestinale cronice. Acest lucru pune in evidenta importanta tratamentului cu imunomodulatoare precum si necesitatea unor studii suplimentare.
Tratamentul bolii Crohn are scopul de a preveni acutizarile si de a mentine cat mai mult perioadele de remisiune. O parte dintre pacienti au simptome mult mai grave si necesita terapii comlementare, precum chirurgia. Terapia corecta a bolii Crohn se realizeaza in functie de tipul si gravitatea bolii.
In tratamentul bolii Crohn se folosesc mai multe clase de medicamente: compusi de 5-ASA (acid 5 amino acetil salicilic), cum ar fi sulfasalazina (Azulfidine) si mesalamina (Pentasa, Asacol, Dipentum, Colazal, Rowasa clisma), antibiotice (Metronidazol si ciprofloxacina) precum si imunomodulatoare (6- mercaptopurina, azatioprina, infliximab, adalimumab, metotrexat).
2.1. DEFINITIE
Boala inflamatorie intestinala este un termen utilizat pentru desemnarea unui grup de boli inflamatorii cronice, de cauza necunoscuta, ale tractului gastrointestinal. Manifestarile lor sunt suficient de caracteristice pentru a permite un diagnostic de acuratete in majoritatea cazurilor.
Descrierea originala a bolii, realizata in 1932 de Crohn, Ginzberg si Oppenheimer, a localizat aceasta afectiune la segmentele ileonului. Totusi, acelasi proces poate afecta mucoasa bucala, esofagul, stomacul si duodenul, ca si jejunul sau ileonul. Boala Crohn a intestinului subtire mai este cunoscuta si sub denumirea de enterita regionala.
Un aspect inflamator similar poate aparea si la nivelul colonului, fie izolat, fie in asociere cu afectarea intestinului subtire. In majoritatea cazurilor, aceasta forma de colita poate fi diferentiata clinic si anatomopatologic de colita ulceroasa, purtand si denumirea de boala Crohn a colonului. Colita granulomatoasa este un termen inadecvat, deoarece numai o parte din cazuri prezinta granuloame. Din punct de vedere clinic, aceste boli sunt caracterizate de afectarea inflamatorie recurenta a segmentelor intestinale, cu manifestari clinice variate, determinand frecvent o evolutie cronica, impredictibila.
Boala Chron este greu de diagnosticat datorita simptomelor foarte variate si asemanatore cu ale colitei ulceroase sau sindromului de intestin iritabil. In cazul bolii Crohn este afectata doar partea superficiala a mucoasei intestinale spre deosebire de colita ulcerata in care sunt afectate toate staturile peretelui intestinal.
In prezent nu exista tratament curativ in cazul bolilor intestinale inflamatorii cronice, pacientii fiind nevoiti sa urmeze tratamente toata viata.
2.2. EPIDEMIOLOGIE
Se estimeaza ca 1.4 milioane de americani sufera de boala Chron sau de colita ulcerativa. Incidenta anuala in America si Europa este de 1-6/105 locuitori si prevalenta de 10-100/105. Incidenta a crescut continuu in ultimele trei decade.
Incidenta si prevalenta bolilor inflamatorii intestinale recunosc o ampla variabilitate geografica. S-au descris arii geografice cu frecventa mare (nord-vestul Europei, America de Nord) si arii geografice cu frecventa mica (S-E Europei, Orientul Mijlociu, America Latina, Afica ), gradientul intre aceste arii ajungand pana la de 10 ori .
Ambele sexe sunt egal afectate, desi in ariile cu frecventa mare (populatii de origine nord-vest europeana) se remarca o incidenta cu 30% mai mare la sexul feminin.
Bolile inflamatorii intestinale cronice pot afecta orice grup de varsta dar adolescentii si tinerii adulti intre varstele de 15 si 35 de ani sunt cei mai afectati. Copiii sunt foarte rar afectati. Incidenta acestor boli la populatia sub 18 ani este de 10% sau 100.000 de cazuri estimate.
Conform internarilor din Anglia din anul 2002 varsta medie de internare a pacientilor care sufera de boala Chron este de 39 de ani.
Din motive necunoscute bolile infamatorii intestinale cronice afecteaza tarile dezvoltate (in principal U.S.A si Europa). Sunt mai frecvente in mediul urban decat in cel rural, mai mult in climatele nordice decat in cele sudice. Incidenta acestor boli creste odata cu migrarea populatiei din tarile nedezvolate in tarile dezvoltate si scade in caz contrar. Tind sa afecteze persoanele cu statut socioeconomic inalt, educate, persoanele sedentare, care lucreaza in spatii inchise.
In raport cu factorii rasiali si etnici frecventa este de 2-5 ori mai mare la albi decat la populatia afro-americana si de 3-8 ori la evrei, evreii Ashkenazi (est europeni si americani ) fiind mai frecvent afectati decat cei Sepharzi (cu origine orientala).
Evreii de origine europeana au riscul de 5 ori mai crescut decat populatia generala de a dezvolta boala Chron.
Desi o serie de date sugereaza interventia factorilor dietetic (alimentatia la san limitata, consumul de dulciuri rafinate, dieta saraca in fructe si legume crude, prelucrarea termica excesiva) si a contraceptivelor orale ca factori generatori ai inflamatiei intestinale, asocierea statistica este inconsistenta.
13 studii efectuate intre anii 1987 si 1999 au demostrat ca apendicectomia poate sa scada riscul aparitiei bolii Chron cu pana la 69%.
Dintre factorii de mediu, numai fumatul se asociaza semnificativ cu riscul dezvoltarii bolii Chron (de 2-4 ori mai mare la fumatori). Fumatul este asociat cu aparitia bolii dupa varsta de 40 de ani dar si cu dezvoltarea stricturilor sau a perforatiilor.
Agregarea familiala- istoricul familial pozitiv constituie factorul de risc cel mai bine documentat pentru bolile inflamatorii intestinale, indeosebi pentru boala Crohn; aproximativ 6-37% dintre pacientii cu boli inflamatorii intestinale prezinta un istoric familial pozitiv.
Incidenta bolilor inflamatorii intestinale la rudele de gradul I ale pacientilor cu boala Crohn si colita ulcerativa este de 30-100 de ori mai mare decat la populatia generala. Sunt afectate preponderant rudele de gradul I ale subiectilor afectati. Riscul de a dezvolta aceeasi afectiune este semnificativ mai mare, desi agregarea familiala mixta este intalnita in aproximativ 25% din cazuri. Aceste date sustin ipoteza conform careia colita ulcerativa si boala Chron sunt afectiuni inrudite. Rata de concordanta la gemenii monozigoti este mai mare decat la gemenii dizigoti.
Exista si o asociere cu alte sindroame genetice rare cum ar fi sindroame de imunodeficienta, sindromul Turner, glicogenoze tip Ib.
2.3. ETIOPATOGENEZA
Etiologia bolii Crohn si a colitei ulcerative nu este pe deplin cunoscuta. Se iau in discutie atat factorii genetici cat si componentele antigenice din mediu.
Cea mai raspandita teorie privind etipatogeneza bolilor infamatorii intestinale cornice este cea a a atacului imun mediat celular de limfocitele T asupra bacteriilor intestinale comensuale la pacientii cu teren genetic susceptibil, atac care este declansat sau reactivat de o multitudine de factori de mediu. Aceasta teorie complexa presupune existenta a 4 componente care trebuie sa se intersecteze in mai multe planuri ca boala sa fie aparenta clinic.
Susceptibilitatea genetica este influentata de microorganismele din lumenul intestinal care vor fi recunoscute de sistemul imun ca adjuvanti sau antigene si vor declansa un raspuns imun protector sau patogenic. Triggerii din mediu sunt necesari pentru declansarea sau reactivarea bolii.
FACTORII GENETICI
In ultimii ani s-au facut numeroase studii privind factorii genetici ai bolilor inflamatorii intestinale cornice, studii care au au implicat pe de-o parte fragmente polimorfice alcatuite dintr-o singura nucleotida si diferite gene si pe de alta parte studii cu soareci transgenici care sufereau de colita. Rezultatele ambelor teste s-au suprapus in sensul existentei mai multor gene implicate atat in bolile inflamatorii intestinale cat si in colita indusa prin mutatii transgenice ale soarecilor. Aceste gene comune sunt implicate in mai multe procese biochimice printre care imunoreglarea, integritatea mucoaselor si clearance-ul si homeostaza microflorei intestinale.
A. GENA CARD15
Prima gena care s-a demonstrat ca ar face parte din etiopatogenia bolii Crohn a fost gena CARD15(domeniul de recrutare al caspazei, domeniul 15) care a fost denumita initial gena NOD2. Este vorba de trei mutatii, substitutia argininei din pozitia 702 cu triptofanul si a glicinei din pozitia 908 cu arginina, si frameshiftul 1007fs din regiunea genei CARD15, regiune care codifica o portiune bogata in leucina necesara pentru identificarea bacteriana. Cel putin una dintre aceste mutatii este prezenta la pacientii cu boala Crohn din U.S.A dar nu si la pacientii din Africa sau Asia. Mutatii ale genei CARD15 s-au gasit la pacientii cu boala Crohn in regiunea ileala care prezinta stricturi. Regiunea bogata in leucina a genei CARD15 leaga dipeptidul muramil(MDP) care reprezinta componenta activa a peptidoglicanului, un polimer ubiquitar al peretelui celular bacterian. Legarea MPD de dimerii codificati de CARD15 activeaza factorul nuclear (NF)kb care face parte dintr-un proces care stimuleaza transcriptia mai multor gene care codifica atat molecule proinflamatoare cat si protectoare. Mutatiile argininei din pozitia 702 a glicinei din pozitia 908 precum si deletia din pozitia 1007fs determina legarea defectuoasa la MDP insa studiile nu sunt concludente privind urmarile acestui fapt.
Gena CARD15 mutanta nu mai poate indeparta Salmonella din celulele epiteliale deoarece factorul de activare nuclear (NF)Kb nu mai poate induce formarea proteinei reglatoare a mortii celulare GRIM-19.
Este posibil ca gena CARD15 defectiva sa fie asociata si cu cresterea populatiei bacteriene in special la nivelul criptelor. CARD15 este exprimata in celulele Panneth fiind sursa unor peptide antimicrobiene numite alpha-defensine. Deletia intentionala a genei CARD15 la soareci scade productia de alpha defensine si creste susceptibilitatea la infectia cu Listeria monocytogenes dupa administrarea orala dar nu si cea sistemica. Aceste rezultate sunt asemanatoare cu scaderea de alpha defensine din cazul bolii Crohn cauzate de mutatii ale CARD15. Totodata celulele Panneth se gasesc la nivelul ileonului ceea ce ar explica faptul ca mutatii ale genei CARD15 sunt corelate mai ales cu existenta bolii la acest nivel.
Strober si colegii sai au incercat sa propuna o supraactivare a factorului nuclear Kb mai degraba decat o pierdere a functiei genice printr-o mutatie. Investigatiile lor au demonstrat ca in celulele cu gena CARD15 defectiva receptorul Toll-like 2 (TLR2) nu putea inhiba activarea factorului nuclear Kb (vezi figura 1).
Aceste anomalii pot rezulta in incapacitatea modularii raspunsului imun innascut stimulat de adjuvantii bacterieni, clearance-ul deficitar al infectiilor bacteriene intacelulare dar si proliferarea si adezivitatea bacteriilor comensuale din lumenul intestinal. Toate aceste situatii au fost demonstrate in cazul pacientilor cu boala Crohn.
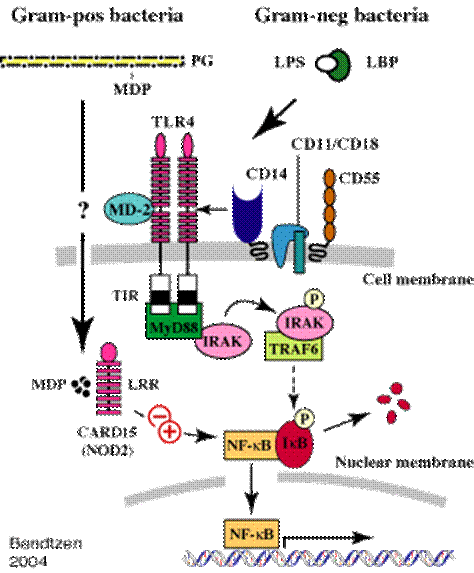
Figura 1 Interrelatia intre gena CARD15, receptorul Toll-like 2 (TLR2) si factorul nuclear Kb
B. GENA SLC22A4 si SLC22A5
Doua variante functionale ale transportorilor de cationi organici (OTC1, OTC2) au fost demonstrate in asociere cu mutatii ale genei CARD15 in cazul pacientilor cu boala Crohn. Este vorba de mutatii la nivelul regiunii transcriptionale ale genei SLC22A4 care codifica OTC1 si mutatii la nivelul regiunii promoter ale genei SLC22A5 care codifica OTC2, ambele proteine fiind implicate in transportul carnitinei si alor ioni organici in celula. Aceste variante functionale sunt exprimate mai ales in celulele intestinale epiteliale, macrofage, limfocitele T si determina o rata scazuta de transport al carnitinei. Multe studii au asociat cromozomul 5 care contine genele SLC22A4 si SLC22A5 cu aparitia bolii Crohn insa exista si cercetatori care au ezitat sa puna aparitia bolii pe seama acestor mutatii datorita unui dezechilibru de linkage care implica mai multe gene din aceasta regiune cromozomiala.
C. GENA DLG5
Doua haplotipuri ale genei DLG5, gena care codifica o proteina necesara pentru mentinerea integritatii epiteliului intestinal au fost asociate atat cu boala Crohn cat si cu colita ulcerata. Ca si genele OTC1 si OTC2 aceasta mutatie coexista cu mutatii ale genei CARD15 la pacientii cu boala Chron.
D GENA MDR1
Gena MDR1 este o gena de rezistenta multi drog care codifica glicoproteina P130 , aceasta fiind un transportor implicat in efluxul mai multor droguri sau produse xenobiotice din celula. Aceasta glicoproteina ar fi implicata si in clivarea de grupari amfipatice de la nivelul membranei celulare. Variante ale genei MDR1 au fost associate atat cu boala Crohn cat si cu colita ulcerativa.
Gena MDR1 are o importanta aparte datorita faptului ca este asociata cu formele de boala inflamatorie intestinala refractara la tratament dar si datorita faptului ca la soarecii la care aceasta gena a fost stearsa au dezvoltat colita.
E. GENA PPARG
Variante ale genei PPARG au fost associate cu susceptibilitatea sorecilor de a dezvolta ileita cronica dar si cu aparitia bolii Crohn la oameni. PPARG este un receptor nuclear care inhiba NFkB : expresia sa este scazuta la pacientii cu colita ulcerata si este up-regulata de acidul 5-aminosalicilic. Pe langa faptul ca are rol antiinflamator intestinal, ligandul de PPARG, rosiglitazone a avut efecte benefice cand a fost administrat atat pacientilor cu colita ulcerata cat si soarecilor cu colita indusa experimental.
Pana in momentul de fata trei gene au fost asociate cu boala Crohn si una cu colita ulcerata. Aceste gene au fost confirmate prin multiple studii. Exista si alte asocieri de gene care intervin atat in patogeneza bolilor inflamatorii intestinale (NFkB, TLR5) dar si in aparitia manifestarilor extraintestinale ale bolii ( HLA-B27, HLA-DR0103 ) si cu raspunsul la tratamentul farmacologic. Aceste gene sunt implicate in modularea raspunsului imun innascut , functia barierei mucosale si cu omorarea bacteriana.
RASPUNSUL IMUN
Atat pacientii cu boala Crohn cat si cei cu colita ulcerata au atat raspunsul imun innascut (macrofage, neutrofile) cat si raspunsul imun dobandit (limfocitele T si limfocitele B ) activate dar si pierderea tolerantei fata de bacteriile comensuale intestinale. Toleranta la persoanele normale este mediata de limfocitele T , limfocitele B, celulele natural killer, interferonul alpha, beta si prostaglandina J2 (vezi figura 2). Studiile de neutralizare cu anticorpi au demonstrat ca in patogeneza bolii Crohn sunt implicate mai ales IL-12 P40 si factorul de necroza tumorala (TNF).
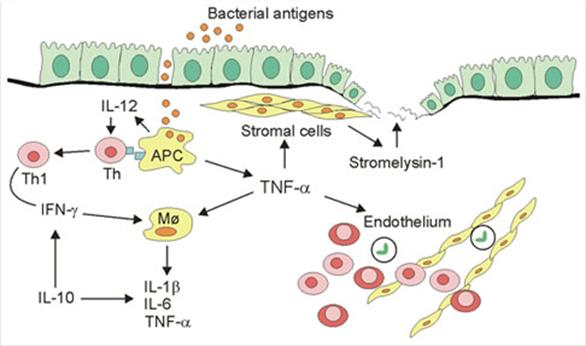
Figura 2. Raspunsul imun mucosal in bolile inflamatorii intestinale nespecifice
A. RASPUNSUL IMUN INNASCUT
Macrofagele si celulele dendritice sunt crescute si activate in lamina propria in ambele boli inflamatorii intestinale cronice. Productia de citokine proinflamatorii si chemokine precum si expresia moleculelor de adeziune si a moleculelor co-stimulatoare sunt crescute in boala Chron. In particular sunt crescute limfocitele T helper 1 si limfocitele T helper 17 precum si citokinele implicate in imunitatea innascuta (IL12, IL23, IL 27).
Moleculele de adeziune precum moleculele de adeziune intercelulara 1 (ICAM1) sunt necesare pentru ca celulele din circulatie sa se lipeasca pe endoteliul acesta fiind primul pas in extravazarea monocitelor si macrofagelor din circulatie in focarul inflamator. In plus aceste molecule de adezivitate mediaza migrarea celulelor imune prin stroma conjunctivala pana la locul de maxima concentratie al citokinelor dar si in sens invers catre lumenul intestinal pentru a produce abcese criptice.
Moleculele proinflamatorii sunt produse indeosebi de monocitele si macrofagele ancorate din circulatie si care au migrat la focarul inflamator decat de macrofagele rezidente. Macrofagele rezidente au o capacitate limitata de a raspunde la adjuvantii bacterieni datorita scaderii receptorilor de recunoastere bacteriana cum ar fi TLR si CD14, co-liganzii pentru lipopolizaharide. Similar, celulele epiteliale intestinale au nivel scazut de TLR, ceea ce le permite supravietuirea la concentratii bacteriene crescute din ileon si colon. Moleculele TLR sunt exprimate pe suprafata mai multor celule efectoare ale sistemului imun innascut. Ca si gena CARD15 aceste molecule se leaga de adjuvantii bacterieni si initiaza semnale de activare NFkB. Desi fiecare tip de TLR se leaga de un anumit tip de adjuvant bacterian (TLR4 si CD14 se leaga de lipopolizaharide si TLR2 se leaga de peptidoglican ) toate converg in formarea proteinei de diferentiere mieloida primara MYD88 care va activa NFkB(vezi figura 3).
Activarea NFkB stimuleaza expresia a numeroase molecule relevante in patogeneza bolilor inflamatorii intestinale cronice. Dintre acestea fac parte moleculele implicate in raspunsul inflamator cum ar fi IL-1, IL-6, IL-8 si alte chemokine, ICAM1 si alte molecule de adezivitate , molecule co-stimulatorii ca CD40, CD80 si co-stimulatorul ICOS al limfocitelor T. Expresia tuturor acestor molecule proinflamatorii este crescuta. Prin contrast in boala Chron este crescuta expresia activatorilor limfocitelor T helper 1 si T helper 12 in timp ce in colita ulcerativa nu. Tratamentul cu anticorpi monoclonali impotriva TNF este eficient atat in boala Chron cat si in colita ulcerativa in timp ce anticorpii impotriva IL-12 p40 sunt folositi numai in tratamentul bolii Crohn. Pe langa faptul ca activeaza genele pentru moleculele proinflamatorii. Factorul nuclear NFkB activeaza si expresia anumitor molecule protectoare cum ar fi proteina 3 indusa de TNF (A20), CARD15, ciclooxigenaza 2, beta defensinele, PPAR si propriul inhibitor, IkBa care inhiba raspunsurile inflamatorii.
NFkB este activat la pacientii cu boli intestinale inflamatorii cronice si inhibitia sa poate atenua colita indusa experimental la soareci totodata exista studii privind rolul sau protector. Deletia selectiva a anumitor gene a demonstrat atat rolul benefic dar si daunator asupra citokinelor inflamatorii avand functii diferite in diferite tipuri de celule. De exemplu, NFkB este implicat in homeostazia epiteliala dar este implicata si in patogeneaza inflamatiei intestinale mediate de monocite si macrofage la pacientii supusi unui transplant de maduva hematogena(vezi figura 4). Similar, la soareci deletia Myd88 exacerbeaza colita indusa de sulfatul sodic de dextran, prin blocarea activarii NFkB de bacteriile comensale enterice.
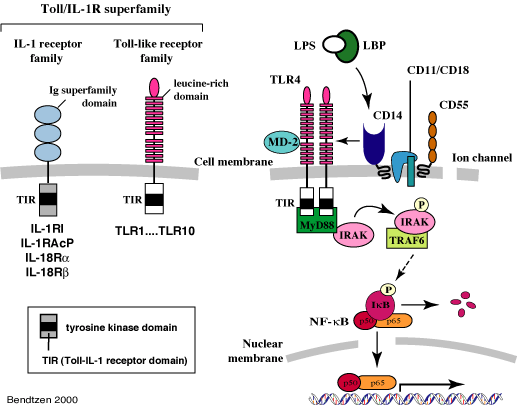
Fig 3. Super familia receptorilor Toll/IL1 Fig4. Activarea NF-kb
B. RASPUNSUL T CELULAR
Spre deosebire de raspunsul imun innascut care este activat in mod asemanator in colita ulcerativa si boala Crohn, limfocitele T prolifereaza si se activeaza in mod diferit in cele doua boli.
In boala Crohn profilul citokinelor activatoare de limfocite T helper 1 care include in IFN-γ si IL-12 p40 este dominant. Raspunsul limfocitelor T helper 1 este mediat de IFN- a carei productie este stimulata de IL12, produsa de celulele prezentatoare de antigene (APC). Majoritatea colitelor induse experimental au un raspuns de limfocite T helper 1 dominant dar acest raspuns se poate modifica pe masura ce procesul inflamator se matureaza, limfocitele T helper 1 se pot transforma in limfocite T helper 2. Modul de gandire privind limfocitele T helper 1 s-a schimbat odata cu descoperirea limfocitelor T helper 17. IL 17 este cea care mediaza activarea Limfocitelor T helper 17. Producerea acestor citokine este stimulata de productia de IL-6, TGFB si IL-23 de catre celulele raspunsului imun innascut si de celulele prezentatoare de antigene in special celulele dendritice. Nivelele de IL-23 si ale IL-17 sunt crescute in boala Crohn precum si in colita indusa experimental la soareci(vezi figura 5). Caile metabolice ale IL-12, IFN gamma si ale IL-23 si IL-17 se exclud reciproc deoarece IFN gamma inhiba IL-17 si vice versa.
Caile metabolice ale proteinelor asociate IL-12 si IL-17 sunt deasemenea crescute in boala Crohn. Dealtfel productia de IL-21 este crescuta selectiv de prezenta IL-12. Ca si IL-12, IL-21 stimuleaza T-bet, un factor intracelular activator al transcriptiei care este esential pentru diferentierea celulara si proliferarea limfocitelor T.
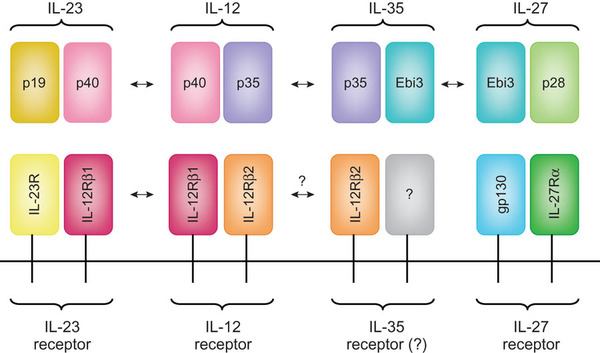
Fig 5. Expresia interleukinelor in Boala Crohn.
C. MIGRAREA CELULARA
Celulele circulatoare efectoare si regulatoare intra in intestine printr-un mecanism inalt selectiv care implica interactiunea cu endoteliul vascular, diapedeza prin peretele vascular si migrarea in lamina propria. Limfocitele T care au integrina-a b7 se leaga de endoteliul venulelor postcapilare din colon si intestinul subtire care exprima selectiv molecula de adeziune vasculara MAdCAM. Expresia acestei molecule este crescuta in intestinul inflamat ceea ce duce la cresterea numarului de limfocite T specifice intestinului. Celulele endoteliale din intestinul subtire exprima selectiv si CCL25( numita si chemokina exprimata de timus TECK), o molecula de adeziune a limfocitelor T care prezinta receptorul CCR9. Ileonul inflamat contine limfocite T CD4 care exprima receptorul de chemokine CCR2 care se leaga de CCL2 (cunoscut si ca factorul chemotactic pentru macrofage 1).
Expresia selectiva a moleculelor de adeziune vasculara reprezinta un mecanism selectiv de recrutare a limfocitelor T in intestinal subtire mai mult decat in colon. Citokinele inflamatorii ca TNF, IL-1b si IL-6 cresc expresia locala de molecule de adeziune vasculara 1 (VCAM1), antigenul 4(VLA4) si ICAM1 care vor determina neutrofilele si monocitele circulante sa adere la endoteliul inflamat. Chemokinele secretate de celulele sistemului imunitar innascut din lamina propria vor recruta noi celule circulante la focarul inflamator pentru a sustine si potenta raspunsului inflamator. Aceste celule ale sistemului imunitar innascut sunt sensibile in particular la activarea data de adjuvantii bacterieni cum ar fi lipopolizaharidele, peptidoglicaul si flagelina.
Intelegerea indeaproape a traficului celular in intestine a adus la noi tinte moleculare pentru blocarea inflamatiei din bolile infalamatorii intestinale cronice. Anticorpii monoclonali impotriva integrinei-a4 (natalizumab) care leaga atat integrina-a b7( ligandul MAdCAM1) si integrina-a b1 (ligandul VLA4 ) este eficient in tratamentul bolii Crohn.
D. STIMULANTII MICROBIENI COMENSUALI
Microflora enterica poate stimula aparitia unui raspuns imun atat prin functia de adjuvanti dar si ca antigene. Ca adjuvanti stimuleaza raspunsul imun innascut prin celulele dendritice si alte celule prezentatoare de antigene iar ca antigene stimuleaza expresia clonala a limfocitelor T care vor recunoaste antigenul prin intermediul receptorilor specifici.
E. ADJUVANTII
Numerosi adjuvanti bacterieni, in special polizaharidele, peptidoglicanul, flagelina si ADN-ul nemetilat se pot lega de numeroase TLR-uri ale celulelor raspunsului imun innascut, celulelor intestinale si celulelor mezenchimale. Legarea acestor TLR activeaza NFkB si protein kinazele mitogene care vor stimula transcriptia mai multor gene proinflamatorii si regulatoare.
Activarea macrofagelor la indivizii susceptibili de catre lipopolizaharide, peptodoglican si flagelina stimuleaza productia de IL-1b,TNF, IL-6, IL-8 si alte chemokine IL-12 p40 ( IL-12, IL-23), molecule de adeziune, IL-18, specii reactive de oxigen, oxid nitric si leucotriene, toate participand in raspunsuri inflamatorii. In aditie activarea NFkB de catre celulele prezentatoare de antigene induce expresia de MHCII, molecule costimulatoare, IL-12 si IL-23, care activeaza limfocitele T helper 1 si T helper 17.
Lipopolizaharidele stimuleaza productia de IL-12 si p40 de catre celulele dendritice din maduva hematogena la soarecii care nu prezinta IL-10 precum si colonizarea cu bacterii comensuale a sorecilor care nu prezentau germeni in prealabil. Studiile in vivo demonstreaza ca bacteriile comensale activeaza IL-20 in celulele dendritice ale ileonului. Flagelina bacteriana este atat adjuvant cat si antigen. O forma de flagelina s-a demonstrat a fi antigenul dominant in colita experimentala si induce productia de anticorpi in 50% din cazurile de pacienti cu boala Crohn. Flagelina se leaga de TLR5 ca sa activeze NFkB.
Pe langa rolul lor proinflamator adjuvantii au si anumite proprietati anti inflamatoare. De exemplu, lipopolizaharidele stimuleaza productia de IL-10 in celulele dendritice ale soarecilor normali si anumite CpG preparate pot preveni aparitia colitei experimentale prin inducerea productiei de IFN γ in celulele dendritice prin legarea de TLR9.
F. ANTIGENELE
Gazdele susceptibile genetic, inclusiv pacientii cu boli intestinale inflamatorii cronice, precum si soarecii obtinuti prin inginerie genetica sau cu mutatii spontane au raspunsuri agresive mediate de limfocitele T impotriva florei comensuale. Desi raspunsurile stimulatoare de limfocite B la flora comensuala sunt exagerate in boala Crohn, colita ulcerativa si inflamatia intestinala indusa experimental, anticorpii nu sunt implicati in transmiterea bolii ci sunt mai degraba regulatori decat patogeni. Anticorpii antibacterieni au fost folositi pentru prima data in diagnosticarea bolii precum si pentru identificarea subseturilor clinice de boli inflamatorii intestinale care raspund la diferiti agenti terapeutici.
Foarte putine studii au fost efectuate in vederea specificitatii antigenice, insa rezultatele studiilor pe animale de experienta au demonstrat ca boala poate fi transferata la pacientii imunodeficitari prin intermediul limfocitelor T activate impotriva florei enterice. Studiiile au demostrat ca doar limfocitele T activate de flora cecala pot transmite colita la soarecii care prezinta sindrom de imunodeficienta, nu si cele nespecifice. Dealtfel si transferul de clone de limfocite T activate de flagelina pot transmite boala la soarecii cu imunodeficienta.
A fost demonstrat astfel ca stimularea antigenica persistenta la lumenului intestinal este necesara pentru transferul colitei. Limfocitele T CD4 ale soarecilor cu colita indusa experimental au fost capabile sa induca colita prin transferul acestora la soarecii cu flora microbiana antigen-specifica, insa nu au putut induce colita la soarecii fara flora. Dupa transfer limfocitele T au inceput sa raspunda la stimularea din lumenul intestinal. Specificitatea raspunsului dat de limfocitele T helper este data atat de gazda cat si de antigenele bacteriene. Raspunsul selectiv al limfocitelor T a fost demonstrate pe studii cu soareci al caror intestine au fost colonizate selectiv cu E.coli si Enteroccocus faecalis. Astfel limfocitele T obtinute de la soarecii colonizati cu E.coli vor produce IFN-g numai la stimularea cu E.coli nu si Enterococcus faecalis. Soarecii cu gena HLA-B27TG carora li s-a administrat E.coli sau Enterococcus faecalis nu au dezvoltat colita in schimb la administrarea de Bacteroides vulgatus au dezvoltat.
S-a incercat gasirea unui antigen dominant in colita indusa experimental. Studiul Lodes a identificat o forma specifica de flagelina din speciile comensuale de Clostridium ca antigen dominant. Aproape o jumatate din pacientii cu boala Crohn, dar nu si cei cu colita ulcerata, prezinta un raspuns serologic declansat de acest tip de flagelina. Aceasta demonstreaza relevanta acestor modele experimentale.
Conform studiului Tannock in soarecii cu deficit de IL-10 si care sufereau de colita indusa experimental erau prezente in intestine antigene ale Bifidobacterium, Clostridium cocleatum, Bacteroides si Enterococcus. Conform studiilor preliminarii administrarea de Bifidobacterium animalis la soarecii cu deficit de IL-10 produce colita si raspuns imun mediat de limfocitele T helper1. Proteina 60 a fost identificata ca fiind antigenul dominant in cazul soarecilor cu gena HLA-B27TG care au fost infectati cu Bacteroides vulgatus. Aceste rezultate sunt foarte importante deoarece atat proteina 60 a Bacteroides vulgatus cat si flagelina sunt adjuvanti puternici dar si antigene datorita legarii lor de TLR4 si de TLR5.
ROLUL FLOREI COMENSALE IN INFLAMATIA INTESTINALA
Exista numeroase dovezi privind rolul florei comensale in patogeneza bolilor inflamatorii intestinale si colita experimentala. Cele mai convingatoare studii au fost facute pe animale gnotobiotice (animale coarora li se cunosc in totalitate flora si fauna).
In cel putin 11 studii realizate pe animale colita si activarea raspunsului imun nu s-au dezvolatat in absenta bacteriilor comensale si majoritatea cazurilor de colita raspund la antibiotice si probiotice. Aceste studii au demostrat ca atat speciile bacteriene cat si specificitatea gazdei sunt importante in inducerea colitei experimentale.
Asocierea E.coli si a E.faecalis la soarecii cu deficit de IL-10 a indus forme distincte fenotipic de colita. Colita indusa de E.faecalis a avut un debut insiduos (10 -12 saptamani dupa colonizarea intestinului) si s-a localizat la nivelul colonului distal fiind asociata cu colita transmurala , displazie si obstructie duodenala dupa 24 de saptamani. In contrast colita indusa de E.coli a aparut rapid dupa numai 3 saptamani si a fost caracterizata prin inflamatie moderata la nivelul cecului. Asocierea cu ambele tipuri de bacterii a dus la aparitia relativ rapida (o saptamana) de pancolita si displazie dupa 5 saptamani.
Studiile preliminarii au demostrat ca asocierea cu Klebsiella induce pancolita moderata si asocierea cu Bifidobacterium determina inflamatie la invelul colonului si duodenului. Aceste studii au demonstrat ca pana si bacteriile probiotice traditionale pot sa determine inflamatie intr-o gazda susceptibila acest lucru ridicand un semn de intrebare prinvind siguranta terapiilor probiotice. O exceptie o reprezinta colita indusa de dextran-sodiu-sulfat care in absenta florei comensuale are un prognostic mai prost. Acesta injurie acuta asupra epiteliului intestinal demostreaza rolul protector al NFkB in homeostazia celulelor epiteliale. Trei tipuri de colita experimentala indusa de 3 tipuri diferite de bacterii au demonstrat importanta susceptibilitatii gazdei. Astfel E.coli si E.faecacium induc colita la soarecii cu deficit de IL-10 in schimb B.vulgatus nu induce. B.vulgatus induce colita la soarecii transgenici HLA-B27. Nici una din aceste bacterii nu induce colita la soarecii tansgenici cu CD3e. Similar diferite specii probiotice au rezultate diferite in aceeasi gazda si diferite gazde raspund diferit la aceleasi specii probiotice (vezi figura 6).
Aceste studii arata ca diferite specii de bacterii pot sa determine fenotipuri diferite in aceeasi gazda, diferite specii de bacterii reprezinta stimulul dominat pentru boala si diferite specii probiotice reprezinta tratamentul in gazde cu susceptibilitate genetica diferita. Aceste observatii au relevanta in raspunsul terapeutic la diferite antibiotice si probiotice.
Bolnavii cu boli intestinale inflamatorii cronice raspund favorabil la tratamentul cu probiotice si antibiotice. Cateva mesaje patofiziologice provin din aceste studii. In primul rand, antibioticele au efect in colita produsa de boala Crohn dar nu si in ileita izolata, cu exceptia cazului postoperator in care in absenta valvei ileocecale modifica flora luminala. In al doilea rand antibioticele nu sunt eficiente in colita ulcerativa dar pot trata pouch-ita. In al treilea rand probioticele pot preveni reactivarea colitei ulcerative cronice dar nu sunt eficiente in tratarea bolii active. Diferite preparate probiotice produc raspunsuri diferite in acelasi tablou clinic. Aceste raspunsuri terapeutice sugereaza ca stimuli bacterieni dominanti sunt diferiti in boala Crohn cu localizare ileala si colonica si ca bacteriile comensale sunt mai importante in boala Crohn decat in colita ulcerativa.
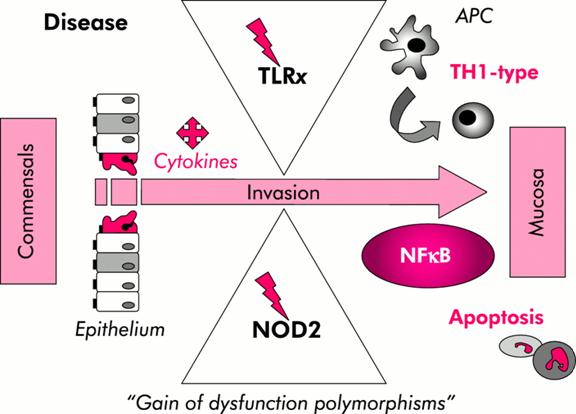
Figura 6. Rolul florei comensuale in inflamatia intestinala.
STIMULII DIN MEDIU
Studiile au demonstrat existenta mai multor stimuli din mediu implicati in patogeneza bolilor inflamatorii intestinale cronice. Acesti factori sunt fumatul care este protector in colita ulcerativa si agraveaza boala Crohn, dieta, folosirea de antibiotice si antinflamatorii nesteroidiene, stress-ul si infectiile. Din nefericire, mecanismele prin care pot sa initieze bolile sau prin care le reactiveaza nu sunt pe deplin cunoscute. Privind in ansamblu, acesti triggeri din mediu intervin in alterarea integritatii de bariera a epiteliului intestinal, in raspunsurile imune, in flora microbiana, fiecare avand un rol bine determinat in susceptibilitatea la aparitia inflamatiei.
Infectiile si antiinflamatoarele nesteroidiene pot sa initieze inflamatia nespecifica, pot intrerupe bariera de mucoasa si sa activeze raspunsul imun innascut. Aceste evenimente pot duce la captarea de adjuvanti si antigene ale bacteriilor comensale care vor stimula inflamatia intestinala mediata de limfocitele T la pacientii susceptibili genetic. Un exemplu il reprezinta inducerea colitei cronice la soarecii cu deficit de IL-10 prin expunerea la piroxicam (antiinflamator nesteroidian) pe parcursul a 2 saptamani.
Desi in bolile inflamatorii intestinale cronice sunt implicate dieta si stress-ul, mecanismul prin care acestea actioneaza nu este pe deplin cunoscut. Aditivii alimentari precum aluminiul si fierul au rol de adjuvanti si stimuleaza virulenta bacteriana. Stress-ul poate altera permeabilitatea mucosala, fluxul sangvin la acest nivel, electrolitii din epiteliu si secretia de apa si expresia de citokine si neuropeptide.
Fumatul este cel mai documentat stimul din mediu implicat in bolile inflamatorii cronice dar efectul sau este contradictoriu in boala Crohn si in colita ulcerativa, lucru care este greu de inteles. Nicotina, monoxidul de carbon si hipoxia sunt mediatori ai efectelor fumatului in aceste boli.
TEORII SPECIFICE
Dupa cum s-a discutat in introducere, mai multe teorii incearca sa explice inflamatia persistenta si reactivarea la pacientii cu boala Crohn si colita ulcerata. Pentru fiecare teorie s-au adus imbunatatiri care vor fi explicate mai jos.
A.INFECTIA PATOGENICA PERSISTENTA
Desi numeroase ipoteze privind rolul agentilor infectiosi in aparitia bolii Crohn si a colitei ulcerative au aparut inca de la descrierea bolilor, doar in patogenia bolii Crohn s-au gasit 2 infectii care au fost acreditate prin studii experimentale concludente.
SUBSPECII DE MICOBACTERIUM-AVIUM
Inflamatia granulomatoasa din boala Crohn seamana cu tuberculoza intestinala sau cu enterita spontana cauzata de Micobacterium avium (MAP) la rumegatoare, aceasta fiind cunoscuta sub denumirea de boala Johne. MAP a fost implicata pentru prima data in boala Crohn in 1984 cand organismul a fost cultivat din trei intestine rezecate.
Studiile necontrolate au raportat ca pana la 84% din pacienti raspund la tratamentul cu combinatii de antibiotice efciente impotriva MAP. Controversa a fost identificata de faptul ca MAP se gaseste in laptele pasteurizat si in laptele matern reprezentand astfel un mod de transmisie. Controversa a fost mentinuta si de faptul ca MAP a fost cultivata din sangele a 55% din pacientii cu boala Crohn si 22% din pacientii cu colita ulcerativa. Studiile recente au identificat prezenta unei portiuni de ADN( secventa de insertie 900) apartinand MAP pe segmente de intestine la 52% din pacientii cu boala Crohn, 2% din pacientii cu colita ulcerata si 5% din controale. Aceste rezultate sunt consistente cu majoritatea studiilor care detecteaza MAP mai mult in boala Crohn decat in colita ulcerativa sau controale, desi rezultatele sunt foarte variabile si ratele de detectie ale MAP variaza intre 0-100%.
Exista posibilitatea unei zoonoze cu MAP. In America de Nord, Europa si Australia MAP se gaseste in produsele lactate. MAP poate fi cultivata din apa si pamantul cirezilor, se transmite in laptele vacilor si supravietuieste pasteurizarii datorita capacitatii sale de supravietuire intracelulara. Aceasta teorie are slabiciunile sale mai ales datorita faptului ca nu exista evidente histochimice de infectie tisulara si incarcatura bacteriana in pacientii cu boala Crohn este extrem de mica.
Lezarea tesutului de o infectie paucibacilara ar fi rezulatul activarii unui raspuns mediat celular impotriva MAP insa acest lucru nu s-a identificat la pacientii cu boala Crohn. Mai mult o infectie cu mycobacterii ar fi intensificat imunosupresia adusa de tratamentul cu corticosteroizi, anti-TNF in cazul pacientilor infectati concomitent cu HIV. Simptomele pacientilor cu boala Crohn se amelioreaza in starile de imunodeficienta. Un studiu dublu orb privind elucidarea acestei infectii a avut loc pe parcusul a 2 ani in Australia folosindu-se antibioterapie tripla. Studiile preliminarii au aratat o rata de raspuns de 33% la pacientii tratati cu antibiotice pe langa 18% la controale (P<0.5) dar nu exista persistenta raspunsului la 1 an de la incetarea tratamentului. Este posibil ca un subset de pacienti cu boala Crohn care sunt susceptibili genetic, mai ales cei care nu sunt capabili sa lupte impotriva unei infectii intracelulare (polimorfism CARD15) sa aiba o infectie persistenta cu MAP cauzatoare de boala sau organismul potenteaza raspunsurile mediate celular la flora comensala enterica. Secventa de ADN IS900 a MAP nu se gaseste preferential in ileon ceea ce ar fi de asteptat daca MAP ar fi asociata cu polimorfismul genei CARD15. Mai probabil este faptul ca agenti comuni din mediu colonizeaza selectiv mucoasa ulcerata a pacientilor cu boala Crohn decat sa cauzeze boala.
E.COLI ENTEROADERENTA SI INVAZIVA
Darfeuille-Michaud si Colombel au descoperit o tulpina virulenta de E.coli din 22% din biopsiile de mucoasa ale pacientilor cu boala Crohn cu infectie recurenta postoperatorie in neoileonul terminal. Aceste tulpini de E.coli adera de epiteliul celular prin intermediul pililor de tipul 1, invadeaza macrofagele printr-un mechanism dependent de monofilamente si microtubuli si persista si se replica in macrofage. Infectia macrofagelor induce proliferarea TNF-ului dar nu apoptoza celulara. Dupa infectia cu tulpina de E.coli monocitele pacientilor cu polimorfism CARD15 au nivel scazut de TNF si IL-10 comparativ cu celulele din mucoasa normala. Aceste rezultate sunt consistente cu rapoarte imunohistochimice privind cresterea aderentei E.coli la mucoasa, invadarea ulcerelor si a fistulelor, prezenta bacteriei in macrofagele din lamina propria la pacientii cu boala Crohn, precum si cu conceptul de clearance deficitar al infectiilor intracelulare la pacientii cu polimorfism al genei CARD15.
B DISBIOZA
Alterarea balantei dintre efectele benefice si cele agresive ale speciilor microbiene poate duce la aparitia inflamatiei intestinale cronice la o gazda susceptibila. Numeroase studii au implicat anumite bacterii comensuale cum ar fi E.coli, Bacteroides, Enterococcus si Klebsiella in patogeneza colitei indusa experimental si in bolile inflamatorii intestinale cronice. In contrast specii cum ar fi Lactobacillus si Bifidobacterium ar avea efecte predominat benefice si pot fi folosite terapeutic ca probiotice. Mai multe studii au demonstrat alterarea florei microbiene comensale in boala Crohn si colita ulcerativa.
Prin achizitia factorilor de virulenta flora comensala a putut astfel declansa raspunsuri imune agresive impotriva epiteliului intestinal. Cum s-a discutat inainte, E.coli enteroadeziva si enteroinvaziva a fost identificata in neoileonul terminal al pacientilor cu recurente postoperatorii ale bolii Crohn. Flagelina obtinuta de la speciile de Clostridium se pare ca ar fi un antigen dominant in colita indusa experimental si determina aparitia de raspunsuri serologice la aproximativ 50% din pacientii cu boala Crohn. Prezenta superoxid dismutazei altereaza patogenitatea lui E.faecalis.
Componentii dietetici pot sa altereze compozitia si virulenta bacteriilor enterice comensale, explicand astfel cresterea incidentei bolilor inflamatorii intestinale cronice in tarile vestice mai ales in a cea de-a doua jumatatea a secolului douazeci, mai recent si in tarile estice dupa ce acestea au inceput sa adopte dieta vestica. Carbohidratii nonabsorbabili (prebioticele) cum ar fi oligozaharidele de inulina si fructoza potenteaza cresterea speciilor de Bifidobacterium si Lactobacillus si reprezinta substratul necesar producerii de acizi grasi cu lant scurt de atomi de carbon. Acesti acizi grasi in special butiratul reprezinta substratul metabolic preferential al colonocitelor si stimuleaza numeroare functii necesare in pastrarea barierei epiteliale intacte. Fierul stimuleaza cresterea si diferentierea bacteriilor intracelulare iar aluminiul este un adjuvant in initierea raspunsurilor imune. Atat fierul cat si aluminiul sunt aditivi alimentari ubiquitari in dietele vestice. Atat fierul cat si aluminiul din dieta potenteaza colita experimentala.
Teoria igienica ofera o explicatie alternativa pentru cresterea incidentei bolilor intestinale inflamatorii cronice, astmului si bolilor autoimmune cum ar fi artrita reumatoida si diabetul zaharat tip I in tarile vestice. Aceasta teorie sugereaza ca expunerea la patogeni sau paraziti, in special in primii ani ai vietii, stimuleaza imunitatea protectoare si mai tarziu aparitia unor raspunsuri imune agresive. Weinstock a propus ipoteza conform careia eliminarea infectiilor helmitice prin masurile de sanatate publica a dus la cresterea incidentei bolilor inflamatorii intestinale cronice si a demonstrat efectele terapeutice ale Tricuris suis (tenia porcului) in tratamenul colitei ulcerate, bolii Crohn si colitei indusa experimental.
C. DEFECTELE FUNCTIEI DE BARIERA DE LA NIVELUL MUCOASEI
Un defect in integritatea barierei intestinale ar putea duce la captarea crescuta a antigenelor luminale si a adjuvantilor care ar supresa tonul imunitatii locale. Alternativ, un defect in repararea epiteliala ar putea potenta efectele negative ale unor stimuli cum ar fi antiinflamatoarele nesteroidiene sau infectiile care ar determina numai efecte trecatoare la gazdele normale.Efectul net al ambelor cai este stimularea constanta a raspunsurilor imune innascute si dobandite la nivelul mucoasei de catre adjuvantii luminali si antigene. Exista numerose gene implicate in functia epiteliala cum ar fi CARD15, OCTN1, OCTN2, DLG5 si MDR1. Gena MDR1 se pare ca mediaza excretia moleculelor xenobiotice si bacteriene din celulele epiteliale, in timp ce gena CARD15 mediaza clearance-ul bacterian si productia de a defensine antimicrobiene de catre celulele Paneth.
D. CLEARANCE-UL MICROBIAN DEFECTIV
Asocierea bolii Crohn cu gena CARD15 precum si efectele terapeutice ale factorului stimulator de colonii de monocite-macrofage (GM-CSF) sustin noua ipoteza conform careia boala Crohn este rezultatul unui defect in distrugerea bacteriana. Gena CARD15 este exprima constitutiv in celulele Paneth ale intestinului subtire si determina exprimarea de a defensine si criptidina si mediaza distrugerea bacteriilor intracelulare.
Stimularea orala cu Listeria monocitogenes a sorecilor care nu prezinta gena CARD15 duce la o rata de mortalitate mai mare decat a soarecilor normali, dar nu determina cresterea mortalitatii la administrarea sistemica. Autorii acestui studiu atribuie cresterea mortalitatii la administrarea orala datorita deficitului criptidinei aceasta fiind produsa de gena CARD15 dar si datorita clearance-ului defectiv al antigenelor bacteriene. Swidsinski a demostrat si cresterea adezivitatii bacteriilor enterice la pacientii cu boala Crohn activa si colitei ulcerative. Aceste experimente pe soareci sunt consistente cu observatiile independente ale lui Wehkamp care a demostrat deficiente in expresia a defensinelor si b defensinelor la pacientii cu boala Crohn care prezinta polimorfisme ale genei CARD15.
Korzenik si Dieckgraefe au postulat faptul ca boala Crohn apare ca un deficit in distrugerea bacteriilor de catre raspunsul imun innascut pe baza asemanarii patologice dintre boala Chron si enterocolita din boala granulomatoasa cronica si boala de stocarea a glicogenului IIB. Persistenta bacteriilor in tesuturile pacientilor cu boala Chron a fost detectata prin tehnici de imunohistochimie si prin culturi obtinute din ganglionii limfatici mezenterici. Intr-un studiu orb randomizat administrarea zilnica de GM-CSF recombinant a indus remisie la 40% din pacientii cu boala Chron moderat-severa. Pe langa activarea macrofagelor, monocitelor si neutrofilelor, GM-CSF afecteaza si functia celulelor dendritice stimulatoare a plasmocitelor, celulor Paneth si celulelor epiteliale deoarece aceste celule prezinta receptori pentru acest factor de crestere.
E IMUNOREGLARE ABERANTA
Studiile pe animale au demonstrat ca inflamatia intestinala cronica poate sa rezulte din imunosupresie defectiva, hiperactivitatea limfocitelor T helper 1 sau hipersecretie de citokine. Principalii mediatori ai imunosupresiei sunt IL-10 si TGF-b ale caror functii interactioneaza. Majoritatea studiilor umane demostreaza insa ca activarea imunitara este data de raspunsul agresiv al limfocitelor T ale raspunsului imun innascut mai degraba decat o deficienta in autoreglare. Pacientii cu boli intestinale inflamatorii cronice au toleranta orala scazuta. Un potential mecanism de deficit dobandit in functia imunoregulatoare a fost sugerat de McDonald care a descris expresia genei SMAD7 la pacientii cu boala activa. Proteina indusa de SMAD7 blocheaza activitatea TGF-b prin inhibarea fosforilarii SMAD2/4. In boala Crohn au fost deasemenea documentate crestera expresiei de citokine produse de limfocitele T helper 1 si 17 cum ar fi TNF, IL-6, IL-12, IL-17, IL-23 iar in colita ulcerativa are loc cresterea de citokine induse de limfocitele T helper 2 IL-4 si IL-13.
Inducerea celulelor T efectoare si nu a celor regulatoare se face datorita interactiunilor dintre celulele prezentatoare de antigen si limfocitele T dar si prin interactiuni celulare mediate de molecule co-stimulatoare si prin legarea receptorilor limfocitelor T de moleculele MHC, dar si prin intermediul semnalelor induse de citokine. Exista trei fenotipuri de limfocite T cu rol regulator, fiecare cu origine unica, functie si antigene stimulatoare. Limfocitele T regulatoare si limfocitele Th1 pot preveni aparitia inflamatiei intestinale si limfocitele T CD4 si CD25 pot reversa colita indusa experimental.
Studiile preliminare au demostrat faptul ca celulele prezentatoare de anticorpi (APC) sunt cele care determina fenotipul limocitelor T(reglatoare sau efectoare) la soarecii cu colita indusa experimental si cu deficit de IL-10. Limfocitele T CD4 din ganglionii limfatici mezenterici de la soarecii cu deficit de IL-10 si de la soarecii normali au fost incubate cu celule prezentatoare de antigen stimulate in prealabil cu bacterii din cec. A fost observata productia de IFN-g de catre limfocitele T CD4 la soarecii cu deficit de IL-10.
Aceste studii demonstreaza importanta celulelor prezentatoare de antigen in reglarea functiilor limfocitelor T. Mai multe studii au adus o lumina noua privind rolul raspunsului imun innascut si functia celulelor dendritice in inflamatia intestinala. Card15 poate inhiba activarea celulara de NFkB si secretia de IL-12 p40 prin stimularea ligandului TLR2, punand in evidenta un potential mecanism care sa explice activarea NFkB la pacientii cu boala Crohn. Activarea excesiva a NFkB a fost observata si la soarecii carora li s-au indus mutatii la nivelul genei Card15. ADN-ul bacterian care previne si trateaza colita experimentala pe mai multe modele inhiba activarea NFkB prin inducerea de IFN-a b in celulele dendritice. In final, GM-CSF stimuleaza functiile regulatorii ale celulor dendritice stimulatoare de plasmocite prin intermediul IFN-a b, acesta fiind un rol alternativ al GM-CSF in afara faptului ca intervine in stimularea raspunsului imun innascut. Dealtfel, functia defectiva a APC, masurata prin scaderea raspunsului imun innascut la liganzii bacterini, a fost implicata in raspunsuri patologice ale limfocitelor T helper 1, posibil prin alterari genetice in functia NFkB.
Numarul de celule inflamatorii din intestine este determinat de recrutarea acestora din circulatie, proliferarea si moartea lor prin necroza sau apoptoza. Datele arata ca limfocitele T la pacientii cu boala Crohn sunt rezistente la apoptoza, ceea ce va duce la o populatie crescuta de limfocite T helper 1 activate. Mecanismele moleculare care explica aceasta rezistenta sunt alterarea activitatii moleculelor proapoptotice si a celor antiapoptotice prin legarea de IL-6 sau de receptorii solubili de IL-6 de catre glicoproteina membranara 130. Semnalul produs de legarea IL-6 va determina activarea genelor antiapoptotice BCL2 si BCL2L1( fosta BCL-XL) in timp ce anticorpii anti receptor de IL-6 sau proteina de fuziune a glicoproteinei 130 induce apoptoza si atenueaza colita. Numeroare terapii care sunt eficiente in bolile inflamatorii intestinale cronice cum ar fi corticosteroizii, sulfasalazina, azatioprina, 6-mercaptopurina, infliximab si anticorpii anti IL-12 induc apoptoza si activarea limfocitelor T in unele monocite. Capacitatea lor de a induce apoptoza in celulele activate care exprima TNF poate sa explice diferitele efecte terapeutice ale agentilor anti-TNF folositi in boala Crohn.
2.4. TABLOU CLINIC
Boala Crohn (BC) este
caracterizata de exacerbari focale, cu activitate intermitenta
de-a lungul vietii pacientului.
Manifestarile initiale sunt adesea insidioase si vagi. Simptomele sistemice includ febra inexplicabila,
scadere in greutate, artralgii si abcese perianale.
Boala poate fi
localizata pe tot parcursul sistemului gastro-intestinal si
caracteristicile histologice de
inflamatie pot fi evidente in zonele endoscopic aparent neafectate.
Cu toate acestea, marea
majoritate a cazurilor noi de BC sunt situate in
trei locuri:doar in intestinul subtire , doar in colon sau in ambele. Caracteristicile clinice depind de
localizarea anatomica, extinderea bolii, aparitia unor complicatii,
si implicarea extraintestinala. Acestea pot fi explicate in
continuare, cel putin in parte, de
pacienti cu diferite medii
genetice.
Simptomele
clinice
Simptomele includ
frecvent diaree pentru mai mult de 6
saptamani, dureri abdominale, si / sau scadere in greutate
.
Doar la o minoritate de pacienti este implicat
duodenul sau jejunul, in principal
asociate cu ileita, si doar un numar foarte mic de pacienti
au localizare jejunala .Evolutia endoscopiei, a aratat o frecventa mai mare de BC in tractul gastro-intestinal
superior (5-7%) . Aproximativ
1-4% dintre pacienti sufera de manifestari atipice, cu afectare
orala
boli faringiene si esofagiene
si implicarea gastrica
Evolutia bolii
Procesul de inflamatie cronica transmurala
poate duce la stricturi
intestinale si fistule conectate la
piele sau in apropierea organelor.
Comportamentul bolii variaza
pe parcursul timpului; la10 ani, aproape 50% din pacienti au o schimbare in
comportamentul bolii . Majoritatea pacientilor nu prezinta stricturi
si fistule la diagnostic, dar
dupa 25 de ani de evolutie acestea apar in majoritatea cazurilor.
Dezvoltarea acestora reprezinta un fenomen multifactorial fiind
implicati factori de mediu si genetici. Factorii de mediu includ
boli, tratamente, fumatul, acesta din urma fiind asociat cu formele agresive . Factorii genetici par sa
influenteze viteza cu care apar fistule sau stricturi mai degraba decat comportamentul final
al bolii. Comportamentul bolii este asociat cu dezvoltarea de complicatii
si nevoia de interventii chirurgicale.
O asociere exista intre localizarea izolata la nivelul intestinului subtire si prezenta stricturilor dar si afectarea colonului si aparitia fistulelor. Aceasta asociere a fost prezenta la momentul diagnosticului si a fost mai proeminenta dupa 10 ani. Recent, boala perianala s-a dovedit a fi asociata cu un risc crescut de aparitie si progresie a complicatiilor.
Manifestari extraintestinale
Boala
Crohn este asociata cu o varietate
de manifestari sistemice care influenteaza cursul sau, raspunsul
terapeutic, precum si calitatea vietii pacientului. Frecventa de
manifestari extraintestinale variaza de la 16 pana la 25% . Mai
multi factori
pot fi responsabili pentru implicarea organelor extraintestinale si poate fi
dificil
de distins intre adevaratele manifestari extraintestinale si
complicatii din cauza disfunctiei intestinale sau efectelor adverse
la tratament. In timp ce unele manifestari, de exemplu, cele asociate cu
dereglare autoimuna, nu pot fi corelate cu activitatea bolii, acestea se
suprapun cu evolutia clinica a bolii intestinale. Mecanisme autoimune
includ sensibilitatea genetica, afisarea de autoantigene, auto-recunoasterea
aberanta si autoanticorpi impotriva elementelor celulare colonice sau
extracolonice.
Clasificarea Montreal
Se definesc grupuri de bolnavi dupa localizarea bolii, dupa patternul evolutiv, dupa severitatea bolii (cel mai folosit este CDAI -Crohn's Disease Activity Index), dupa
prezenta complicatiilor.Clasificarea Montreal din 2005 a revizuit vechea clasificare a bolii Crohn adoptata in 1998.
TABELUL 1: CLASIFICAREA VIENNA SI MONTREAL
|
VIENNA |
MONTREAL |
|||
|
VARSTA LA DIAGNOSTIC |
A1- |
<40 ani |
A1- |
≤16 ani |
|
A2- |
≥40 ani |
A2- |
17- 40 ani |
|
|
A3- |
>40 ani |
|||
|
LOCALIZARE |
L1- |
Ileonul terminal |
L1- |
Ileonul terminal |
|
L2- |
Colon |
L2- |
Colon |
|
|
L3- |
Ileo-colon |
L3- |
Ileo-colon |
|
|
L4- |
Tractul GI superior |
L4- |
Afectarea izolata a tractului GI superior * |
|
|
PATTERN EVOLUTIV |
B1- |
Non-obstructiva , non-fistulizanta |
B1- |
Non-obstructiva , non-fistulizanta |
|
B2- |
Obstructiva |
B2- |
Obstructiva |
|
|
B3- |
Fistulizanta |
B3- |
Fistulizanta |
|
|
p |
Afectare perianala** |
|||
*L4 poate fi adaugat localizarii L1-L3 atunci cand este prezenta afectarea concomitenta
a tractului gastro-intestinal superior.
**p de adauga la B1- B3 atunci cand exista boala perianala concomitenta
Afectarea perianala in BC este un alt tablou clinic obisnuit, leziunile perianale pot
preceda manifestarile intestinale ale BC cu o medie de 4 ani. Afectarea anoperineala
defineste deasemenea un grup cu evolutie severa, prezenta ulceratiilor anale fiind un
index fiabil pentru o evolutie severa pe termen scurt sau lung.
2.5. DIAGNOSTIC POZITIV SI DIFERENTIAL
De-a lungul ultimelor decenii,
endoscopia a devenit un instrument esential pentru tratarea pacientilor cu boala Crohn
. Indicatiile pentru endoscopie in
pacientii cu BC includ un diagnostic corect (atat endoscopic si histologic),
evaluarea
localizarii si activitatii bolii, diagnosticul de
recurenta postoperatorie,
evaluarea bolii perianale, dilatarea stricturilor, si supravegherea pacientilor cu boala de colon de
lunga durata.
DIAGNOSTIC POZITIV
Colonoscopia cu intubatie
a ileonului terminal trebuie sa fie prima procedura efectuata
in evaluarea initiala a
pacientilor cu simptome clinice sugestive de boala inflamatorie intestinala, deoarece
permite vizualizarea directa si biopsia a mucoasei
si este utila pentru distinctia intre boala Crohn si colita
ulceroasa dar si pentru a exclude alte cauze de colita, cum ar
fi infectiile bacteriene, ischemia sau utilizarea de antiinflamatorii
nesteroidiene
In scopul de a
diferentia boala Crohn de pacientii cu colita ulcerativa este foarte important a se efectua o
endoscopie inainte de inceperea tratamentului. Chiar daca unele
caracteristici endoscopice (ulcere aftoide, ulcere serpinginoase) sunt
sugestive pentru boala Crohn, nici unul dintre ele nu este specific. Caracteristicile cele mai
utile utilizate pentru a diferentia boala Chron de colita ulcerata sunt
afectarea segmentara de colon, afectarea distala a ileonului si
boala perianala.
Un endoscopist experimentat
este capabil sa faca diferenta intre boala Crohn si colita
ulcerativa la aproximativ 90% dintre pacienti. Biopsiile luate in timpul endoscopiei sunt
importante pentru a distinge intre bola Crohn si colita ulcerativa
si alte forme mai putin frecvente de colita cronica, cum ar
fi colita limfocitara .
Din pacate, desi
criteriile histologice pentru a distinge diferite forme de
boli inflamatorii intestinale sunt bine stabilite, un diagnostic final nu ar
trebui sa se bazeze pe examenul histopatologic singur, ci si pe
criterii clinice, radiologice si endoscopice.
Evaluarea endoscopica a tractului
gastro-intestinal superior poate fi importanta, fie de pentru evaluarea localizarii
bolii dar si pentru un tratament corect sau in diagnosticul de boala
Crohn la un pacient cu colita nedeterminata .Implicarea tractului
intestinal superior apare la pana la 13% dintre pacienti si pot include esofagul, stomacul, duodenul
Este interesant de observat ca granuloame (40-60%) sunt mai frecvent
detectate in duoden decat in biopsia de colon
Fig. 7 Imagine endoscopica cu ulceratii liniare si aplatizarea plicilor ileale la un pacient in varsta de 21 de ani cu boala Crohn ileala
Leziunile de intestin
subtire pot fi vizualizate si prin capsula endoscopica. Tehnologia
permite vizualizarea directa a
intestinului subtire. Capsula este o camera mica, de dimensiunea unei
pastile de vitamine si are
doua imagini pe secunda. Este usor de inghitit si
transmite imagini pentru 8 ore la un dispozitiv de inregistrare localizat
in jurul abdomenului. Imaginile sunt descarcate la un computer si
apoi revizuite de catre un gastroenterolog. Leziunile mai frecvente
vizualizate cu aceasta tehnica includ eroziuni mucoase, afte, leziuni
liniare si serpiginoase , ulceratii, si fisuri.
Capsula endoscopica este considerata neinvaziva, o procedura bine tolerata
si
acceptata de catre pacienti; cu toate acestea, pana in
prezent nu exista criterii
standardizate pentru diagnosticul de boala Crohn. Odata ce
diagnosticul de boala Crohn se face,
indicatii pentru a repeta aceasta procedura se refera numai la
aspecte particulare ale bolii.
In boala Crohn standardul de aur
pentru a monitoriza activitatea bolii este
indicele de activitate al bolii (CDAI), un scor clinic care nu include
evaluarea endoscopica. In consecinta, repetarea colonoscopiei nu
a fost sustinuta deoarece cele
mai multe medicamente prescrise pentru a induce remisie clinica nu sunt
utile in inducerea vindecarii mucoasei.
Exista dovezi recente
care demostreaza ca imunosupresia si tratamentul cu infliximab
determina o vindecare a intestinului
a.Diagnosticul de Recurenta postoperatorie
Recurenta dupa o
interventie chirurgicala este una din principalele probleme la pacientii
cu boala Chron. La majoritatea pacientilor boala reapare in primul an
dupa operatie . Acesta recurenta este limitata la
anastomoza ileocolica, cu ulcere aftoase sau liniare de cativa
centimetri in peretele colonului adiacent si ileonului neoterminal. Severitatea
reaparitiei endoscopice se calculeaza folosind scorul Rutgeerts .Se
pare ca reaparitia dupa interventia chirurgicala prezice
un curs mai agresiv al bolii, sugerand necesitatea unei abordari
terapeutice mai agresiva.
Ileo-colonoscopia este
considerata standardul de aur in detectarea reaparitiei
post-chirurgicale cu o sensibilitate de 90% si o specificitate de
100%.Capsula endoscopica a fost
propusa ca un instrument alternativ pentru diagnosticul de
recurenta, dar sensibilitatea sa este scazuta, 50-79%, cu o
specificitate de 90%. Unele studii au aratat ca exista o
subestimare a scorului Rutgeerts in leziuni detectate prin capsula
endoscopica comparativ cu cele identificate de catre
ileocolonoscopie. In afara de reaparitia la nivel ileal, nici o
leziune proximala nu a fost
detectata prin aceasta procedura. In contrast, capula endoscopica
ar putea fi utila la pacientii cu recidive stabilite la nivel ileal,
deoarece 50% dintre pacienti au leziuni concomitente in ileonul proximale
sau in jejun
b. Boala perianala
In ultimii 10 ani,
combinatia de endoscopie cu ultrasunete (EUS) s-a dovedit a fi un
instrument util in evaluarea tulburarilor colorectale, anale, si
pelviene, datorita inaltei
rezolutii a acestei tehnici.
Pana
in prezent, rolul EUS in bolile inflamatorii este limitat la evaluarea bolii
perianale la pacientii cu boala Chron si complicatiile
perirectale .
EUS
permite diferentierea de fistule simple si complexe si evaluarea cailor fistulei. Este o
procedura extrem de sensibila pentru detectarea abceselor perianale
si poate fi considerata o alternativa valabila RMN-ului
si endoscopiei.
c.
Dilatarea stricturilor
Cursul bolii este deseori complicat de fibroza
gastro-intestinala si stricturi care ar putea duce la obstructie
intestinala si care necesita o interventie chirurgicala
la 20% dintre pacienti. Din pacate, boala se repeta frecvent
dupa rezectie, uneori conducand la repetate interventii
chirurgicale. Pentru stricturi sunt accesibile abordari endoscopice cum ar
fi dilatarea balon-endoscop.Rata de complicatii majore, inclusiv
perforarea intestinului, a fost de 2%, suficient de scazuta pentru a
lua in considerare procedura ca fiind relativ sigura. Dilatarea pneumatica a stenozei, a
fost atinsa la 90% dintre pacienti.
Majoritatea
pacientilor care au suferit o dilatare au avut rezultate foarte bune pe
termen scurt. Doar 30% dintre ei au mentinut succesul pe termen lung dupa o singura dilatare.
Din acest motiv, dilatari ulterioare ar trebui sa fie efectuate, chiar si
in absenta unor simptome obstructive.
d. Colonoscopia de supraveghere in colita cronica din boala Crohn
Importanta colonoscopiei
de supraveghere in colita Crohn a devenit deosebit de evidenta dupa
un raport al grupului Prezent, efectuat la pacientii cu colita Chron
de lunga durata . In
aceasta serie longitudinala de 259 pacienti,displazia de grad
inalt sau cancerul a fost gasit la 32 de
pacienti (12%) . Dupa un rezultat de screening negativ,
probabilitatea de diagnosticare a neoplaziei prin examinarea de supraveghere a
fost de 22%. Rezultatele actualizate ale acestui studiu au fost: toti
pacientii au avut cel putin 7 ani de colita Crohn care
afecteaza cel putin o treime din colon; pacientii au fost
urmariti la fiecare 1-2 de ani, riscul cumulativ de a detecta o
displazie certa sau cancer dupa o colonoscopie de screening negativa
a fost de 25% dupa a zecea examinare. Prin urmare, colonoscopia de
supraveghere periodica ar trebui sa faca parte din urmarirea de rutina
a pacientilor cu colita cronica din boala Crohn .
Chromoendoscopia cu indigo-carmin
sau albastru de metilen este utila pentru a detecta schimbari subtile
ale mucoasei si creste randamentul endoscopiei de supraveghere la
pacientii cu boli inflamatorii intestinale . Desi aceste date trebuie
sa fie confirmate, chromoendoscopia ar putea sa devina procedura
de alegere pentru aceasta indicatie.
TESTELE DE LABORATOR
Este neobisnuit
pentru pacientii cu boli inflamatorii intestinale sa se prezinte cu simptome si semne
clinice aproape specifice sau patognomonice. Aceasta implica faptul
ca diagnosticarea bolii Crohn sau a colitei ulcerative este dependenta
in mod substantial
de o combinatie de teste clinice, radiologice, endoscopice si histologice
Mai multi biomarkeri de laborator sunt utili in gestionarea acestor pacienti, proteina C reactiva fiind cea mai utilizata in practica clinica. Nivelurile de de calprotectina si lactoferina fecala sunt markeri promitatori pentru a fi utilizate in viitorul apropiat, in acest domeniu, dar datele din literatura de specialitate bazate pe dovezi sunt relativ limitate si investigatii suplimentare sunt necesare.
Proteina C reactiva
Concentratiile sanguine
de CRP, reactant de faza acuta sunt
puternic crescute intr-o gama larga de afectiuni inflamatorii .
CRP este crescuta precoce dupa declansarea procesului inflamator
si, ca urmare a timpului de injumatatire scurt face ca CRP sa fie un marker de activitate a
bolii. In plus, testarea CRP este ieftina si usor de realizat
si nivelurile sale nu sunt afectate
de medicamente, cu exceptia corticosteroizilor care afecteaza in mod
direct procesele inflamatorii. Alt avantaj de masurare a CRP este
ca nu exista nici o cerinta de post peste noapte inainte de
prelevare.
Diferente importante in
randul pacientilor IBD, cu privire la concentratiile din sange ale CRP
au fost identificate: Cu toate acestea, mecanismele responsabile pentru aceste
diferente sunt inca incomplet intelese. De exemplu, CRP
creste puternicin timpul episoadelor acute inflamatorii de boala Chron
in schimb la pacientii cu colita ulcerativa nivelele sunt usor
crescute sau normale chiar si in
timpulul celei mai severe
inflamatii .
Motivele
pentru aceasta diferenta intre BC si CU sunt inca necunoscute.
In plus in sange si la nivelul tesutului citokinele pro-inflamatorii, cum ar fi interleukina (IL)
-6, IL-1
si factorul de necroza
tumorala (TNF)- ,
au crescut puternic in ambele conditii. Exista unele dovezi ca exista
o crestere mai mare in sangele periferic a IL-6 la pacientii cu BC
decat la pacientii CU si acest lucru ar putea, cel putin in
parte, sa explice de ce concentratiile CRP in sange sunt mai ridicat.
De asemenea, este demn de remarcat faptul ca inflamatia este limitata
la mucoasa colonului in CU iar in BC-ul
exista o inflamatie granulomatoasa care in mod indirect
sugereaza o reactie inflamatorie
sistemica cu nivele ridicate in sange ale CRP.
Masurarea CRP are sensibilitate si specificitate de 80-85%
in randul pacientilor care prezinta manifestari clinice compatibile
cu boli inflamatorii intestinale . Cresterea
sensibilitatii si specificitatii la aproape 100% are
loc in cazul pacientilor cu BC-uri iar in cazul celor cu CU scade la
50. In plus, din cauza timpului de injumatatire scurt de aproximativ 19 h, nivelurile de proteina C sunt considerate bune pentru a reflecta
variatiile in activitatea inflamatorie fiind mai fiabile decat alte proteine de faza acuta cum ar fi fibrinogenul. Cu
toate acestea, exista, de asemenea, dovezi ca aproximativ 10% din pacienti
cu BC activa au nivel scazut de CRP sangvin. Motivele
pentru aceasta discrepanta sunt neclare; cu toate acestea, se
pare ca acesti pacienti sufera de afectare ileala cu un fenotip stenozant cu
un risc mai mare de rezectie intestinala, mai degraba decat fenotipul
cu fistule intestinale. CRP este astfel cel mai bun marker de activitate
clinica in BC comparativ cu alte biomarkeri, cum ar fi viteza de sedimentare
a hematiilor (VSH), dar VSH se coreleaza mai bine cu activitatea
endoscopica a bolii.
Prin urmare, CRP este un util
bio-marker pentru a monitoriza longitudinal evolutia clinica a bolii
in fiecare pacient, mai degraba decat sa se compare activitatea
clinica intre diferiti subiecti.
Un punct important este
faptul ca probabilitatea de a experimenta o recadere a BC pare sa
fie semnificativ mai mare la pacientii care au nivele ridicate de CRP
decat la cei cu un nivel scazut . Cu toate acestea, mai multe studii au
demonstrat clar ca cel putin o treime din pacientii cu recadere
a bolii au nivel scazut sau normal de
PCR inainte de debutul unei noi acutizari. In plus,
exista, de asemenea, dovezi ca un procent deloc neglijabil de
pacienti cu BC inactiva au niveluri crescute de PCR . Prin urmare,
functia de predictie a CRP de a estima riscul de recidiva in randul
pacientilor cu BC inactiva ramane sa fie stabilita
si sunt necesare mai multe studii.
Un avantaj relevant in cazul
folosirii CRP ca un marker de activitate inflamatorie a BC este ca nivelurile sale sanguine nu sunt
direct afectate de utilizarea de anti-inflamatorii sau imuno-modulatoare. Mai
degraba, modificarile in sange ale CRP par sa
reflecte impactul tratamentului pe
parcursul bolii si activitatea inflamatorie. Acest lucru sugereaza
ca, atunci cand CRP scade dupa un ciclu de tratament cu antiinflamatoare,
aceasta reflecta un efect pozitiv al tratamentului asupra inflamatiei
intestinale, chiar si atunci cand nu a existat nici o
imbunatatire clara in parametrii clinici de activitate a
bolii.
In schimb, in cazul in care nivelurile de PCR
raman in mod constant ridicate in ciuda tratamentului, este rezonabil pentru
a concluziona ca inflamatia intestinala care sta la baza
nu este eficient scazuta prin tratament.
Calprotectina fecala
Avantajul markerilor fecali, cum ar fi
calprotectina este specificitatea mai mare pentru diagnosticul si
urmarirea tulburari intestinale, inclusiv BC-uri si CU. Mai multe tulburari intestinale se
caracterizeaza prin excretie fecala abundenta de leucocite.
Calprotectina reprezinta aproximativ 60% din proteinele din citosolul leucocitar.
Astfel, cantitatea de calprotectina fecala reflecta suma de leucocite
excrete in fecale dar si gravitatea si amploarea inflamatiei
intestinale. Cateva studii au demonstrat, intr-adevar o relatie
stransa intre calprotectina fecala si leucocitele marcate cu
indiu-111. In plus, calprotectina ramane in fecale timp de o
saptamana si nu mai mult de 5 grame de materii fecale sunt
necesare pentru a masura concentratiile in materiile fecale. Un dezavantaj important
este reprezentat de faptul ca nivelurile fecale de calprotectina pot
fi afectate in mod substantial prin utilizarea de medicamente anti-inflamatorii
si inhibitori ai pompei de protoni . In plus, nivelurile de calprotectina
se poate schimba, de asemenea, cu inaintarea in varsta, indiferent de prezenta
unei tulburari intestinale, cu dieta, si, de asemenea, cu activitatea
fizica.
Calprotectina fecala
nu pare sa fie standardul de aur pentru diagnostic si urmarire
al bolii Chron, deoarece multe alte tulburari intestinale, variind de la
cancer la infectii, ar putea duce la o crestere puternica in
excretia fecala de calprotectina . De exemplu, nu exista
diferente semnificative in nivelurile de calprotectina fecala
intre pacientii IBD si cei cu cancer colorectal. Cu toate acestea,
trebuie avut in vedere faptul ca concentratiile fecale de calprotectina
sunt normale la pacientii cu
tulburari functionale, cum ar fi sindromul de colon iritabil, prin
urmare, aceasta pozitie ar putea fi un instrument util in a
diferentia in mod eficient sindromul de colon iritabil fata de
cancerul colorectal .
Printre pacientii care prezinta manifestari clinice
compatibile cu BC sau CU, masurarea calprotectinei fecale a fost
estimata sa aiba o sensibilitate si o specificitate pentru
corecta diagnosticul de aproximativ 90% .Calprotectina fecala pare a fi
mai ridicata in randul pacientilor cu BC decat in randul celor cu CU,
cu sensibilitate si specificitate de 95%.
Unele studii au raportat un
nivel crescut de calprotectina fecala printre rudele de gradul intai
sanatoase ale pacientilor cu BC. Fapul ca ar putea
reprezenta
un marker pentru identificarea subiectilor sanatosi cu un risc mai mare de
a dezvolta BC sau CU este inca nedovedit si trebuie sa fie
explorat in alte studii.. Exista unele dovezi ca calprotectina fecala
este mai fiabila in a reflecta activitatea inflamatorie evaluata
histologic, mai degraba decat constatarile endoscopice. Acest lucru sugereaza
in mod indirect ca calprotectina fecala este un marker mai sensibil
decat endoscopia pentru a estima activitatea inflamatorie.
Un avantaj
promitatoar in folosirea calprotectinei fecale este potentialul
de a prezice riscul de recidiva. Concentratiile crescute de calprotectina
fecala sunt strans asociate cu un risc semnificativ de recidiva. S-a
estimat ca sensibilitatea si specificitatea calprotectinei fecale
pentru estimarea recidivei sunt in jur de 90% si 83%, respectiv.
De
asemenea, este demn de remarcat faptul ca valoarea predictiva a PCR
sau VSH-ului cu privire la recidiva bolii ramane sa fie bine
stabilita.
Lactoferina fecala
Lactoferina este o glicoproteina a neutrofilelor activate, care este mult mai
stabila in fecale decat alte proteine leucocitare.Concentratiile
acesteia sunt puternic crescute in
bolile inflamatorii intestinale dar de asemenea si la pacientii cu
enterita infectioasa si colita, fie virale sau
bacteriene
De aceea, diagnosticul
diferential intre BC sau CU si enterita infectioasa nu
poate fi stabilit pe baza nivelurilor de
lactoferina numai. Este neclar daca niveluri ridicate de lactoferina
fecala la pacientii cu boli intestinale inflamatorii cronice sunt
declansate de o precedenta infectie cu Clostridium difficile. La
pacientii cu nivelurile de lactoferina crescute, este obligatorie efectuarea
endoscopiei pentru a nu trece cu vederea un cancer sau boala inflamatorie
Printre pacientii care
prezinta caracteristici clinice concordante cu BC sau CU, lactoferina
fecala are o sensibilitate si specificitate pentru diagnostic de 82%
si 93%. Cu toate acestea, masurarea lactoferinei fecale pare sa
fie mai putin eficace decat masurarea calprotectinei pentru diagnosticul diferential intre boala
inflamatorie intestinala cronica si sindromul de colon iritabil.
Nici un studiu nu a
demonstrat cu siguranta ca concentratiile de
lactoferina reflecta indeaproape activitatea inflamatorie fie in BC
sau in CU, in principal din cauza suprapunerii mari in nivelurile de lactoferina
a celor cu boli inactive si cei cu boala activa.
Doar un singur studiu a
evaluat eficacitatea utilizarii lactoferinei fecale ca un marker pentru a
analiza raspunsul clinic la tratament in randul pacientilor cu
IBD.
Buderus si colegii au observat intr-adevar o relatie stransa intre scaderea lactoferinei la pacienti cu BC care au redusa activitatea inflamatorie datorita tratamentului cu infliximab. Chiar daca aceste rezultate sunt promitatoare, studiul are mai multe limitari, inclusiv numarul mic de pacienti si lipsa unui control corespunzator al grupului.
Autoanticorpii
Anticorpii antineutrofilici perinucleari citoplasmatici (pANCAs) pot fi
gasiti in 60-70% dintre pacienti CU si 5-10% dintre
pacientii BC. Antigenele corescunzatoare acestor autoanticorpi nu au
fost inca identificate, dar nu exista dovezi ca acestea sunt
diferite de cele asociate cu vasculita sistemica si ar putea sa
reprezinte anticorpi care reactioneaza cu o gama larga de
bacterii din intestin. Pozitivitatea p-ANCA este de obicei asociata cu
pancolita, chirurgia precoce, colangita sclerozanta primara
si la pacientii CU si BC.. In contrast, anticorpii anti-cerevisiase
(ASCAs) sunt detectati in aproximativ 70% dintre pacientii cu BC
si la 15% dintre pacienti CU. Pozitivitatea ASCA este asociata
cu un risc crescut de complicatii in BC precoce si pare sa
prezica riscul ca pacientii sa necesite o interventie
chirurgicala la nivelul intestinului subtire.
PROCEDURILE IMAGISTICE
Modalitatile
imagistice joaca un rol important in diagnosticarea si gestionarea
pacientiilor cu boala Crohn . Imagistica este folosita in scopuri de
diagnosticare, precum si in evaluarea de naturii, gravitatii si
complicatiilor extraintestinale ale bolii. Acesta ofera, de asemenea,
informatii cu privire la gradul de inflamatie si feedback-uldupa terapia clinica sau
chirurgicala. In acest scop, endoscopia, radiologia conventionala
si metodele imagistice transversale (ecografie, CT, MR si) sunt in principal
utilizate. Radiologia este deosebit de importanta in evaluarea intestinului subtire, avand in vedere
faptul ca endoscopia este aproape imposibila.
a. Radiologia conventionala
Atunci cand se ocupa cu BC,
clinicianul ar trebui sa nu mai priveasca radiologia
traditionala cu bariu ca strategie de screening de prima linie,
cu toate acestea aceasta procedura inca mai are un rol
complementar. Desi studiile de radiologie cu bariu au fost singurul mijloc
de pentru a investiga practic orice boala a intestinului pentru mai mult
de 50 de ani, utilizarea acestei metode in clinica a scazut progresiv
in ultimii 20 de ani.
Mai multe tehnici au fost
propuse pentru a imbunatati eficacitatea radiologiei cu bariu
per os. Acestea au avut ca scop accelerarea progresiei agentului de contrast
prin ansele intestinale, care rezulta in timp de examinare mai scurt
si o reducere a artefactelor. Distensia anselor intestinale este necesara pentru a vizualiza
corespunzator modificari in peretele intestinului. Acest lucru se
realizeaza de regula prin pozitionarea unui cateter la nivelul
unghiului lui Treitz (enterocliza).
Atunci cand este aplicata la BC aceasta tehinca prevede evaluarea exacta a intestinului, care este extrem de valoroasa in diagnosticul diferential, clasificarea si stadializarea de BC. In special, aceasta permite o estimare atenta a extinderii bolii, identificarea de leziuni discrete, caracterizarea stricturilor, si masurarea lungimii neafectate. In plus prevede descrierea exacta a leziunilor BC foarte timpurii, astfel incat hiperplazia si ulcerele aftoide pot fi identificate. Prin urmare, specificitatea este foarte mare, 96.9 - 98.3%, cu o precizie de diagnostic de ansamblu de 93-99.3% in serii diferite. In timpul progresiei bolii ulcerul aftoid se poate mari si fuzioneaza pentru a forma ulcere liniare. Mucoasa dintre ulcere este ingrosata din cauza inflamatiei, rezultand imaginea pietrelor de pavaj. Pe masura ce boala continua sa evolueze, de obicei apare ingrosarea concentrica a peretelui intestinal la nivelul ileonului distal. In acest stadiu, obstructia este mai frecventa din cauza unei componente spastice, mai degraba decat a unui proces fibros. Aspectul tipic de BC implica de asemenea extensii extra-luminale ale leziunilor cu formarea de fistule entero-enterice sau entero-colice.
b. Examinarea cu ultrasunete
Examinarea cu ultrasunete traditionala ofera un diagnostic precis la pacienti cu BC si reprezinta o procedura de screening pentru pacientii cu dureri abdominale si diaree. Acesta este putin invaziva si poate fi repetata in timpul fazei de urmarire pentru a evalua raspunsul la tratament si eventualele complicatii. De asemenea evidentiaza orice recurenta a bolii la pacientii tratati chirurgical si la pacientii cu contraindicatii relative sau absolute (copii, gravide, persoane cu handicap) la investigatiile radiologice sau endoscopice.
Sensibilitatea
examinarilor cu ultrasunete in studiul BC este 60-95%, cu o specificitate
de 80-100% . La pacientii suspectati a avea boala, se mareste
sensibilitatea la 74-92%. Sensibilitatea este de asemenea mare la
pacientii cu boala activa
si in detectarea de complicatii, din cauza naturii transmurale a
procesului inflamator . Cu toate acestea, ultrasunetele au o serie de
deficiente, nu ofera acces la colon si portiunile de jos ale
intestinului subtire, spre
deosebire de CT si RMN . In plus, mai multi factori impiedica o
examinare precisa, cum ar fi meteorismul, peristaltismul intestinal, si
obezitatea. Pentru a face un diagnostic precis cu ultrasunete, pacientul ar
trebui sa se abtina de la produse alimentare pentru cel
putin 4 ore pentru a reduce peristaltismul intestinal.
Examinarea se face
initial fara nici o substanta de contrast; cu toate acestea,
evaluarea cu exactitate a indicelui de activitate
a bolii, agentii de contrast pot fi ulterior
administrati, fie pe cale orala sau prin injectie
intravenoasa. Studiile recente au aratat ca
utilizarea de substante de contrast endoluminale creste sensibilitatea in
diagnosticul
bolilor intestinale care implica jejunul sau colonul. In cazul in care
agentii de contrast intravenos bazati pe microbule de fluorura
de sulf sunt folositi, este necesara obtinerea
consimtamantului si o anamneza pentru a determina orice alergie
la agentul de contrast sau o istorie de infarct miocardic recent sau boli
cardiace ischemice, ambele fiind contraindicatii.
Diagnosticul cu ultrasunete
se efectueaza pe baza mai multor parametri
referindu-se la grosimea parietala, caracteristicile anselor intestinale
si anomalii extraparietale, cum ar fi ingrosari mezenterice, limfoadenopatie
regionala sau localizata,
abcese,fistule si inflamatii ale zonelor adiacente, cum ar fi la
nivelul vezicii urinare si organelor genitale.
Criteriul cel mai frecvent utilizate in diagnosticul de BC este grosimea parietala si echostructura. Gradul de ingrosare a peretelui este influentat de mai multi factori cum ar fi edemul si infiltratia celulara, fibroza si distensia. La pacientii cu BC, o crestere in grosime a submucoasei este cauza principala de ingrosare parietala. Alti factori sunt aspectul neregulat din cauza ulcerelor mucoase, intreruperi ale mucoasei ca urmare a formarii de microabcese si fistule intramucosale.
Ecografia
Doppler color este utilizata pentru a evalua neovascularizatia.
Astfel, in cazul in care ingrosarea parietala este asociata cu
inflamatie activa, semnalele intraparietale ale fluxului pot fi
vizualizate.In prezenta unor complicatii, Doppler color poate distinge
masele mezenterice vascularizate cu semnale
interne de curgere, de abcese, care sunt
vazute ca colectii fluide cu vascularizatie periferica.
Dupa cum s-a
mentionat mai sus, agentii de contrast pot fi utili atat in
diagnosticul de BC dar si evaluarea a indicelui de activitate a bolii.
Agenti de contrast administrati pe cale orala permit distensia
anselor intestinale. Polietilen glicolul este oferit de obicei la o doza
de 200-600 ml (400 ml in medie) si permite vizualizarea obstructiilor
intestinale. Acest lucru duce la o observare mai precisa a zonei
afectate in comparatie cu ecografia traditionala. Aceasta
prevede, de asemenea, o mai buna evaluare a stenozei. A doua
generatie de agenti de contrast intravenos a facilitat studiile microcirculatiei
organelor parenchimatoase si a
neoangiogenezei tesuturilor tumorale.
c. Tomografia computerizata (CT)
Succesul CT in diagnosticul
de BC sau a complicatiilor sale se bazeaza pe o serie de proceduri,
cum ar fi o pregatire corespunzatoare a pacientului, utilizarea unor instrumente
multi-detector (MDCT) si administrarea de substante de contrast
intravenos sau orale. Pentru CT-ul facut pentru scopuri de screening,
pacientii trebuie sa se abtina de la alimente pentru cel
putin 6 h si laxativele sunt administrate pentru o curatare
intestinala buna. CT este, de asemenea, utilizat in urgente sau
in evaluarea de complicatii post-chirurgicale.
Pacientilor supusi screeningului
le sunt administrate un agent de contrast endoluminal fie pe cale orala
fie printr-un tub introdus prin nas cu varful pozitionat la nivelul
unghiului lui Treitz. Agentul de contrast poate fi pozitiv, de exemplu 1500 ml
de suspensie de bariu 2% sau o suspensie hidrosolubila de contrast iodat,
sau negativ, de exemplu, in cazul in care apa este utilizata, o solutie
PEG sau 5% metilceluloza diluata CT este de asemenea folosit
la pacientii cu BC cu localizare de colon si ofera o
alternativa la colonoscopie, care este adesea incompleta,
datorita complicatiilor stenotice. Pacientul urmeaza o dieta
saraca in fibre timp de 2-3 zile inainte si laxativele sunt
luate cu o zi inainte. In timpul examinarii, un cateter Foley se introduce
prin
rect si droguri sunt administrate pentru hipotonie.
Principalele criterii imagistice de
diagnosticare a BC sunt ingrosarea parietala si
pierderea stratificarii, edem si proliferarea fibro-adiposa a
grasimii mezenterice, ocluzia de vasa recta sau semnul pieptenelui,
infiltrarea submucoasei si adenopatie mezenterica. Mai multe studii
au aratat ca ingrosarea parietala de 2.5 - 10 mm este un
indiciu clar al bolii, iar valorile de peste 3 mm sunt considerate ca fiind deosebit
de semnificative in acest context. Prin urmare, CT este mai putin
utila in evaluarea bolii in faza initiala. Sensibilitatea CT
depinde de faza bolii, dar variaza intre 70% in faza initiala
si de 98% in boala transmurala.
Printre
cele mai frecvente complicatii ale BC care sunt diagnosticate CT sunt
fistulele, abcesele si stenozele intestinale. Traiectele fistulose (enteroenteric,
enterocolic, enterovezical sau vaginale si enterocutanate) pot fi fie hiperdense,
in prezenta agentilor de contrast, sau hipodense fara
utilizarea de substante de contrast negative. Abcesele sunt
usor identificate, inclusiv extinderea lor mezenterica si
retroperitoneala, si pot fi ulterior monitorizate pentru
raspunsul la tratament.
Datorita rezolutiei sale
spatiale, CT este deosebit de importanta in diagnosticul de activitate a
bolii si progresiei precum si in detectarea complicatiilor extraintestinale.
Aceasta modalitate se recomanda, pentru ca este rapida,
usor accesibila si mai putin
invaziva decat alte tehnici. Cu toate acestea, are cateva limitari,
cum ar fi sensibilitate redusa la leziuni superficiale, comparativ cu
clisma intestinului subtire, expunerea pacientului la o doza mare de
radiatii ionizante, reactii posibile la agentii iodati
si o rezolutie de contrast mai mica decat cele obtinute cu RMN.
d. Imagistica prin rezonanta magnetica (RMN)
Avantajul RMN-ului este faptul ca este o tehnica imagistica non-invaziva, care nu implica utilizarea de radiatii ionizante. Aceasta ofera imagini mai mult plane si, astfel, informatiile privind extensia parietala si extraparietala a inflamatiei in BC nu sunt complete. La inceputul anilor 1990, RMN-ul a devenit o tehnica din ce in ce mai comuna in clinica datorita progresului tehnologic. Aceste progrese au imbunatatit imaginile de contrast obtinute in timpul perioadelor scurte de apnee, adresandu-se astfel multor probleme in studiul abdomenului, in special cele privind circulatia si peristaltismul intestinal.
Curatarea
intestinala este necesara inainte de diferite proceduri de testare
si pentru a realiza o distensie completa si optima a
anselor intestinale. Agentul de contrast poate fi endoluminal sau intravenos. Mediile
de contrast utilizate sunt pozitive, negative, si bifazice. Mediile de
contrast pozitive (gadolinium chelat, citrat de amoniu feric, clorura de
mangan) cresc intensitatea semnalului in secventele T1 si T2. Mediile
de contrast negative, cum ar fi oxizii de fier au semnal slab in aceasta
frecventa. Mediile de contrast bifazice (solutii de apa PEG,
metil-celuloza, si manitol), care in prezent sunt favorizate, poat
actiona fie ca agenti pozitivi sau negativi, in functie de
secventa, generand astfel o intensitate mica a semnalului in
secventele T1-ponderate si un semnal de intensitate mare in secventele T2-ponderate.
Ca si in CT sau
examinarea radiologica conventionala, agentii de contrast
pot fi administrati in cantitati de 1000-2500 ml prin
intermediul unei pompe de perfuzie (cu o viteza de 100-250 ml / min), printr-un
tub nasojejunal sau pe cale orala. Administrarea orala a agentului de
contrast este cea mai comuna si este, fara indoiala, cea
mai bine tolerata de pacienti.
RMN-ul descrie, de asemenea, unele dintre modificarile superficiale de BC cum ar fi ulcere, ingrosarea plicilor si aplatizarea faldurilor circulare care marcheaza faza initiala a bolii.
Prin urmare, RMN-ul poate fi privita
ca o procedura optima pentru a diagnostica corect BC bazata pe caracteristicile tehnicii
multi-plan si multi-parametrice dar si un contrast si o rezolutie mai mare in
comparatie cu tomografia, si lipsa de radiatii ionizante.
Precizia RMN-ului este 85%.
Cu toate acestea, RMN-ul are cateva limitari, sensibilitatea la
modificarile initiale cauzate de boala este relativ scazuta
din cauza rezolutiei spatiale reduse. De asemenea,
RMN-ul este costisitor, consumator de timp si nu pote fi efectuat la
pacientii claustrofobici sau asupra persoanelor cu implanturi metalice.
DIAGNOSTICUL DIFERENTIAL
Diagnosticul diferential al bolilor inflamatorii intestinale nespecifice reprezinta o problema practica majora. Din punct de vedere terapeutic si prognostic se impune, pe de-o parte, diagnosticul diferential dintre bolile inflamatorii intestinale si alte afectiuni, iar pe de alta parte, cel dintre colita ulcerativa si boala Crohn.
Rareori, debutul bolii Crohn impune diagnosticul diferential cu apendicita acuta. Daca la interventia chirurgicala indicata pentru suspiciunea de apendicita acuta, intraoperator aspectul sugereaza boala Crohn, rezectia nu este recomandata decat in cazuri bine definite.
Ileita acuta cu Yersinia se diagnosticheaza prin examene coproparazitologice iar tratamentul antibiotic este curativ.
Cea mai frecventa problema de diagnostic diferential al bolilor infalamatorii intestinale idopatice la debut o reprezinta excluderea colitelor infectioase cu Shigella, Entamoeba hystolitica, Campylobacter, Giardia, Escherichia coli. Colita determinta de aceste microorganisme produce manifestari clinice si endoscopice similare cu colita ulcerativa. Coproculturile si testele serologice permit diagnosticul diferential.
Tuberculoza intestinala poate mima boala Crohn clinic si endoscopic.In prezenta tuberculozei pulmonare diagnosticul diferential nu ridica probleme. Examenul histologic este cel care poate stabili diagnosticul diferential intre cele doua afectiuni.
Transmiterea sexuala a germenilor patogeni intestinali prin practici homosexuale poate determina proctite asemanatoare colitei ulcerative. Neisseria gonorrhaea, Chlamydia, Herpes simplex si Treponema pallidum pot determina colite indistinctibile de colita ulcerativa si boala Crohn. Cresterea prevalentei infectiei HIV a largit spectrul germenilor patogeni intestinali cu microorganisme ca Isospora, Cryptosporidium, Mycobacterium avium, Citomegalovirus. Pacientii cu risc pentru aceste infectii necesita examene bacteriologice si parazitologice sistemice si rectosigmoidoscopie cu prelevare de biopsii.
Limfomul intestinal poate determina simptome semanatoare cu boala Crohn.
In cazul colitelor microscopice(colita colagenica si limfocitara), tabloul histologic este cel care permite diagnosticul diferential.
Colita ischemica trebuie considerata in diagnosticul diferential al bolilor inflamatorii intestianale idopatice la persoanele in vasta, cu afectiuni cardiovasculare associate.
Boala Behcet este individualizata prin ulceratii aftoide in regiunea ileocecala si infiltrate limfocitare, in asociere cu ulcere orale si genitale. Afectiunea se aseamana cu boala Crohn.
O alta conditie ce impune diagnosticul diferential cu boala Crohn la varstnici este diverticulita. Spre deosebire de boala Crohn, ea tinde sa aiba un caracter acut (durere abdominala, febra diaree, rectoragii) si sa afecteze segemente colonice limitate.
Colita pseudomembranoasa necesita pentru excludere examen endoscopic si evidentierea citotoxinei Cl. Difficile.
Colonul iritabil este dificil de diferentiat de formele blande de boala Crohn cu localizare intestinala, avand un curs clinic trenant.
2.6. COMPLICATII INTESTINALE SI EXTRANTESTINALE
COMPLICATII INTESTINALE
a. Abcese si fistule
Reprezinta efectul extinderii fistulelor prin peretele intestinal in tesuturile extraintestinale. Abcesele sunt intalnite in 15-20% din cazurile de boala Crohn. Antibioticele si rezectia segmentului intestinal inflamat reprezinta terapia adecvata, drenajul reprezinta numai o solutie temporara. Prevalenta fistulelor este de 20-30% majoritatea sunt entero-enterale si enterocutanate, un numar mic fiind entero-vezicale si enterovaginale.
b. Stenozele(tipul obstructiv)
Stenozele intestinale reprezinta o complicatie frecventa, indeosebi in localizarea la nivelul intestinului subtire. Frecvent acestea sunt stenoze fibroase, mai rar sunt cauzate de inflamatia activa transmurala sau de aderente abdominale.Evaluarea agresiva a stenozelor se impune datorita proportiei crescute de stenoze maligne.
c. Manifestarile perianale(tipul perianal)
Sunt complicatii commune si invalidante. Fistulele si hemoroizii reprezinta manifestari frecvente. Fistulele si abcesele perianale sau perirectale sunt evaluate prin anoscopie, rectoscopie si CT. Metronidazolul(20mg/kgc/zi) si drenajul abceselor sau traiectelor fistuloase reprezinta tratamentul optim.
d. Cancerul colorectal
Pacientii cu boli inflamatorii intestinale idiopatice prezinta un risc crescut de a dezvolta cancer colorectal comparativ cu populatia generala. Riscul este apreciabil in formele extinse, cu evolutie indelungata. Varsta la debut nu constituie un factor de risc independent, dar subiectii la care afectiunea este diagnosticata la varsta tanara prezinta un risc crescut de malignizare din cauza perioadei indelungate de evolutie. Malignizarea se produce la nivelul leziunilor displazice. Displazia poate fi severa sau blanda, prezenta in arii extinse sau limitate. Desi asocierea displaziei cu cancerul este bine documentata, posibilitatea de a utiliza acest marker histologic in supravegherea endoscopica a pacientilor cu risc crescut este limitata.
Desi riscul de a dezvolta cancer colorectal este de doua ori mai mic la pacientii cu boala Crohn decat cei cu colita ulcerativa, este de 20-40 de ori mai mare decat in populatia generala. Factorii asociati cu un risc crescut sunt evolutia indelungata(peste 10 ani), debutul la varsta tanara sub 30 de ani si prezenta stenozelor sau a segmentelor intestinale excluse din tranzit. O asociere bine documentata exista intre boala Crohn localizata la nivelul intestinului subtire si adenocarcinomul.
COMPLICATII EXTRAINTTESTINALE
Boala Crohn se asociaza cu variate manifestari extraintestinale.Ele pot fi clasificate in manifestari extraintestinale a caror activitate clinica este corelata cu activitatea inflamatorie intestinala si manifestari care evolueaza independent de inflamatia intestinala. Manifestarile extraintestinale se asociaza frecvent cu colita ulcerativa si colita Crohn, fiind rareori intalnite in boala Crohn cu localizare la nivelul intestinului subtire.
Artrita reprezinta manifestarea extraintestinala cel mai frecvent intalnita. In bolile inflamatorii intestinale idiopatice se descriu doua tipuri de artrita: artita asociata colitei din bolile inflamatorii si spondilita anchilozanta. Artrita asociata colitei inflamatorii nespecifice este o artrita migratorie care afecteaza cateva articulatii mari periferice: puseele artritice evolueaza concomitent cu puseele inflamatorii intestinale si raspund la terapia specifica acestora, indeosebi la corticoterapie. Sechelele clinice si radiologice sunt intalnite in mai putin de 25% din cazuri. Sacroileita si spondilita anchilozanta se intalnesc de 30 de ori mai frecvent la pacienti cu afectiuni inflamatorii intestinale idiopatice fata de populatia generala, se asociaza in 80% din cazuri cu HLA-B27 si evolueaza independent de inflamatia intestinala. Tratamentul afectiunii intestinale nu influenteaza afectiunea articulara. Terapia medicala sau mijloace fizice pot ameliora manifestarile clinice dar nu intervin in progresia afectiunii articulare. Complicatiile cutanate sunt reprezentate de eritemul nodos si pioderma gangrenosum. Eritemul nodos se asociaza frecvent colitei Crohn, activitatea sa este dependenta de inflamatia intestinala si raspunde tratamentului acesteia.
Pioderma gangrenosum se asociaza cu colite si ileocolite extinse, cu evolutie prelungita. Complicatia se asociaza unor pusee severe de activitatea inflamatorie, fiind controlata de obicei prin tratamentul specific al colitei si tratament local.
Complicatiile oculare sunt reprezentate de uveite si episclerite, corticoterapia locala este eficienta. Artrita, uveita si eritemul nodos se intalnesc frecvent impreuna, constituind triada cea mai comuna de manifestari extraintestinale in bolile inflamatorii intestinale idiopate.
Complicatiile hepatobiliare sunt reprezentate de steatoza hepatica, pericolangita,, hepatita cronica, ciroza hepatica, colangita scerozanta primitiva si colangiocarcinom. Pericolangita reprezinta cea mai frecventa complicatie hepatica in bolile inflamatorii intestinale. Pacientii sunt, de regula, asimptomatici, diagnosticul este histologic.
Colangita sclerozanta este intalnita la 1-4% dintre pacientii cu colita ulcerata si o proportie mai mica de pacinti cu boala Crohn. Prevalenta afectiunii la pacienti cu boli inflamatorii intestinale este atat de mare incat, in prezenta ei, efectuarea colonoscopiei se impune chiar la pacientii fara manifestari intestinale. In prezenta testelor biologice indicand colestaza, colangiografia endoscopica retrograda reprezinta metoda optima de diagnostic. Stricturile biliare si colangiocarcinomul reprezinta complicatiile majore reale colangitei sclerozanate.
In cadrul complicatiilor reno-urinare, litiaza renala este de cateva ori mai frecventa la pacientii cu boala Crohn ileala sau rezectii ileale decat in populatia generala. Afectarea extinsa sau rezectii ileale determina malabsorbtia lipidelor; acizii grasi malabsorbiti leaga calciul, iar oxalatul liber se absoarbe in cantitate crescuta. Amiloidoza renala este o complicatie severa asociata bolii Croh; nu raspunde la tratamentul afectiunii intestinale sau la rezectia segementului intestinal inflamat si conduce la insuficienta renala. Doua complicatii urinare se asociaza specific cu boala Crohn: extensia retroperitoneala a inflamatiei transmurale intestianle cu ureterohidronefroza ( frecvent in dreapta, de la ileocolita Crohn) si fistulele entero-urinare determinand infectii urinare trenante.
Manifestarile tromboembolice secundare activarii coagularii si trombocitozei se asociaza atat colitei ulcerative cat si bolii Crohn.
2.7.TRATAMENTUL BOLII CROHN
Simptomele si severitatea bolii Crohn variaza in randul pacientilor.
Patients with mild or no symptoms may not need treatment.Pacientii fara simptome sau cu simptome usoare nu au nevoie de tratament. Patients whose disease is in remission (where symptoms are absent) also may not need treatment.Pacientii a caror boala este in remisie (in cazul in care simptomele sunt absente) nu au , de asemenea, nevoie de tratament.
There is no medication that can cure Crohn's disease. Nu exista nici un medicament care sa vindece boala Crohn. Patients with Crohn's disease typically will experience periods of relapse (worsening of inflammation) followed by periods of remission (reduced inflammation) lasting months to years. During relapses, symptoms of abdominal pain, diarrhea, and rectal bleeding worsen. Pacientii cu boala Crohn de obicei, vor experimenta perioade de recadere (agravarea inflamatiei), urmate de perioade de remisiune (inflamatie redusa) de durata lunilor sau anilor. In timpul recaderilor, simptomele de dureri abdominale, diaree si sangerari rectale se vor agrava.
During remissions, these symptoms improve. Remissions usually occur because of treatment with medications or surgery, but occasionally they occur spontaneously without any treatment.In timpul remisiunii, aceste simptome se imbunatatesc. Remisii apar, de obicei din cauza tratamentului cu medicamente sau interventii chirurgicale, dar uneori ele apar spontan, fara nici un tratament.
Since there is no cure for Crohn's disease, the goals of treatment are to 1) induce remissions, 2) maintain remissions, 3) minimize side effects of treatment, and 4) improve the quality of life. Deoarece nu exista nici un leac pentru boala Crohn, obiectivele tratamentului sunt: 1) inducerea remisiei, 2) mentinerea remisiei, 3) minimizarea efectelor adverse ale tratamentului, si 4) imbunatatirea calitatii vietii. Treatment of Crohn's disease and ulcerative colitis with medications is similar though not always identical.Tratamentul bolii Crohn si a colitei ulcerate este la fel, desi nu intotdeauna identic.
Medications for treating Crohn's disease include 1) antiinflammatory agents such as 5-ASA compounds, corticosteroids, topical antibiotics, 2) immuno-modulators, 3) other medications. Medicamente pentru tratarea bolii Crohn includ 1) antiinflamatoare, cum ar fi 5-ASA,corticosteroizi, antibiotice topice, 2) imuno-modulatoare 3) alte medicamente.
Antiinflammatory medicationsmMED MEDICAMENTELE ANTIINFLAMATOARE
Antiinflammatory medications that decrease intestinal inflammation are analogous to arthritis medications that decrease joint inflammation. Different types of antiinflammatory medications used in the treatment of Crohn's disease are: Medicamentele antiinflamatorii folosite in inflamatia intestinala sunt similare cu medicamentele folosite in artrita. Diferitele tipuri de medicamente antiinflamatorii utilizate in tratamentul bolii Crohn sunt:
5-ASA compounds such as sulfasalazine (Azulfidine) and mesalamine (Pentasa, Asacol, Dipentum, Colazal, Rowasa enema, Canasa suppository) that act via direct contact (topically) with the inflamed tissue in order to be effective. 1. Compusi de 5-ASA (acid 5 amino acetil salicilic), cum ar fi sulfasalazina (Salazopirina) si mesalamina (Pentasa, Salofalk, Asacol, Dipentum, Colazal, Rowasa clisma, Canasa supozitor), care actioneaza prin contactul direct (local) cu tesutul inflamat, pentru a fi eficiente.
Corticosteroids that act systemically (without the need for direct contact with the inflamed tissue) to decrease inflammation throughout the body. 2. Corticosteroizii pe cale sistemica reduc inflamatia in tot corpul. Systemic corticosteroids have important and predictable side effects if used long-term. Corticosteroizii sistemici prezinta insa efecte secundare daca sunt utilizati timp indelungat.
A new class of topical corticosteroid (for example, budesonide ) that acts via direct contact (topically) with the inflamed tissue. Se folosesc si corticosteroizi topici (de exemplu, budesonid), care actioneaza prin contact direct (local) cu tesutul inflamat. This class of corticosteroids has fewer side effects than systemic corticosteroids which are absorbed into the body. Aceasta clasa de corticosteroizi are efecte secundare mai putine decat corticosteroizi sistemici.
3.Antibiotics such as metronidazole (Flagyl) and ciprofloxacin (Cipro) that decrease inflammation by an unknown mechanism Antibioticele, cum ar fi metronidazolul si ciprofloxacina care reduc inflamatia printr-un mecanism necunoscut
5-ASA (mesalamine) oral medications A. COMPUSII 5-ASA CU ADMINISTRARE ORALA
Acidul 5-aminosalicilic (5-ASA), de asemenea, numit mesalamina este similar cu chimic cu aspirina. Aspirin has been used for many years for treating arthritis, bursitis , and tendonitis (conditions of tissue inflammation). Aspirin, however, is not effective in treating Crohn's disease and ulcerative colitis, and even may worsen the inflammation. Aspirina a fost utilizata de multi ani pentru tratarea artritei, bursitei , si tendinitei. Aspirina, totusi, nu este eficace in tratarea bolii Crohn si colitei ulcerative, si chiar poate agrava inflamatia. On the other hand, 5-ASA can be effective in treating Crohn's disease and ulcerative colitis if the drug can be delivered topically onto the inflamed intestinal lining. Pe de alta parte, acidul 5-ASA poate fi eficient in tratamentul bolii Crohn si colitei ulcerative daca medicamentul este administrat topic. For example, mesalamine (Rowasa) is an enema containing 5-ASA that is effective in treating inflammation in the rectum. De exemplu, mesalamina este o clisma care contin acid 5-ASA eficace in tratarea inflamatiei in rect. However, the enema solution cannot reach high enough to treat inflammation in the upper colon and the small intestine. Cu toate acestea, solutia nu poate trata inflamatia la nivelul colonului superior si intestinului subtire. Therefore, for most patients with Crohn's disease involving both the ileum (distal small intestine) and colon, 5-ASA must be taken orally. Prin urmare, pentru majoritatea pacientilor cu boala Crohn, cu afectare ileala si colonica, acidul 5-ASA trebuie administrat pe cale orala.
If pure 5-ASA is taken orally, however, most of the 5-ASA would be absorbed in the stomach and the upper small intestine, and very little 5-ASA would reach the ileum and colon.Desi administrat oral, acidul 5-ASA ar fi absorbit in stomac si intestinul subtire superior, si foarte putin ar ajunge in ileon si colon. To be effective as an oral agent in treating Crohn's disease, 5-ASA has to be modified chemically to escape absorption by the stomach and the upper intestines. Pentru a fi eficient ca agent oral in tratarea bolii Crohn,acidul 5-ASA trebuie sa fie modificat chimic pentru a scapa de absorbtia si degradarea de la nivelul stomacului si intestinului superior.
SULFASALAZINA
Sulfasalazine (Azulfidine)
Sulfasalazine (Azulfidine) was the first modified 5-ASA compound used in the treatment of Crohn's colitis and ulcerative colitis.Sulfasalazina a fost primul compus 5-ASA modificat folosit in tratamentul colitei si bolii Crohn . It has been used successfully for many years to induce remissions among patients with mild to moderate ulcerative colitis. Sulfasalazine also has been used for prolonged periods for maintaining remissions.Acesta a fost folosita cu succes de mai multi ani pentru a induce remisii printre pacientii cu colita ulcerativa usoara sau medie. Sulfasalazina a fost folosita de asemenea pentru mentinerea remisiei pe perioade prelungite.
Sulfasalazine consists of a 5-ASA molecule linked chemically to a sulfapyridine molecule. Sulfasalazina este o molecula de acid 5-ASA legata chimic de o molecula sulfapiridina. (Sulfapyridine is a sulfa antibiotic.) Connecting the two molecules together prevents absorption by the stomach and the upper intestines.Conectarea celor doua impiedica absorbtia la nivelul stomacului si intestinului superior. When sulfasalazine reaches the ileum and the colon, the bacteria that normally are present break the link between the two molecules. Cand sulfasalazina ajunge la ileon si colon, bacteriile care in mod normal sunt prezente rup legatura dintre cele doua molecule. After breaking away from 5-ASA, sulfapyridine is absorbed into the body and later eliminated in the urine. Dupa desprinderea de acidul 5-ASA, sulfapiridina este absorbita in organism, iar mai tarziu eliminata in urina. Most of the active 5-ASA, however, is available within the terminal ileum and colon to treat the colitis. Majoritatea acidului 5-ASA este disponibil in ileonul terminal si in colon pentru a trata colita.
Most of the side effects of sulfasalazine are due to the sulfapyridine molecule. Cele mai multe dintre efectele secundare ale sulfasalazinei sunt datorate moleculei de sulfapiridina. These side effects include nausea, heartburn, headache , anemia, skin rashes, and, in rare instances, hepatitis and kidney inflammation. Aceste efecte secundare includ greata, arsuri epigastrice, dureri de cap, anemie, eruptii cutanate si, in cazuri rare, hepatita si nefrita. In men, sulfasalazine can reduce the sperm count.La barbati, sulfasalazina poate reduce cantitatea de spermatozoizi. The reduction in sperm count is reversible, and the count usually becomes normal after the sulfasalazine is discontinued or changed to a different 5- ASA compound. Reducerea numarului de spermatozoizi este reversibila, iar numarul de obicei, devine la normal dupa ce sulfasalazina este intrerupta sau este schimbata cu un alt compus 5-ASA.
Because the newer 5-ASA compounds [for example, mesalamine (Asacol and Pentasa)] do not have the sulfapyridine component and have fewer side effects than sulfasalazine, they are being used more frequently in treating Crohn's disease and ulcerative colitis. Deoarece noii compusi de acid 5-ASA nu au componenta sulfapiridina si au efecte secundare mai putine decat sulfasalazina, acestia sunt folositi mai frecvent in tratamentul bolii Crohn si colitei ulcerative.
ASA ASACOL
Asacol is a tablet consisting of the 5-ASA compound surrounded by an acrylic resin coating.Asacol este un comprimat constand dintr-un compus de acid 5 -ASa inconjurat de un strat de rasina acrilica. Asacol is sulfa-free. Asacol nu contine molecule sulfa. The resin coating prevents the 5-ASA from being absorbed as it passes through the stomach and the small intestine. Stratul de rasina previne ca acidul 5-AAS sa fie absorbit, deoarece trece prin stomac si intestinul subtire. When the tablet reaches the terminal ileum and the colon, the resin coating dissolves, and the active 5-ASA drug is released. Cand comprimatul ajunge la nivelul ileonului terminal si colonului, rasina de acoperire se dizolva, si acidul 5-AAS este eliberat.
Asacol is effective in inducing remissions in patients with mild to moderate ulcerative colitis. It also is effective when used in the longer term to maintain remissions. Some studies have shown that Asacol also is effective in treating Crohn's ileitis and ileo-colitis, as well as in maintaining remission in patients with Crohn's disease. Asacol este eficace in inducerea remisiei la pacientii cu colita ulcerativa usoara pana la moderata. De asemenea, este eficient atunci cand este utilizat pe termen mai indelungat pentru a mentine remisia.
The recommended dose of Asacol for inducing remissions is two 400 mg tablets three times daily (a total of 2.4 grams a day).
Doza recomandata de Asacol pentru inducerea remisiei este de doua comprimate de 400 mg de trei ori pe zi (un total de 2,4 grame pe zi). At least two tablets of Asacol twice daily (1.6 grams a day) is recommended for maintaining remission.Cel putin doua comprimate de Asacol de doua ori pe zi (1,6 grame pe zi) sunt recomandate pentru mentinerea remisiei. Occasionally, the maintenance dose is higher. Ocazional, doza de intretinere este mai mare.
As with Azulfidine, the benefits of Asacol are dose-related. Ca si in cazul Salazopirinei, beneficiile Asacol sunt legate de doza. If patients do not respond to 2.4 grams a day of Asacol, the dose frequently is increased to 3.6 - 4.8 grams a day to induce remission. Daca pacientii nu raspund la 2,4 grame pe zi de Asacol, doza este crescuta la 3.6 la 4.8 grame pe zi pentru a induce remisie. If patients fail to respond to the higher doses of Asacol, then other alternatives such as corticosteroids are considered.Daca pacientii nu raspund la doze mai mari de Asacol, atunci alte alternative, cum sunt corticosteroizii, sunt luate in considerare.
PentasaP PENTASA
Pentasa is a capsule consisting of small spheres containing 5-ASA.Pentasa este o capsula formata din sfere mici care contin acid 5-ASA. Pentasa is sulfa-free. Pentasa nu contine molecule sulfa. As the capsule travels down the intestines, the 5-ASA inside the spheres is released slowly into the intestine. Unlike Asacol, the active drug 5-ASA in Pentasa is released into the small intestine as well as the colon. Capsula ajunge in intestine si acidul 5-ASA din sfere este eliberat lent. Pentasa spre deosebire de Asacol este eliberat in intestinul subtire, precum si in colon. Therefore, Pentasa can be effective in treating inflammation in the small intestine and is currently the most commonly used 5-ASA compound for treating mild to moderate Crohn's disease in the small intestine. Prin urmare, Pentasa poate fi eficient in tratarea inflamatiei la nivelul intestinului subtire.
Patients with Crohn's disease occasionally undergo surgery to relieve small intestinal obstruction, drain abscesses, or remove fistulae. Pentasa ajuta la mentinerea remisiei si reduce sansele de reaparitie a bolii Crohn dupa interventia chirurgicala.
In the treatment of Crohn's ileitis or ileocolitis, the dose of Pentasa usually is four 250 mg capsules four times daily (a total of 4 grams a day). In tratamentul ileitei Crohn sau ileocolitei, doza de Pentasa, de obicei, este de patru capsule de 250 mg de patru ori pe zi (un total de 4 grame pe zi). For maintenance of remission in patients after surgery, the dose of Pentasa is between 3-4 grams daily. Pentru intretinerea remisiei in cazul pacientilor dupa o interventie chirurgicala, doza de Pentasa este intre 3-4 grame pe zi.
OLSALAZINA
Olsalazine (Dipentum)OOO
Olsalazine (Dipentum) is a capsule in which two molecules of 5-ASA are joined together by a chemical bond. In this form, the 5-ASA cannot be absorbed from the stomach and intestine. Intestinal bacteria are able to break apart the two molecules releasing the active individual 5-ASA molecules into the intestine. Olsalazine este o capsula in care doua molecule de acid 5-AAS sunt unite prin legaturi chimice. In acesta formula acidul 5- ASA nu poate fi absorbit de stomac si bacteriile intestinale sunt capabile sa rupa cele doua molecule si sa elibereze moleculele individuale active in intestin. Since intestinal bacteria are more abundant in the ileum and colon, most of the active 5-ASA is released in these areas.Olsalazina este cea mai eficienta pentru boala limitata la ileon sau colon. Although clinical studies have shown that olsalazine is effective for maintenance of remission in ulcerative colitis, up to 11% of patients experience diarrhea when taking olsalazine. Desi studiile clinice au aratat ca olsalazina este eficace pentru mentinerea remisiei in colita ulcerativa, pana la 11% din pacienti prezinta diaree atunci cand iau olsalazina. Because of this, olsalazine is not often used. Din acest motiv, olsalazina de multe ori nu este folosita. The recommended dose of olsalazine is 500 mg twice a day. Doza recomandata de olsalazina este de 500 mg de doua ori pe zi.
BALSALAZIDA
Balsalazide (Colazal)
Balsalazide (Colazal) is a capsule in which the 5-ASA is linked by a chemical bond to another molecule that is inert (without effect on the intestine) and prevents the 5-ASA from being absoBalsalazida este o capsula, in care acidul 5-ASA este legat printr-o legatura chimica la alta molecula care este inerta (fara efect asupra intestinului) si previne ca acidul 5-ASA sa fie absorbit. This drug is able to travel through the intestine unchanged until it reaches the end of the small bowel (terminal ileum) and colon. Acest medicament este capabil sa treaca prin intestin neschimbat pana cand ajunge la sfarsitul intestinului subtire (ileonul terminal) si la colon. There, intestinal bacteria break apart the 5-ASA and the inert molecule releasing the 5-ASA. Acolo, bacteriile intestinale rup acidul 5-ASA de molecula inerta si il elibereaza. Because intestinal bacteria are most abundant in the terminal ileum and colon, balsalazide is used to treat inflammatory bowel disease predominantly localized to the colon.Deoarece bacteriile intestinale sunt cele mai abundente in ileonul terminal si colon, balsalazida este utilizata pentru a trata bolile inflamatorii ale intestinului terminal si colonului.
EFECTELE SECUNDARE ALE COMPUSILOR 5-ASA
Side effects of oral 5-ASA compounds
The 5-ASA compounds have fewer side effects than Azulfidine and also do not reduce sperm counts. They are safe medications for long-term use and are well-tolerated. Compusii cu acid 5-ASA au mai putine efecte secundare decat mesalamina si nu reduc numarul de spermatozoizi. Acestea sunt medicamente sigure pe termen lung si sunt bine tolerate.
Patients allergic to aspirin should avoid 5-ASA compounds because they are similar chemically to aspirin. Pacientii cu alergie la aspirina ar trebui sa evite compusii cu acid 5-ASA, deoarece acestea sunt similare chimic cu aspirina.
Rare kidney and lung inflammation has been reported with the use of 5-ASA compounds. Rare inflamatii ale rinichilor si pulmonare au fost raportate la utilizarea acestora. Therefore, 5-ASA should be used with caution in patients with kidney disease. Prin urmare,acidul 5-ASA ar trebui sa fie utilizat cu precautie la pacientii cu boala de rinichi. It also is recommended that blood tests of kidney function be done before starting and periodically during treatment. De asemenea, este recomandat ca testele functiei renale sa fie facute inainte de a incepe si periodic in timpul tratamentului.
Rare instances of worsening of diarrhea, cramps, and abdominal pain, at times accompanied by fever, rash , and malaise, may occur. Cazuri rare de agravare a diareei, crampe, dureri abdominale si, uneori insotite de febra, eruptii cutanate, si stare de rau, pot sa apara. This reaction is believed to represent an allergy to the 5-ASA compound. Aceasta reactie este considerata o alergie la compusii cu acid 5-ASA.
Rowasa is 5-ASA in enema form.Rowasa este acidul 5-ASA in forma de clisma. Acidul5-ASA by enema is most useful for treating ulcerative colitis involving only the distal colon since the enema easily can reach the inflamed tissues of the distal colon. 5-ASA sub forma de clisma este cel mai util pentru tratarea colitei ulcerative care implica numai colonul distal, deoarece clisma poate ajunge cu usurinta in tesuturile inflamate de la acest nivel. Rowasa also is used in treating Crohn's disease in which there is inflammation in and near the rectum. Rowasa, de asemenea, este utilizata in tratarea bolii Crohn in care exista inflamatii si in apropierea rectului. Each Rowasa enema contains 4 grams of 5-ASA.Fiecare clisma Rowasa contine 4 grame de acid 5-ASA. The enema usually is administered at bedtime, and patients are encouraged to retain the enema through the night. Clisma de obicei este administrata la culcare, iar pacientii sunt incurajati sa retina clisma peste noapte. The enema contains sulfite and should not be used by patients with sulfite allergy.Clisma contine sulfiti si nu ar trebui sa fie utilizata de catre pacientii cu alergie la sulfiti. Otherwise, Rowasa enemas are safe and well-tolerated.In caz contrar, clismele Rowasa sunt sigure si bine tolerate.
CCC B. CORTICOSTEROIZII
Corticosteroids
Corticosteroids (for example, prednisone prednisolone , hydrocortisone, etc.) have been used for many years to treat patients with moderate to severe Crohn's disease and ulcerative colitis and to treat patients who fail to respond to 5-ASA. Unlike 5-ASA, corticosteroids do not require direct contact with the inflamed intestinal tissues to be effCorticosteroizi (de exemplu, prednison prednisolon , hidrocortizon, etc) au fost utilizati de multi ani pentru tratamentul pacientilor cu boala Crohn si colita ulcerativa moderata pana la severa si pentru a trata pacientii care nu raspund la acid 5-ASA. Spre deosebire de acidul 5-ASA, corticosteroizii nu necesita contact direct cu tesuturile inflamate pentru a fi eficiente.
Oral corticosteroids are potent antiinflammatory medications. Corticosteroizii pe cale orala sunt medicamente antiinflamatoare puternice. After absorption, corticosteroids exert prompt antiinflammatory actions throughout the body, including the intestines. Dupa absorbtie, corticosteroizi exercita actiuni antiinflamatoare prompte. Consequently, they are used in treating Crohn's disease anywhere in the small intestine, as well as ulcerative and Crohn's colitis. In critically ill patients, intravenous corticosteroids (such as hydrocortisone) can be given in the hospital.In consecinta, ele sunt folosite in tratarea bolii Crohn oriunde in intestinul subtire. For patients with proctitis, hydrocortisone enemas ( Cortenema ) can be used to deliver the corticosteroid directly to the inflamed tissue.Pentru pacientii cu proctita, clisme cu hidrocortizon pot fi folosite pentru a furniza corticosteroizi direct in tesutul inflamat. By using the corticosteroid topically, less of it is absorbed into the body and the frequency and severity of side effects are lessened (but not eliminated) as compared with systemic corticosteroids. Prin utilizarea de corticosteroizi topic, mai putina substanta activa este absorbita in organism si frecventa si gravitatea efectelor secundare este diminuata comparativ cu corticosteroizi sistemici.
Corticosteroids are faster-acting than 5-ASA, and patients frequently experience improvement in their symptoms within days of beginning them. Corticosteroizii nu par a fi utili in mentinerea remisiei in boala Crohn si colitei ulcerative sau in prevenirea recidivei bolii Crohn dupa interventia chirurgicala.
REACTII ADVERSE ALE CORTICOSTEROIZILOR
Side effects of corticosteroids
The frequency and severity of side effects of corticosteroids depend on the dose and duration of their use.Frecventa si severitatea efectelor secundare ale corticosteroizilor depind de doza si durata de utilizare a acestora. Short courses of corticosteroids, for example, usually are well-tolerated with few and mild side effects.Cursuri scurte de corticosteroizi sunt bine tolerate cu cateva efecte secundare usoare. Long-term use of high doses of corticosteroids usually produces predictable and potentially serious side effects. Utilizarea pe termen lung a unor doze mari de corticosteroizi, de obicei, produce efecte secundare grave. Common side effects include: Reactii adverse frecvente includ:rounding of the face (moon face),rotunjirea fetei (fata luna plina), acne acnee, hirsutism, diabet zaharat, hipertensiune arteriala, cataracta, glaucom, cresterea sensibilitatii la infectii, slabiciune musculara, depresie, insomnie, modificari de personalitate, iritabilitate, osteoporoza cu fracturi ale coloanei vertebrale.Children receiving corticosteroids experience stunted growth.
The most serious complication from long term corticosteroid use is aseptic necrosis of the hip joints. Aseptic necrosis is a condition in which there is death and degeneration of the hip bone. O grava complicatie a utilizarii de corticosteroizi pe termen lung este necroza aseptica a articulatiilor soldului.
Prolonged use of corticosteroids can depress the ability of the body's adrenal glands to produce cortisol (a natural corticosteroid necessary for proper functioning of the body). Therefore, abruptly discontinuing corticosteroids can cause symptoms due to a lack of natural cortisol (a condition called adrenal insufficiency). Symptoms of adrenal insufficiency include nausea, vomiting, and even shock. Utilizarea prelungita de corticosteroizi poate deprima capacitatea glandelor suprarenale de a produce cortizol. Prin urmare, intreruperea brusca a corticosteroizilor poate cauza simptome ca urmare a lipsei de cortizol natural. Simptomele de insuficienta suprarenala includ greata, varsaturi, si chiar soc. Withdrawing corticosteroids too quickly also can produce symptoms of joint pain , fever, and malaise. Therefore, when corticosteroids are discontinued, the dose usually is tapered gradually rather than stopped abruptly.Retragerea corticosteroizilor prea repede poate produce simptome de dureri articulare, febra, stare generala de rau . Prin urmare intreruperea corticosteroizilor trebuie facuta treptat.Even after corticosteroids are discontinued, the adrenal glands' ability to produce cortisol can remain depressed from months up to two years.Proper use of corticosteroids
Once the decision is made to use systemic corticosteroids, treatment usually is initiated with prednisone , 40-60 mg daily.Odata ce este luata decizia de a utiliza corticosteroizi sistemici, tratamentul este de obicei initiat cu prednison 40-60 mg pe zi. The majority of patients with Crohn's disease respond with an improvement in symptoms within a few weeks. Majoritatea pacientilor cu boala Crohn raspund cu o ameliorare a simptomelor in cateva saptamani. Once symptoms have improved, prednisone is reduced by 5-10 mg per week until a dose of 20 mg per day is reached. Dupa ce simptomele s-au imbunatatit, prednisonul este redus cu 5-10 mg pe saptamana pana la o doza de 20 mg pe zi. The dose then is reduced at a slower rate until the corticosteroid is discontinued.Apoi doza este redusa la un ritm mai lent, pana ce corticosteroizii sunt intrerupti. Gradually reducing corticosteroids not only minimizes the symptoms of adrenal insufficiency, it also reduces the chances of an abrupt recurrence of inflammation.
Many doctors use 5-ASA compounds and corticosteroids together.Multi medici utilizeaza compusi de acid 5-AAS si corticosteroizi impreuna. In patients who achieve remission with corticosteroids, 5-ASA compounds often are continued alone to maintain remissionIIIIIn cazul pacientilor care ating remisiuneae cu corticosteroizi, compusiicu acid 5-AAS sunt adesea continuati numai pentru a mentine remisie.
Din pacate, multi pacienti care au nevoie de corticosteroizi pentru a induce remisiuni au devenit dependenti de corticosteroizi. These patients consistently develop symptoms whenever the corticosteroid dose falls below a certain level. Acesti pacienti dezvolta in mod constant simptome ori de cate ori doza de corticosteroizi scade sub un anumit nivel. In such patients who are corticosteroid dependent as well as in patients who are unresponsive to corticosteroids and other antiinflammatory medications, immuno-modulator medications or surgery must be considered. The management of patients who are corticosteroid dependent or patients with severe disease that responds poorly to medications is complex. Doctors who are experienced in treating ulcerative colitis and Crohn's disease and in using immuno-modulators should evaluate these patients. La astfel de pacienti care sunt dependenti de corticosteroizi, precum si la pacientii care nu raspund la corticosteroizi si alte medicamente antiinflamatoare, medicamentele imunomodulatoare sau interventii chirurgicale trebuie luate in considerare.
Regular weight-bearing exercise and stopping smoking (cigarettes). Budesonide (Entocort EC) is a new type of corticosteroid for treating Crohn's disease.Budesonide este un nou tip de corticosteroizi pentru a trata boala Crohn. Like other corticosteroids, budesonide is a potent antiinflammatory medication. Ca si in cazul altor corticosteroizi, budesonide este un medicament antiinflamator puternic. Unlike other corticosteroids, however, budesonide acts only via direct contact with the inflamed tissues (topically) and not systemically. Spre deosebire de alti corticosteroizi actioneaza numai prin contactul direct cu tesuturile inflamate si nu sistemic. As soon as budesonide is absorbed into the body, the liver converts it into inactive chemicals. De indata ce budesonide este absorbit in organism, in ficat se transforma in substante chimice inactive. Therefore, for effective treatment of Crohn's disease, budesonide, like topical 5-ASA, must be brought into direct contact with the inflamed intestinal tissue. Prin urmare, pentru un tratament efficient al bolii Crohn trebuie administrat local.
Budesonide capsules contain granules that allow a slow release of the drug into the ileum and the colon. Budesonide capsule contine granule, care permit o eliberare lenta a medicamentului in ileon si colon. In a double-blind multicenter study (published in 1998), 182 patients with Crohn's ileitis and/or Crohn's disease of the right colon were treated with either budesonide (9 mg daily) or Pentasa (2 grams twice daily). Intr-un studiu multicentric dublu-orb (publicat in 1998), 182 pacienti cu ileita Crohn si / sau boala Crohn de colon drept au fost tratati fie cu budesonide (9 mg pe zi) sau Pentasa (2 grame de doua ori pe zi). Budesonide was more effective than Pentasa in inducing remissions while the side effects were similar to Pentasa. Budesonide a fost mai eficace decat Pentasa in inducerea remisiei in timp ce efectele adverse au fost similare cu Pentasa. In another study comparing the effectiveness of budesonide with corticosteroids, budesonide was not better than corticosteroids in treating Crohn's disease but had fewer side effects.Intr-un alt studiu care a comparat eficacitatea budesonidului cu corticosteroizi, budesonidul nu a fost mai bun decat corticosteroizi in tratarea bolii Crohn dar a avut mai putine efecte secundare.
Because budesonide is broken down by the liver into inactive chemicals, it has fewer side effects than systemic corticosteroids. Deoarece budesonidul este metabolizat de catre ficat in substante chimice inactive, are efecte secundare mai putine decat corticosteroizii sistemici. It also suppresses the adrenal glands less than systemic corticosteroids. De asemenea, suprima glandele suprarenale mai putin. Budesonide will be available as an enema for the treatment of proctitis. Budesonide este disponibil ca o clisma pentru tratamentul proctitei.
Budesonide has not been shown to be effective in maintaining remission in patients with Crohn's disease. Budesonide nu a fost dovedit a fi eficace in mentinerea remisiunii la pacientii cu boala Crohn. If used long-term, budesonide also may cause some of the same side effects as corticosteroids.Daca este folosit pe termen lung, pote provoca efectele secundare identice cu cele ale corticosteroizilor. Because of this, the use of budesonide should be limited to short-term treatment for inducing remission. Din acest motiv, utilizarea budesonidului ar trebui limitata la tratamentul de scurta durata pentru inducerea remisiunii.
Most budesonide is released in the terminal ileum, it will have its best results in Crohn's disease limited to the terminal ileum.
It is not known whether budesonide is effective in treating patients with ulcerative colitis, and it is currently not recommended for the treatment of ulcerative colitis.
ANTIBIOTICE PENTRU BOALA CHRON
Antibiotics for Crohn's disease
Antibiotics such as metronidazole (Flagyl) and ciprofloxacin (Cipro) have been used for treating Crohn's colitis. Antibioticele, cum ar fi metronidazolul si ciprofloxacina au fost utilizate pentru tratarea colitei Crohn. Flagyl also has been useful in treating anal fistulae in patients with Crohn's disease.Metronidazolul a fost util in tratarea fistulelor anale la pacientii cu boala Crohn. The mechanism of action of these antibiotics in Crohn's disease is not well understood. Mecanismul de actiune al acestor antibiotice in boala Crohn nu este bine inteles.
METRONIDAZOL
Metronidazole (Flagyl)
Metronidazole (Flagyl) is an antibiotic that is used for treating several infections caused by parasites (for example, giardia) and bacteria (for example, infections caused by anaerobic bacteria, and vaginal infections). It is effective in treating Crohn's colitis and is particularly useful in treating patients withMetronidazolul este un antibiotic utilizat pentru tratarea infectiilor cauzate de paraziti ( Giardia) si bacterii (de exemplu, infectii cauzate de bacterii anaerobe, si infectii vaginale). Este eficient in tratarea colitei Crohn si este deosebit de util in tratarea pacientilor cu fistule anale. Chronic use of metronidazole in doses higher than 1 gram daily can be associated with permanent nerve damage ( peripheral neuropathy Utilizarea cronica de metronidazol in doze mai mari de 1 gram pe zi, poate fi asociata cu leziuni nervoase permanente ( neuropatie periferica The early symptoms of peripheral neuropathy are numbness and tingling in the fingertips, toes, and other parts of the extremities. Simptome precoce de neuropatie periferica sunt amorteala si furnicaturi in varful degetelor si alte parti ale extremitatilor. Metronidazole should be stopped promptly if these symptoms appear. Metronidazolul trebuie oprit imediat daca apar aceste simptome. Metronidazole and alcohol together can cause severe nausea, vomiting, cramps, flushing, and headache. Metronidazolul si alcoolul impreuna poat provoca greata severa, varsaturi, crampe, inrosirea fetei si dureri de cap. Patients taking metronidazole should avoid alcohol. Pacientii care au luat metronidazol trebuie sa evite alcoolul. Other side effects of metronidazole include nausea, headaches, loss of appetite , a metallic taste, and, rarely, a rash. Alte efecte adverse ale metronidazolului includ greata, dureri de cap, pierderea poftei de mancare, un gust metalic, si, rareori, o eruptie cutanata.
CIPROFLOXACINA
Ciprofloxacin (Cipro)
Ciprofloxacin (Cipro) is another antibiotic used in the treatment of Crohn's disease. Ciprofloxacina este un alt antibiotic folosit in tratamentul de bolii Crohn. It can be used in combination with metronidazole. Acesta poate fi folosita in combinatie cu metronidazolul.
Summary of antiinflammatory medications MEDICAMENTELE IMUNO-MODULATOARE
Immuno-modulator medications
Immuno-modulators are medications that affect the body's immune system. Imuno-modulatoarele sunt medicamente care afecteaza sistemul imunitar al organismului. The immune system is composed of immune cells and the proteins that they produce.La pacientii cu boala Crohn si colita ulcerata, sistemul imunitar este anormal si cronic activat.
Immuno-modulators decrease tissue inflammation by reducing the population of immune cells and/or by interfering with their production of proteins. Imuno-modulatoarele scad inflamatia tesutului prin reducerea populatiei de celule ale sistemului imunitar si scad productia lor de proteine. Decreasing the activity of the immune system with immuno-modulators increases the risk of infections; however, the benefits of controlling moderate to severe Crohn's disease usually outweigh the risks of infection due to weakened immunity. Reducerea activitatii sistemului imunitar cu imuno-modulatoare creste riscul de infectii; cu toate acestea, beneficiile sunt mai mari decat riscurile. Examples of immuno-modulators are 6-mercaptopurine (6-MP), azathioprine (Imuran), methotrexate (Rheumatrex, Trexall), infliximab (Remicade), adalimumab (Humira). Exemple de imuno-modulatoare sunt 6-mercaptopurina (6-MP), azatioprina, metotrexat, infliximab, adalimumab.
Azathioprine (Imuran) and 6-mercaptopurine (6-MP, Purinethol) AZATIOPRINA SI 6-MERCAPTOPURINA
Azathioprine (Imuran) and 6-mercaptopurine (6-MP, Purinethol) are medications that weaken the body's immune system by reducing the population of a class of immune cells called lymphAzatioprina si 6-mercaptopurina sunt medicamente care slabesc sistemul imunitar al organismului, prin reducerea populatiei dintr-o clasa de celule imunitare numite limfocite. Azathioprine and 6-MP are related chemically. Azatioprina si 6-MP sunt legate chimic. (Actually, azathioprine is converted into 6-MP within the body.) In high doses, these two drugs have been useful in preventing rejection of transplanted organs and in treating leukemia
In low doses, they have been used for many years to treat patients with moderate to severe Crohn's disease and ulcerative col In doze mici, ele au fost folosite de mai multi ani pentru a trata pacientii cu boala Crohn si colita ulcerativa moderata pana la severa.
Azathioprine and 6-MP are increasingly recognized by doctors as valuable drugs in treating Crohn's disease and ulcerative colitis. Azatioprina si 6-MP sunt tot mai recunoscute de medici ca medicamente valoroase in tratamentul de bolii Crohn si colitei ulcerative. Some 70% of patients with moderate to severe disease will benefit from these drugs. Circa 70% din pacientii cu boala moderata pana la severa, vor beneficia de aceste medicamente. Azathioprine and 6-MP are used primarily in the following situations:Azatioprina si 6-MP sunt utilizate in principal in urmatoarele situatii:
Severe Crohn's disease and ulcerative colitis not responding to corticosteroids. forma severa a bolii Crohn si colitei ulcerative care nu raspunde la corticosteroizi.
The presence of undesirable corticosteroid-related side effects.2.efecte secundare ale corticosteroizilor.
Corticosteroid dependency, a condition in which patients are unable to discontinue corticosteroids without developing relapses of their disease.3.dependenta de corticosteroizi.
MENTINEREA REMISIEI
Maintenance of remission.
When azathioprine and 6-MP are added to corticosteroids in the treatment of Crohn's disease not responding to corticosteroids alone, there may be an improved response. Also, smaller doses and shorter courses of corticosteroids may be able to be used. Cand azatioprina si 6-MP sunt adaugate la corticosteroizi in tratamentul bolii Crohn poate exista un raspuns imbunatatit. De asemenea, doze mai mici si cursuri scurte de corticosteroizi pot fi utilizate. Some patients can discontinue corticosteroids altogether without experiencing relapses of their disease. Unii pacienti pot intrerupe corticosteroizii cu totul, fara a se confrunta cu o recurenta a bolii lor. This corticosteroid-lowering effect has earned azathioprine and 6-MP their reputation as 'steroid-sparing' medications.
In doze mai mici folosite pentru a trata boala Crohn, efectele secundare pe termen lung ale azatioprinei sau 6-MP sunt mai putin grave decat cele ale corticosteroizilor pe termen lung sau cursuri repetate de corticosteroizi.
Patients with Crohn's disease may undergo surgery to remove a segment of the intestine that is obstructed or contains a fistula. Long-term 5-ASA (such as Pentasa) and 6-MP both are effective in reducing the chances of recurrence after surgery. Pe termen lung acidul 5-ASA si 6-MP ambele sunt eficiente in reducerea sanselor de recidiva dupa interventia chirurgicala.
Anal fistulae can develop in some patients with Crohn's disease. Fistule perianale se pot dezvolta la unii pacienti cu boala Crohn. Anal fistulae are abnormal tracts (tunnels) that form between the small intestine or colon and the skin around the anus.Drainage of fluid and mucous from the opening of the fistula is a troublesome problem.These fistulae are difficult to treat and do not heal readily.Aceste fistule sunt dificil de tratat si nu se vindeca rapid. Metronidazole (Flagyl) has been used with some success in promoting healing of these fistulae. Metronidazolul a fost utilizat cu un oarecare succes in promovarea vindecarii acestor fistule. In difficult cases, azathioprine and 6-MP may be successful in promoting healingIIn cazuri dificile, azatioprina si 6-MP pot fi de succes in vindecare.
Side effects of azathioprine and 6-MP
EFECTELE SECUNDARE ALE AZATIOPRINEI SI 6-MP
Side effects of azathioprine and 6-MP include increased vulnerability to infections, inflammation of the liver (hepatitis) and the pancreas ( pancreatitis ), and bone marrow toxicity (interference with the formation of cells that circulate in the blood). Efectele secundare ale azatioprinei si 6-MP includ vulnerabilitate mai mare la infectii, hepatita si pancreatita, toxicitate la nivelul maduvei osoase.
The goal of treatment with azathioprine and 6-MP is to lower the body's production of certain types of white blood cells (lymphocytes) in order to decrease the inflammation in the intestines; however, lowering the number of lymphocytes may increase vulnerability to infections. Scopul tratamentului cu azatioprina si 6-MP este de reducere a productiei anumitor tipuri limfocite, in scopul de a reduce inflamatia in intestine; cu toate acestea, scaderea numarului de limfocite ar putea spori vulnerabilitatea la infectii. For example, in a group of patients with severe Crohn's disease unresponsive to standard doses of azathioprine, raising the dose of azathioprine helped to control the disease, but two patients developed cytomegalovirus (CMV) infection.
Azathioprine and 6-MP can induce inflammation of the liver (hepatitis) and pancreas ( pancreatitis Azatioprina si 6-MP poat determina inflamarea ficatului (hepatita) si a pancreasului (pancreatita). Pancreatitis typically causes severe abdominal pain and sometimes vomiting. Pancreatita se manifesta prin dureri abdominale severe si uneori varsaturi. Pancreatitis due to azathioprine or 6-MP occurs in 3%-5% of patients, usually during the first several weeks of treatment. Pancreatita datorata azatioprinei sau 6-MP apare la 3% -5% dintre pacienti, de obicei in timpul primelor saptamani de tratament. Patients who develop pancreatitis should not receive either of these two medications again. La pacientii care dezvolta pancreatita se intrerupe tratamentul.
Azathioprine and 6-MP also suppress the bone marrow.Azatioprina si 6-MP, de asemenea, suprima maduva osoasa. The bone marrow is where the red blood cells, white blood cells, and platelets are made. Actually, a slight reduction in the white cell count during treatment is desirable since it suggests that the dose of azathioprine or 6-MP is high enough to have an effect; however, excessively low red or white blood cell counts indicates bone marrow toxicity.De fapt, o usoara leucopenie in timpul tratamentului este de dorit, deoarece sugereaza ca doza de azatioprina sau 6-MP este suficient de mare pentru a avea un efect, insa, leucopenia sau anemia severa indica o toxicitate la nivelul maduvei osoase. Therefore, patients on azathioprine or 6-MP should have periodic blood counts (usually every two weeks initially and then every three months during maintenance) to monitor the effect of the drugs on the bone marrow. Prin urmare, pacientii sub tratament cu azatioprina sau 6-MP ar trebui sa faca teste sangvine la fiecare doua saptamani initial si apoi la fiecare trei luni in intretinere pentru a monitoriza efectul drogurilor asupra maduvei osoase.
Patients on long-term, high dose azathioprine to prevent rejection of the kidney after kidney transplantation have an increased risk of developing lymphoma, a malignant disease of lymph cells.There is no evidence at present that long term use of azathioprine or 6-MP, in the lower doses used in Crohn's disease, increases the risk of lymphoma, leukemia or other malignancies. Nu exista dovezi ca, in prezent, utilizarea pe termen lung a azatioprinei sau 6-MP, in dozele mai mici folosite in boala Crohn creste riscul de limfom, leucemie sau alte afectiuni maligne.
The use of azathioprine and 6-MP in pregnant women must be carefully considered.Utilizarea azatioprinei si 6-MP la femeile gravide trebuie sa fie analizata cu atentie. There are reports suggesting that the use of azathioprine or 6-MP in pregnancy is safer than once thought. Exista rapoarte care sugereaza ca utilizarea de azatioprina sau 6-MP in timpul sarcinii este mai siguar decat s-ar fi crezut. The risk of continuing azathioprine or 6-MP during conception and pregnancy must be weighed against the risk of worsening disease if they are stopped. Riscul de a continua azatioprina sau 6-MP in timpul sarcinii trebuie pus in balanta cu riscul de agravare a bolii, daca acestea sunt oprite. On the other hand, worsening disease has been shown clearly to be a significant risk to the fetus. Pe de alta parte, agravarea bolii este un risc semnificativ pentru fat.
One problem with 6-MP and azathioprine is their slow onset of action.O problema legata de 6-MP si azatioprina este debutul lor de actiune foarte lent. Typically, full benefit of these drugs is not realized for three months or longer. De obicei, beneficiul pe deplin al acestor medicamente nu se realizeaza timp de trei luni sau mai mult. During this time, corticosteroids frequently have to be maintained at high levels to control inflammation. In acest timp, corticosteroizii trebuie sa fie mentinuti la un nivel ridicat pentru a controla inflamatia.
INFLIXIMAB
Infliximab
(Remicade) este un anticorp anti- factorul de necroza tumorala alfa
(TNF-alfa). TNF-alfa este una dintre proteinele produse de celulele imune in
timpul raspunsului imun. TNF-alfa, la randul sau, stimuleaza alte
celule ale sistemului imunitar de a produce si elibera alte proteine care
promoveaza inflamatia. In boala Crohn, exista o productie
continua a TNF-alfa, ca parte a activarii imune. Infliximab, prin
atasarea la TNF-alfa scade inflamatia.
Infliximab
este produs de catre sistemul imunitar al soarecilor dupa
injectarea de TNF-alfa uman. Anticorpii soarecelui
sunt modificati apoi pentru a face sa arate mai mult ca un
anticorp uman. Aceste modificari sunt necesare pentru a reduce riscul de
reactii alergice atunci cand anticorpul este administrat la om. Infliximab
este administrat prin perfuzie intravenoasa cu durata de doua ore.
Pacientii sunt monitorizati pe parcursul perfuziei pentru
reactiile adverse. Infliximab este un medicament eficace si rapid
pentru tratamentul bolii Crohn active. Intr-un studiu care a implicat
pacienti cu boala Crohn moderata pana la severa care nu au
raspuns la corticosteroizi sau imuno-modulatoare, s-a obtinut 65% ameliorare
dupa o perfuzie cu Infliximab. La unii pacienti s-a observat ameliorarea simptomelor in termen de
zile de la perfuzie. Cei mai multi pacienti au prezentat ameliorare
in termen de doua saptamani.
La pacientii care raspund la infliximab, imbunatatirile in simptome pot fi dramatice. In plus poate fi o vindecare rapida a ulcerelor si inflamatiei in intestine, dupa doar o perfuzie. Infliximab a fost gasit a fi eficace pentru tratarea fistulelor. La majoritatea pacientilor care au raspuns la o prima perfuzie de infliximab boala lor a reaparut in termen de trei luni.Cu toate acestea, studiile au aratat ca perfuzii repetate de infliximab la fiecare opt saptamani, sunt sigure si eficiente in mentinerea remiterii la multi pacienti pe o perioada de unul, doi ani.
Raspunsul la infliximab dupa perfuziile repetate, uneori, se pierde in cazul in care pacientul incepe sa dezvolte anticorpi la infliximab. Studii se fac acum pentru a determina gradul de securitate pe termen lung si a eficacitatii perfuziei repetate de infliximab. Unul este pentru eventuala utilizare a infliximab pentru a controla boala rapid. Administrarea de Inliximab de intretinere se asociaza cu un tratament de intretinere cu azatioprina, 6-MP.
Azatioprina sau 6-MP pot fi utile in prevenirea dezvoltarii de anticorpi impotriva infliximab. Infliximab, in general, este bine tolerat. S-au raportat cazuri rare de efecte secundare in timpul perfuziei, inclusiv durere precordiala, dispnee si greata. Aceste efecte se rezolva, de obicei, spontan in cateva minute in cazul in care perfuzia este oprita. Alte efecte adverse frecvent raportate includ cefalee si infectii ale tractului respirator superior.
TNF-alfa este o
proteina importanta pentru apararea organismului impotriva
infectiilor. Infliximab, ca imuno-modulator creste riscul de
infectii. Un caz de colita cu Salmonella si mai multe cazuri de
pneumonie au fost raportate cu utilizarea de infliximab.Au fost raportate si
cazuri de tuberculoza.
In plus fata de
reactiile adverse care apar atunci cand perfuzia este administrata pacientii mai pot dezvolta o
reactie 'intarziata alergica' care apare in 7-10 zile.
Acest tip de reactie poate provoca simptome asemanatoare gripei,
cu febra, dureri articulare si o inrautatire a
simptomelor bolii Crohn. Au fost raportate si rare
cazuri de inflamatii ale nervilor, cum ar fi nevrita optica si
neuropatie la nivelul mainii.
Infliximab
poate agrava si cauza raspandirea unei infectii existente. Prin
urmare, nu trebuie administrat la pacientii cu pneumonie, infectii ale
tractului urinar sau abcese. In prezent se recomanda ca pacientii
sa fie testati pentru TBC inainte de primirea infliximab. Infliximab
poate provoca raspandirea celulelor canceroase, de aceea, nu trebuie
administrat la pacientii cu cancer. Infliximab poate
promova cicatrizarea intestinala si, prin urmare, poate agrava
stricturile si poate conduce la obstructie intestinala.
De asemenea, poate provoca vindecarea partiala (inchiderea partiala) a fistulelor perianale. Efectele infliximab asupra fatului nu sunt cunoscute. Exista unele rapoarte de agravare a bolii cardiace la pacientii care au primit Remicade.
ADALIMUMAB
Adalimumab este un agent
anti-TNF similar cu infliximab si scade inflamatia prin blocarea
factorul de necroza tumorala (TNF-alfa). In contrast cu infliximab,
adalimumab este un anticorp complet umanizat anti-TNF.Este administrat
subcutanat.
Patru
studii clinice recente (implicand aproape 1.500 de pacienti) au comparat
adalimumab cu placebo, au demonstrat ca adalimumab este, de asemenea,
eficient in tratarea inflamatiei in intestinul pacientilor cu
boala Crohn si in reducerea semnelor si simptomelor bolii Crohn.
Adalimumab
este comparabil cu infliximab in eficacitatea si siguranta pentru
inducerea si mentinerea remisiunii la pacientii care sufera
de boala Crohn. Adalimumab este, de asemenea, eficient in vindecarea fistulelor
perianale. Adalimumab a fost dovedit a fi eficace pentru pacientii care
fie nu au sau nu pot tolera infliximab. Adalimumab
(Humira) este administrat subcutanat la fiecare doua saptamani.
Adalimumab este in general bine tolerat. Mai
frecvente efecte secundare sunt reactii cutanate la locul de injectare cu
umflaturi, mancarimi, sau roseata. Alte reactii
adverse frecvente includ infectii respiratorii superioare, sinuzita,
si greata. Adalimumab,
precum infliximab, creste riscul de infectie. Au existat cazuri de
tuberculoza (TBC) raportate dupa utilizare. In prezent se recomanda
ca pacientii sa fie testati pentru TBC inainte de a primi aceste
medicamente.
Prin urmare, nu trebuie
administrat la pacientii cu pneumonie, infectii ale tractului urinar
sau abcese. Cazuri rare de limfom au fost raportate cu utilizarea de adalimumab.
Rare cazuri de inflamatie la nivelul sistemului nervos au fost raportate
cu utilizarea de adalimumab. Simptomele pot include parestezii, tulburari
de vedere, slabiciune in picioare. Unii pacientii care au primit
adalimumab pot dezvolta rareori simptome care mimeaza lupusul sistemic;
Aceste simptome includ eruptii pe piele, artrita, dureri precordiale
sau dispnee. Aceste simptome asemanatoare lupusului se pot rezolva
dupa oprirea medicamentului. Exista unele cazuri de agravare a bolii
cardiace, cum ar fi insuficienta cardiaca la pacientii care au
primit adalimumab.
Reactii
alergice severe cu eruptii cutanate, dispnee, si hipertensiune
arteriala severa sau soc sunt rare, dar reactii alergice
grave pot sa apara.
METOTREXAT
Metotrexat este atat un
imuno-modulator cat si antiinflamator.Acesta
a fost de ajutor in tratarea pacientilor cu boala Crohn moderat
pana la severa, care nu raspunde la azatioprina si 6 -
MP. Metotrexatul poate fi eficace la pacientii cu colita ulcerativa
moderat pana la severa care nu raspund la corticosteroizi,
azatioprina sau 6-MP. Acesta poate fi administrat pe cale orala sau
prin injectii intramusculare, dar este mult mai bine absorbit ca preparat
injectabil.
O complicatie
majora a metotrexatului este
dezvoltarea de ciroza hepatica in cazul in care medicamentul este
administrat pe o perioada indelungata de timp (ani). Riscul de
aparitie a leziunilor hepatice este mai mare la pacientii careconsuma
alcool sau sunt obezi sever. Alte efecte secundare includ scaderea numarului leucocite din sange si fibroza pulmonara.
Metotrexatul nu trebuie utilizat la femeile gravide, din cauza efecte toxice
asupra fatului.
Summary of antiinflammatory medications CHIRURGIA IN
BOALA CHRON
Nu exista nici un
tratament chirurgical pentru boala Crohn. Chiar si atunci cand toate
partile bolnave din intestine sunt eliminate, inflamatia se
repeta frecvent in partile anterior sanatoase dupa
operatie.
Prin urmare, o interventie
chirurgicala in boala Crohn este utilizata in principal pentru:
1. Indepartarea unui segment bolnav de intestin
care cauzeaza obstructie.
2. Drenaj de puroi din abcese abdominale si
peri-rectale.
3. Tratamentul fistulelor anale severe care nu
raspund la medicamente.
4. Rezectia de fistule interne (cum
ar fi o fistula intre colon si vezica urinara) care cauzeaza
infectii.
Chirurgia,
atunci cand este efectuata cu
succes,poate duce la o imbunatatire marcata a
calitatii vietii. La multi pacienti, cu toate acestea,
boala Crohn se intoarce in cele din urma, si afecteaza intestinele
anterior sanatoase. Boala recurenta,
de obicei, se afla la sau langa locul anterior interventiei
chirurgicale. De fapt, 50% dintre pacienti se pot astepta sa
aiba o reaparitie a simptomelor in termen de patru ani de la
interventia chirurgicala. Droguri, cum
ar fi Pentasa sau 6-MP au fost utile la unii pacienti pentru a reduce
riscul de recadere a bolii lui Crohn dupa interventia
chirurgicala.
Summary of antiinflammatory medicationsMASURI GENERALE
Masuri generale care pot ajuta la controlul bolii Crohn includ schimbarile de dieta si suplimente.Fibrele sunt slab digerate si pot agrava simptomele de obstructie intestinala. Prin urmare, o dieta saraca in fibre poate fi recomandata, in special la pacientii cu afectarea intestinului subtire. O dieta cu lichide poate fi benefica atunci cand simptomele sunt mai severe. Nutritia intravenoasa sau TPN (nutritie periferica totala) pot fi utilizate atunci cand se considera ca este nevoie de intestin la 'odihna'. Suplimentarea de calciu, acid folic si vitamina B12 este utila atunci cand apare sindromul de malabsorbtie. Utilizarea antidiareicelor diphenoxilat, loperamid si spasmoliticelor, de asemenea, poate ajuta la ameliorarea simptomelor de crampe si diaree.
|
Politica de confidentialitate |
| Copyright ©
2026 - Toate drepturile rezervate. Toate documentele au caracter informativ cu scop educational. |
Personaje din literatura |
| Baltagul caracterizarea personajelor |
| Caracterizare Alexandru Lapusneanul |
| Caracterizarea lui Gavilescu |
| Caracterizarea personajelor negative din basmul |
Tehnica si mecanica |
| Cuplaje - definitii. notatii. exemple. repere istorice. |
| Actionare macara |
| Reprezentarea si cotarea filetelor |
Geografie |
| Turismul pe terra |
| Vulcanii Și mediul |
| Padurile pe terra si industrializarea lemnului |
| Termeni si conditii |
| Contact |
| Creeaza si tu |