I. Introducere
In timp ce CET-urile conventionale folosesc pentru obtinerea si conversia energiei combustia combustibililor fosili, centralele nuclearo-electrice si implicit centralele CANDU, utilizeaza energia rezultata din fisiunea atomilor de uraniu existenti in combustibilul nuclear. In consecinta, fiecare centrala nuclearo-electrica cuprinde o componenta nucleara conventionala si una clasica.
Principalele materiale structurale utilizate la executia componentelor din circuitul primar si secundar al unei CNE CANDU sunt incluse in tabelul 1.
Tabelul 1. Principalele materiale structurale utilizate pentru executia componentelor din circuitele unei CNE CANDU
|
COMPONENTE |
MATERIALE |
|
Vasul Calandria |
Otel inox 304 L |
|
Placi tubulare |
Otel inox 304 L |
|
Scuturi de admisie la moderator |
Otel inox 304 L |
|
Tuburi Calandria |
Zircaloy-2 |
|
Inele in scutul de capat |
Otel carbon |
|
Scuturi de capat |
Otel inox 304 L |
|
Conducte de alimentare |
Otel carbon |
|
Racorduri de capat |
Otel martensitic 403m |
|
Tuburi de presiune |
Zr-2,5%Nb |
|
Teci combustibile |
Zircaloy-4 |
|
Inele distantiere |
Inconel-750 |
|
Patine si distantiere |
Zircaloy-4 |
|
Tubulatura schimbatoarelor de caldura |
Avand in vedere ca majoritatea proceselor de coroziune care se petrec intr-o centrala CANDU au loc la interfata metal/ solutie, clasificarea principalelor forme de coroziune caracteristice materialelor utilizate in acest tip de centrale nuclearo-electrice se va face in functie de caracteristicile fizico-chimice ale ambelor componente ale interfetei. In continuare, vor fi prezentate principalele forme de coroziune care pot afecta componentele structurale, in contextul celor aratate mai sus:
Coroziunea generalizata: poate fi susceptibil orice material prezent in circuitele primar si secundar al centralei.
Coroziunea localizata (pitting, intergranulara, transgranulara, etc): aliajele de Zr in prezenta produsilor de fisiune si a ionilor de halogeni, tuburile Generatorului de Abur executate din aliaje cu continut ridicat in Ni in conditii de pH neadecvat si in prezenta ionilor de halogeni si/ sau aparitia unor zone care formeaza crevase, conductele de alimentare din otel carbon in prezenta unor solutii care contin diversi ioni agresivi, etc.
3.Coroziunea nodulara: este susceptibil in special Zy-ul-4 expus la temperaturi mai mari de 450oC, sau in prezenta unor concentratii de oxigen mai mari decat cele normale;
4.Coroziunea fisuranta sub sarcina: sunt susceptibile, in general, materialele tensionate mecanic si expuse concomitent unui mediu agresiv, ca de ex. Zy-ul- 4 tensionat in prezenta produsilor de fisiune si a ionilor de halogeni, aliajele cu continut ridicat in Ni tensionate expuse in solutii contaminate cu ioni de halogeni; tevile schimbatoarelor de caldura tensionate si racordurile si zonele sudate expuse in solutii contaminate cu diversi ioni, etc.
5.Coroziunea in crevasa poate apare in: zonele de imbinare ale tuburilor de presiune cu racordurile de capat si in zonele de contact ale acestora cu patinele fasciculelor combustibile; in zonele de imbinare tub/placa tubulara existente in Generatorul de Abur sau sub depunerile existente pe placa tubulara, etc.
6.Coroziunea galvanica poate apare la contactul a doua metale diferite:ex. in zona de imbinare a tubului de presiune din Zr-2,5%Nb cu racordul de capat din otel martensitic 403m;
7.Fisurarea cu hidrogen: sunt susceptibile, in special, zonele tensionate mecanic ale unui tuburile de presiune care au un continut ridicat in hidrogen;
8.Coroziunea-eroziunea; un tip particular al acesteia este coroziunea accelerata de curgere (FAC - Flow Accelerated Corrosion) care poate apare pe:
conductele de alimentare din otel carbon la iesirea din zona activa a reactorului;
conductele din circuitul condensatorului;
separatorul de picaturi;
pompe, duze si valvele de control.
9.Coroziunea fretting poate apare pe:
a) tuburile Generatorului de Abur in zonele de contact cu suportii intermediari si in
zonele de contact cu barele antivibratie.
b) tecile elementelor combustibile aflate in zonele de contact cu patinele fasciculelor combustibile;
c) in zona superioara a preincalzitorului, etc
10.Coroziunea la oboseala poate apare pe tuburile Generatorului de Abur in zona invecinata cu placa tubulara.
II. Teste de coroziune prin autoclavizare
Modalitatea cea mai sigura si reproductibila de determinare a vitezei de coroziune a unui aliaj consta in expunerea acestuia in mediul in care opereaza in mod normal, la parametrii normali de exploatare, urmata de determinarea coroziunii acestuia in acel mediu specific. In majoritatea cazurilor, aceste experimente dureaza mult timp si implicit sunt foarte costisitoare. De aceea, un procedeu de obtinere mai rapida a datelor referitoare la viteza de coroziune a unui metal (aliaj)
intr-un mediu specific este fie folosirea unor echipamente in care sa fie simulati cat mai multi parametri de operare, fie utilizarea unor teste chimice accelerate executate in medii mult mai agresive, perioade mult mai scurte de timp.
|
Fig.1 Schita unei autoclave Prolabo de un litru |
incinta de testare cu volum variabil cuprins intre 0,5 si 13 litri, capacul de etansare prevazut/ sau nu cu lacas pentru termocuplu, o teava din otel inox care face legatura cu manometrul si o vana pentru degazare prevazuta cu robinet de inchidere pentru inalta presiune;
discul de rupere asezat in partea superioara a autoclavei pe aceeasi trecere cu manometrul;
cuptorul electric de incalzire alimentat la 380 V/50 Hz, care, asigura incalzirea uniforma a incintei de testare respective si
aparatura de comanda si control care consta din:
dintr-un dispozitiv de automatizare pentru reglajul automat al temperaturii prestabilite pentru testare, prin intermediul unui termoregulator;
un senzor de temperatura, care este un termocuplu cromel-alumel pentru domeniul de temperatura 0-600 C;
un manometru pentru controlul si indicarea presiunii in plaja de presiuni cuprinse intre 0 si 400 atm.
Inaintea utilizarii lor in testele propriuzise sau dupa anumite perioade in care in autoclave au fost executate autoclavizari in medii relativ contaminate, autoclavele trebuie pasivate. Pasivarea consta in executarea unuia sau mai multor cicluri de autoclavizare a cate 72 ore la 350oC (16,7 MPa) in apa demineralizata avand conductivitatea initiala de maxim 0,5mS/cm si pH-ul cuprins intre 6 si 7. Ciclurile de testare de cate 72 ore au fost repetate pana cand conductivitatea apei scoase din autoclava a devenit mai mica de 15mS/cm; in acel moment, se poate considera ca incinta propriuzisa a autoclavei este pasivata. Actualmente, in cadrul LADICON exista o autoclava care functioneaza in regim dinamic.
In SCN Pitesti exista urmatoarele dispozitive experimentale utilizate in testele efectuate sub iradiere in reactorul TRIGA: capsulele si respectiv buclele.
Bucla si capsulele de coroziune reprezinta dispozitive in care poate fi studiata coroziunea probelor in regim dinamic.Capsula este un dispozitiv mai putin sofisticat decat bucla, care permite executarea de teste si sub iradiere in regim dinamic. In SCN Pitesti, testele sub iradiere au fost executate in capsula C7 instalata in reactorul TRIGA. Capsula permite iradierea in mediu apos in conditii de temperatura ridicata (max.310oC) si presiune ridicata (max.110 atm) a esantioanelor prelevate din diverse materiale. Ea este prevazuta cu un incalzitor electric pentru realizarea temperaturii de testare, port-esantion pentru prinderea probelor, termocuple cromel-alumel pentru masurarea temperaturii mediului, canale uscate pentru probe activate, preincalzitor si presurizor pentru realizarea parametrilor apei, pompa dozatoare pentru reglarea chimiei apei, puncte de prelevare a probelor de apa din capsula, sistem de purificare a apei prin trecerea peste rasini schimbatoare de ioni.
Ca urmare a testelor de autoclavizare executate in diferite medii apoase, functie de pH-ul si compozitia acestora si de parametrii de operare( temperatura, presiune, continut de oxigen sau alte gaze introduse in mediul din autoclava, etc), probele metalice se vor acoperi cu diversi compusi functie de tipul aliajului autoclavizat. De exemplu:
- aliajele de Zr autoclavizate in conditii de mediu si la parametri similari celor existenti in circuitul primar (cca.300oC - 10,5MPa) prezinta post-autoclavizare cresteri in greutate, care indica formarea unor straturi superficiale de oxizi; tipurile de oxizi au fost identificate ulterior prin difractie de raze X, analiza XPS, etc;
- otelurile carbon autoclavizate in conditii de mediu si la parametrii specifici de operare celor existenti in circuitul secundar (cca.270oC - 6,5MPa), prezinta in primele 20-30 zile post-autoclavizare usoare pierderi in greutate, pentru ca ulterior sa se acopere cu straturi superficiale de oxi-hidroxizi si respectiv oxizi, mai mult sau mai putin protectoare, functie de compozitia chimica a otelului carbon.
Utilizand metoda gravimetrica si deci evaluand periodic pierderile sau castigurile in greutate realizate post-autoclavizare, se poate trasa curba cinetica a coroziunii materialului respectiv in mediul specific in care a fost autoclavizat.
III. Metode electrochimice
Coroziunea metalelor fiind un proces electrochimic, este evident ca metodele electrochimice vor fi foarte utile in detectarea si evaluarea coroziunii acestora. Se stie ca stabilitatea metalelor este determinata de procesele care au loc la interfata metal/electrolit [3]. Daca consideram o reactie generala de forma:
xA + mH+ + ne- yD + zH2O (1)
observam ca ea implica atat un transfer de protoni cat si unul de electroni. In consecinta, potentialul ei de echilibru va varia cu pH-ul. Pentru a afla care este reactia cea mai probabila, se va folosi diagrama Pourbaix specifica sistemului respectiv, in care la un anumit pH, trasand cele doua drepte corespunzatoare reactiilor de mai jos, vor putea fi stabilite atat domeniile de pasivitate cat si cele de coroziune specifice aliajului respectiv[2]:
M Mn+ + ne- (2)
xA + mH+ + ne- yD + zH2O (3)
Pentru exemplificare, in fig.2 este prezentata diagrama Pourbaix specifica sistemului Fe/ apa.
Procesele electrochimice necesitand existenta unor anozi si catozi aflati in contact electric cu o sursa de tensiune, in urma imersarii electrodului de lucru metalic in solutia din celula electrochimica, vor apare implicit caile electronice si ionice de conductie prin electrolit. Curentul de electroni dintre zonele anodice si catodice va fi proportional cu vitezele reactiilor de oxidare si reducere.
|
|
Fig. 2[2]
Diagrama de echilibru Pourbaix potential/ pH corespunzatoare sistemului Fe/ apa la 25oC
Monitorarea curentilor rezultati in urma proceselor de coroziune ne ofera mijloacele de evaluare a cineticii proceselor de coroziune si nu tendinta termodinamica ca procesul de coroziune sa aiba loc. Exista trei tipuri de reactii care pot avea loc la intefata metal(M)/apa in prezenta de oxigen :
M = Mn+ + ne- (4) producerea de cationi metalici.
M + nH2O = M(OH)n + nH+ + ne- (5) formarea de oxid sau hidroxid si
M + nH2O = Mnn- + 2nH+ + ne- (6) producerea de anioni.
Reactiile catodice tipice in mediu apos implica reducerea oxigenului, protonilor si apei:
O2 + 2H2O + 4e- = 4OH- (7) in medii neutre aerate sau alcaline
O2 + 4H+ + 4e- = 2H2O (8) in medii acide aerate
2H+ + 2e- = H2 (9) in medii acide
2H2O + 2e- = H2 + 2OH- (10) in medii neutre sau alcaline
Ecuatia Nernst descrie potentialul electrodului reversibil sau potentialul la echilibru, Eredox, asociat tendintei termodinamice ca reactia electrochimica sa se produca spontan. Pe masura ce potentialele devin mai pozitive decat potentialul la echilibru asociat unei reactii electrochimice particulare, oxidarea decurge in mod spontan, in timp ce la potentiale mai negative reducerea decurge in mod spontan. Formele ecuatiei Nernst pentru reactiile de oxidare date in ecuatiile reactiilor (2) si (3) sunt respectiv:
Eredox = E0 + (2,3RT/nF)log(Mn+) (1*)
si
Eredox = E0 - 2,3RTpH/F (2*)
in care:
R - constanta gazelor ideale [cal/mol K];
T - temperatura [K] si
E0 - potentialul standard al unei semicelule a carei activitate a speciilor dizolvate este egala cu 1 la temperatura si presiune normala.
Referitor la coroziunea in medii apoase, reactiile de oxidare ale metalelor [vezi ecuatiile reactiilor(1 3)] la potentiale de echilibru mai negative decat potentialele asociate reactiilor tipice catodice date de ecuatiile reactiilor (4 6), vor avea loc spontan.
Dintre tehnicile electrochimice cele mai uzitate, mentionam: metoda polarizarii care include atat metoda potentiodinamica cat si pe cea a polarizarii ciclice;metoda galvanostatica; metoda potentiostatica si metoda spectroscopiei impedantei electrochimice (EIS).
In fig.3 sunt prezentate schematic urmatoarele curbe:o curba a polarizarii ciclice, una galvanostatica si doua curbe potentiostatice.
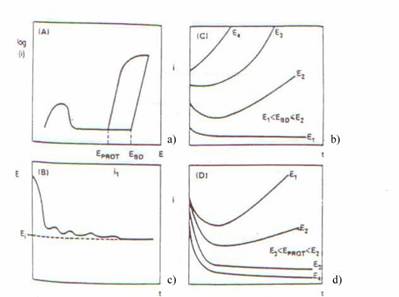
Fig. 3. Reprezentarile schematice ale unei: a)curbe de polarizare ciclica; b) curbe galvanostatice; c) curbe potentiostatice in care E1<Ebd<E2 ; d) curbe potentiostatice in care E3<Eprot<E2
III.1. Aparatura electrochimica experimentala
Caracteristicile electrochimice ale probelor metalice neacoperite sau filmate au fost stabilite prin intermediul masuratorilor executate pe sistemul electrochimic Princeton Model 2273 alcatuit dintr-un potentiostat/ galvanostat si un aparat Lock-in interfatat cu computerul PC. Pentru a nu afecta integritatea filmelor superficiale, masuratorile electrochimice au fost executate in diverse solutii mai mult sau mai putin conductoare, functie de interesul cercetatorului. In celula electrochimica(fig.4[1]) este introdus electrolitul in care sunt imersati cei trei electrozi: electrodul de lucru - proba de testat, electrozii auxiliari - din grafit si electrodul de referinta (calomel) (SCE).
|
|
Fig.4[1] Schita unei celule electrochimice |
Masuratorile electrochimice pot fi executate fie la temperatura camerei, fie la temperaturi 95oC. In cazul masuratorilor executate la temperaturi mai mari decat temperatura camerei, testele au fost efectuate in celula electrochimica plasata pe o plita prevazuta cu incalzire si agitare electromagnetica.
III.2. Masuratori ale potentialului de coroziune in circuit deschis
Tendinta termodinamica de corodare a unui sistem meta l/solutie, evaluata pe baza diagramelor Pourbaix si a vitezele de coroziune determinate din curbele potentiodinamice, sunt indicii importante referitoare la corodarea sistemului respectiv. Evolutia in timp a potentialului de coroziune poate furniza informatii in ceea ce priveste comportarea sistemului respectiv metal /solutie in timp. Masurarea potentialului in circuit deschis functie de timp nu reprezinta o metoda cantitativa de determinare a rezistentei la coroziune a sistemului, ea dand indicatii referitoare doar la probabilitatea producerii unor reactii metal/mediu.
Masuratorile de potential se fac la temperaturi constante, rezultatele fiind prezentate sub forma unor diagrame Ecor/timp. Valoarea potentialului stabilit in momentul introducerii metalului in solutie este mai putin importanta pentru comportarea sistemului respectiv decat variatia acestuia in timp. Forma curbelor potential/timp depinde de natura si viteza proceselor de coroziune care au loc in circuit deschis la interfata metal/electrolit: daca potentialul devine mai negativ aceasta va indica o tendinta de corodare a metalului si invers. Aparitia unor variatii bruste de potential spre valori mai electronegative si revenirea la cele pozitive poate indica ruperea filmului pasiv de pe suprafata metalului si ulterior refacerea acestuia. Cu alte cuvinte, aceste variatii pot indica existenta unor reactii concurente la interfata metal/solutie.
In fig. 5[2] este prezentata spre exemplificare o curba Ecor/ timp.
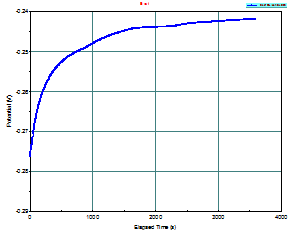
Fig. 5 Curba variatiei lui Ecor functie de timp aferente sistemului otel carbon filmat/ solutie AVT.
III.3. Metodele polarizarii electrochimice
Masuratorile electrochimice de polarizare se pot executa in urmatoarele doua situatii:
a) sub controlul curentului ( adica al vitezei de coroziune) cand se va masura potentialul rezultat si respectiv
b) sub controlul potentialului( adica a puterii oxidante), cand se va masura curentul rezultat.
In fiecare din aceste cazuri potentialul electrodului intr-un mediu conductor va varia cu densitatea de curent in celula electrochimica. Aceasta variatie a potentialului de la potentialul reversibil sau in stare stationara pana la o anumita valoare - functie de intentia cercetatorului - datorata trecerii curentului, este numita polarizare.
III.3.1. Metoda potentiodinamica
In fig este prezentata o curba potentiodinamica. Metoda potentiodinamica consta in varierea potentialului electrodului de lucru ca urmare a devierii valorii sale de la valoarea inregistrata in circuit deschis, cu inregistrarea simultana a curentului care trece prin sistem. Cu alte cuvinte, curba potentiodinamica reprezinta inregistrarea grafica a variatiei curentului functie de variatia potentialului electrodului polarizat. In cazul masuratorilor potentiodinamice, potentialul aplicat intre electrodul de lucru si cel de referinta este baleiat cu viteza constanta.
Exista trei tipuri fundamentale de polarizari anodice si catodice: polarizarea de activare, de concentrare si rezistenta de polarizare. In cazul polarizarii de activare, secventa de reactie de la interfata metal/ electrolit este cea care controleaza procesul electrochimic. Un exemplu este coroziunea care are loc in medii care contin o concentratie mare in specii active, ca de ex. acizii relativ concentrati. Sub controlul activarii, curba potentialului functie de log(densitatea curentului aplicat) este o linie dreapta. Aplicand tehnica polarizarii electrochimice si existand urmatoarea relatie intre potentialul aplicat si curentul rezultat, se poate calcula rezistenta de polarizare Rp si pantele Tafel folosind relatiile de mai jos:
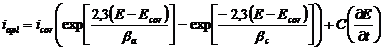 (3*) in care:
(3*) in care:
ba si bc - pantele anodice si catodice Tafel 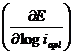 date de tangentele
anodice si respectiv catodice la curba de polarizare, iar
date de tangentele
anodice si respectiv catodice la curba de polarizare, iar
![]() - variatia in timp a potentialului aplicat sau a vitezei de
baleiere a potentialului.
- variatia in timp a potentialului aplicat sau a vitezei de
baleiere a potentialului.
Al doilea termen al ecuatiei (3*) tinde spre zero cand vitezele de baleiere ale potentialului sunt foarte coborate. La supratensiuni inalte, valoarea lui iapl devine practic egala cu iox, sau cu ired.
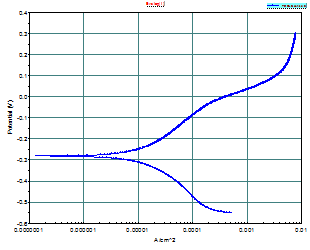
Fig.6 Curba potentiodinamica a otelului carbon filmat, testat in solutie AVT.
Cand vitezele de reactie sunt controlate de difuzia speciilor in blocul electrolitului de la interfata metal/ electrolit, incepe sa se simta influenta polarizarii de concentratie. Aceasta isi face simtita prezenta, in special, atunci cand concentratia speciilor reducatoare in mediu este mica, de ex. in cazul coroziunii in solutii de saruri aerate. In asemenea cazuri, apare o schimbare destul de brusca in potential atunci cand curentul atinge valoarea densitatii curentului-limita de difuzie.
![]()
![]()
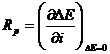
![]() (4*)
(4*)
in care diferenta DE = E - Ecor reprezinta polarizarea fata de potentialul de coroziune, iar i este densitatea de curent corespunzatoare unei valori particulare a lui DE.
Utilizand valoarea rezistentei de polarizare Rp, poate fi calculat curentul icor folosind relatia:
![]() (5*)
(5*)
in care B este o combinatie a pantelor anodice si catodice Tafel (ba, bc
![]() (6*)
(6*)
Dimensiunea lui Rp este W.cm2.
Principalul avantaj al masurarii rezistentei de polarizare este inregistrarea instantanee a vitezelor de coroziune si folosirea acestei tehnici pentru monitorarea on-line a unui numar mare de procese de coroziune care ar putea provoca probleme.
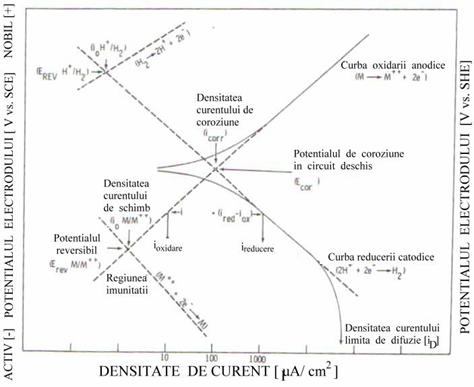
Fig.7[4] Portiunea catodica a unei curbe clasice potentiodinamice si reactiile
electrochimice aferente fiecarei zone
III.3.2.Metoda polarizarii ciclice
ASTM G61[6] descrie procedeul de conducere a testelor de polarizare ciclica in scopul determinarii susceptibilitatii la coroziune localizata. In cadrul acestor masuratori, potentialul se baleiaza in directie anodica cu viteza constanta de baleiaj, masurandu-se curentul care rezulta in sistem. Pe curba polarizarii ciclice exista doua tipuri de puncte semnificative pentru pitting: Ebd (in cazul probelor filmate) sau Ei ( in cazul probelor neacoperite) care reprezinta potentialul la care se constata o crestere brusca a curentului si respectiv Eprot sau Erp care reprezinta potentialul la care se inchide bucla de histerezis (Fig.8 .
|
|
Fig. Curba tipica de polarizare ciclica |
In general, cu cat valoarea lui Ebd este mai nobila, cu atat metalul testat va fi mai putin susceptibil la atac localizat. In cazul potentialului Eprot, cu cat este mai pozitiva valoarea acestuia, cu atat va fi mai putin probabil ca coroziunea localizata, odata initiata, sa se propage. Desi metoda polarizarii ciclice(PC) da, in general, rezultate reproductibile, pot apare, uneori si erori. Astfel, valorile lui Ebd si Eprot sunt puternic dependente de modul in care sunt executate testele si in particular de viteza de baleiaj a potentialului. In consecinta, valorile lui Ebd vor depinde de timpul de inductie necesar initierii pittingului. O alta complicatie care poate apare este legata de o propagare prea extinsa a pittingului in decursul baleierii potentialului in directie anodica. Aceasta va altera fie chimismul local din pituri (afectand adancimea piturilor sau/ si numarul piturilor), fie marimea difuziei.
III.4. Metoda galvanostatica
In general, in masuratorile executate sub curent constant - galvanostatice - este folosit acelasi sistem cu 3 electrozi in care un curent constant, preselectat, este impus intre electrodul de lucru si cel auxiliar. Variatia potentialului rezultat este masurata si inregistrata functie de timp; o curba tipica este prezentata in fig.9[5].
|
|
Fig. 9[5] Curba galvanostatica -variatia potentialului functie de timp la curent constant |
Testele galvanostatice executate in vederea determinarii susceptibilitatii la coroziune pitting au devenit tot mai uzuale, ele fiind executate conform prevederilor ASTM G-100[5]. In unele cazuri au fost obtinute valori mai reproductibile ale potentialelor de repasivare ale piturilor (Erp) lucrand in regim galvanostatic decat utilizand polarizarea ciclica. Astfel, pentru determinarea potentialului de nucleere a piturilor (Ebd sau Ei) este recomandabila metoda galvanostatica, notandu-se potentialul quasiconstant atins sub polarizarea anodica la curent constant pe o curba potential functie de timp. In mod uzual sunt utilizate urmatoarele densitati de curent: 0,01, 0,1 si 1 mA/cm2.
III.5. Metoda potentiostatica
Pe baza curbelor potentiostatice curent/timp, se poate determina perioada de timp dupa care are loc degradarea unui film preexistent sau format pe probe; aceasta perioada de timp este indicata printr-o scadere exponentiala a curentului (fig.10[4]).
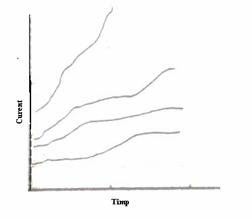
Fig. 10[4] Curba potentiostatica a variatiei curentului functie de timp, la potential constant
In masuratorile executate sub potential constant -potentiostatice - este folosit acelasi sistem cu 3 electrozi in care un potential constant, generat de un potentiostat este mentinut automat intre electrodul de lucru si cel auxiliar. Curentul rezultat este masurat si inregistrat functie de timp folosind un potentiometru-electrometru de mare impedanta si un ampermetru cu mai multe scale. Principalele domenii in care este folosit acest tip de teste sunt urmatoarele: pentru simularea coroziunii spontane, pentru prognozarea coroziunii care se poate produce in decursul protectiei anodice si pentru accelerarea coroziunii in anumite conditii.
In cazul testelor potentiostatice, potentialele pot fi selectate din oricare din cele trei regiuni caracteristice curbelor de polarizare potentiodinamica: regiunea activa, cea de tranzitie activ-pasiv si regiunea transpasiva.
Pentru determinarea potentialelor de initiere a piturilor sunt utilizate masuratorile potentiostatice pe termen lung; ele au, insa, dezavantajul ca sunt mari consumatoare de timp si implicit scumpe. Pentru accelerarea procesului de initiere si implicit pentru micsorarea duratei testelor potentiostatice a inceput sa se utilizeze prefisurarea mecanica a probelor, care inlaturand filmul superficial, creaza o zona mai susceptibila la coroziune pitting decat in restul probei.
IV. Analiza fizico-chimica pentru evaluarea comportarii la coroziune
IV.1 .Metoda gravimetrica
O metoda de monitorare a coroziunii uniforme a materialelor este metoda gravimetrica. Aceasta consta in determinarea masei probelor ori de cate ori este necesar prin cantarire, cantarire care se face utilizand balante care au precizia egala cu ( 1.10-4)g in vederea stabilirii variatiilor de masa in timp.
Inainte de aplicarea metodei gravimetrice probelor proaspat debitate, este necesar sa fie parcurse urmatoarele etape: pregatirea si curatarea suprafetei, masurarea si cantarirea probelor uscate.
De exemplu, in cazul aliajelor de zirconiu, pregatirea probelor se va face conform ASTM G2[7] , iar probele din otel vor fi pregatite anterior testarii conform LI-TH-33. Functie de natura materialului, dupa expunerea probelor perioade diferite de timp intr-un mediu apos, unele pot prezenta castiguri in greutate(ca de ex. aliajele de zirconiu), iar altele pierderi in greutate.
Pe baza cantaririi probelor care au suferit o coroziune uniforma se poate calcula viteza de coroziune in mediul respectiv, corespunzatoare fiecarei periode a expunerii in mediul apos. Reprezentand grafic variatia vitezelor de coroziune functie de perioadele de timp dupa care au fost masurate, se va obtine cinetica coroziunii materialului respectiv in mediul de expunere.
Exista diverse sisteme de unitati in care poate fi exprimata viteza de coroziune si anume:
in unitati englezesti ca mils/year (mpy) sau in unitati metrice ca mm/an; folosind o constanta se poate face conversia de la un tip de unitati la altul.
In ASTM G1[8] este prezentata metodologia de preparare, curatire si evaluare a probelor supuse testelor de coroziune utilizand metoda gravimetrica. Dupa completarea perioadei de testare, viteza coroziunii uniforme inregistrata, in special, in cazul probelor de oteluri, poate fi calculata cu urmatoarea formula:
Viteza de coroziune= (K x W)(A x T x D) (7*)
in care: K - constanta;
T - timpul de expunere (h);
A - aria (cm2);
W - variatia in greutate (g);
D - densitatea (g/cm3);
IV.2. Examinarea metalografica
Examinarea metalografica se executa la microscopul metalografic Neophot. Pentru punerea in evidenta a oxizilor, o portiune din proba oxidata este inglobata in folie de cupru tratata, dupa ce se definitiveaza inglobarea in rasina termoplastica cu ajutorul presei metalografice "Prestopress". Slifurile astfel pregatite trebuiesc slefuite pe hartie abraziva pana la granulatia 800 si apoi pe pasla acoperita cu pasta diamantata, pana la disparitia tuturor rizurilor de pe probe. Urmeaza apoi examinarea la microscopul metalografic si fotografierea portiunilor interesante.
Pentru evidentierea structurii sau a hidrurilor, slifurile vor fi atacate cu solutii specifice. Astfel, pentru evidentierea hidrurilor existente in aliajele de Zr, slifurile sunt atacate cu o solutie continand: 45ml HNO3 (d=1,33 g/cm3); 45ml H2O2 30% si 7 ml HF 40% (d=1,13g/cm3) prin tamponare cu vata infasurata pe o bagheta timp de maxim 10 secunde. In schimb, pentru evidentierea structurii Zy-ului-4 s-a facut tamponarea slifurilor timp de maxim 10 secunde cu o alta solutie avand compozitia: 25 ml HNO3 (d=1,33 g/cm3); 25 ml acid lactic si 4-5 picaturi de HF 40% (d=1,13 g/cm3).
IV.3.Examinari prin difractie de raze X
Examinarile prin difractie de raze X se executa pe difractometrul DRON 2,0 echipat cu tub cu anod de Cu si monocromator de grafit.
Difractia de raze X este utilizata cu succes in identificarea tipurilor de compusi formati pe toate tipurile de materiale feroase si neferoase, cu conditia ca acestea sa posede o structura cristalina.
De exemplu, in cazul probelor din aliaje de zirconiu, pentru a elimina influenta texturii, s-a folosit ca etalon o proba decapata din acelasi material, determinarile facandu-se pe cele 4 maxime de difractie ale Zr-a: (103), (004), (114), (105). Examinarile prin difractie de raze X au ca scop: identificarea tipurilor de compusi formati pe suprafetele probelor (oxizi, hidruri, etc.) a structurilor oxizilor, hidrurilor si a celorlalti compusi, a tensiunilor existente in acestia si a grosimilor filmelor de oxid. Pentru estimarea grosimii filmelor de oxid de zirconiu se foloseste legea Bragg:
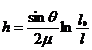 (8*)
(8*)
in care:
h - grosimea stratului de oxid absorbant;
q - unghiul corespunzator maximului de difractie;
l0 - intensitatea liniei etalonului;
l - intensitatea liniei in proba oxidata;
m - coeficient de absorbtie.
IV.4. Examene efectuate prin microscopie electronica
Microscopia electronica de baleiaj(SEM) ofera posibilitatea investigarii morfologiei suprafetei materialelor vizualizand detalii de ordinul micronului si chiar mai mici. Deci, in cazul metalelor se poate studia morfologia chiar la nivel de graunte.
In studierea comportarii de coroziune a metalelor, microscopia electronica de baleiaj este utila in vizualizarea modului in care se amorseaza si inainteaza atacul coroziv, concomitent cu vizualizarea comportamentului limitelor de graunte.
In cazul coroziunii fisurante sub sarcina (SCC), prin microscopie electronica de baleiaj se poate afla cum se amorseaza si cum inainteaza fisura: inter- sau transgranular, cunoasterea morfologiei fisurilor fiind utila in precizarea mecanismului SCC.
Asemenea examinari prin microscopie de baleiaj au fost executate in cadrul laboratorului nostru pe un microscop electronic J.E.O.L. si actualmente pe TESCAN VEGA II LMU.
IV.5. Analize prin spectroscopie de electroni
Cercetarile prin spectroscopie de electroni au fost realizate cu ajutorul spectrometrului de electroni ESCALAB MK II produs de firma V.G.Scientific Anglia. Facilitatile oferite de acest spectrometru sunt urmatoarele: tehnica XPS (spectroscopie de fotoelectroni excitati cu radiatie X), AES (spectroscopie de electroni Auger), SAM (microscopie Auger) si UPS (spectroscopie de electroni excitati cu radiatie ultrevioleta).
In timpul analizelor, in vasul experimental al spectrometrului sunt mentinute conditiile de vid ultrainalt (10-6 - 10-10torr). Este posibila, de asemenea, curatirea suprafetei analizate prin bombardament cu ioni de argon, iar in timpul analizelor este posibila incalzirea controlata a probelor pana la 100oC sau racirea lor pana la temperatura azotului lichid.
Tehnica XPS este folosita pentru excitarea fotoelectronilor fie radiatia X generata de un tub de raze X cu anozi de Al si Mg, fie radiatia X monocromatizata generata de un tub de raze X cu anod de Al.
Tehnicile AES si SAM folosesc ca sursa de excitare tunul de electroni cu o tensiune de accelerare variabila in domeniul 1-10 KV. Un oscilator cuplat cu un fotomultiplicator colecteaza electronii secundari emisi de suprafata bombardata cu electroni de energie mare, moduland semnalul in imagine TV. Imaginea obtinuta permite mariri de 100 - 50000 de ori, acces la orice zona din suprafata de interes si focalizeaza fasciculul incident cu rezolutie spatiala de 2000Å.
Pe langa posibilitatea achizitiei de spectre AES, practic din orice punct al suprafetei analizate, este posibila intocmirea de harti chimice care sa descrie distributia elementelor chimice pe suprafata prin baleierea controlata de calculator a fasciculului de electroni incident pe intreaga suprafata continuta in imaginea TV.
IV.6. Analize prin spectroscopie de impedanta electrochimica
Spectroscopia de impedanta electrochimica (EIS) este o metoda sensibila, utila in studiul proprietatilor filmelor de oxizi de formate pe suprafetele materialelor testate. Tehnica impedantei in curent alternativ are multe aplicatii in cercetarile de coroziune pentru ca foloseste semnale foarte mici care nu perturba proprietatile electrozilor. Aplicarea unei tensiuni alternative unei probe imersate in electrolit conduce la obtinerea unor informatii referitoare la starea suprafetei acesteia.
Masuratorile EIS s-au efectuat in solutii de acid boric / borat de sodiu, la temperatura camerei, pe probe filmate si apoi probe curatite chimic. Solutia de acid boric / borat de sodiu este inerta chimic fata de electrodul de lucru si are conductivitatea necesara delurarii masuratorilor de impedanta electrochimica. De asemenea, masuratorile EIS au fost inregistrate si in solutii de curatire chimica cu si fara inhibitor, la temperatura de 850C.
Spectrele de impedanta au fost inregistrate la potentialul in circuit deschis, in domeniul de frecventa (0,01 - 100000)Hz, la o amplitudine de 20mV.
Lucrul la potentialul in circuit deschis se justifica prin aceea ca la aceasta valoare nu este afectata grosimea stratului de oxid, modificarile care apar datorandu-se doar electrolitului si nu campului electric. Practic, valoarea corespunde unui curent foarte mic prin stratul de oxid. Calculul valorilor obtinute s-a realizat cu softul PowerSine, iar prelucrarile spectrelor de impedanta au fost facute cu softul ZsimpWin.
Bibliografie
[1] M.Pourbaix " Atlas d'equilibres electrochimiques" CEBELCOR Bruxelles;
[2] ASTM G3 "Recommended Practice for Convention Applicable to Electrochemical Measurements in Corrosion Testing";
[3] "Handbook on Corrosion Testing and Evaluation" Ed.Ailor W.H. (1971);
ASTM G5 "Recommended Practice for Standard Reference Method for Making Potentiostatic and Potentiodynamic Anodic Polarization Measurements";
ASTM G61" Conducting cyclic polarization measurements";
[7] ASTM G2 " Test Method for Corrosion Testing of Products of Zr, Hf and Their Alloys in Water at 3600C"
[8] ASTM G1 " Practice and Preparing, Cleaning and Evaluating Corrosion Test Specimens"
|
Politica de confidentialitate |
| Copyright ©
2026 - Toate drepturile rezervate. Toate documentele au caracter informativ cu scop educational. |
Personaje din literatura |
| Baltagul caracterizarea personajelor |
| Caracterizare Alexandru Lapusneanul |
| Caracterizarea lui Gavilescu |
| Caracterizarea personajelor negative din basmul |
Tehnica si mecanica |
| Cuplaje - definitii. notatii. exemple. repere istorice. |
| Actionare macara |
| Reprezentarea si cotarea filetelor |
Geografie |
| Turismul pe terra |
| Vulcanii Și mediul |
| Padurile pe terra si industrializarea lemnului |
| Termeni si conditii |
| Contact |
| Creeaza si tu |