In procesele redox nu participa numai substantele cu legaturi ionice ci si substante cu molecule covalente si de aceea s-a introdus notiunea de numar de oxidare (NO). Numarul de oxidare reprezinta numarul de electroni proprii implicati in formarea de legaturi ionice sau covalente. Stabilirea NO pentru fiecare specie atomica dintr-o molecula asculta de urmatoarele reguli:
NO pentru elemente aflate in stare fundamentala se considera
NO al ionilor mono- si poliatomici este egal cu sarcina ionului ( exemplu: Cl-1 are NO = -1; Na+1 are NO = +1)
NO al H2 in toti compusii in care se gaseste este , cu exceptia hidrurilor metalelor alcaline si alcalinopamantoase in care hidrogenul are NO= -1. ( exemplu: H din NaH are NO = -1; H din CaH2 are NO = -1)
NO al oxigenului in toti compusii este intotdeauna , cu exceptia compusilor peroxidici si apa oxigenata unde are valoarea ( R-O-O-H, H-O-O-H)
NO depinde de electronegativitatile partenerilor in cazul substantelor organice
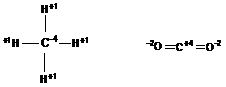
Suma NO a tuturor atomilor ce formeaza o molecula neutra este egala cu
Suma NO a tuturor atomilor ce alcatuiesc un ion este egala cu sarcina ionului.
Exemplu: care este NO al cromului din molecula de bicromat de potasiu ?
K+12CrX2O-27 2 x = 0
2-14+2x=0
-12 +2x=0
X=+6
O data introdusa notiunea de numar de oxidare, reactiile redox pot fi definite astfel: oxidarea este acel proces in care are loc cresterea numarului de oxidare; reducerea este acel proces in care are loc scaderea numarului de oxidare.
Oxidarea nu se poate desfasura independent de reducere pentru ca nu exista donor de electroni fara acceptor. Asadar cele doua reactii se studiaza impreuna, sub numele de reactii de oxidoreducere sau mai simplu reactii redox.
|
Politica de confidentialitate |
| Copyright ©
2025 - Toate drepturile rezervate. Toate documentele au caracter informativ cu scop educational. |
Personaje din literatura |
| Baltagul caracterizarea personajelor |
| Caracterizare Alexandru Lapusneanul |
| Caracterizarea lui Gavilescu |
| Caracterizarea personajelor negative din basmul |
Tehnica si mecanica |
| Cuplaje - definitii. notatii. exemple. repere istorice. |
| Actionare macara |
| Reprezentarea si cotarea filetelor |
Geografie |
| Turismul pe terra |
| Vulcanii Și mediul |
| Padurile pe terra si industrializarea lemnului |
| Termeni si conditii |
| Contact |
| Creeaza si tu |