
PRINCIPIUL AL DOILEA
CICLUL CARNOT DIRECT, REVERSIBIL
1 Entropia
Entropia este o functie de stare, care nu se poate defini pe baza fenomenelor fizice.
Entropia nu se poate masura direct. Functia aceasta de stare, notata cu S, pentru o masa oarecare si cu s pentru masa unitara, se stabileste pe calea deductiilor indirecte :
Pornind de la relatia (2.25) scrisa sub forma:
(2.25a) ![]()
se
observa ca ![]() nu este
diferentiala totala exacta:
nu este
diferentiala totala exacta:
![]()
deoarece caldura
specifica la presiune ![]() , este independenta de presiune
, este independenta de presiune 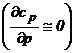 , pe cand
volumul unui gaz depinde de temperatura ,
, pe cand
volumul unui gaz depinde de temperatura , ![]() .
.
Daca inmultim fiecare membru
al relatiei (2.25a) cu factorul
integrant ![]() , obtinem o diferentiala totala
exacta, pe care o vom nota cu ds
, obtinem o diferentiala totala
exacta, pe care o vom nota cu ds
![]()
![]()
Integrand de la valorile initiale ![]() si
si ![]() ale temperaturii
si presiunii , pana la valorile lor finale, obtinem :
ale temperaturii
si presiunii , pana la valorile lor finale, obtinem :
![]()
![]() este entropia
initiala specifica corespunzatoare valorilor
este entropia
initiala specifica corespunzatoare valorilor![]() si
si ![]() . Valoarea
. Valoarea ![]() nu intereseaza in
calcule. Intereseaza doar variatia entropiei in timpul unei transformari oarecare.
nu intereseaza in
calcule. Intereseaza doar variatia entropiei in timpul unei transformari oarecare.
Relatia anterioara mai poate fi pusa sub forma:
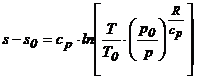
dar ![]() , deci :
, deci :
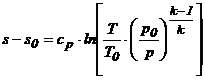
Dar, din
ecuatia de stare a gazelor perfecte, scrisa atat pentru starea
initiala cat si pentru cea finala, obtinem: ![]()
Rezulta ca:
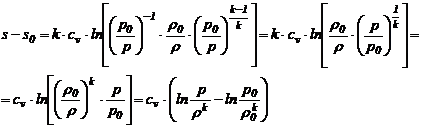
Din relatia (6) se
observa ca entropia ramane ![]() , daca intre presiune si densitate avem
relatia
, daca intre presiune si densitate avem
relatia
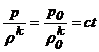
Transformarea care asculta de aceasta lege se numeste transformare izentropica. In acest caz avem:
(8 a) ![]() , pentru masa unitara, sau
, pentru masa unitara, sau
(8 b) ![]() , pentru o masa oarecare,m.
, pentru o masa oarecare,m.
Deci, caldura introdusa in sistem din
afara, sau scoasa din interiorul sistemului, ![]() , este nula. Rezulta ca are loc o transformare adiabatica. Pentru
fluidele ideale (cand nu sunt pierderi prin frecare) transformarea
adiabatica este si izentropica .
, este nula. Rezulta ca are loc o transformare adiabatica. Pentru
fluidele ideale (cand nu sunt pierderi prin frecare) transformarea
adiabatica este si izentropica .
Pentru fluidele reale intervine o serie de fenomene precum frecarea intre straturi datorita vascozitatii, miscarile turbionare si turbulente, care conduc la o pierdere de energie mecanica numita energie de disipatie.
Energia disipata se regaseste in complexul energetic al fenomenului, fiind transformata in caldura, numita caldura de disipatie .
2 Efectul caldurii de disipatie
Aplicand principiul I al termodinamicii unui gaz real , vom constata ca o parte din lucrul mecanic efectuat de gaz:
![]()
va
fi consumat sub forma de energie disipata, care se transforma in
caldura . Caldura de disipatie ramane in interiorul
gazului, daca acesta este izolat perfect. O vom nota cu ![]() .
.
Notam ![]() acea parte din lucrul
mecanic care se efectueaza in exterior si vom avea :
acea parte din lucrul
mecanic care se efectueaza in exterior si vom avea :
![]()
Notam cu ![]() caldura introdusa
din exterior, iar principiul intai va fi exprimat prin relatia:
caldura introdusa
din exterior, iar principiul intai va fi exprimat prin relatia:
![]()
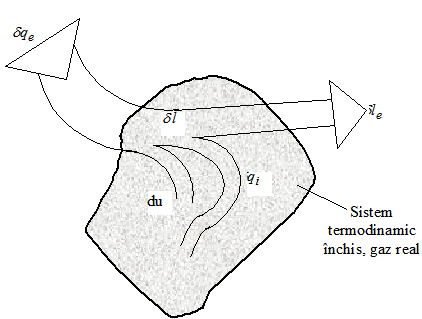
Fig.1 Ilustrarea principiului I al termodinamicii aplicat unui gaz real
Notam cu![]() suma dintre cantitatea de caldura exterioara,
suma dintre cantitatea de caldura exterioara,
![]() si cea
interioara
si cea
interioara ![]() :
:
![]()
si obtinem din nou relatia primului principiu al termodinamicii pentru sisteme inchise, sub forma cunoscuta:
![]()
Rezulta ca relatia primului principiu al termodinamicii se aplica atat gazelor ideale, cat si celor reale.
Un efect important al pierderilor prin
caldura de disipatie este modul in care se
desfasoara transformarea adiabatica la fluidele reale.
Consideram nula caldura introdusa din exterior (![]() ) si atunci transformarea este adiabatica, dar nu
si izentropica, deoarece caldura de disipatie nu este
niciodata nula:
) si atunci transformarea este adiabatica, dar nu
si izentropica, deoarece caldura de disipatie nu este
niciodata nula:
(13) ![]()
Daca totusi pierderile prin disipatie sunt foarte mici, asa cum este cazul frecarilor in stratul limita , care se refera la un procent mic din masa totala a gazului, atunci ele pot fi neglijate:
![]()
astfel
incat transformarea adiabatica poate fi considerata in acelasi
timp si izentropica (![]() ) , ca si pentru fluidele ideale, unde avem riguros
) , ca si pentru fluidele ideale, unde avem riguros
![]()
![]()
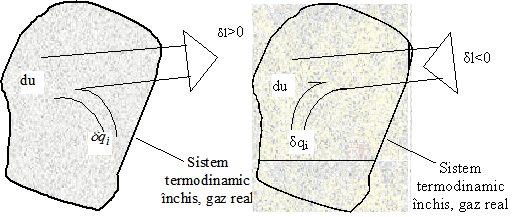
a) b)
Fig.2 Ilustrarea transformarii adiabate in cazul unui gaz real
In mod general insa,
miscarile sunt foarte dezordonate, pierderile nu pot fi neglijate
si, deci, nici caldura de disipatie (![]() ), astfel incat transformarea adiabatica nu corespunde
unei transformari izentropice. In acest caz , observand ca aceste
pierderi reprezinta un lucru mecanic intern pozitiv (
), astfel incat transformarea adiabatica nu corespunde
unei transformari izentropice. In acest caz , observand ca aceste
pierderi reprezinta un lucru mecanic intern pozitiv (![]() ) , ceea ce corespunde la o caldura de
disipatie tot pozitiva (
) , ceea ce corespunde la o caldura de
disipatie tot pozitiva (![]() ), se poate vedea ca la o transformare
adiabatica a gazelor reale (
), se poate vedea ca la o transformare
adiabatica a gazelor reale (![]() ), entropia creste:
), entropia creste:
![]()
Relatia (15) reprezinta o concluzie corespunzatoare celui de-al doilea principiu al termodinamicii.
3 Formularea principiului al doilea al termodinamicii
Principiul al doilea al termodinamicii afirma ca:
Entropia, intr-un sistem izolat, niciodata nu poate descreste:
![]()
Principiul a fost formulat dupa ce s-a obsevat experimental ca niciodata caldura nu poate trece, de la sine, de la o sursa rece la una calda.
Termenul de entropie are sens negativ, cresterea entropiei indicand faptul ca o parte din energia disponibila la inceputul unui proces termodinamic, nu mai poate fi utilizata la sfarsitul acelui proces, pentru transformari ulterioare. Astfel, o interpretare intuitiva a principiului al doilea al termodinamicii ar fi aceea ca, la sfarsitul unui proces termodinamic, energia utilizabila a sistemului izolat nu poate sa fie mai mare decat la inceputul procesului, deoarece o parte din ea s-a disipat. Energia utilizabila a sistemului izolat poate fi aceeasi, daca nu exista pierderi prin frecare, sau poate fi mai mica, atunci cand apar pierderi prin disipatie.
In concluzie, daca in decursul
unui proces termodinamic entropia ramane ![]() , (deci nu exista disipari de energie), atunci
procesul este reversibil. Daca in timpul procesului se
genereaza entropie
, (deci nu exista disipari de energie), atunci
procesul este reversibil. Daca in timpul procesului se
genereaza entropie ![]() (apar disipari), atunci procesul este ireversibil.
(apar disipari), atunci procesul este ireversibil.
In cazul in care, din calcule,
rezulta o scadere a entropiei unui sistem izolat, ![]() , atunci procesul considerat este imposibil. El
contravine celui de-al doilea principiu al termodinamicii.
, atunci procesul considerat este imposibil. El
contravine celui de-al doilea principiu al termodinamicii.
4 Exergia
Ridicand analiza energetica pe un plan superior celui oferit de entropie, se introduce notiunea de exergie. In timpul unui proces ireversibil, generarea de entropie determina scaderea exergiei sistemului, adica scaderea capacitatii sistemului de a mai efectua, in continuare, un lucru mecanic.
Prin prisma notiunilor de entropie si exergie, principiul al doilea conduce la diferentierea calitativa a energiei, dupa cum urmeaza:
energie ordonata: energia mecanica, energia electrica;
energie dezordonata: energia termica.
In aceasta idee, viteza de degradare a energiei ordonate in energie dezordonata (termica) poarta numele de disipatie. Disipatia este insotita de generare de entropie. Scoala de Bruxelles considera ca, din punct de vedere cantitativ, disipatia este data de produsul dintre temperatura absoluta si generarea de entropie determinata de ireversibilitate
Exergia, Ex, este, prin definitie, fractiunea maxima a unei forme de energie transformabila in energie ordonata.
Anergia An, este, prin definitie, fractiunea minima a unei energii care nu poate fi transformata in energie ordonata.
Considerand definitiile de mai sus, energia, E, este compusa din:
![]()
Astfel, pentru formele ordonate de energie
avem ![]() si
si ![]() , iar pentru formele dezordonate
, iar pentru formele dezordonate ![]() si
si ![]() . Deci, o mai mica parte din energia dezordonata
poate fi utilizata din punct de vedere tehnic.
. Deci, o mai mica parte din energia dezordonata
poate fi utilizata din punct de vedere tehnic.
Valoarea exergiei depinde atat de parametrii agentului de lucru, cat si de parametrii mediului ambiant. Exergia unui agent termic este cu atat mai mare, cu cat presiunea si temperatura acestuia sunt mai ridicate. Considerand o cantitate oarecare de caldura, Q, componentele ei vor fi de forma:
![]()
unde To temperatura mediului, mai mica decat temperatura agentului termic;
![]() entropia generata
din cauza ireversibilitatii.
entropia generata
din cauza ireversibilitatii.
Consideram cazul general al transformarii politropice.
Cantitatea elementara de
caldura![]() se inlocuieste in integrala entropiei:
se inlocuieste in integrala entropiei:
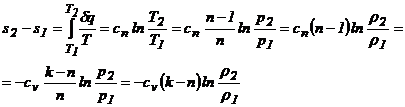
In cazul transformarilor simple se obtin urmatoarele relatii pentru calculul variatiei entropiei:
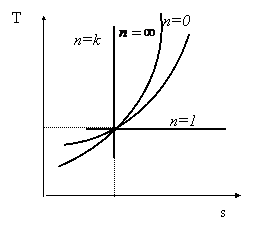
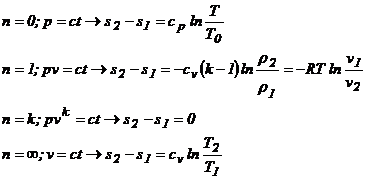
Reprezentarea grafica a variatiei temperaturii termodinamice in functie de entropie poate fi urmarita in fig.3, pentru toate cele patru cazuri particulare de mai sus.
Fig.3 Reprezentarea in diagrama calorica (in coordonate T-s) a proceselor simple
6.Ciclul Carnot direct, reversibil
Termenul de ciclu desemneaza un ansamblu de transformari de stare care conduc gazul la o stare finala identica cu cea initiala si care se poate repeta apoi.
Sadi Carnot a analizat conditiile optime de transformare continua a caldurii in lucru mecanic. Concluzia a fost ca singurul ciclu care realizeaza aceasta transformare la randament maxim este ciclul reversibil, compus din doua adiabate si doua izoterme, numit ciclul Carnot. Importanta acestei observatii este ca ciclul Carnot stabileste limita impusa de natura pentru transformarea caldurii in lucru mecanic. Agentul termic se considera gaz ideal.
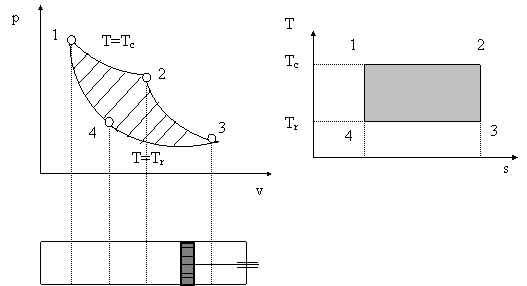
a) b)
Fig.6 Diagrama ciclului Carnot, in coordonate p-v (a) si T-s (b)
Fie un piston care se
misca intr-un cilindru perfect izolat adiabat. Fie doua surse
foarte mari de caldura, una calda la temperatura ![]() si alta la
temperatura mai joasa
si alta la
temperatura mai joasa ![]() <
<![]() . Problema studiata este scoaterea caldurii din
prima sursa si transformarea ei in lucru mecanic, cu ajutorul
sistemului piston-cilindru, utilizand o transformare reversibila
inchisa..
. Problema studiata este scoaterea caldurii din
prima sursa si transformarea ei in lucru mecanic, cu ajutorul
sistemului piston-cilindru, utilizand o transformare reversibila
inchisa..
Agentul termic (gazul) este luat de la sursa calda. Fazele transformarii sunt
a)Expansiunea izoterma
(T=![]() ) de la starea 1 la starea 2 , timp in care gazul se
introduce in cilindru .
) de la starea 1 la starea 2 , timp in care gazul se
introduce in cilindru .
b)Expansiunea adiabata
,de la starea 2 la 3 , timp in care intrarea gazului din prima sursa ![]() este inchisa, iar
schimbul de caldura cu exteriorul este nul, sistemul fiind izolat.
Temperatura scade de la valoarea
este inchisa, iar
schimbul de caldura cu exteriorul este nul, sistemul fiind izolat.
Temperatura scade de la valoarea ![]() la
la ![]() , corespunzatoare sursei a II-a .
, corespunzatoare sursei a II-a .
c)Comprimarea izoterma (T=Tr) a gazului de la starea 3 la 4 , in care timp gazul cu caldura continuta se scurge in sursa a-II-a. Sursa a-II-a este deschisa si are loc evacuarea.
d)Comprimarea adiabatica,
timp in care sursa a II-a este inchisa si temperatura este
ridicata din nou de la ![]() la
la![]() .
.
Diagramele procesului sunt indicate in figura 6. In diagrama mecanica, fig.6a, suprafata hasurata este proportionala cu lucrul mecanic extern in coordonate p-v. In diagrama calorica, fig.6b, suprafata gri reprezinta echivalentul de caldura absorbita de sistem, in coordonate T-s.
O parte din caldura
transportata de catre gaz , s-a transformat in lucru mecanic, iar o
parte s-a scurs in sursa a doua, ![]() , odata cu gazul evacuat.
, odata cu gazul evacuat.
Gazul scos din sursa calda,![]() , are continutul total de caldura:
, are continutul total de caldura:
![]() ,
,
unde ![]() -poarta numele de capacitate calorica.
-poarta numele de capacitate calorica.
In sursa rece, ![]() , este varsat gazul cu continutul de
caldura:
, este varsat gazul cu continutul de
caldura:
![]() ,
,
Rezulta ca diferenta de caldura care s-a transformat in lucru mecanic este:
![]()
Eficienta cu care se realizeaza o transformare energetica intr-o masina este data de randament. In cazul unei masini termice care ar lucra dupa ciclul Carnot direct, reversibil, randamentul este raportul dintre lucrul mecanic produs si caldura extrasa in acest scop.
Randamentul constituie raportul dintre diferenta de caldura scoasa si continutul total initial de caldura:
![]()
Randamentul corespunzator ciclului Carnot reversibil direct este maxim. Nu exista alt ciclu care sa dea o diferenta mai mare de caldura utilizata.
Variatia entropiei sistemului, in timpul unui ciclu, este nula. Aceasta variatie se poate calcula ca suma a variatiilor pe fiecare transformare componenta a ciclului. Rezulta:
![]()
unde ![]() , caldura extrasa din sursa calda, la
temperatura constanta Tc, in timpul expansiunii izoterme;
, caldura extrasa din sursa calda, la
temperatura constanta Tc, in timpul expansiunii izoterme;
![]() , caldura evacuata in sursa rece, la temperatura
constanta Tr, in timpul comprimarii izoterme.
, caldura evacuata in sursa rece, la temperatura
constanta Tr, in timpul comprimarii izoterme.
Gazul fiind ideal, transformarile adiabatice sunt si izentropice.
Se observa ca in relatia (31) primul termen este pozitiv, iar al doilea este negativ. Sistemul nefiind izolat, entropia sa creste in faza de expansiune izoterma si scade, cu aceeasi cantitate, in faza de compresiune izoterma. Are loc, deci, un schimb de entropie intre sistem si mediu.
Expresia randamentului cu care se efectueaza transformarea caldura-lucru mecanic, intr-o masina termica ce ar lucra dupa ciclul Carnot direct reversibil poate fi considerata o formulare a principiului al doilea al termodinamicii. De fapt, primul care a enuntat acest principiu a fost Sadi Carnot, in anul 182 Enuntul este urmatorul:
Pentru ca o masina termica sa functioneze, ea trebuie sa primeasca o cantitate de caldura de la o sursa cu temperatura ridicata si sa cedeze o parte din caldura primita unei alte surse, cu temperatura mai scazuta.
Se afirma, astfel, imposibilitatea crearii unui perpetuum mobile de speta a doua (termic), adica a unei masini termice care ar functiona cu o singura sursa de caldura, de temperatura constanta.
Randamentul masinilor termice este strict mai mic decat randamentul ciclului Carnot direct, reversibil, care lucreaza intre aceleasi temperaturi extreme, deoarece vitezele de desfasurare a ciclului masinii termice reale sunt finite. Randamentul poate fi ridicat prin cresterea temperaturii calde Tc, si/sau prin scaderea temperaturii reci, Tr. Se subliniaza ca, temperatura Tc poate fi crescuta numai in limitele permise de materialele din care este construita masina termica, iar temperatura Tr poate fi diminuata numai pana la valoarea temperaturii mediului ambiant.
Intrebari test
1.Entropia unui gaz real care sufera o transformare adiabatica:
![]() a)
creste;
a)
creste;
b) ramane constanta; a) b) c)
c) descreste.
2. Entropia unui gaz ideal (lipsit de vascozitate) care sufera o transformare adiabatica:
![]() a)creste;..
a)creste;..
b)ramane constanta; a) b) c)
c)descreste.
3.Principiul al doilea al termodinamicii spune ca:
![]() a)Entropia,
intr-un sistem izolat, niciodata nu poate descreste;........
a)Entropia,
intr-un sistem izolat, niciodata nu poate descreste;........
b)Entropia,
intr-un sistem deschis, ramane intotdeauna
c)Caldura nu poate trece, in mod spontan, de la o sursa rece , la una calda..
Ciclul Carnot reversibil este alcatuit din :
a)doua izobare
si doua izentrope ![]()
b)doua izoterme si doua izocore; a) b) c)
c)doua izoterme si doua adiabate.
5.Ciclului Carnot reversibil direct ii corespunde :
![]() a)randamentul maxim de transformare a caldurii in
lucru mecanic;
a)randamentul maxim de transformare a caldurii in
lucru mecanic;
b)randamentul minim de extragere a caldurii dintr-o sursa calda; a) b) c)
c)randamentul maxim de transformare a energiei cinetice in energie potentiala.
6.In coordonate T-s, ciclul Carnot reversibil direct este reprezentat printr-un:
![]() a)pentagon
regulat;
a)pentagon
regulat;
b)dreptunghi; a) b) c)
c)dreptunghi curbiliniu.
Problema 1
Intr-un detentor cu
piston, aerul comprimat la presiunea ![]() se destinde politropic, la presiunea
se destinde politropic, la presiunea ![]() . Coeficientul politropic are valoarea medie
. Coeficientul politropic are valoarea medie ![]() . Cunoscand ca temperatura initiala este
. Cunoscand ca temperatura initiala este ![]() , iar caldura specifica sub volum constant este
, iar caldura specifica sub volum constant este ![]() , sa se calculeze:
, sa se calculeze:
a)temperatura finala ![]() ;
;
b)variatia entropiei
specifice a aerului, ![]() .
.
a)Legea politropei ![]() se mai scrie:
se mai scrie:
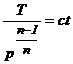
Rezulta
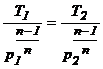 , deci
, deci 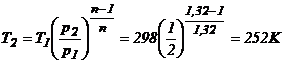
b)Variatia de entropie specifica:
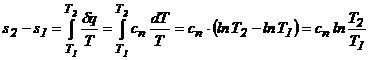
unde caldura specifica
politropica este ![]()
![]()
Rezulta
![]()
Dioxidul de carbon, cu
masa ![]() , aflat intr-o butelie, trece printr-un proces izocor,
pana cand presiunea sa creste de 1,8 ori. Dioxidul de carbon
este considerat gaz perfect, avand caldura specifica sub presiune
constanta
, aflat intr-o butelie, trece printr-un proces izocor,
pana cand presiunea sa creste de 1,8 ori. Dioxidul de carbon
este considerat gaz perfect, avand caldura specifica sub presiune
constanta ![]() si constanta
si constanta ![]() . Sa se calculeze variatia de entropie intre starea
initiala, 1, a sistemului si starea sa finala, 2.
. Sa se calculeze variatia de entropie intre starea
initiala, 1, a sistemului si starea sa finala, 2.
3. Gazul dintr-un cilindru cu
piston se destinde suficient de rapid pentru ca transformarea sa poata fi considerata
adiabata. Gazul este perfect. Se cunosc masa gazului, ![]() , caldura specifica sub presiune constanta,
, caldura specifica sub presiune constanta, ![]() si constanta
gazului,
si constanta
gazului, ![]() . Sa se determine:
. Sa se determine:
a)lucrul mecanic specific schimbat de sistem cu exteriorul,
b)variatia de entropie.
Un gaz perfect, avand
caldura specifica ![]() parcurge un ciclu Carnot
direct, reversibil, pentru care temperatura sursei calde este
parcurge un ciclu Carnot
direct, reversibil, pentru care temperatura sursei calde este ![]() , iar temperatura sursei reci este
, iar temperatura sursei reci este ![]() . Sa se determine:
. Sa se determine:
a)caldura
transformata in lucru mecanic de catre![]() de gaz, in timpul ciclului; sa se reprezinte grafic
caldura schimbata;
de gaz, in timpul ciclului; sa se reprezinte grafic
caldura schimbata;
b)randamentul ciclului.
RASPUNSURI SI REZOLVARI
1.a; 2.b; 3.a, c; c; 5.a; 6.b.
Variatia de entropie a sistemului, in cazul acestui proces izocor:
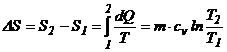
Intr-o transformare la volum constant, raportul presiunilor este egal cu raportul temperaturilor:
![]() ,
, ![]() deci,
deci, ![]()
Caldura specifica la volum constant se calculeaza din relatia Mayer:
![]()
![]()
Entropia sistemului variaza cu:
![]() .
.
Exponentul adiabatic, k, se poate afla din relatia:
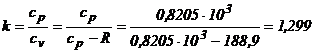
a)Lucrul mecanic specific este :
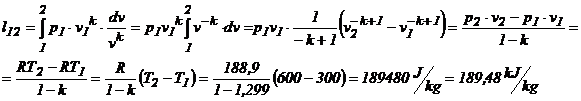
b)Caldura schimbata cu exteriorul este nula intr-o transformare adiabata. In acest caz, pentru un gaz ideal (gazul perfect este si ideal, adica lipsit de frecare), entropia sistemului nu variaza:
![]() , deci
, deci ![]()
Rezolvare
a)Ciclul Carnot direct, reversibil este alcatuit din doua transformari izoterme si doua adiabate. Caldura transformata in lucru mecanic este diferenta dintre entalpia gazului scos din sursa calda, Hc, si entalpia gazului evacuat in susra rece, Hr.
![]()
Caldura schimbata este proportionala cu aria dreptunghiului inchis de cele doua adiabate si cele doua izoterme din reprezentarea grafica in coordonate T-S.
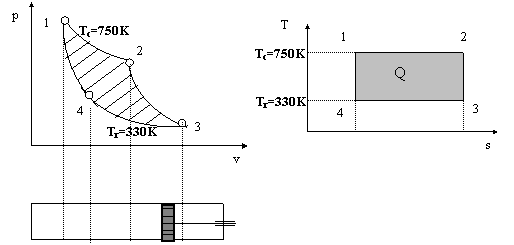
Fig.5.Ciclul Carnot direct, reversibil, corespunzator problemei 5
b)Randamentul ciclului Carnot direct, reversibil este raportul dintre caldura tansformata in lucru mecanic si entalpia (continutul total de caldura ) extrasa din sursa calda. Randamentul devine:
![]()
|
Politica de confidentialitate |
| Copyright ©
2026 - Toate drepturile rezervate. Toate documentele au caracter informativ cu scop educational. |
Personaje din literatura |
| Baltagul caracterizarea personajelor |
| Caracterizare Alexandru Lapusneanul |
| Caracterizarea lui Gavilescu |
| Caracterizarea personajelor negative din basmul |
Tehnica si mecanica |
| Cuplaje - definitii. notatii. exemple. repere istorice. |
| Actionare macara |
| Reprezentarea si cotarea filetelor |
Geografie |
| Turismul pe terra |
| Vulcanii Și mediul |
| Padurile pe terra si industrializarea lemnului |
| Termeni si conditii |
| Contact |
| Creeaza si tu |