
Metodele spectroscopice de investigare a calitatii alimentelor
Moleculele unei substante sunt sisteme cuantice aflate intr-o anumita stare energetica. Ca particula cuantica unei molecule i se poate asocia o functie de unda Ψ (numita Hamiltonian) cu care se poate descrie starea energetica a acesteia utilizand Ecuatia lui Schroedinger (Atkins, 1998):
-h2δ2 Ψ(x)/2m δ2(x) + V(x) Ψ(x) = E Ψ(x)
Pe baza aproximatiei Born-Oppenheimer rezolvarea se poate simplifica si solutiile ecuatiei pot fi separate pe nivele energetice corespunzatoare nucleului, electronilor, miscarii vibrationale si rotationale:
Ψ tot = Ψnucl + Ψel + Ψvibr + Ψrot
Prin absorbtia sau emisia de energie moleculele pot suferi tranzitii intre diferite nivele energetice. In functie de cantitatea de energie necesara tranzitiilor acestea sunt de patru tipuri (in ordinea descresterii energiei): tranzitii nucleare, tranzitii electronice, tranzitii vibrationale si tranzitii rotationale ().
ΔE mol = ΔEnucl + ΔEel + ΔEvibr + ΔErot
ΔE nucl > ΔEel > ΔEvibr > ΔErot
Aceasta separare a energiilor este un rezultat al aproximatiei Born-Oppenheimer asupra solutiilor ecuatiei Schroedinger pentru sisteme cuantice polinucleare.
Investigarea acestor tranzitii se face prin metode spectroscopice. De interes pentru analiza calitatii alimentelor sunt metodele spectroscopice care investigheaza tranzitiile electronice, vibrationale si rotationale ale moleculelor ce intra in componenta alimentelor.
O prezentare sistematica a metodele spectroscopice simple si combinate folosite in studiul alimentelor este redata in Tabelul 1.
Tabel 1.Metodele spectroscopice simple si combinate folosite in Studiul alimentelor
|
Nr. crt. |
Informatia oferita |
Metoda spectroscopica (abrevieri) |
Starea si cantitatea probei de analizat |
Observatii |
|
Analiza elementara |
Emisie, absorbtie atomica in flacara, arc electric, plasma (FAAS, GFAAS, ICP-AES) |
Solutie; de ordinul µg sau mg, functie de metal |
Necesita aducerea probei in solutie prin dezagragare;cantitatea de proba (solutie)este cu atat mai mare cu cat se vor analiza mai multe elemente si concentratia lor este mai redusa (doar la FAAS); folosite indeosebi la analiza metalelor. |
|
|
Emisie in plasma cuplata cu Spectrometrie de masa (ICP- MS) |
Solutie; ng sau/pana la µg |
Metodele combinate permit analiza unui numar mai mare de elemente din aceeasi proba, analiza izotopica a elementelor grele. |
||
|
Fluorescenta de raze X |
Solid, maruntita foarte fin;mg. |
Folosita indeosebi pentru analiza elemetelor cu masa atomica mare. |
||
|
Analiza chimica complexa (a substantelor componente cat si a structurii acestora) |
Absorbtia in : |
Solid sau lichid, solutie; mg -g. |
Substantele colorate ( |
|
|
-ultraviolet si vizibil (UV-VIS) |
||||
|
-IR (MIR) -NIR -Raman |
Solid sau lichid, extracte, uneori si gaz; mg-g |
Indeosebi in medii neapoase, probe native sau prelucrate, posibiliate de cuplare cu metodele cromatografice; informatii asupra configuratiei proteinelor si polizaharidelor. |
||
|
-Rezonanta magnetica nucleara (RMN) |
Solid, lichid, extracte,cantitati mari, de ordinul g. |
Se poate utiliza materialul in stare nativa; rezultate mai bune la analiza in stare lichida. |
||
|
-Sp.de masa - Sp. de masa cuplata cu cromatografia de gaz (GC-MS) sau lichide (LC-MS) |
Extracte solide sau lichide; ng-μg-mg |
Separare izotopica a elementelor usoare, identificare structurii chimice, determinari de cantitati foarte mici, de ordinul ng (10-9g) sau pg (10-12g) |
||
|
Analiza starii fizice |
-RMN -RES (Rezonanta electronica de spin) - IR(MIR) -Dicroism circular (DC) |
Stare nativa, g de substanta Solutie optic activa; mg-g. |
Calcularea raporturilor starilor cristaline/amorfe, vascozitate, starea dielectrica,conformatia moleculelor de polizaharide si proteine. Analiza conformationala a proteinelor, determinarea cantitativa a glucidelor si altor substante optic active. |
1.1. Radiatiile electromagnetice
Radiatiile electromagnetice pot interactiona cu substantele prin fenomene de absorbtie, dispersie, reflexie si difractie. La randul lor substantele aduse in anumite conditii energetice pot emite radiatii electromagnetice.
Fenomenele de absorbtie si emisie a luminii sunt insusiri caracteristice materiei, respectiv atomilor si moleculelor.
Pe baza lor se poate realiza atat analiza calitativa a unor elemente sau substante prezente in alimente in diferite cantitati cat si analiza cantitativa a acestora.
Radiatia electromagnetica este caracterizata de lungimea de unda (λ), a carei marime delimiteaza domeniile spectrale de interes in metodele spectroscopice de analiza (Tabelul 2).
Pe langa notiunea lungime de unda (λ), se utilizeaza si notiunea de numar de unda (ν*), care este proportional cu energia radiatiei, intre ele existand relatia
ν* = 1/ λ = ν/c, c fiind viteza luminii in vid (3.108 m/s)
sau ν*( cm-1) = 10 000/ λmm
respectiv λ mm ν* cm
ν* se exprima in cm-1 si 1 cm-1 = 2,8564 cal/mol
Tabel 2. Domeniile spectrale de interes in spectroscopie (Skoog, D.A., Leary J.J., 1996, p. 63; Stefanescu M., 1998 p. 110 )
|
Regiunea spectrala |
Lungimea de unda (numar de unda) |
Tranzitia |
|
Raze X |
< 200 nm (< 0,2 mm) |
Ruperea legaturilor dintre atomi |
|
UV/Visibil |
200-800 nm mm) |
Electronica, la nivelul legaturii interatomice ( molecular) |
|
Infrarosu (IR) Apropiat (NIR) Mediu (MIR) Indepartat (FIR) |
mm mm (12 800-4000cm-1) mm(4000-400 cm-1 ) mm (400-10 cm-1) |
Vibrationala, la nivel molecular |
|
Domeniul uzual |
mm (4000-670 cm-1 ) | |
|
Microunde |
> 1000 mm MW < 1 m |
Rotationala, la nivel molecular |
|
Radiofrecventa |
1-5 m |
RMN/RES, in camp magnetic |
Realizarea si analiza fenomenelor spectroscopice se face cu ajutorul spectrometrului. Procesele de baza ce stau la baza unui spectrometru sunt (Wilson R.H., 1994, p.2):
a- excitarea
b- colectarea si ordonarea
c- detectarea
Ordinea acestora poate diferi, functie de echipament, dar intotdeauna procesul de excitare a substantei este inaintea procesului de detectare a efectului
Excitarea
In timpul acestui proces are loc cresterea starii energetice a probei, care se poate realiza prin diferite tehnici, specifice fiecarei metode spectroscopice.
In spectroscopia de emisie cresterea starii energetice a probei se poate realiza pe cale termica (incalzire, flacara, arc electric, plasma), in spectroscopia de masa excitarea energetica se realizeaza prin bombardarea cu electroni sau atomi usori, in spectroscopia RMN pulsatorie excitarea se realizeaza prin iradiere, similar cu luminescenta, dar la alte energii ale radiatiilor.
Cresterea
starii energetice prin absorbtia cuantificata a radiatiilor
electromagnetice ce iradiaza proba sta la baza metodele
spectroscopice de absorbtie in domeniile UV,
Un alt mod de excitare a probei are la baza comportarea radiatiei ca particula. Fotonul in ciocnirea sa cu moleculele sau atomii substantelor din proba sufera fenomenul de imprastiere.
In urma acestei interactiuni neelastice (energia cinetica transformandu-se in alte forme de energie) a fotonului cu atomii sau moleculele probei are loc modificarea frecventei fotonului cat si starea energetica a substantelor din proba.
Fenomenul este folosit in spectroscopia Raman, oferind informatii pretioase asupra structurii moleculare (complementare spectroscopiei in IR).
Colectarea si ordonarea
Procesul de colectare si ordonare a informatiilor spectrale rezultate in urma procesului anterior poate fi considerat ca "inima" spectroscopiei (Wilson R.H., 1994, p.3).
Aceste informatii sunt colectate intr-un spectru, care reprezinta o ordonare a fotonilor sau altor particule dupa energie.
Exprimarea energiei se poate face sub forma de lungime de unda (λ), numar de unda (ν*), frecventa (ν), raportul m/z sau alte forme, in functie de metoda spectroscopica.
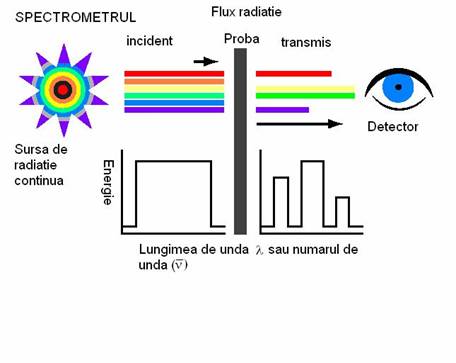
Fig 1. Schema de principiu a obtinerii unui spectru de absorbtie
Ca tehnica de lucru intr-un spectrometru, colectarea si ordonarea datelor energetice se poate realiza prin doua metode: metoda masurarilor secventiale si metoda masuratorilor multiplex.
Masuratorile secventiale constau in masurarea si colectarea secventiala a informatiilor energetice. Ele au fost folosite la primele aparate si sunt mai avantajoase atunci cand se masoara energii relativ mari, pana in domeniul vizibil.
Astazi
aceasta tehnica este folosita indeosebi in spectrometrele
dispersive, in domeniile UV,
Masuratorile multiplex constau in masurarea simultana a tuturor semnalelor spectrale si se pot aplica benefic doar atunci cand semnalul de zgomot este independent de semnalul analitului, ceea ce se intampla indeosebi la energii mici, in domeniul IR, RMN. In cazul acestor masuratori, pentru obtinerea unui spectru conventional care sa reprezinte ordonarea particulelor dupa energie (Intensitate versus frecventa) este necesara prelucrarea datelor printr-o operatie matematica cunoscuta sub numele de transformarea Fourier.
Detectarea
Detectarea
informatiilor energetice rezultate in urma proceselor de excitare a
sistemelor cuantice reprezentate de proba se realizeaza cu
diferiti detectori, specifici fiecarui tip de spectrometrie.
Cerintele impuse acestora se
refera indeosebi la reproductibilitatea si
1.3. Spectroscopia tranzitiilor vibrationale moleculare
Tranzitiile vibrationale moleculare de pe starea fundamentala pe prima stare energetica excitata corespund domeniului radiatiilor infrarosii medii (MIR), cu lungimi de unda cuprinse intre 2,5-25 mm. Overtonurile (tranzitiile de pe starea energetica fundamentala pe stari energetice superioare) cat si combinatiile modurilor vibrationale se situeaza in infrarosul apropiat (NIR) cu lungimi de unda cuprinse intre 0,8-2,5 mm iar infrarosul indepartat cu lungimi de unda cuprinse intre 25-1000 mm corespunde miscarii scheletului polimeric sau a miscarilor de rotatie. Corespondenta cu energia nivelelor vibrationale exprimata prin numarul de unda se poate vedea in Tabelul 2.
In cazul oscilatorului armonic ideal overtonurile si combinatiile nu ar trebui sa apara in spectrul IR. Teoretic aceste absorbtii sunt interzise de regulile de selectie ale mecanicii cuantice. In mod practic insa aceste aborbtii apar, datorita anarmonicitatii sau rezonantei Fermi dar au intensitati slabe. Daca nu ar fi posibila aparitia acestor absorbtii nu ar exista spectroscopia NIR, deoarece toate frecventele fundamentale de vibratie se situeaza in domeniul MIR al spectrului infrarosu. Intensitatea overtonurilor scade drastic o data cu cresterea ordinului acestora. Vibratiile cu frecvente inalte (vibratiile legaturii O-H de exemplu) deoarece au putine overtonuri au si intensitati ridicate ale acestora an regiunea NIR a spectrului infrarosu. Pe langa legatura O-H si celelalte legaturi ale hidrogenului cu nemetale C-H, N-H, P-H, S-H, cat si legatura C=O, datorita anarmonicitatii pronuntate si numarului redus de overtonuri, prezinta absorbtii puternice inacest domeniu spectral.
Cele mai
deosebite aplicatii din ultimii 80 de ani in analiza alimentelor au fost
realizate in domeniul NIR al radiatiilor infrarosii (
Spectroscopia Raman se bazeaza pe ciocnirea neelastica a fotonilor cu moleculele si are frecventele de vibratie tot in domeniul IR. Desi initial s-a utilizat doar la studiul structurii moleculare, fiind complementara spectroscopiei IR, a inceput sa fie folosita si in studiul alimentelor. In spectrul IR apar doar frecventele vibratiilor care produc o variatie a momentului de dipol molecular, manifestandu-se indeosebi legaturile polare (C-H, C=O, C-N, O-H, N-H, C-X ), pe cand in spetrul Raman apar frecventele vibratiilor care produc o variatie a polarizabilitatii moleculare, putandu-se manifesta indeosebi legaturile simetrice nepolare (C-C, C=C). Semnalul apei fiind foarte slab in spectrul Raman permite determinarea altor componenti la continuturi foarte variate in apa a alimentelor.
Spectrometria in domeniul spectral infrarosu (IR)
Spectrometriei in domeniul infrarosu al spectrului radiatiilor electromagnetice ii corespunde spectroscopia vibrationala si rotationala. Atat din punct de vedere al aplicatiilor, dinamici moleculare cat si al echipamentelor folosite, acest domeniu se poate subimpati in trei:
- infrarosul apropiat (near infrared, NIR) caruia ii corespunde intervalul mm (12 800-4000cm-1), corespunzator overtonurilor si combinatiilor frecventelor de vibratie din domeniul infrarosului mijlociu.
- infrarosu mijlociu (mid infrared, MIR) caruia ii corespunde intervalul
mm(4000-400 cm-1 ) de lungimi de unda si este specific miscarii vibrationale a moleculei;
- infrarosul indepartat (far infrared, FIR) caruia ii corespunde intervalul mm (400-10 cm-1) de lungimi de unda si este specific miscarii rotationale a moleculelor.
1.3.2. Domeniul infrarosului mijlociu (MIR)
Fiecare legatura chimica dintr-un compus absoarbe in mod caracteristic in acest domeniu, intensitatea si frecventa absorbtiei depinzand de intreaga structura moleculara. Astfel spectrul in IR poate fi considerat o autentica amprenta a fiecarei substante, neexistand doua substante cu acelasi spectru IR. Deoarece fiecare legatura chimica poate vibra in moduri diferite, figura 11 (alungire, deformare, rasucire, etc.), unei legaturi chimice pot sa-i corespunda mai multe frecvente in spectrul IR. Pentru ca o vibratie sa fie IR activa, ea trebuie sa produca o deformare a momentului de dipol molecular, ceea ce are loc indeosebi la legaturile polare, care prezinta absorbtii puternice in IR. Vibratiile legaturilor nepolare cat si vibratiile simetrice nu sunt IR active, adica acestea nu apar in spectrul IR, ele prezentand insa absorbtii in spectrul Raman. Cei mai importanti factori moleculari care determina intensitatea si frecventa absorbtiei sunt ordinul de legatura si tipul atomilor ce formeaza legatura. Conjugarea sau atomii invecinati pot insa influenta intr-o oarecare masura pozitia si intensitatea absorbtiei. Astfel este posibila atribuirea unui domeniu de frecvente pentru diferite grupari functionale, aflate in molecule diferite. Aceste informatii sunt prezentate in tabele de absorbtie IR.In aceste tabele pentru exprimarea intensitatii absorbtiei se folosesc urmatoarele prescurtari (provenite din limba engleza): s (puternic-strong), m (mediu-medium), w (slab-weak), br (larg-broad), sh(umar-should).
Vibratii de alungire (intindere) a legaturilor
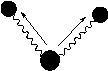

simetrice asimetrice
Vibratii de deformare unghiulara
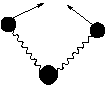
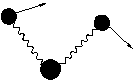
Pendulare simetrica in plan Pendulare asimetrica in plan
(forfecare)

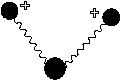
Pendulare simetrica Pendulare asimetrica in afara planului
in afara planului (basculare) (rasucire)
Fig 2.Cateva tipuri de vibratii ale legaturilor (Skoog, p.277)
Tabelul 3. Gruparile functionale si absorbtiile in MIR
|
Grup functional |
Numar de unda (cm-1)/ tip de vibratie |
Intensitate |
Alcani, grparile alchil-C-H -CH2 -CH3 |
3000-2840, stretch ~1465, bend ~ 1375, bend |
Mediu-puternic Mediu-puternic Mediu-puternic |
Alchene=C-H =C-H C=C |
3095-3010, stretch 100-650, bend (oop) 1660-1600, bend |
Mediu-puternic Mediu-puternic Mediu-puternic |
AlchinesC-H sC-H -CsC- |
3300, stretch 650-600, bend 2150, stretch |
Puternic Puternic Medium |
Halogenuri de alchilC-F C-Cl C-Br C-I |
1400-1000,stretch 785-540, stretch 650-510, stretch 600-485, stretch |
Puternic Puternic Puternic Puternic |
AlcoliO-H C-O-H C-O |
3400-3300, stretch 1440-1220, bend 1260-1000, stretch |
Puternic Larg- slab Medium |
Aromatic=C-H =C-H C=C |
3050-3010, stretch 900-690, bend (oop) 1600-1475, bend 2000-1667, overtones |
Medium Slab- medium Mediu-puternic slab |
EteriC-O |
1300-1000,stretch |
Puternic |
AldehideC=O C=O + α or β C=C Ar-CH=O |
1740-1725, stretch 1700-1680, stretch 1700-1660, stretch |
Puternic Medium Puternic |
|
Cetone C=O C=O + α or β C=C Ar-CR=O C=O |
1720-1708, stretch 1700-1675, stretch 1700-1680, stretch 1300-1100, bend |
Puternic Puternic Puternic Medium |
AmineN-H N-H C-N |
3500-3300, stretch 1640-1560, bend in 1s amines, 1500 for 2s amines 1350-1000, stretch |
Medium Medium Medium slab - Medium |
AmideC=O N-H N-H |
1680-1630, stretch 3350-3180, stretch-2 bands for 1s 3300, stretch-1 band for 2s 1640-1550, bend |
Puternic Puternic Puternic Puternic |
Acizi carboxiliciO-H C=O C-O |
3400-2400, stretch 1730-1700, stretch 1320-1210, bend |
Puternic, f. larg Puternic-larg Medium |
EsteriC=O C=O + α or β C=C Ar-COR=O C-O |
1750-1735, stretch 1740-1715, stretch 1740-1715, stretch 1300-1400, stretch |
Puternic Puternic Puternic Mediu-puternic |
Cloruri acideC=O C-Cl |
1810-1775, stretch -unconjugated 1780-1760, stretch-conjugated 730-550, stretch |
Puternic Puternic Puternic |
AnhidrideC=O C-O |
1830-1800 & 1775-1740, stretch 1300-900, stretch (multiple) |
Variabil Puternic-larg |
NitriliCsN |
2250, stretch |
Medium |
Nitro compusiNO2 |
1600-1530, asymmetric stretch 1390-1300, symmetric stretch |
Puternic Medium |
La modul general un spectru IR poate fi impartit in doua regiuni:
Regiunea peste 2000 cm-1, ce contine relativ putine picuri (absorbtii) dar de intensitate mare si caracteristice legaturilor C-H, N-H, O-H din diferite grupari functionale.
Regiunea sub 2000 cm-1, ce contine un numar mare de picuri, de intensitati variabile si care se mai numeste si regiunea de amprenta (fingerprint) deorece este caracteristica fiecarei substante .
In aceasta regiune absoarbe foarte puternic, la cca. 1700 cm-1 gruparea carbonil si la cca. 1200 cm-1 legatura C-O (uzual 2 picuri).
1.3.3. Spectrometria FT-IR (spectrometria in IR cu transformata Fourier)
La modul general un spectru de absorbtie al unei substante reprezinta reprezentarea grafica a variatiei intensitatii energiei absorbite (exprimata prin absorbanta sau transmisie) functie de lungimea de unda (Figura 12).
A B
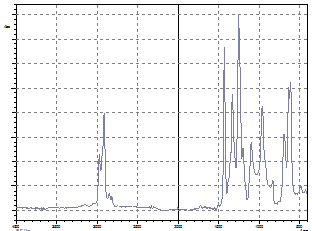
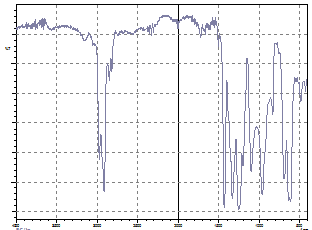
Fig 3. Specrul IR al unei probe de PVC (a-absorbanta, b-transmisie)
Tehnicile spectrometrice clasice in IR se bazau pe metoda dispersiva (Figura 13), in care radiatia continua a sursei era separata in componente cu ajutorul unei prisme sau retea de difractie (monocromatorul). La spectrometrele in IR clasice, dispersive, la care sursa deobicei are o intensitate mai redusa, monocromatorul se afla inainte de detector, pentru ca prin proba sa treaca o cantitate cat mai mare de energie (radiatie). Datorita dezavantajelor prezentate de aceasta metoda, constand indeosebi in timpul lung necesar inregistrarii spectrului, raportului scazut intre semnal/zgomot, s-a dezvoltat tehnologia masurarii simultate a frecventelor pe baza codarii cu ajutorul interferometrului. Prin aceasta timpul de inregistare s-a redus de la citeva minute la secunde sau chiar mai putin de o secunda. Intr-un spectrometru FTIR se inregistreaza interferograma semnalului probei care masoara simultan toate frecventele absorbite. Interferograma digitizata este preluata de un computer unde este decodata prin aplicarea functiilor Fourier, reultand in final un spectru obisnuit.
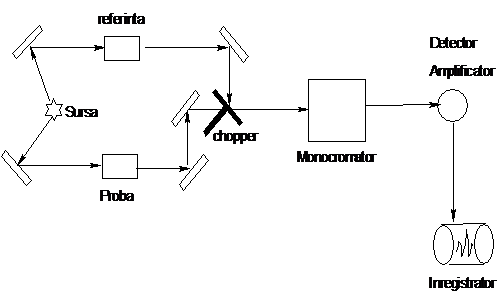
Fig 4. Spectrometrul dispersiv cu dublu fascicul
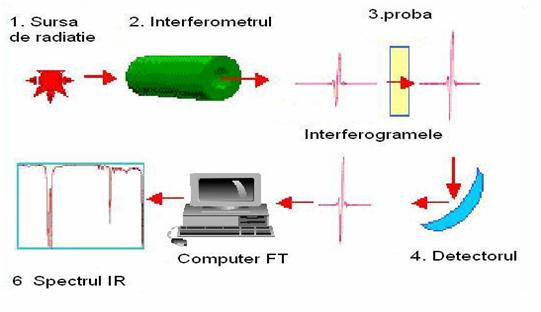

Fig 5.Schema de principiu a unui Spectrometrul FT IR (Brian C. Smith, Fundamentals of Fourier Transform Infrared spectroscopy, CRC press, Boca Raton, 1996.) si spectrometrul FTIR S 8400 Shimadzu pe care au fost realizate masuratorile.
Interferometrul utilizeaza un separator de radiatie (beam spliter) care desface radiatia incidenta in doua. Una din ele este refelctata de o oglinda plana fixa iar cealalta este refelctata deasemenea de o oglinda plana care insa se misca pe o distanta de cativa mm fata de cealalta. Cele doua radiatii reflectate de oglinzile respective se recombina rezultand o interferograma. Aceasta are codate toate frecventele radiatiei incidente. Interferograma poate fi reflectata sau absorbita de proba cand frecventele caracteristice, continute codat in interferograma, sunt absorbite de vibratiile caracteristice grupului functional al moleculei din proba. Rezulta astfel un semnal in IR caracteristic, unic pentru proba respectiva. Acest semnal este masurat de detector, dar el nu poate fi prelucrat direct ci este necesara decodarea lui prin aplicarea tehnicii matematice cunoscuta ca Transformarea Fourier (FT). Aceasta decodare necesitand calcule laborioase se realizeaza cu ajutorul computerului rezultand in final un specru normal.
|
Politica de confidentialitate |
| Copyright ©
2025 - Toate drepturile rezervate. Toate documentele au caracter informativ cu scop educational. |
Personaje din literatura |
| Baltagul caracterizarea personajelor |
| Caracterizare Alexandru Lapusneanul |
| Caracterizarea lui Gavilescu |
| Caracterizarea personajelor negative din basmul |
Tehnica si mecanica |
| Cuplaje - definitii. notatii. exemple. repere istorice. |
| Actionare macara |
| Reprezentarea si cotarea filetelor |
Geografie |
| Turismul pe terra |
| Vulcanii Și mediul |
| Padurile pe terra si industrializarea lemnului |
| Termeni si conditii |
| Contact |
| Creeaza si tu |