
GLUCIDE. REACTII CARACTERISTICE DE IDENTIFICARE
1.Consideratii generale
Glucidele sunt substante cu functiuni mixte, care contin in molecula lor grupari carbonilice si grupari hidroxilice. Ele sunt polihidroxialdehide sau polihidroxicetone. Sub aspectul compozitiei, cu exceptia unor derivati azotati, sunt substante ternare, formate din carbon, hidrogen si oxigen. Alaturi de lipide si protide, reprezinta constituentii de baza ai materiei vii.
Glucidele constituie o clasa de substante naturale, universal raspandite in organismele vegetale si animale, alcatuind cea mai mare parte a substantei organice de pe pamant. Peste 65% din substantele care intra in alcatuirea celulelor si tesuturilor vegetale sunt glucide.
Sub aspect biochimic si fiziologic, glucidele prezinta importanta deosebita, avand rol structural si energetic important.
Glucidele(hidratii de carbon) se impart in trei clase:
Monozaharide;
Oligozaharide;
Polizaharide.
Monozaharidele sunt polihidroxialdehide sau polihidroxicetone, cu grupa carbonil in parte modificata prin formare de semiacetali interni.
Oligozaharidele sunt derivati functionali ai monozaharidelor cu caracter de eteri, rezultati din unirea a doua sau mai multe molecule de monozaharide, prin eliminare de apa. Legatura dintre moleculele de monozaharide in oligozaharide se face prin atomi de oxigen.
Polizaharidele sunt compuse dintr-un numar mare de monozaharide, unite in acelasi mod, adica prin atomi de oxigen.
Reactiile caracteristice glucidelor se datoreaza gruparilor aldehidice sau cetonice, gruparilor hidroxilice primare sau secundare si legaturilor chimice realizate prin participarea acestor grupe functionale.
Reactiile chimice care se utilizeaza pentru recunoasterea, identificarea si dozarea glucidelor sunt reactii de culoare, condensare, deshidratare, oxidoreducere, hidroliza etc.
2.Extragerea glucidelor din produse alimentare
Extragerea monoglucidelor si a oligoglucidelor din alimente si produse alimentare se poate realiza atat prin presare, cat si prin tratarea produsului respectiv cu diferiti solventi.
2.1.1. Extractia prin presare se aplica produselor (alimentelor) cu continut mare in apa si in glucide solubile. In urma presarii se obtine un suc, care contine glucide solubile si alte substante solubile in apa, existente in materialul de analizat. Uneori, acest suc se utilizeaza la dozarea glucidelor prin metode rapide, cum sunt cele refractometrice si densitometrice. Rezultatele acestor masuratori sunt orientative, de apreciere generala, datorita prezentei substantelor neglucidice existente in sucul primar supus analizei.
2.1.2. Extractia cu solventi specifici. Aceasta metoda se utilizeaza cel mai frecvent in scopuri analitice si industriale. Ca solventi se folosesc: apa la 75 - 800C sau etanolul la temperatura de fierbere.
a. Extractia apoasa la cald cu defecare. Prin aceasta metoda se obtine un extract primar cu un grad mai mare de puritate decat prin presare, intrucat prin procesul de defecare (lat. defecare = desfacere, purificare) se indeparteaza substantele neglucidice (acizi organici, protide, amine, alcaloizi etc.) cu ajutorul unor reactivi numiti defecanti.
b. Extractia alcoolica se foloseste mai ales pentru produsele cu continut ridicat de amidon sau in scopuri microanalitice. Amidonul este insolubil in etanol si astfel se inlatura posibilitatea antrenarii sale in extract, ceea ce nu se poate evita in cazul extractiei apoase.
In cazul microanalizei glucidelor se aplica extractia alcoolica, deoarece etanolul are un dublu rol, atat de extractant, cat si de defecant, astfel ca se evita pierderile de glucide care s-ar produce prin operatii de reextragere si purificare. Extractul alcoolic poate fi tratat cu schimbatori de ioni, care scot eventualii anioni si cationi existenti in extract sau cu carbune activ, pentru inlaturarea pigmentilor solubili in etanol.
3. Reactii de identificare a glucidelor
Diferitele tipuri de glucide pot fi identificate prin diverse reactii si metode, dintre care metodele chimice (reactii de culoare, deshidratare, oxidoreducere etc.) si cele fizico-chimice (refractometrie, polarografie, densitometrie etc.) sunt cele mai des utilizate.
3.1.Reactii de culoare
Reactiile de culoare ale glucidelor au la baza reactii de deshidratare si de condensare, cu formare de compusi colorati. Unele reactii sunt generale (pentru toate grupele de glucide), altele sunt caracteristice numai pentru anumite glucide.
Sub actiunea acizilor minerali concentrati (H2SO4, HCl etc.), monoglucidele se transforma in furfurol sau derivati ai furfurolului. Astfel, din pentoze se obtine furfurolul, din metilpentoze se obtine metilfurfurolul, iar din hexoze se formeaza hidroximetilfurfurolul. Furfurolul si derivatii sai reactioneaza cu diferiti fenoli si formeaza produsi de condensare colorati si de aceea aceste reactii se numesc reactii de culoare.
Formula simplificata a furfurolului si a derivatilor sai poate fi redata astfel:
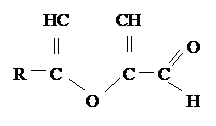
R= H furfurol
R = -CH3 metilfurfurol
R = CH2OH hidroximetilfurfurol
3.1.1. Reactia generala a glucidelor- Reactia Molisch- Udranski
Principiu:
Reactia Molisch - Udranski este o reactie generala pentru toate glucidele. Monoglucidele, oligoglucidele si poliglucidele dau cu a-naftolul, in prezenta acidului sulfuric concentrat, compusi colorati in violet. Oligoglucidele si poliglucidele, in prezenta acidului sulfuric, la inceput se hidrolizeaza pana la monoglucide, iar acestea prin deshidratare, se vor transforma in furfurol sau derivatii sai.
In urmatoarea schema se reda obtinerea hidroximetilfurfurolului din glucoza si condensarea acestuia cu a-naftolul.
Reactii chimice:
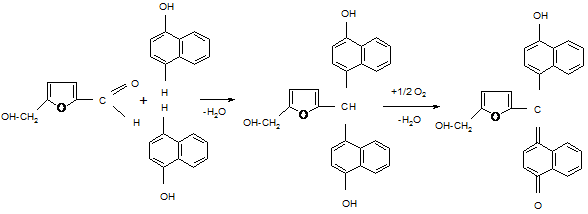
Experienta: Substante necesare:
solutie 1% a - naftol in alcool etilic (proaspat)
solutii de glucide 1 - 2% glucoza, fructoza, arabinoza, zaharoza, amidon etc.
Mod de lucru:
Experienta se executa cu diferite glucide. Se iau mai multe eprubete si in fiecare se introduce cate 1 ml din solutia glucidei de cercetat. Se adauga apoi 3-4 picaturi din solutia de a - naftol si se agita continutul eprubetei. Se toarna apoi in fiecare eprubeta cu atentie, inclinand eprubeta, cate 1 ml acid sulfuric concentrat, in asa fel, incat sa se prelinga pe peretii interiori ai eprubetei si sa nu se amestece cu continutul eprubetei. La limita de separare a celor doua lichide se formeaza un inel rosu - violet.
Acidul sulfuric fiind mai dens se lasa in partea de jos a eprubetei, iar solutia glucidelor va fi deasupra acidului sulfuric.
Reactia este pozitiva si cu glicoprotide si nucleoprotide, deoarece aceste substante contin in molecula lor monoglucide.
3.1.2.. Reactia de diferentiere a cetozelor de aldoze. Reactia Selivanov
Principiu:
Aceasta reactie permite identificarea cetozelor atat libere, cat si combinate. Ea se bazeaza tot pe formarea furfurolului sau a derivatilor sai sub actiunea acizilor tari minerali. In reactia Selivanov se foloseste HCl concentrat, iar ca fenol rezorcina.
Cetozele reactioneaza mai activ decat aldozele; coloratia ce o dau cu rezorcina apare de 20 de ori mai repede decat in cazul aldozelor.
Experienta: Substante necesare:
solutie de glucoza 1%
solutie de fructoza 1%
reactiv Selivanov (0,1 g rezorcina + 10 ml apa + 10 ml HCl)
Mod de lucru:
Experienta se executa simultan cu glucoza si fructoza. Se introduce 1 ml solutie de glucoza intr-o eprubeta, iar in alta 1 ml solutie de fructoza. Se adauga in ambele eprubete cate 2 ml reactiv Selivanov. Se introduc eprubetele intr-o baie de apa fierbinte timp de 15 minute. Solutia de fructoza se coloreaza repede in rosu deschis, cea de aldoza mult mai incet.
Reactii chimice:
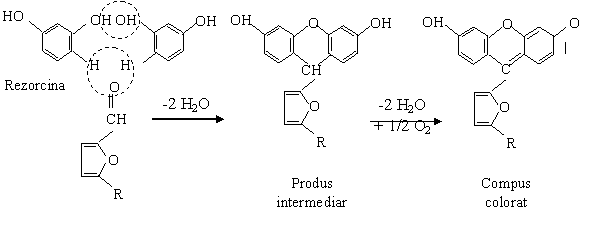
Experienta se poate executa si cu acid clorhidric diluat 1:1,dar in acest caz se pun 2 - 3 picaturi de glucide la 2 ml reactiv Selivanov.
Eprubetele se incalzesc 15 minute pe baia de apa sau direct pe flacara.
3.1.3.. Reactia Thomas
Principiu:
Reactia se bazeaza pe formarea unui produs de condensare caracteristic colorat in albastru, intre b-naftol si furfurol; derivatii furfurolului dau produsi de culoare bruna caracteristica.
Experienta: Substante necesare:
solutie de b-naftol 0,3% in H2SO4 concentrat
solutie de glucoza 1%
solutie de arabinoza 1%
Mod de lucru:
Se introduce intr-o eprubeta 1 ml glucoza, in cealalta 1 ml arabinoza. Se adauga cu atentie ca si in cazul reactiei generale, cate 1 ml acid sulfuric concentrat, care contine b-naftol. In eprubeta cu pentoza se formeaza un inel albastru, la nivelul separatiei intre cele doua lichide, apoi se coloreaza asemanator tot stratul de acid sulfuric. In cazul hexozelor apare un inel si o coloratie bruna - verzuie necaracteristica.
3.2. Reactii de oxidoreducere
Monoglucidele si oligoglucidele reducatoare manifesta caracter reducator datorita gruparilor carbonilice pe care le contin, respectiv gruparilor semiacetalice libere. Aceste tipuri de glucide reduc in mediu alcalin si la cald, sarurile metalelor grele (Ag, Cu, Hg, Bi etc.) si unele substante organice (acid picric, indigo etc.). Caracterul reducator este mai pronuntat la monoglucide si scade cu cresterea masei moleculare a oligoglucidelor.
La monoglucide, caracterul reducator scade concomitent cu cresterea masei moleculare, fiind mai accentuat in mediu alcalin, slab in mediu neutru si nu apare in mediu acid, sub pH=3-4.
Oligoglucidele nereducatoare pot deveni reducatoare in urma reactiei de hidroliza, prin care are loc scindarea oligoglucidei in monoglucidele componente. In cazul zaharozei, care este o diglucida, in mediu acid sau sub actiunea enzimelor(zaharaza),se poate transforma in glucoza si fructoza.
![]()
3.2.1. Reactia oglinzii de argint (Tollens)
Principiu:
Glucidele reducatoare reduc argintul din combinatiile lui la argint metalic.
Astfel, glucidele reduc hidroxidul diaminoargentic la argint metalic, gruparea carbonilica (semiacetalica), oxidandu-se la gruparea carboxilica.
Reactii chimice:
![]()
Hidroxidul diamino-argentic se obtine prin dizolvarea in hidroxid de amoniu a oxidului de argint rezultat din sarurile de argint in mediu alcalin.
![]()
Experienta: Substante necesare:
- azotat de argint (2%)
- hidroxid de sodiu (5%)
- hidroxid de amoniu (diluat)
- glucide reducatoare (glucoza 2%)
Mod de lucru:
Intr-o eprubeta curata se pun 2 ml solutie de azotat de argint si se adauga, picatura cu picatura, hidroxid de amoniu diluat, pana la dizolvarea precipitatului de oxid de argint ce se formeaza initial. Trebuie sa se evite adaugarea unui exces de hidroxid de amoniu. Se adauga apoi o cantitate de hidroxid de sodiu egala cu 1/10 din volumul solutiei si la sfarsit 2-3 ml solutie de glucoza. Se amesteca si se lasa cateva minute pe baia de apa (60-800C). Daca peretii eprubetei au fost curati, argintul metalic care se separa se depune sub forma de oglinda, in caz contrar se depune un precipitat negru.
3.2.2. Reactia de reducere a sarurilor cuprice
Glucidele reducatoare reduc cuprul din combinatiile cuprice pana la cupru monovalent (combinatii cuproase). Acest principiu sta la baza celor mai importante reactii prin care se pune in evidenta caracterul reducator al glucidelor, reactia Fehling si reactia Trommer.
3.2.2.1. Reactia Trommer
Principiu:
In reactia Trommer, glucida reducatoare actioneaza asupra hidroxidului cupric
Lucrandu-se in mediu alcalin, hidroxidul cupric albastru ce se formeaza prin actiunea hidroxidului de sodiu asupra sulfatului de cupru, este redus la hidroxid cupros, care pierzand apa, se transforma in oxid de cupros rosu (Cu2O).
Reactii chimice:
![]()
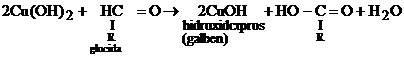
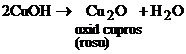
Experienta- Substante necesare
- sulfat de Cu (10%)
- hidroxid de sodiu (10%)
- glucoza sau alta glucida reducatoare (1%)
Mod de lucru:
2 ml de glucoza se alcalinizeaza cu 2 ml hidroxid de sodiu, apoi se adauga sulfat de cupru, picatura cu picatura, pana la formarea unui precipitat albastru.
Amestecul obtinut se incalzeste pana aproape de fierbere, iar in acest timp isi schimba culoarea in rosu, datorita aparitiei oxidului cupros.
3.2.2.2. Reactia Fehling
Principiu:
Hidroxidul cupric este in prealabil dizolvat in tartrat dublu de sodiu si potasiu sub forma de complex cupro-tartric.
Hidroxidul cupric (albastru) se dizolva in solutia Fehling II (tartrat de sodiu si potasiu + NaOH), cu formarea unei combinatii complexe de culoare albastru intens. In prezenta ozelor, hidroxidul cupric din complex se reduce la hidroxid cupros (galben), apoi la oxid cupros (rosu), iar ozele se transforma prin oxidare in acizi aldonici.
Reactii chimice:
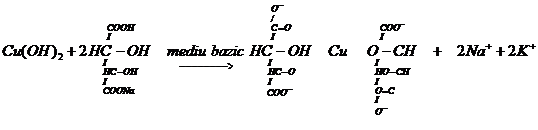
Tartrat de sodiu si potasiu Complex colorat in albastru intens
Experienta: Substante necesare
1. glucoza
2. fructoza
3. maltoza
4. zaharoza
5. lactoza
1 - 5 - solutii apoase 1%.
6. reactiv Fehling I (sulfat de cupru 35 g la 1000 ml solutie)
7. reactiv Fehling II -sare Seignette -(tartrat dublu de sodiu si potasiu 150 g, hidroxid de sodiu 90 g la 1000 ml solutie).
Solutiile Fehling I si II se amesteca numai in momentul intrebuintarii in volume egale.
Experienta se executa simultan cu diferite solutii de glucide. Inainte de inceperea lucrarii, se masoara exact si se amesteca volume egale din solutiile Fehling I si II, iar lichidul albastru - inchis obtinut se toarna in epubete cate 2 ml. Numarul de eprubete este corespunzator numarului de glucide cercetate. In fiecare etapa se adauga apoi 1 ml din glucida de cercetat si se incalzeste la fierbere pana la aparitia unui precipitat galben - brun. In eprubeta cu zaharoza nu se observa nici o schimbare. Prin hidroliza insa (vezi hidroliza zaharozei) se obtine glucoza si fructoza care sunt reducatoare. Cantitatea de precipitat si intensitatea culorii sunt proportionale cu concentratia in monoglucide reducatoare.
Reactia Fehling este utilizata pentru identificarea si dozarea glucozei din lichide biologice.
|
Politica de confidentialitate |
| Copyright ©
2026 - Toate drepturile rezervate. Toate documentele au caracter informativ cu scop educational. |
Personaje din literatura |
| Baltagul caracterizarea personajelor |
| Caracterizare Alexandru Lapusneanul |
| Caracterizarea lui Gavilescu |
| Caracterizarea personajelor negative din basmul |
Tehnica si mecanica |
| Cuplaje - definitii. notatii. exemple. repere istorice. |
| Actionare macara |
| Reprezentarea si cotarea filetelor |
Geografie |
| Turismul pe terra |
| Vulcanii Și mediul |
| Padurile pe terra si industrializarea lemnului |
| Termeni si conditii |
| Contact |
| Creeaza si tu |