Izotopii importanti pentru omenire
Izotopul este specia de atom cu acelasi numar de protoni
dar numar diferit de neutroni. Majoritatea elementelor chimice sunt amestecuri de doi sau mai multi izotopi. Din cele 92 de elemente chimice naturale, 69 sunt amestecuri de izotopi stabili. Numarul elementelor monoizotopice este foarte redus. Dintre acestea fac parte: F, Na, Al, P ,Co, ect. Cuvantul 'izotop' provine din grecescul isos (egal) si topos (loc). Deoarece majoritatea elementelor din natura contin 2 sau mai multi izotopi, s-au efectuat experiente pentru a stabili proportia din fiecare izotop care se gaseste in amestecul de izotopi aflat in natura.Aceste experiente au aratat ca, in majoritatea cazurilor, un anumit izotop se gaseste intr-o proportie mult mai mare decat ceilalti.Izotopii anumitor elemente, au nuclee instabile.Acestia sunt numiti izotopi radioactivi.Izotopii radioactivi ai mai multor elemente usoare pot fi preparati in laboratoare care dispun de acceleratoare de particule de inalta energie.Izotopii radioactici artificiali, cunoscuti de asemenea ca radioizotopi, au fost produsi pentru prima data in 1933 de fizicienii francezi Marie si Pierre Joliot-Curie.Radioizotopii sunt produsi pentru bombardare naturala gasita a atomilor cu particule nucleare, de asemea ca protonii, neutronii, electronii, si particulele alfa, folosind particule accelerator.
Fizicianul de origine britanica, Sir Joseph Thomson a demonstrate in 1912 existenta unor izotopi stabili care, la trecerea completa a neonului are loc o descarcare intr-un tub si o ricosare a ionilor de neon in apropierea mijloacelor campurilor magnetice si electrice; aceasta arata ca elementul stabil de neon exista in mai multe forme. Thomson gaseste doi izotopi de neon, unul cu masa de 20 si celalalt cu masa de 22. Urmatoarele experimente arata ca intamplarea naturala a neonului contine 90% din izotopul de neon cu masa de 20, 9,73% din izotopul cu masa de 22, si 0,27% din izotopul cu masa de 21.
Importanta unor izotopi
Izotopii radioactivi artificiali si naturali constituie un instrument efficient si de mare finite pentru creearea unor procedee extreme de sensibile de analiza si control in industrie, un mijloc unic de diagnoza medicala si de terapie a diferitelor boli, o unelata uimitoare cu care se poate actionaasuprea diferitelor substante.Importanta:
- In metalurgie izotopii sunt utilizati la elaborarea fontelor, a otelurilor si pentru studiul feroaliajelor; astfel, prin adaugarea unui izotop radioactive in aliajele topite se poate face vizibila structura acestora dupa solidificare.
- Cu ajutorul izotopilor se pot descoperi defecte ale unor materiale, se pot controla sudurile, care se utilizeaza fecvent in industria construnctoare de masini
- In domeniul chimiei s-au elaborate o serie de procedee, care se utilizeaza izotopii radioactivi, ce prezinta un mare interes practice, cum ar fi: vulcanizare cauciucurilor, obtinerea unor polimeri cu calitati deosebite, obtinerea unor materiale speciale prin tratarea lemnului si a unor mteriale plastice cu izotopi radioactivi, descompunerea grasimilor, prelucrarea pentrolului etc.
- Izotopii sunt folositi in agricultura, ca metoda de cercetare stiintifica ca in selectia plantelor si pentru cresterea productivitatii acestora; cu ocazia studierii contaminarii radioactive a solului, a plantelor si a animalelor, in vederea elaborarii de metode de combatere a acestei contaminari.S-au realizat diferite aparate, care utilizeaza izotopii, pentru masurarea umiditatii si a densitatii solurilor si a terenurilor.
- In zilele noastre, medicina a devenit un mare utilizator de izotopi radioactivi, atat pentru diagnosticarea si pentru terapia diferitelor boli, obtinandu-se numeroase preparate.Pentru diagnosticarea tumorilor cerebrale se utilizeaza un izotop al fosforului; pentru studiul glandei tiroide se foloseste izotopul radioactive al iodului etc.Frecvent, in tratarea tumurilor canceroase se utilizeaza izotopul radioactive al cobaltului
- In arheologie, pentru datarea diferitelor materiale se utilizeaza izotopul carbonului.
- La industria nucleara(izotopii uraniului,plutoniului si torului)
- Stabilirea tipului de sol(acid sau bazic)
- La determinarea gradului de duritate si de uzura a aliajului pe baza de fier(izotopul carbonului)
Separarea izotopilor aceluiasi element de la unul la altul este dificila. Separarea totala intr-un pas prin metode chimice este imposibila, deoarece izotopii aceluiasi element, au aceleasi proprietati chimice; metodele fizice sunt in general bazate pe deosebiri extrem de mici, in proprietatile fizice au cauzat diferente majore ale izotopilor. Separarea electrolitica si diverse proceduri de schimburi pentru separarea izotopilor, oricat, bazandu-se pe un ritm chimic sau diferente de echilibru, care se bazeaza in mod primar pe diferentele in energie de legaturi chimice, care are un rol al masei izotopilor.
Izotopii de hidrogen, deuteriu (hidrogen -2) si hidrogenul obisnuit (hidrogen -1), primul a fost separat in cantitati apreciabile. Aceasta realizare este acreditata chimistului american Harord Urey, care a descoperit deuteriul in 1932.
De asemenea o revarsare este extrem de flexibila, si elementul poate fi schimbat de la o etapa a separarii inca este dorita. De exemplu, la separarea uraniului, o mare cantitate a materialului trebuie manipulata de la inceput, unde uraniul dorit-235 este amestecat de aproximativ 140 de ori cu toate ca uraniu-238; la sfarsitul procesului, uraniu-235 este aproape pur, si volumul materialului este mult mai mic. Intr-o masura mai mare cu numai schimband snurul, este posibil sa schimb etapele inlocuite pentru completare la o etapa intermediara a acelui material rezultand din imbogatirea preliminara pana la un proces diferit.
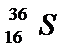
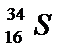
![]()
![]() Izotopii sulfului
Izotopii sulfului
Masa atomica relativa:32
![]() 1 mol atomi de S=6,0255 ·
1 mol atomi de S=6,0255 ·
Atomi de S=32g
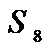
Molecula octoatomica:
Caracterul chimic: Nemetal
Valenta variabila: II, IV, VI
Stare naturala(libera):
- zacaminte subterane
- suprafata scoartei terestre
Sub forma de compusi:
-H2S, SO2, sulfati(CaSO4 ·2H2O: ghipsul)
-Sulfuri: FeCuS2(calcopirita), FeS2(pirita), ZnS(blenda), PbS(Galena)
Sub forma de compusi organici:
- proteine
-vitamina B1
-substante de origine vegetala : mustar, usturoi
|
Politica de confidentialitate |
| Copyright ©
2026 - Toate drepturile rezervate. Toate documentele au caracter informativ cu scop educational. |
Personaje din literatura |
| Baltagul caracterizarea personajelor |
| Caracterizare Alexandru Lapusneanul |
| Caracterizarea lui Gavilescu |
| Caracterizarea personajelor negative din basmul |
Tehnica si mecanica |
| Cuplaje - definitii. notatii. exemple. repere istorice. |
| Actionare macara |
| Reprezentarea si cotarea filetelor |
Geografie |
| Turismul pe terra |
| Vulcanii Și mediul |
| Padurile pe terra si industrializarea lemnului |
| Termeni si conditii |
| Contact |
| Creeaza si tu |