Conduita terapeutica in urgente
Supradozajul este o mare urgenta medicala, pentru ca angajeaza prognosticul vital prin deprimare respiratorie si insuficienta cardiovasculara. De aceea, prima masura consta in spitalizarea intr-un spatiu de reanimare.
Masurile terapeutice indicate in cazul unui pacient comatos sunt:
-asigurarea permeabilitatii cailor aeriene superioare;
-subluxarea mandibulei;
-montarea unei pipe Guedel;
-inceperea miscarilor de asistenta ventilatorie mecanica, daca este nevoie cuplate cu manevre de masaj cardiac extern
-oxigenoterapie.
Daca venele pacientului nu sunt trombozate:
- injectare in bolus intravenous a unei fiole de Naloxona (0,4 mg) cu efect cvasiimediat prin vigilizarea pacientului; apoi se va instala o perfuzie ce va contine 2-4 fiole de Naloxona in 500 mL glucoza izotonica (cu vitamina B1 si B6);
- adaptarea debitului perfuziei se va face in functie de nivelul de vigilenta si de frecventa respiratorie (in absenta edemului pulmonar acut) care trebuie sa fie superioara sau egala cu 14 respiratii/minut (doza orala corespunde cu 2/3 din doza injectata initial).
Daca venele pacientului sunt trombozate:
-se va administra intramuscular o fiola de Naloxona, urmata de reanimarea respiratorie pana la aparitia efectului Naloxonei (cateva minute)
-ulterior se vor repeta injectiile intramusculare in doze de 0.1-0.2 mg de Naloxona, pana cand frecventa respiratorie este inferioara cifrei de 12 respiratii/minut; se va adapta doza de Naloxona in asa maniera incat sa se evite o trezire prea rapida si riscul unei reintoxicatii acute;
-se va supraveghea continuu starea clinica cu monitorizare functiilor vitale.
Masurile terapeutice indicate in cazul unui pacient constient:
- injectarea in bolus a unei jumatati de fiole de Naloxona, apoi asigurarea unei viteze de perfuzie care sa asigure obtinerea unei frecvente respiratorii de peste 14 respiratii/minut;
- daca starea de constienta se estompeaza dupa injectarea de Naloxona, trebuie sa suspectam o anoxie cerebrala prelungita sau coadministrarea de psihotrope deprimante ale sistemului nervos central;
- absenta miozei ne va face sa suspectam ingestia simultana a unei substante atropinice sau a uneia simpatomimetice (cocaine).
Orice coma cu debut brutal si insotita de mioza bilaterala este sugestiva de supradozaj de heroina.
Naloxona suprima apneea si coma din cadrul intoxicatiei acute cu heroina, morfina, codeina, eventual chiar si din cadrul intoxicatiei cu pentazocina si metadona.
Efectele sale adverse sunt reduse: greata, varsaturi, hiperventilatie si in caz de injectare prea rapida, declansarea unui sindrom de sevraj, a unei hipertensiuni arteriale sau in cazul unei doze mai mari declansarea unui edem pulmonar acut.
Nalorfina (N-alil-normomorfina), avand in vedere ca poseda proprietati agoniste partiale, se recomanda administrare cu prudenta, deoarece in caz de eroare diagnostica, ea poate agrava o insuficienta respiratorie existenta.
Atitudinea terapeutica in caz de sevraj
1) Sevrajul heroinic-
Reducerea simptomatologiei in sevraj este psihofarmaceutica ; se disting doua atitudini terapeutice
- utilizarea unui agonist opiaceu
- provocarea sevrajului (farmacologic sau natural)
In practica, se va folosi una din urmatoarele strategii farmacologice :
a) a) oprirea brutala a drogului si utilizarea clonidinei pentru tratamentul sindromului de sevraj
b) b) utilizarea naloxonei pentru inducerea sevrajului si apoi tratamentul cu clonidina
c) c) substitutia drogului prin buprenorfina urmata de oprirea acesteia progresiv sau brutal
d) d) Substitutia prin metadona cu reducerea progresiva a dozelor acesteia
a) Sevrajul fara agonisti opiacei
Pentru tratamentul simptomatologiei de sevraj, in practica se utilizeaza doua categorii de agenti terapeutici specifici si nespecifici
Tratamentul nespecific
Atitudinea terapeutica clasica consta in prescrierea de medicamente care permit controlul simptomatologiei
-antialgice (paracetamol, aspirina)
- spasmolitice (amidopirina)
- antiemetice (metoclopramid, metoprimazina)
- antidiareice (loperamid)
- sedative
- hipnotice
Tratamentul specific
Este vorba in principal de utilizarea de clonidina (catapressan)
Sevrajul antreneaza o hiperfunctionare noradrenergica responsabila de simptomatologie.
Clonidina este un antihipertensiv adrenergic de tip alfa. Ea are un efect benefic semnificativ asupra hipersecretiei lacrimale, rinoreei, transpiratiei, insa are un efect minim (chiar nul) asupra crampelor musculare, insomniei, anxietatii. Va fi deci utila o coprescriptie simptomatica.
Acest tip de tratament, este propus numai in cazurile in care este posibila supravegherea medicala permanenta a pacientului.
b) Inducerea sevrajului prin naltrexona si coprescriptia clonidinei
Clonidina permite tratamentul sindromului de sevraj, dar nu reduce semnificativ durata acestuia si nici nu creste procentajul de succese terapeutice
.Pentru a solutiona aceste doua probleme, se foloseste combinatia clonidina - naltrexona. Deplasarea opiaceelor din receptorii centrali prin naltrexona, va provoca un sevraj rapid si sever. Utilizarea clonidinei inainte si dupa administrarea naltrexonei, permite ameliorarea simptomelor si tratare sindromului de abstinenta.
c )Substituirea toxicului prin buprenorfina, urmata de oprirea acesteia (progresiva sa brutala)
Avantajul metodei consta in faptul ca utilizarea buprenorfinei va provoca un sindrom de sevraj mult mai putin violent decat cel dat de metadona.
Acest lucru faciliteaza acceptabilitatea si accesibilitatea protocolului.
A) A) Substitutia prin metedona, urmata de reducerea progresiva a dozelor
Cea mai frecventa metoda terapeutica este substitutia opiaceelor consumate de pacient prin metadona, urmata de sevrajul la metadona. Avantajele utilizarii acestei metode sunt:
- eficacitatea administrarii orale
- durata lunga de actiune
- prescriptia facila si usor controlata
Metodologia tratamentului prin metadona
Protocolul propus in AMJ Practice Guideline (1995), consta in prescrierea unei doze de 10 mg hipoclorit de metadona la 2-4 ore, in functie de raspunsul pacientului (apreciat prin semnele obiective de sevraj). Dupa atingerea acestei doze de echilibru, metadona va fi redusa progresiv, in trepte de 5 mg pe zi, aceasta atenuand evolutia clinica. Totusi, atunci cand se ajunge la pragul de 20-30 mg/zi, pacientii se plang de reaparitia unor discrete simptome de sevraj, ceea ce ridica problema recidivei.
Inconvenientele acestei metode constau in necesitatea unei autorizatii pentru prescrierea metadonei si in rebound-ul sindromului de sevraj - ceea ce duce frecvent la recidiva.
In ciuda prescrieri sub forma de doze degresive, simptomatologia legata de sevraj nu dispare complet, persistand discret dupa ultima priza. Crampele, durerile musculare, insomnia, vor necesita deci un tratament simptomatic.
Utilizarea concomitenta a clonidinei ca tratament de atac intr-un protocol de dezintoxicare prin metadona, nu este eficient.
Detoxifierea sau tratamentul sindromului de abstinenta, al dependentei fizice, (in regim de internare, ambulator, internare de zi sau contentie) implica protocoale de tratament ce-si propun sa faca suportabil sevrajul[1]. In prevenirea instalarii sindromului de abstinenta se foloseste uzual methadona - timp de 3-5 zile, sau pina la stabilizare, ulterior dozele fiind scazute treptat, asociindu-se si medicamente simptomatice (clonidina, antiemetice - prometazina, metocarbamol pentru ameliorarea crampelor musculare, antiinflamatorii - ibuprofenul scade febra si reduce durerile musculare, antidiareice - kaolin) . Alti agenti folositi pentru detoxifiere sint clonidina, cu scaderea activitatii simpatice centrale, prin administrare la 12 ore a 5mg/kg corp timp de 12 zile, uneori asociata naltrexonei . Efectele neplacute din sevraj mai pot fi reduse si prin administrarea de difenoxilat asociat cu un anxiolitic - hipnotic. Lofexidina, un alt alfa2-agonist, pare a fi mai eficienta, neavind efectul hipotensor intens al clonidinei[4]. Protocolul cu buprenorphine, 2 mg sublingual (desi doze de 8 mg/zi par a creste complianta la tratament si rata de abstinenta - atentie totusi la riscul instalarii sindromului de sevraj fata de buprenorfina la doze de 16 mg-zi), precum si cel cu levomethadil acetat sint in curs de evaluare (studii incomplete aratind ca in circa 80% din cazuri detoxifierea a putut fi considerata reusita), anuntindu-se de perspectiva. In formele usoare de dependenta, la care se prognozeaza cel mult un sevraj de intensitate medie, se poate asocia si naloxona. In formele severe sau cu patologie asociata severa, ce contraindica sevrajul, se prefera cura prelungita peste 10 zile cu levomethadil acetat. Studii largi au aratat eficacitatea relativ apropiata a tuturor acestor medicamente pe termen scurt in reducerea manifestarilor de sevraj, diferentele majore aparind pentru prognosticul indepartat.
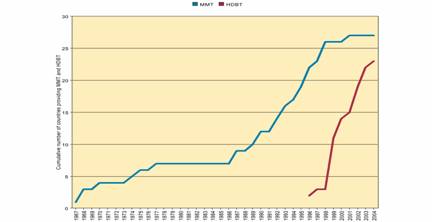

Introducerea pe scara larga a tratamentului cu metadona si buprenorfina
Se discuta inca foarte mult despre rolul fumatului in timpul detoxifierii (plecind de la constatarea ca apar frecvente exceptionale ale fumatului in timpul tratamentului), acesta fiind considerat mult timp ca un trigger al recaderilor, ca un semn al ineficientei tratamentului, dar se pare ca nu se pot face corelatii semnificative statistic.
Metode recente, ce inca trezesc suspiciuni, uneori intemeiate, implica asocierea psihoterapiei cu administrarea de halucinogene, ketamina (2 mg/kg corp, intramuscular - doza halucinogena), ce ar reduce pe termen lung cravingul si ar creste durata mentinerii abstinentei[5]. Se incearca si tratamentul cu Ibogaina, un alcaloid indolic extras din coaja arborelui african Tobernanthe Iboga, cu mecanism de actiune inca neclar (fiind demonstrata cuplarea cu receptori opioizi kappa si sigma, receptorii NDMA si nicotinici), avind efect la circa 1 ora de la administrare ce dureaza circa 8 ore. In doze de 10 mg/kg corp (doze de 100mg/kg corp s-au dovedit neurotoxice, in special la nivel cerebelos) produce o diminuare marcata a semnelor de sevraj, ca si a craving-ului, dar si insomnie si rememorari vizuale ale memoriei de lunga durata .
O noua promisiune, raportat la eficienta ridicata (metoda este intens aplicata in Olanda), este detoxifierea rapida, ce implica un algoritm de tratament in conditii de terapie intensiva, incepind cu administrarea unei premedicatii (clonidina, octreotid, cimetidina) cu rol de a cupa simptomatologia de sevraj consecutiva antagonizarii drogului prin decuplarea de receptori, urmata de sedare si anestezie generala sub intubatie oro-traheala (midazolam). Pe sonda naso-gastrica se administreaza continuu, timp de 4-8 ore, naltrexona, apoi dupa trezirea din anestezie se continua tratamentul cu naltrexona oral. Recent, pentru reducerea simptomatologiei reziduale datorata naloxonei (greata, varsaturi), se tenteaza inlocuirea cu buprenorfina, cu rezultate similare, atit pe termen scurt, cit si la distanta[7].
Sevrajul la nou-nascut se abordeaza cu administrarea de metadona (0,1-0,5 mg/kg/zi), paregoric - solutii diluate de morfina (0,2 ml oral la 3-4 ore), fenobarbital (8 mg/kg/zi), doze care se scad progresiv in 10-20 de zile.
Tratamentul dependentei psihologice cunoaste mai multe laturi, bazindu-se pe principiul "politica raului mai mic". Mentinerea (substitutia) cu analogi opioizi este cea mai aplicata si cea mai veche metoda terapeutica, inca existenta, introdusa in 1964. Programul de substitutie cu metadona (derivat difenilpropilaminic) a fost introdus prima oara la Spitalul Lexington - New York (Programul Synanon) de catre Vincent Doyle si Marie Nyswander. Ei au propus ca medicatie de substitutie metadona si levomethadil acetatul, plecind de la premisa teoretica cunoscuta, ca blocind competitiv efectul euforizant al opiodului si dezvoltarea tolerantei incrucisate, pacientul nu mai intareste comportamentul de cautare a senzatiei, si implicit al drogului prin absenta efectelor scontate si, de asemenea, scade cravingul. Administrata sub forma "acuta", in doza mare, unica si parenteral, are efecte de tip miu, asemanatoare morfinei. Administrata oral, timp indelungat, datorita latentei mari de atingere a virfului de concentratie (2-6 ore), precum si datorita tendintei de stocare in tesuturi, nu va avea manifestarile brutale ale celorlalte opioide si nici nu va declansa un sindrom de abstinenta sever la oprirea administrarii. Nu va declansa cercul vicios al heroinei, administrare - rush - crash - craving. Metadona are si ea un potential apreciabil de creare a dependentei, dar cu manifestari mai putin intense si sevraj mai usor suportat de catre pacient si nu se considera ca inlocuieste o dependenta (la heroina de exemplu) cu o alta. Astfel se elimina calea parenterala de administrare cu toate riscurile ce decurg din ea[8]. Metadona produce o minima euforie, fara sedare si depresie, previne reinstalarea dependentei fizice, deci inlatura noi manifestari de sevraj, ajuta la echilibrarea balantei financiare a pacientului, permite reluarea activitatii. Este ideal sa fie administrata sub forma de sirop galenic, reducindu-se astfel posibilitatea traficului ilegal.
Administrarea incepe in urma semnarii unui contract incheiat intre medic si pacient, si numai pentru cei ce indeplinesc criteriile cerute de legea 143/2000 - v. anexa - in doze echivalente cu cea de drog uzuala (1 mg methadona / 3 mg morfina / 1 mg heroina / 20 mg meperidina). Dozele administrate in urma cu 10 ani erau ridicate (120 mg/zi), ulterior acestea scazind spre 60-100 mg/ zi. Dozele de 90 mg/zi sint urmate de o mentinere in tratament a unui numar de pina la doua ori mai mare de pacienti decit cele mai mici de 60 de mg (80% la o luna, 67% la 3 luni si 52% la 6 luni)[9]. Este necesara permanenta ajustare a dozelor in cazul in care este posibila o modificare a concentratiei plasmatice (scaderea concentratiei sangvine dupa administrarea de rifampicina, fenitoina, barbiturice, carbamazepina, alcool sau cresterea concentratiei sangvine de catre eritromicina, ketoconazol, cimetidina) . Nezodiazepinele cresc biodisponibilitatea metadonei, prin CYP 3A4 Principalele reactii neplacute constau in constipatie, transpiratii, scaderea libidoului, somnolenta.
Eficacitatea terapeutica ramine scazuta, la ani de zile de reevaluare procentul de abstinenta fiind mai mic de 25%, iar pentru cei ce au beneficiat de toate etapele terapiei de pina la 40%[11].
Levometadil acetatul (L alfa acetil metadol), un miu agonist, este introdus in terapia de substitutie din 1993, fiind administrat in doze de 100 mg de 3 ori pe saptamina, recent protocolul fiind implementat si in Danemarca, Spania si Portugalia, cu o rata de mentinere in program de 84% la 3 luni
Tratamentul cu buprenorfina (miu agonist partial) are la baza aceleasi principii, doze mai mari de 8 mg/ zi avind o rata de succes mai buna, fiind principala medicatie de substitutie in Franta. Eficacitatea ei se datoreaza afinitatii ridicate pentru receptorii miu, activitatii intrinseci scazute, timpului prelungit de injumatatire - 32 de ore - cu atingerea unui virf de concentratie la 1 ora[13] si disocierii mici, ceea ce-i confera siguranta in manipularea dozelor, generarea unei minime dependente fizice si flexibilitate in ajustarea dozelor. Efectele administrarii sint asemanatoare celor date de doze mici de morfina, dar niciodata de aceeasi intensitate sau cu depresie respiratorie severa asociata . Preparatele existente, Suboxone, ce contine buprenorfina si naloxona - in proportii de 4 la 1 , sau Subutex, continind buprenorfina, indicat mai ales in debutul tratamentului, se administreaza sublingual, in doza unica, noile protocoale cerind 12-16 mg/zi. Reactiile adverse sint depresia respiratorie (mai ales in administrarea concomitenta a unui opioid sau de alcool), cefalee, sindrom pseudogripal, greata, tulburari de somn[17]. Studiul Iron a urmarit 503 dependenti de opiacee tratati cu 1 mg, 3 mg, respectiv 8 mg de buprenorfina, constatind ca la 6 luni de la initierea tratamentului doar 305 pacienti mai ramasesera in program, dintre care 33,9% dintre cei tratati cu 1 mg, 64,3% dintre cei ce primeau 3 mg si 80,1% din cei tratati cu doze de 8 mg/zi . Un alt studiu franez arata ca la un an, mentinerea in tratament a fost de 75%, ca si procentul celor la care testarile au fost negative, comparativ cu studiile placebo, la care procentele au fost foarte aproape de 0%. Desi costul este mai mare decit tratamentul cu metadona, raportul cost-eficacitate nu difera semnificativ , In Finlanda circa 80% din DRD se datoreaza buprenorfinei, deturnata din uzul medical.
Buprenorfina ramine medicatia de baza in substitutia la gravide, riscul manifestarilor de abstinenta la nou-nascut fiind mult mai redus decit in cazul altor protocoale, si cu participarea sistemului nervs autonom mult mai redusa - au necesitat tratament doar 48% dintr-un lot de 309 de copii ce au fost expusi in utero la buprenorfina, 62% avind manifestari ale sevrajului la circa 12-48 de ore de la nastere , .
Recent, un studiu efectuat la Universitatea Yale, Connecticut, a relevat rolul pe care il are in scaderea manifestarilor din sevraj o neuropeptida numita galanina, scazind eleiberarile noradrenergice de la nivelul locus ceruleus. Plecind de la aceasta constatare a fost sintetizat galnonul, preparat ce se anunta de mare persepectiva in tratarea sevrajului la opioide, dar si ca potential anestezic lipsit de riscuri adictive .
Prescrierea metadonei ca substituent ofera posibilitatea mai multor tipuri de tratament: detoxifiere pe termen scurt, eforturi pe termen lung de mentinere a abstinentei, tratament de intretinere ce-si propune nu abstinenta, ci reducerea dozelor de drog folosite, reducerea frecventei de administrare, reducerea delictelor, stabilizare sociala si psihologica, scaderea riscului de deces (de 7 ori mai mic decit la consumatorii de droguri ce nu beneficiaza de tratament). Farmacocinetica si efectele metadoni sint modificate de diazapam si flunitrazepam, dar nu si de catre oxazepam (substabnta glucuronizata). Are tendinta de a se acumula in tesuturi.
Un studiu comparativ pe doua loturi aflate sub tratament substitutiv cu metadona (doza medie de 81.5±36.4 mg) si buprenorfina (doza medie de 9.2±3.4 mg) a aratat rezultate mai bune (rata mai mare a testelor negative de urina - 32.1% versus 25.6%, rata mai mare de complianta la tratament - 78.2 versus 65.8) .
In ultimii 3 ani, mortalitatea prin metadona a crescut cu 213%. Aceste cazuri trebuie analizate din perspectiva urmatoare: decesul a survenit in prima zi de tratament? Atunci se poate vorbi fie de o sipradoza, fie de malpactice. Decesul a survenit la concentratii in probele biologice sub nivelul letal? Atunci trebuie cautata fie alta cauza de deces, fie posibilitatea administrarii concomitente si a altor substante. Toleranta la depresia respiratorie este doar partiala, si de aici posibilitatea aparitiei riscului de deces la cresterea dozei!!!!
Ca tratament de lunga durata se pot folosi si antagonistii opioizilor, ce decupleaza drogul de pe receptori prin mecanism antagonist. Se foloseste naltrexona, ciclazocina (2 mg de 2 ori pe zi) sau nalmefina ce are actiune mai lunga[25]. Naltrexona este administrata de 3 ori pe saptamina, in doze de 100 mg luni - 100 mg miercuri si 150 mg vinerea, doze ce blocheaza total efectele unei eventuale administrari de heroina, insa rata recaderilor este mare (eficienta la 1 an de 92%, dar cu prabusire la intreruperea administrarii) . Folosirea naltrexonei retard - implant ce elibereaza timp de 6 luni cantitati reduse de substanta, realizind un nivel seric constant de 2 ng/ml - pare a avea rezultate mult mai bune decit preparatele orale, scazind semnificativ incidenta supradozelor (criteriul urmarit de studiul respectiv) din timpul tratamentului de substitutie.[27]
Tratamentul de mentinere cu heroina (practica intilnita in Elvetia, Marea Britanie si Olanda, in Germania din 2001 si in Luxemburg din 2002, si in studiu in Australia, Belgia, Canada, Franta, Spania) este o practica intens contestata si discutabila (aplicata in cazul heroinomanilor cronici refractari la orice tratament, dupa ce toate metodele terapeutice au fost epuizate), intrucit prin oferirea in cadrul programelor terapeutice a heroinei, pacientul ramine atasat de "cultura drogului", este dispus sa-si vinda dozele astfel capatate, creste mortalitatea prin supradoze. Totusi, rezultatele bune obtinute (absenta noilor cazuri de infestare HIV sau cu virusuri hepatitice, precum si rata mare de mentinere in progam - 61,7% la 3 ani) au facut ca aceasta metoda sa fie in curs de extindere . Se citeaza insa numeroase efecte adverse (prurit accentuat, transpiratii, constipatie, tulburari de ciclu menstrual, cognitive, dureri precordiale, crampe musculare, paralizii temporale ale membrelor) in cazul administrarii controlate de diacetilmorfina. De asemenea se ia in discutie forma de administrarea a diacetilmorfinei farmaceutice, astfel incit sa nu dispara peak-ul de concentratie similar formei injectabile, responsabil de rush-ul adictiv, dar si efectul euforizant prlungit al morphine-6-glucuronidului. Se pare ca forma inhalanta dupa volatilizare (similar vinatorii dragonului) este cea mai aproape de aceste 2 deziderate[30].
Un experiment extrem de eficient a avut loc in Elvetia in anii '90, unde in Platzspitz - Zurich, un parc, asa zisul "needle-park", orice persoana primea in mod liber, fara riscuri juridice, si sub supraveghere medicala, doza uzuala de drog (in general pina in 900 de mg/zi), ace si seringi sterile, fiind supravegheati si consiliati la administrarea drogului. Dupa un an de zile s-a remarcat o insignifianta reducere a cazurilor de intoxicatii letale si a mortalitatii generale, a incidentei HIV, in schimb criminalitatea legata de drog a scazut de la 69% din totalul infractiunilor la 10%! Costul extrem de ridicat al proiectului (23$/zi/persoana, in comparatie cu cel de substitutie cu methadona de 3$/zi/persoana) a dus la incetarea acestuia.
La aceste medicamente se pot asocia si alti agenti non-opioizi (in general protocoalele mai vechi ce prevedeau monoterapie cu non-opioide au fost abandonate). Clonidina, agonist alfa 2 adrenergic, in doze de 0,1-0,3 mg / de 3 ori pe zi, scade activitatea simpatica centrala, dar nu reduce craving-ul, si este ineficace fata de starile de insomnie si acuzele de tensiune musculara, avind si un puternic efect de sedare si hipotensor.
Regula prevede ca pe toata perioada tratamentului de substitutie sa se aplice in paralel si consilierea si terapia psiho-comportamentala. Recaderile sint frecvente, 60 - 80% in prima luna de la externare . Daca in 1992 38,9% din toxicomanii tratati erau considerati reabilitati, in 1997 doar 21,1% primeau acest calificativ. Un alt studiu arata ca dupa 7 ani un sfert au devenit abstinenti, iar 20% au decedat din cauze legate de drog (Stimson 1978) . Costul tratamentului de mentinere cu metadona este de circa 4700$/an, spre deosebire de acela al incarcerarii unui detinut de 18 400$/an . Se considera ca un dolar investit in tratarea dependentei salveaza alti 5$ ce ar putea fi cheltuiti drept consecinta a criminalitatii asociata drogurilor si alti 12 $ folositi pentru tratarea complicatiilor consumului de droguri . La acestea, prin tratamentul toxicomanilor se adauga banii salvati din cresterea productivitatii, din impiedicarea pierderii educatiei, din prevenirea accidentelor etc.
Exista tendinta de a scadea durata tratamentului, mai ales in tarile nordice si Grecia, de la 1-2 ani la circa 6 luni, desi studiile arata o legatura directa intre durata tratamentului si rata de succes.
Factori predictivi ai prognosticului indepartat pot fi considerati durata de raminere in programul de tratament, obtinerea si pastrarea unui loc de munca, criminalitatea[35].
Bourgeois a raportat 500 de cazuri (1983) de tratament eficient prin electroterapie timp de 5 zile cu un dispozitiv creat de el.
Dependenta psihica necesita un tratament complex, prelungit, uneori pe parcursul a ani, incluzind substitutia, psihoterapie, consiliere, individuala, de grup sau impreuna cu familia, sevicii postcura, de reabilitare psihosociala, avind drept scop redobindirea functiilor sociale si profesionale, prin mentinerea motivatiei, readaptarea la stilul de viata anterior, prevenirea recaderilor si prin confruntare cu propriile probleme.
Psihoterapia este esentiala in tratamentul toxicomaniei, in special cea cognitiv-comportamentala (bazata pe rolul jucat de teoria invatarii in dezvoltarea comportamentului maladaptiv) are rolul de a creste capacitatea de autocontrol prin explorarea consecintelor (apreciate ca pozitive sau negative) uzului de droguri, pe autorecunoasterea craving-ului, prin identificarea situatiilor de risc ce ar putea conduce la pulsiunea de a lua drogul, precum si prin dezvoltarea de strategii de lupta si evitare a unor astfel de situatii. Rezultate mai bune sint intilnite la cei la care consumul de droguri se suprapune unui fond de depresie, si mult mai slabe la cei ce asociaza personalitate antisociala.
Tratamentul in institutii specializate se adreseaza in special celor cu nevoi speciale (pacienti fara locuinta, adolescenti, bolnavi psihici). Intrarea in comunitati terapeutice isi propune resocializarea bolnavilor cu cresterea responsabilitatilor si adoptarea unui stil de viata productiv, schimbarea caracterului corelat cu uzul drogului. Filozofia de baza este ca toxicomanul este imatur emotional, necesita insertie in structuri sociale speciale pentru a-si modifica stilul de viata si comportamentul autodistructiv. Dezvoltarea onestitatii, capacitatilor sociale, inlaturarea atitudinilor antisociale si a comportamentului criminal sint alte deziderate atasate abstinentei totale. In aceste comunitati, in care programele se desfasoara pe durate mari (12-18 luni), se incearca obtinerea unui substitut familial, asumarea de responsabilitati care sint recompensate prin acordarea de libertati individuale, de crestere a comfortului material, de cistigare a respectului grupului, orice abatere de la reguli fiind sanctionate, violenta sau uzul de droguri putind conduce la expulzia din comunitate. Rata de esec este mare, 30% din rezidenti renuntind in primele 3 luni, 50% in primele 6 luni. Recent, este posibila obligativitatea intrarii in astfel de programe ca urmare a unor sentinte judecatoresti.
Totalul toxicomanilor intrati in programe de tratament in UE[36]
Grupurile de intrajutorare, de tipul Narcoticii Anonimi, si-au dovedit capacitatea de a contribui esential in fazele finale (de intarire a motivatiei si a reinsertiei sociale) ale terapiei, fiind constituite din fosti toxicomani ce impartasesc celorlalti experientele lor si-i indruma pe nou-veniti.
Tratamentul populatiilor speciale (gravide, detinuti, personal medical) necesita anumite ajustari ale programelor terapeutice. Cei aflati in atentia sistemului juridic au tendinta de a raspunde mai bine la tratament, si datorita mijloacelor coercitive disponibile si relativei limitari a alternativelor si aservirii fata de sistem. La gravide se impune inducerea unui sevraj lent, cu o scadere minima de la o zi la alta a dozelor de metadona. Nu au fost identificate riscuri suplimentare ale detoxifierii in sarcina fata de populatia generala.
Personalul medical (mai ales din serviciul anestezie-terapie intensiva) are o rata mare de toxicomanie, datorita disponibilitatii medicamentelor opioide, dar de asemenea si o rata mare de recuperare (85%), fiind extrem de eficiente contractele impuse de angajator ce prevad consecinte aspre la o noua recadere. Exista o serie de ipoteze ce incearca sa explice incidenta mai mare a toxicomaniilor in rindul anestezistilor - acces facil la subtante cu potential dependogen crescut, posibilitatea justificarii lipsurilor de medicamente, contactul zilnic cu aceste substante, stress-ul profesional. Cele mai frecvent intilnite sint ketamina, propofol, tiopental, midazolam, alcool. Comportamentul acestora include tendinta la activitate individuala, refuzul activitatilor comune, pauze frecvente, solicitarea de cazuri suplimentare, refuzul prinzului, intirzieri la program, lucrul pina la ore tirzii, scadere in greutate, malpraxis. Determinarea prezentei acestor substante este foarte dificila, avind in vedere timpul de injumatatire scurt si concentratiile sangvine reduse, de aceea este rezonabila folosirea ca proba biologica a parului, ce va permite si o reconstituire istorica a consumului, admitind o crestere de 1 cm pe luna. Trebuie amintit aici si tratamentul comorbiditatii, frecvente la toxicomani, fapt ce arata o data in plus costul urias suportat de catre individ si societate ca urmare a consumului de droguri.
O'Connor PG, Carroll KM, Shi JM Three methods of opioid detoxification in a primary care setting Annals of Internal Medicine 52630, 1997
Kleber HD. Opioids: detoxification.
In: Galanter M, Kleber HD, eds. Textbook of Substance Abuse Treatment.
Kleber HD, Topazian M, Gaspari J, Riordan CE, Kosten T: Clonidine and naltrexone in the outpatient treatment of heroin withdrawal. Am J Drug Alcohol Abuse 13:1, 1987
Gerra G, Zaimovic A, Giusti F, et al. Lofexidine vs. clonidine in rapid opiate detoxification. J Subst Abuse Treat.;21:11-17. 2001
Evgeny Krupitsky, Andrey Burakov, Tatyana Romanova., Igor Dunaevsky Ketamine psychotherapy for heroin addiction: immediate effects and two-year follow-up Journal of Substance Abuse Treatment Volume 23, Issue 4, December 2002, Pages 273-283
Kenneth R. Alper, Howard S. Lotsof, Geerte M. N. Frenken, Treatment of Acute Opioid Withdrawal with Ibogaine The American Journal on Addictions 8:234-242, 1999
C. Bochud Tornay, B. Favrat, M. Monnat Ultra-rapid opiate detoxification using deep
sedation and prior oral buprenorphine preparation: long-term results Drug and Alcohol Dependence
Volume 69, Pages 283-288, ![]() 2003
2003
Musshoff F., Lachenmeier D. W. Methadone substitution: medicolegal problems in Germany Forensic Science International Volume 133, Issues 1-2, Pages 118-124, 2003
Riitta Alaja Six-month outcomes of hospital-based psychiatric substance use consultations General Hospital Psychiatry * Volume 25, Issue 2 , March-April 2003, Pages 103-107
Gottheil E, Mannelli P, Collins ED, et al.
Recent developments in opiate detoxification. Program and abstracts of the
American Society of Addiction Medicine 33rd Annual Meeting &
Medical-Scientific Conference; April 25-28, 2002;
Michael Gossop, Duncan Stewart, John Marsden Treatment process components and heroin use outcome among methadone patients Drug and Alcohol Dependence Volume 71, Pages 93-102, 2003,
Fudala PJ, Jaffe JH, Dax EM, Johnson RE: Use of buprenorphine in the treatment of opioid addiction, II. Effects of daily and alternate-day administration and abrupt withdrawal. Clin Pharmacol Ther 47:525, 1990
Walsh S., Eissenberg T. The clinical pharmacology of buprenorphine: extrapolating from the laboratory to the clinic Drug and Alcohol Dependence Volume 70, Issue 2, Supplement 1 , Pages S13-S27, 2003
Chiang C. N., Hawks R. Pharmacokinetics of the combination tablet of buprenorphine and naloxone Drug and Alcohol Dependence Volume 70, Issue 2, Supplement 1, Pages S39-S47, 2003
John Mendelson, Reese T. Jones Clinical and pharmacological evaluation of buprenorphine and naloxone combinations: why the 4:1 ratio for treatment? Drug and Alcohol DependenceVolume 70, Issue 2, Supplement 1 , 21 May 2003, Pages S29-S37
Laurie Barclay Buprenorphine/Naloxone
Safe, Effective as Office-Based Treatment for Opiate Addiction
Rolley E. Johnson, Eric C. Strain, Leslie Amass Buprenorphine: how to use it right Drug and Alcohol Dependence Volume 70, Supplement 1 , Pages S59-S77, 2003
G. Gerra, , F. Borellaa, A. Zaimovica Buprenorphine versus methadone for opioid dependence: predictor variables for treatment outcome Drug and Alcohol Dependence
Volume 75, Issue 1 ,
Tami L. Mark Ph.D, Joan D. Dilonardo, Mady Chalk, Rosanna, M. Coffey Factors associated with the receipt of treatment following detoxification Journal of Substance Abuse Treatment Volume 24, Issue 4 , June 2003, Pages 299-304
Rolley E. Johnson, Hendrée E. Jones, Gabriele Fischer Use of buprenorphine in pregnancy: patient management and effects on the neonate Drug and Alcohol Dependence Volume 70, Supplement 1 , Pages S87-S101, 2003,
Jason Luty , Vasilis Nikolaou, Jenny Bearn Is opiate detoxification unsafe in pregnancy? . Journal of Substance Abuse Treatment Volume 24, Issue 4 , June 2003, Pages 363-367
Marina Picciotto Galanin Mitigates Signs of Opiate Withdrawal
Proc Natl Acad Sci
Javier Esteban, Carmen Gimeno, José Barril Survival study of opioid addicts in relation to its adherence to methadone maintenance treatment Drug and Alcohol Dependence Volume 70, Issue 2 , 21 May 2003, Pages 193-200
Dole, V.P.; Nyswander M, Kreek, M.J. Narcotic Blockade. Archives of Internal Medicine 118: 304-309, 1996.
Gale K. Ultra-Low-dose Naltrexone Can Prevent Opioid Tolerance And Dependence Reuters Health Information 06 jun2003. © 2003 Reuters Ltd.
Hulsea G. H., Taita R. J. Reducing hospital presentations for opioid overdose in patients treated with sustained release naltrexone implants Drug and Alcohol Dependence Volume 79, Issue 3 , 1 September 2005, Pages 351-357
Pedram Sendi, Matthias Hoffmann, Heiner C. Bucher Intravenous opiate maintenance in a cohort of injecting drug addicts Drug and Alcohol Dependence Volume 69, Issue 2, 1 March 2003, Pages 183-188
Dürsteler-MacFarlanda K. M., Stohlera R. Complaints of heroin-maintained patients: A survey of symptoms ascribed to diacetylmorphine Drug and Alcohol Dependence Volume 81, Issue 3 , 28 February 2006, Pages 231-239
Klousa M., Van den Brinkb W. Development of pharmaceutical heroin preparations for medical co-prescription to opioid dependent patients Drug and Alcohol Dependence Volume 80, Issue 3 , 12 December 2005, Pages 283-295
O'Connor PG, Waugh ME, Carroll KM Primary carebased ambulatory opioid detoxification: the results of a clinical trial. Journal of General Internal Medicine. 10:25560, 1995
Pincock S. Successful Opiate Detoxification May Increase Subsequent Overdose Risk BMJ:326:959-960. 2003
Christopher M. Doran, Marian Shanahan, Richard P. Mattick Buprenorphine versus methadone maintenance: a cost-effectiveness analysis Drug and Alcohol Dependence Volume 71, Issue 3 , 10 September 2003, Pages 295-302
Michael Gossop , Duncan Stewart, John Marsden Treatment process components and heroin use outcome among methadone patients Drug and Alcohol Dependence Volume 71, Issue 1 , 20 July 2003, Pages 93-102
|
Politica de confidentialitate |
| Copyright ©
2025 - Toate drepturile rezervate. Toate documentele au caracter informativ cu scop educational. |
Personaje din literatura |
| Baltagul caracterizarea personajelor |
| Caracterizare Alexandru Lapusneanul |
| Caracterizarea lui Gavilescu |
| Caracterizarea personajelor negative din basmul |
Tehnica si mecanica |
| Cuplaje - definitii. notatii. exemple. repere istorice. |
| Actionare macara |
| Reprezentarea si cotarea filetelor |
Geografie |
| Turismul pe terra |
| Vulcanii Și mediul |
| Padurile pe terra si industrializarea lemnului |
| Termeni si conditii |
| Contact |
| Creeaza si tu |