
APLICATII ALE COLORANTILOR IN BIOLOGIA MOLECULARA
In 1924, Policard a observat ca porfirinele se gasesc in concentratii mai mari in
Tumorile maligne decat in tesuturile normale. Asemenea porfirine sunt inofensive dar pot avea un efect foarte toxic pentru celulele in care ele sunt concentrate daca sunt expuse la lumina. In acest fel o tumoare poate fi distrusa prin aplicarea luminii, daca contine o concentratie relativ mare de porfirine.
Tesuturile normale, vecine supravietuiesc deoarece ele contin putina porfirina.
Apare astfel o noua terapie a cancerului, "terapia fotocromica" ce se bazeaza pe distrugerea selectiva a tumorilor prin intermediul injectiei intravenoase a o serie de coloranti fototerapeutici, urmata de expunere la lumina rosie. Concentratia marita a acestor coloranti in tumorile maligne poate fi de asemenea folosita pentru detectia cancerului daca sunt coloranti fluorescenti.
Principiul PDT a fost aplicat in jurul anilor 1930 (cand von Tappeiner si Jesionek) cand a fost tratata o tumoare de piele prin aplicarea Eosinei (1) si ulterior iradierii cu lumina alba.
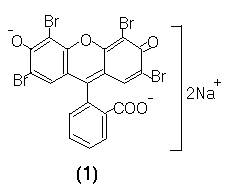
Eosina se obtine conform reactiilor:
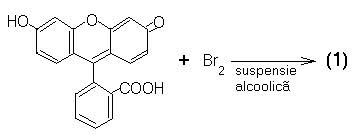
Sarea de sodiu are culoarea rosie cu fluorescenta verde.
In 1948 Figge si colaboratorii sugereaza utilizarea porfirinelor si metalporfirinelor pentru PDT a cancerului. In 1950 a fost utilizata hematoporfirina (2).
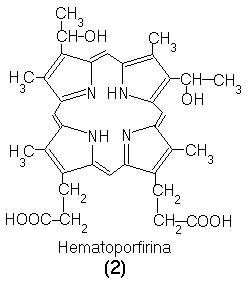
Hematoporfirina se obtine din hemina (hematoporfirina cu grupe -CH=CH2 in loc de HO-CH-CH3 si Fe) prin tratare cu acizi cand are loc eliminarea fierului si aditia apei la cele doua grupe vinilice.
Rezultate mai bune in introducerea PDT pentru tratamentul cancerului s-au obtinut numai in jurul anilor 1970 dupa aparitia pe piata a sursei de lumina laser si a fibrelor optice. Aceste instrumente au permis medicilor accesul direct la sursele de lumina pentru tratamentul tumorilor maligne.
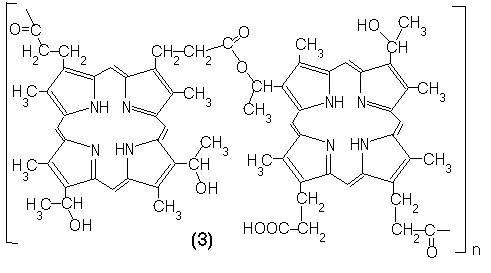
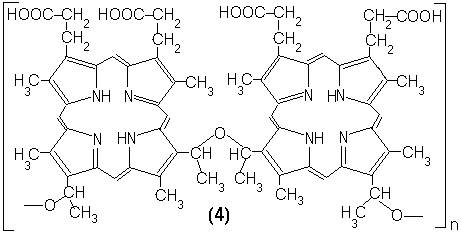
Cercetarile in domeniu sunt in real progres. De exemplu 45% din compusii fotoporfirinelor au fost cunoscuti in 1989. Ester si eteroligomerii hematoporfirinei ca de exemplu (3) si (4) au fost cunoscuti in ultimul timp.
1.1.Mecanismul fotodestructiei
Etapa primara caracteristica a fotodestructiei este absorbtia unui foton de catre colorant ce produce un singlet cu stare excitata
1.1.1.Fotonica colorantilor
ASPECTE STRUCTURALE
Majoritatea sistemelor cromogene contin elemente structurale polimetinice (I) caracterizate prin prezenta unei catene constituita din N atomi X, X Y, apartinand grupelor IV, V, VI din tabelul periodic si a unui sistem format din N+1 electroni π.
Structura polimetinica ideala se caracterizeaza printr-0 distributie simetrica si o delocalizare maxima a electronilor π in catena, adica prin energie de rezonanta mare, intensitate de oscilatie mare, corelata cu benzi de absorbtie de lungime de unda mare, polarizabilitate optica intensa, egalizarea maxima a ordinelor de legatura si distributie alternanta pronuntata a densitatii electronilor π in stare fundamentala.
Alternarea distributiei densitatii electronilor π de-a lungul catenei confera polimetinelor reactivitate electrofila si nucleofila. De fapt, sistemele cromogene ar trebui reprezentate ca intermediari intre structurile limita polimetinice si aromatice, dependent de marimea energiei de rezonanta pentru elementele structurale implicate.
Trecerea de la o structura polimetinica la una aromatica sau polienica este insotita de diminuarea efectelor cauzate de alternarea densitatii sarcinii electrice si de polarizabilitateamare a polimetinelor.
Evident, se considera si eventualele modificari ale geometriei moleculare, corelate cu gradul de hibridizare a atomilor constitutivi, cu caracterul legaturilor implicate, cu efectele inductuve si de hiperconjugare, a interactiilor sterice intra si intermoleculare.
Geometria moleculara si distributia electronilor in substanteleorganice colorate atesta prezenta unor sisteme coplanare, stabilizate energetic datorita prezentei sextetului aromatic si a gruparilor structurale polimetinice. Perturbarea acestor sisteme ideale, consecinta a ramificarii sistemului conjugat sau a asimetriei fragmentelor polimetinice prin efecte de substituent, conduce la cuplarea elementelor structurale aromatice si polimetinice prin intermediul legaturilor polienice. Sunt posibile si interactiuni columbiene, ce determina modificari in alternarea densitatii de sarcina electrica.
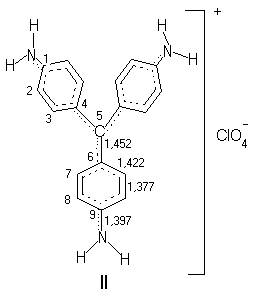
Prezinta interes tratarea comparativa a elementelor structurale si a distributiei electronice din colorantii implicati in transferul de energie. Astfel, in colorantii triamino-trifenilmetanici (II) au fost identificate fragmente metincianinice ramificate.
Colorantii cianinici derivati din colorantii azometinici prin inlocuirea grupelor alchil de la atomii de azot marginali cu inele heterociclice: exemplu
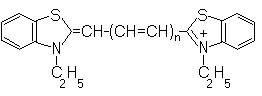
Datorita ramificarii simetrice a sistemului de rezonanta polimetinica in pozitiile para, se remarca diminuarea aromaticitatii ciclurilor benzenice constitutive in favoarea caracterului polienic (doua legaturi centrale ale ciclurilor sunt mai mici).
In cazul colorantilor acridinici si triazinici au fost puse in evidenta structuri aza-polimetinice. Pentru percloratul de bis10-metil-acridin-9-monoaza-monometilcianinice (III) sunt caracteristice structuri aza-hepta-metinice, in timp ce albastrul de metilen (IV) corespunde unei structuri-aza-nonametinice.
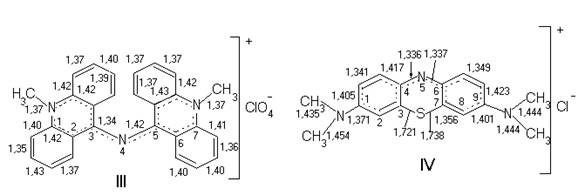
Cationul colorantului acridinic III contine grupe metinice ramificate, precum si 4 cicluri aromatice (6π).
In structura IV se remarca elemente polienice (alternarea legaturilor simple si duble), datorita ramificarii sistemului carbociclic cu rezonanta polimetinica. In plus cele doua legaturi C-S sunt mai scurte decat legatura simpla C-S, ceeea ce indica o rezonanta metinica suplimentara, ce implica atomul de sulf. Aceasta structura favorizeaza agregarea intermoleculara a colorantului.
Derivatii flavinici colorati contin heterocicli condensati liniar si un nucleu fenilic, cromofori de acest tip fiind importanti pentru enzime si coenzime.
De exemplu 5-acetil-3,7,8,10-tetrametil-1,5-dihidroaloxazina (V) dispune, pe langa scheletul aromatic si de elemente structurale macrometinice.
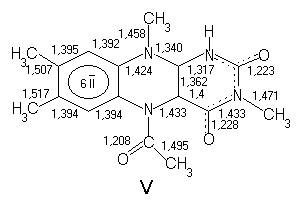
Legatura C=C relativ scurta dintre cele doua inele heterociclice poate fi considerata ca parte constitutiva a unei structuri trimetinmezocianinice (mezocianinele sunt coloranti neionici, ce contin un sistem cromofor de forma >N-(C=C)n-C=O↔>N+-(C-C=)n-C-O-) la care participa atomii de azot 1 si 5 si gruparea 2-carbonilica. Datorita efectului steric, rezonanta monometinica dintre gruparea 5-acetil si atomul de azot heterociclic este redusa.
Cromoforii porfirinelor (VI) si compusilor inruditi sunt polimetine cuplate ciclic, ce contin 18 electroni π, intr-o catena de 6 atomi.
Alternarea densitatii electronilor π conduce la conjugarea interna, ciclica si la proprietatile diamagnetice.
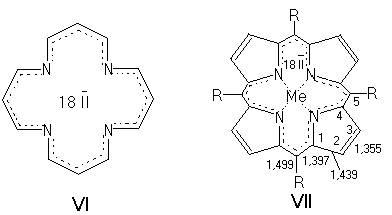
Structura polimetinica, dovedita prin difractie cu raze X, este confirmata de valorile medii ale lungimilor legaturilor din tetrametilporfirine (VII). Distante interatomice de acelasi ordin de marime sunt caracteristice pentru diferiti derivati porfirinici.
Legaturile C-N, de lungime egala, exclud posibilitatea localizarii a doi protoni sau a ionilor metalici la atomii de azot. Lungimea legaturilor in fragmentele trimetincianinice indica o structura polimetinica cu legaturi C-C de ~ 1,39 Å si distante C-N extinse, atribuite efectului de ramificare in ciclurile pirolice. Ramificarea determina caracterul polienic al celorlalte legaturi C-C din ciclurile pirolice, modificate la 1,44 Å in sensul legaturii simple si la 1,36 Å, in directia legaturii duble.
Planurile substituentilor fenil sunt rasucite cu un unghi de 90s fata de cel al ciclului porfirinic, astfel fiind impiedicata rezonanta dintre diferitele sisteme ciclice.
Legaturile specifice polimetinelor cuplate ciclic nu se regasesc, insa, in tetraoxoporfirinogen (VIII), unde predomina caracterul aromatic al ciclurilor pirolice, lungimea legaturilor fiind de ~1,40 Å.
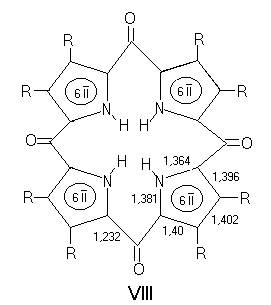
Marirea in mica masura a legaturii C=O (1,23 Å) si micsorarea lungimii legaturii C-C (fata de 1,44 Å in ciclul porfirinic) indica o rezonanta redusa in sistemul macrociclic.
1.1.1.1.Starile electronice excitate
Reactivitatea si timpul de viata al starilor electronice excitate sunt determinate decontinutul energetic, respectiv de distributia sarcinii electrice, corespunzator tranzitiilor unielectronice intre diferite orbitale moleculare.
Comportarea fotofizica si fotochimica a compusilor organici se coreleaza deci, cu energetica intramoleculara, cu caile de populare a orbitalelor moleculare, cu valorile constantelor vitezelor de dezactivare a formelor excitate. Diagrama energetica a nivelelor electronice si vibrationale precum si a tranzitiilor posibile in compusii organici este data de figura 1.Explicarea si detalierea elementelor din figura 1 sunt prezentate in tabelul 2.
Starile electronice implicate in reactiile fotochimice ale colorantilor sunt 1(ππ*), 3(ππ*), 1(nπ*), ca si cele de transfer de sarcini 1(CT) si 3(CT).
Starile ππ*, rezulta in urma tranzitiilor π*←π in sisteme polienice si aromatice, cu conjugare extinsa, caracterizandu-se prin moment de tranzitie paralel cu planul moleculei si absorbtii intense in domeniile vizibil si U.V. apropiat (εmax.>103l.mol.-1.cm-1). Banda de absorbtie poate fi deplasata batocrom in prezenta solventilor polari sau ca urmare a grefarii pe sistemul cromogen a unor substituenti electronodonori.
Compararea proprietatilor starilor ππ* singlet si triplet, indica probabilitatea mare a tranzitiei intercombinationale singlet-triplet, corelate cu delocalizarea pronuntata a orbitalilor in moleculele colorantilor.
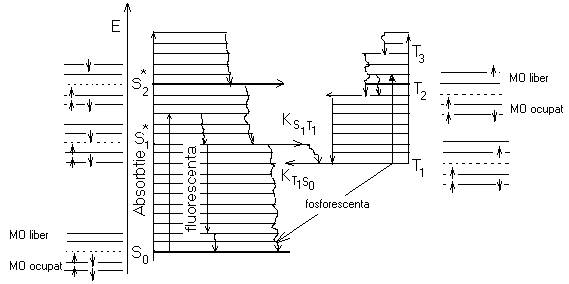
Fig.1. Schema energetica a nivelelor electrono-vibrationale si a tranzitiilor fotofizice in compusi organici
Tabelul 2. Tranzitii electronice
|
Tranzitii electronice |
Interval de timp |
Caracteristici |
Observatii |
|
Absorbtia luminii |
10-15 s |
Prin ocuparea nivelelor de vibratie Superioare, fara modificarea spinului si a configuratiei nucleare a moleculei |
In diagrama energetica: linii verticale cu sageata in sus |
|
Relaxare vibrationala |
10-12 s |
In diagrama linii verticale ondulate |
|
|
Conversie interna |
10-11-10-12 s |
Tranzitie neradianta:izoenergetica Absenta fluorescentei Conversia interna improbabila datorita diferentei mari de energie intre nivelele implicate |
Sageti orizontale scurte |
|
Tranzitii radiante Fluorescenta |
Se apreciaza pe baza constantei vitezei tranzitiei radiante, Krad:Krad.=104εmax., unde εmax. reprezinta coeficientul molar de extinctie εmax.>103, Kf1=10-9-10-7 s-1 εmax.<103, Kf1=106-104 s-1 | ||
|
Fosforescenta |
Kfosf=104-10-2 s-1 | ||
|
Tranzitii intercombinationale |
Tranzitii izoenergetice, intre starile de multiplicitate diferita, interzise de spin, ce depind de diferenta de energie, intre starile implicate si interactia spin-orbita K S*1T1=104-1012 s-1 KT1S0=10-2-105 s-1 |
In diagrama energetica linii ondulate orizontale |
Benzoporfirine-produsi care contin 4 cicluri izoindolice legate prin punti metinice.
Ftalocianine-tetrabenzotetraazoporfirine.
Metaloporfirine-saruri complexe in care atomul de metal este legat de cei 4 atomi de N prin legaturi chimice echivalente.
Porfirinele prezinta spectre electronice similare caracterizate prin prezenta a patru benzi de intensitate mare (banda Soret) la limita U.V.-Viz. Benzile de absorbtie de lungime de unda mare sunt corelate cu tranzitiile ππ* din sistemul electronic extins al macrociclului tetrapirolic, pozitia si intensitatea relativa a acestora depinzand de natura substituentilor.
Pe de alta parte, tranzitiile ππ* in heterocicli cu azot corespund la λ≥310 nm, deplasarile batocrome fiind corelate cu prezenta unor legaturi de hidrogen intramoleculare.
Formarea metalporfirinelor conduce la modificari ale spectrului de absorbtie, care se caracterizeaza in domeniul vizibil prin doua maxime, precum si prin prezenta benzii Soret ingustata, cu pozitia putin modificata de complexare. Deplasarea batocroma mica a maximului de absorbtie
(~30 nm) determinata de natura metalului este insotita de micsorarea stabilitatii complexului in seria:
Pd>Pt>Ni>Co>Ag>Cu>Zn>Mg>Cd>Ca
Deplasarea hipsocroma a maximului de absorbtie, paralela cu cresterea stabilitatii matalporfirinelor, se datoreste interactiei slabe, prin legaturi σ, intre atomul de metal central si sistemul π electronic al ligandului.
Proprietatile optice ale metaloporfirinelor sunt corelate cu tranzitiile electronice intre doua orbitale superioare ocupate (a1n, a2n) si doua orbitale inferioare libere (egu, egy), precum si interactiile configurationale. Prin interactia configuratiilor a1n.eg si a2n.eg se formeaza o stare in care dipolmomentele de tranzitie se modifica si se reduc reciproc, ceea ce conduce la tranzitiile Q slabe (domeniul vizibil) si tranzitiile V intense (limita U.V.-vizibil).
Complexarea porfirinelor cu ioni metalici implica interactie dintre nivelele singlet-triplet ale ligandului si orbitalele d vacante ale metalului, fiind posibile doua cazuri (fig.2).
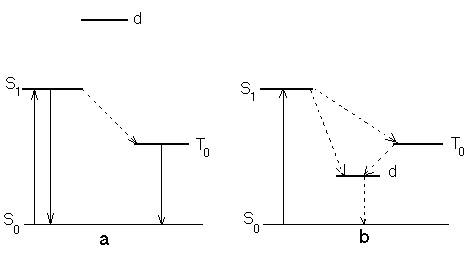
Fig.2. Interactiile intre nivelele singlet-triplet ale ligandului si orbitalele vacante ale metalului in metalo-porfirine.
In primul caz (fig.2a) orbitalele vacante d sunt dispuse mai sus decat nivelul liber egπ al ligandului, nu exista conditii pentru transferul electronului excitat pe nivelul d al metalului, fiind posibile, insa, tranzitii singlet-triplet. In cel de-al doilea caz (fig.2b), electronul de pe nivelele excitate S, T poate trece pe nivelele neocupate ale metalului, diferenta de energie intre nivelele d si π* fiind mica.
Influenta metalului asupra fotonicii metaloporfirinelor a fost pusa in evidenta in procesele redox fotochimice ale derivatilor ce contin diferite metale tranzitionale.
1.1.1.2. Fenomene de asociere
Asocierea moleculelor de coloranti si formarea unor agregate intermoleculare sunt de incontestabil interes teoretic si aplicativ servind la clarificarea unor aspecte legate de natura starilor electronice excitate si rolul acestora in procese chimice, biologice, fotochimice in energetica intermoleculara. Asocierea moleculelor de coloranti influenteaza proprietatile fotofizice ale acestora, cum ar fi pierderea capacitatii luminiscente si redistribuirea energiei de radiatie. Gradul si ordinul de asociere, ca si constitutia agregatelor depind de natura solventului, de structura si concentratia colorantului, precum si de temperatura. Procedeele de studiere a agregarii implica o serie de metode: difuziune, conductibilitate electrica, dispersia luminii, polarografie, rezonanta electronica paramagnetica, spectroscopie de absorbtie si fluorescenta.
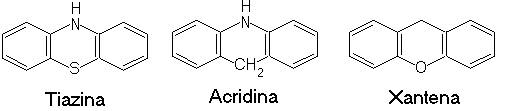
Ca urmare a agregarii, in spectrele electronice ale colorantilor se produc trei categorii de modificari: ingustarea benzii de absorbtie principale (coloranti cianinici), micsorarea intensitatii absorbtiei (coloranti triazinici) si distributia benzii de absorbtie in doua sau mai multe componente (coloranti xantenici, acridinici si alti coloranti nonchinoizi).
|
Politica de confidentialitate |
| Copyright ©
2025 - Toate drepturile rezervate. Toate documentele au caracter informativ cu scop educational. |
Personaje din literatura |
| Baltagul caracterizarea personajelor |
| Caracterizare Alexandru Lapusneanul |
| Caracterizarea lui Gavilescu |
| Caracterizarea personajelor negative din basmul |
Tehnica si mecanica |
| Cuplaje - definitii. notatii. exemple. repere istorice. |
| Actionare macara |
| Reprezentarea si cotarea filetelor |
Geografie |
| Turismul pe terra |
| Vulcanii Și mediul |
| Padurile pe terra si industrializarea lemnului |
| Termeni si conditii |
| Contact |
| Creeaza si tu |