
Numeroase procese fundamentale, care au loc in materialele cristaline (cristalizarea metalelor si aliajelor, deformarea plastica la cald, tratamentele termice si termochimice, sinterizarea din pulberi metalice sau ceramice, etc.), se realizeaza prin difuzie atomicǎ.
Difuzia atomica este un proces de transfer de substanta, care se bazeaza pe migrarea atomilor pe distante mai mari decat distanta medie interatomica.
Daca migrarea atomilor nu este insotita de modificarea concentratiei in volume izolate, fenomenul este numit autodifuzie. Aceasta este specifica metalelor pure, in care se deplaseaza atomi de aceeasi specie.
Daca migrarea atomilor este insotita de modificarea concentratiei, cum este in cazul aliajelor sau al metalelor cu un continut ridicat de impuritati, fenomenul este numit difuzie sau heterodifuzie.
 Fenomenul de
difuzie se poate evidentia cu ajutorul unui cuplu de difuzie, format
prin imbinarea a doua bare din metale diferite, astfel incat intre suprafetele
alaturate sa fie un contact intim.
Fenomenul de
difuzie se poate evidentia cu ajutorul unui cuplu de difuzie, format
prin imbinarea a doua bare din metale diferite, astfel incat intre suprafetele
alaturate sa fie un contact intim.
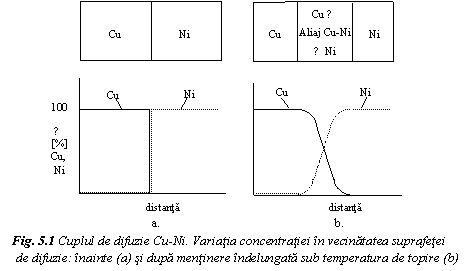
In figura 1 se prezinta variatia concentratiei in vecinatatea suprafetei de difuzie a cuplului Cu-Ni, inainte (a) si dupa o mentinere indelungata la temperaturi sub temperatura de topire a celor doua metale (b). Dupa tratamentul termic de difuzie, se constata ca metalele sunt separate de o zona aliata, in care concentratia de Cu si Ni variaza in functie de distanta de la suprafata initiala de separatie. Aceasta zona s-a creat prin migrarea atomilor de Cu in Ni, respectiv a celor de Ni in Cu, din zona cu concentratie ridicata spre cea cu concentratie scazuta. Procesul in care are loc migrarea atomilor unui metal in matricea celuilalt se numeste interdifuzie.
Difuzia in volumul cristalului se realizeaza prin salturi activate termic ale atomilor de pe o pozitie de echilibru pe alta pozitie vecina. Pentru ca un atom sa realizeze un salt, trebuie indeplinite doua conditii:
- sa existe in vecinatate o pozitie de echilibru libera;
- atomul sa aiba suficienta energie pentru a rupe legaturile cu atomii vecini si pentru a deforma elastic reteaua cristalina in timpul saltului.
Executia saltului unui atom necesita fluctuatii ale energiei de vibratie a atomilor, care sa furnizeze energia de activare a saltului, corelate cu miscarea adecvata a atomilor vecini. Pentru a descrie procesul de difuzie atomica in volumul unui cristal, s-au propus patru mecanisme elementare: ciclic, de schimb, lacunar si interstitial (fig. 2).
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()

![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()

Dupa mecanismul
ciclic un grup de atomi au un salt comun, de exemplu, o rotatie
ciclica (fig. 2a). Aceasta rotatie este putin
probabila, datorita necesitatii de sincronizare a saltului
unui grup de atomi.
Difuzia de schimb este un caz particular al primului mecanism, prin care doi atomi vecini fac schimb de pozitii (fig. 2b).
Mecanismul lacunar se bazeaza pe deplasarea unui atom in pozitia unei lacune vecine (fig. 2c). Energia de activare a acestui mecanism cuprinde energia necesara formarii unei lacune si energia de salt.
In cazul mecanismului interstitial, un atom dispus interstitial sare intr-un interstitiu vecin. Energia de activare este minima, continand numai energia de salt. Acest mecanism prezinta mai multe variante: interstitial direct (fig. 2d), daca saltul are loc dintr-un interstitiu in altul vecin; interstitial indirect (fig. 2e), daca atomul interstitial deplaseaza un atom reticular vecin intr-o pozitie interstitiala, ceea ce conduce la formarea unui interstitial disociat, care se deplaseaza dupa diferite directii in spatiu; interstitial extins (fig. 2f), daca disocierea are loc dupa o directie densa pe lunga distanta; rezulta un crowdion care se deplaseaza in lungul sirului reticular. Ultimele doua variante ale mecanismului interstitial au o energie de formare mai mica, deformatia elastica a retelei fiind mai redusa.
In materialele metalice cele mai frecvente sunt mecanismele c si d. Difuzia lacunara, interstitiala indirecta si extinsa apar la migrarea atomilor metalici, cu raza atomica mare. Este specifica autodifuziei din metalele pure sau interdifuziei in solutiile solide de substitutie. Difuzia interstitiala directa apare la migrarea in solutiile solide interstitiale a atomilor de metaloid cu raza atomica mica (C, N, B, H). Difuzia interstitiala apare mai rapid decat cea lacunara, pe de o parte, pentru ca necesita o energie de activare mai mica si pe de alta parte, pentru ca exista mai multe interstitii libere in vecinatate decat vacante.
 In afara
mecanismelor de difuzie bazate pe defectele punctiforme, difuzia se produce in
lungul dislocatiilor, pe canalul creat de zona dilatata a
retelei cristaline din vecinatatea liniei dislocatiilor.
In afara
mecanismelor de difuzie bazate pe defectele punctiforme, difuzia se produce in
lungul dislocatiilor, pe canalul creat de zona dilatata a
retelei cristaline din vecinatatea liniei dislocatiilor.
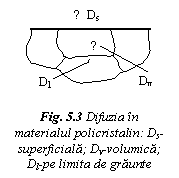
La materialele policristaline, difuzia volumica este insotita de difuzia superficiala si difuzia pe limita de graunte (fig. 3).
Intre energiile de activare ale difuziei pe aceste cai exista relatia: Esuprafata <<Elimita Edislocatii 0,5 Evolum.
Primul studiu matematic al procesului de difuzie a fost facut de Adolphe Fick in anul 185 Prin analogie cu lucrarile lui Fourier asupra transferului de caldura, Fick a definit coeficientul de difuzie D, pentru un transport de masa uniaxial, in directia x, prin ecuatia diferentiala cu derivate partiale:
![]() (1)
(1)
unde J este fluxul de difuzie, care reprezinta cantitatea de substanta a unui component aflat in solutie sau in amestec intr-un solvent, care traverseaza perpendicular unitatea de suprafata, in unitatea de timp, datorita unui gradient de concentratie c/ x. Semnul negativ indica deplasarea atomilor din zonele de concentratie ridicata spre cele cu concentratie scazuta. Coeficientul de difuzie D are unitatea de masura m2/s.
Ecuatia (1) este cunoscuta sub numele de I-a lege a lui Fick pentru difuzie in regim stationar si caracterizeaza un flux de difuzie constant in timp.
In cazul in care fluxul de difuzie si gradientul de concentratie, intr-un punct oarecare in solvent, variaza in timp, rezulta acumularea sau saracirea speciei de difuzie. Pentru difuzie uniaxiala in conditii nestationare, se utilizeazǎ cea de a II-a lege a lui Fick, data de ecuatia diferentiala:
![]() (2)
(2)
Daca se considera coeficientul de difuzie D independent de concentratie, ecuatia se simplifica:
![]() (3)
(3)![]()
Difuzia uniaxiala este valabila pentru difuzia interstitiala in sistemele binare, monofazice si izotrope (solvent cu structura cristalina cubica), mentinute la presiune si temperatura constante.
Daca difuzia interstitiala are loc in medii anizotrope (solvent cu structuri cristaline necubice), atunci difuzia este triaxiala, deoarece coeficientul de difuzie variaza dupa directia de propagare, iar legea a II-a a lui Fick are forma:
![]() (4)
(4)
In cazul difuziei lacunare in
sistemele binare, apare difuzia a doua specii de atomi, iar coeficientul
de difuzie este inlocuit prin coeficientul de interdifuzie ![]() dat de ecuatia
lui Darken:
dat de ecuatia
lui Darken:
![]() =NADB+NBDA (5)
=NADB+NBDA (5)
unde NA, NB - fractiile atomice ale componentilor A si B; DA, DB - coeficientii partiali de difuzie. Coeficientii partiali de difuzie sunt in general diferiti. In consecinta, difuzia este insotita de crearea de vacante in reteaua cristalina. Aceasta determina efectul Kirkendall, de deplasare a unor repere inerte, plasate initial la interfata cuplului de difuzie, spre componentul cu coeficient partial de difuzie mai mare. Efectul Kirkendall a fost confirmat in cuplurile Cu-Zn; Cu-Sn; Cu-Ni; Ni-Au; Au-Ag.
Legile lui Fick nu sunt valabile pentru sisteme multicomponente. Aceasta este confirmata de difuzia in contra sens (in engleza up-hil). De exemplu, in cuplul de difuzie alcatuit dintr-o bara de otel silicios si alta din otel carbon cu acelasi continut in carbon, carbonul migreaza de la otelul silicios catre otelul carbon. Aceasta arata ca factorul determinant al difuziei nu este in mod necesar diferenta de concentratie, ci inegalitatea potentialelor termodinamice (energia libera). Un component difuzeaza din starea cu un potential termodinamic mai mare la starea cu potentialul termodinamic mai scazut.
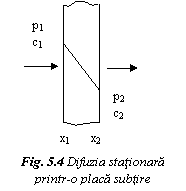
Se considera difuzia atomilor unui gaz printr-o placa
subtire din metal, cu mentinerea
![]() (6)
(6)
 Concentratia se coreleazǎ cu presiunea prin
legea lui Sievert:
Concentratia se coreleazǎ cu presiunea prin
legea lui Sievert:
![]() (7)
(7)
cu s -
![]() (8)
(8)
Aceasta solutie se aplica la difuzia hidrogenului sau
azotului printr-o tabla din otel, cand se mentine
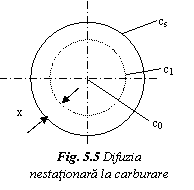
Se considera o piesa cilindrica din otel (fig. 5) cu un continut initial de carbon co, care se imbogateste superficial in carbon intr-o atmosfera gazoasa, capabila sa mentina constanta o concentratie superficiala de carbon cs > co. Concentratia c intr-un punct al zonei carburate, aflat la distanta x de suprafata, dupa timpul t, este dat de solutia ecuatiei (3), care are forma:
![]() (9)
(9)
unde erf este functia erorilor, definita:
![]() (10)
(10)
cu y - variabila de integrare. Functia erorilor
este tabelata in functie de argumentul z =![]() in tabelul 1.
in tabelul 1.
Ecuatia (9) permite calculul duratei de timp, dupa care se obtine o concentratie prescrisa c1 la adancimea x, pentru co, cs si D cunoscute. Pentru aceasta, se reorganizeaza relatia sub forma:
![]() (11)
(11)
Se observa ca pentru c1 dat, partea stanga a
ecuatiei este o
Astfel, pentru (c1 - c0)/(cs - c0) = 0,5, rezulta erf(z) = 0, Din tabelul 1 se obtine z = 0,5205 sau x2 = 1,0837Dt, relatie care exprima dependenta parabolica a adancimii de carburare x de durata de difuzie t.
Tabel 1 Valorile functiei eroare erf(z)
|
z |
erf(z) |
z |
erf(z) |
z |
erf(z) |
|
|
|||||
Marimea coeficientului de difuzie, D, este un indicator al vitezei de difuzie.
Factorii care influenteaza marimea coeficientului de difuzie sunt: temperatura, marimea atomului de difuzie, structura cristalina a solventului, marimea de graunte, densitatea defectelor structurale, concentratia elementului de difuzie, starea de tensiuni.
1. Influenta temperaturii
Temperatura mareste energia de vibratie a atomilor si mareste coeficientul de difuzie. Dependenta coeficientului de difuzie de temperatura se exprima prin relatia:
![]() (12)
(12)
unde D0
- factor de frecventa [m2/s]; E - energia de activare a
difuziei [J/mol]; R = 8,31 J/mol K -
2. Infuenta marimii atomilor de difuzie
Coeficientii de difuzie scad la cresterea razei atomilor de difuzie. Autodifuzia sau interdifuzia atomilor mari metalici prin mecanismul lacunar necesita o energie de activare mai mare decat difuzia atomilor de metaloid cu raza atomica mica prin mecanismul interstitial. Din tabelul 2 reiese ca autodifuzia atomilor de fier este mai dificila decat difuzia la aceeasi temperatura a atomilor de carbon.
3. Influenta structurii cristaline a solventului
Daca solventul prezinta o structura cristalina mai compacta, coeficientii de difuzie sunt mai mici. Astfel, coeficientul de autodifuzie al fierului si cel de difuzie al carbonului in Fea (CVC) sunt, la aceeasi temperatura, mai mari decat in Feg (CFC) cu structura cristalinǎ mai compacta.
4. Influenta marimii de graunte
Din paragraful 2 a reiesit ca in materialele policristaline difuzia poate avea loc: superficial, in volum, pe limita de graunte si prin reteaua de dislocatii (fig. 3) Daca se tine seama de relatia dintre energiile de activare a difuziei, rezulta ca intre coeficientii de difuzie exista inegalitatea: Dsuprafata >>Dlimita Ddislocatii>Dvolum. Cu cat granulatia este mai fina, este o cantitate mai mare de limita de graunte pentru accesul elementului de difuzie, iar difuzia este mai intensa.
Tabel 2 Coeficienti de difuzie si autodifuzie
|
Element de difuzie |
Solvent |
Do [m2/s] |
E [kJ/mol] |
T [oC] |
D [m2/s] |
|
Fe |
Fea (CVC) |
2,0 x 10-4 |
1,1 x 10-20 3,9 x 10-15 |
||
|
Fe |
Feg (CFC) |
5,0 x 10-5 |
1,1 x 10-17 7,8 x 10-16 |
||
|
C |
Fea (CVC) |
6,2 x 10-7 |
2,3 x 10-12 1,6 x 10-10 |
||
|
C |
Feg (CFC) |
1,0 x 10-5 |
9,2 x 10-12 7,0 x 10-11 |
||
|
Cu |
Cu |
7,8 x 10-5 |
4,4 x 10-19 |
||
|
Zn |
Cu |
3,4 x10-5 |
4,3 x 10-18 |
||
|
Al |
Al |
1,7 x10-4 |
4,1 x 10-14 |
||
|
Cu |
Al |
6,5 x 10-5 |
4,8 x 10-14 |
||
|
Mg |
Al |
1,2 x 10-4 |
1,8 x 10-13 |
||
|
Cu |
Ni |
2,7 x 10-5 |
1,5 x 10-22 |
Influenta densitatii defectelor structurale
Coeficientul de difuzie se mareste cu concentratia de vacante si densitatea de dislocatii. De aceea, vitezele rapide de incalzire si deformarea plastica prealabila intensifica difuzia.
6. Influenta concentratiei
Coeficientul de difuzie variaza uneori considerabil cu concentratia. Cercetarile efectuate asupra sistemelor Ni-Cu, Au-Ni etc., au aratat ca D creste cu concentratia elementului de difuzie. La aliajele Fe-C, coeficientul de difuzie a C in Fea nu variaza cu concentratia, datorita slabei solubilitati a C (0,0218%). Limita de solubilitate a C in Feg este 2,11%, ceea ce face ca D sa varieze cu concentratia. Factorul de frecventa Do si energia de activare E scad cu cresterea concentratiei de C. Avand in vedere influenta concentratiei asupra lui D, valoarea determinata experimental are semnificatia unei marimi medii pe intervalul de concentratii considerat.
7. Influenta starii de tensiune
S-a constatat ca, in prezenta unei stari de tensiuni, se produce un flux de difuzie din zonele comprimate catre cele tractionate. Acesta este unul din mecanismele care determina deformarea plastica in conditii de fluaj.
Difuzia atomica este un proces de transfer de substanta in stare solida bazat pe deplasarea atomilor pe distante mai mari decat distanta medie interatomica. Aceasta sta la baza transformarilor in stare solida din aliaje, in timpul deformarii plastice la cald, a tratamentului termic sau termochimic, sinterizarii, omogenizarii chimice la cristalizare, etc. Se diferentiaza autodifuzia (in absenta unui gradient de concentratie) si heterodifuzia (determinata si insotita de modificarea concentratiei locale).
Procesul de difuzie poate fi evidentiat de un cuplu de difuzie, format din doua bare de metal puse in contact intim, incalzite si mentinute timp indelungat sub temperatura de topire. La zona de contact apare o zona aliata, datorata procesului de interdifuzie (deplasarea atomilor unui metal in matricea celuilalt metal).
Difuzia unui atom se face prin salturi activate termic de pe o pozitie de echilibru pe alta vecina. Pentru a difuza un atom trebuie sa aiba atat o pozitie de echilibru libera in vecinatate, cat si energia necesara efectuarii saltului si deformarii elastice a retelei cristaline in timpul saltului.
In volumul cristalului se manifesta mecanisme de difuzie pe baza defectelor punctiforme (ciclic, de schimb, lacunar si interstitial) si pe baza dislocatiilor. Pentru difuzia atomilor metalici, cele mai probabile mecanisme sunt cel lacunar, interstitial indirect si extins. Atomii de metaloid cu raza mica difuzeaza prin mecanismul interstitial direct. In materialele policristaline, difuzia in volumul grauntelui este insotita de difuzia pe limita de graunte si superficiala. Cea mai redusa energie de activare a difuziei este la difuzia superficiala, urmata de difuzia pe limita de graunte si pe reteaua de dislocatii.
Cantitativ, difuzia este evaluata cu ajutorul legilor lui Fick, pentru un regim de difuzie stationar sau nestationar. Legile lui Fick sunt valabile numai pentru difuzia in sistemele bicomponente.
Difuzia este activata de cresterea temperaturii, viteze rapide de incalzire, procese de deformare plastica, stare de tensiuni si prin finisarea granulatiei.
|
Politica de confidentialitate |
| Copyright ©
2025 - Toate drepturile rezervate. Toate documentele au caracter informativ cu scop educational. |
Personaje din literatura |
| Baltagul caracterizarea personajelor |
| Caracterizare Alexandru Lapusneanul |
| Caracterizarea lui Gavilescu |
| Caracterizarea personajelor negative din basmul |
Tehnica si mecanica |
| Cuplaje - definitii. notatii. exemple. repere istorice. |
| Actionare macara |
| Reprezentarea si cotarea filetelor |
Geografie |
| Turismul pe terra |
| Vulcanii Și mediul |
| Padurile pe terra si industrializarea lemnului |
| Termeni si conditii |
| Contact |
| Creeaza si tu |