
Concepte moderne in managementul pacientului politraumatizat
Pacientul politraumatizat reprezinta o preocupare constanta si de actualitate in sistemul medical de urgenta, incidenta acestor cazuri crescand exponential in ultima decada. Sunt sugestive datele statistice care subliniaza ca, in fiecare zi, 70-80 persoane/1.000.000 de locuitori sufera o leziune traumatica; 50% se adreseaza unui serviciu medical, dintre acestia 20% au leziuni cu potential letal, 5% fiind pacienti critici.
Interesul pentru trauma deriva si din faptul ca este un eveniment ce influenteaza semnificativ si constant viata unei comunitati prin variabile statistice, cum sunt mortalitatea, morbiditatea si gradul de invaliditate (deficiente functionale si tulburari asociate irecuperabile). Impactul este si mai mare daca se ia in considerare faptul ca aceasta circumstanta este principala cauza de deces la populatia sub 40 ani, survenind ca un eveniment acut, neasteptat, in plina activitate. La copii, decesele prin trauma au frecventa comparabila cu suma tuturor celorlalte cauze de deces. Chiar daca accidentul este o realitate cotidiana, la noi in tara nu exista o evaluare a fenomenului, in lipsa unui sistem national de monitorizare, de exemplu un registru national de trauma, asa cum s-a initiat in boli oncologice, sfera ORL, etc. De aceea, trebuie sa apelam la date furnizate de National Trauma Data Bank, care subliniaza ca 10% din decesele anuale sunt de cauza traumatica, acestea fiind a treia cauza de deces dupa accidentul vascular cerebral si bolile cardiovasculare.[1] Aceeasi sursa subliniaza ca situatia este dramatica daca analizam decesele la varsta sub 45 ani, categorie la care accidentele rutiere sunt pe primul loc, barbatii tineri totalizand un procent de 40%. Chiar daca in Europa numarul de decese este mai mic (12/100.000 locuitori) fata de alte regiuni ale globului (India 30, Africa 26, America de Sud 18, America de Nord 15/100.000 locuitori), trebuie mentionat ca aceste cifre nu cuprind date din Europa de Est si in nici un caz, din Romania.
Analizand decesele civile prin trauma, Trunkey semnalizeaza distributia trimodala a acestora.[4]
Intr-un prim varf de mortalitate, survenit in primele 30 minute dupa impactul traumatic, sunt cuprinse 50% dintre decese (asocieri traumatice complexe letale), la care supravietuirea este imposibila in conditiile tehnologice si posibilitatilor terapeutice actuale.
Un al doilea varf totalizeaza 30% din decesele prin trauma, care survin in primele 4 ore de la injurie (perioada precoce posttraumatica), fiind vorba aici de pacienti cu instabilitate hemodinamica sau insuficienta ventilatorie majora, care nu pot fi stabilizate.
Cel de-al treilea varf de mortalitate cuprinde 20% dintre decese, care survin peste zile-saptamani dupa trauma, cauzele acestor decese fiind complicatii aparute in perioada de evolutie tardiva prin MSOF, sepsis, tromboembolism pulmonar fatal.
Daca in primul varf de mortalitate, interventia terapeutica nu modifica procentul de mortalitate, al doilea varf poate fi scazut prin imbunatatirea metodelor de evaluare si stabilizare, iar in al treilea varf, mortalitatea poate fi scazuta prin imbunatatirea managementului definitiv, a actului anestezico-chirurgical si a masurilor de terapie intensiva.[5,6]
Una dintre definitiile acceptate, pentru o perioada lunga de timp a fost cea data de Faist, conform careia, politrauma este o stare acuta severa, rezultata in urma unui impact voluntar sau involuntar, mecanic, termic sau chimic din care rezulta leziuni ale mai multor regiuni ale corpului, dintre care cel putin una, sau o combinatie a acestora are impact vital.
Definitiile pun accent insa mai mult pe bilantul lezional si nu subliniaza impactul sistemic pe care il are trauma, impact ce influenteaza direct mortalitatea. Din punct de vedere al consecintelor fizipoatologice, politrauma mai poate fi definitǎ prin prisma scorului de severitate al injuriei (ISS= Injury Severity Score) atunci cand valoarea acestuia este mai mare de 17 si prin prezenta semnelor de SIRS (Systemic Inflammatory Response Syndrome) persistente mai mult de 24 ore, cu aparitia de disfunctii sau chiar insuficiente ale organelor si sistemelor neimplicate initial in injuria traumaticǎ.[2]
Impactul traumatic induce distrugeri locale tisulare de tip contuzie sau
laceratie, hipoxie si hipotensiune ce determina accentuarea
raspunsului de aparare al gazdei atat la nivel local cat si
sistemic cu activarea raspunsului imun si stimularea mecanismelor reparatorii.
Acesta sindrom de raspuns inflamator sistemic (SIRS)
este definit prin prezenta a minimum doua din urmatoarele
criterii clinice (definite de American
Imbunatatirea stategiilor privind ingrijirea pacientului cu leziuni traumatice severe a dus la o scadere semnificativa a mortalitatii de la un procent de 40% in anii '40 la aproximativ 10% in anul 2000 [7]. Acest lucru se datoreaza in principal utilizarii algoritmelor standardizate de ingrijire a pacientului politraumatizat atat in etapa pre-spital cat si in spital. Prognosticul pacientilor este direct legat de timpul scurs de la momentul traumei pana la aplicarea tratamentului definitiv adecvat, de optimizarea transportului catre cel mai apropiat si adecvat spital, intelegand prin acesta ca trebuie sa fie specializat in ingrijirea pacientului politraumatizat [8].
Politraumatismul este entitatea clinica a carei abordare necesita un concept coerent si mai ales unitar, care trebuie sa inceapǎ inca de la locul accidentului, continuandu-se apoi pe parcursul transportului medicalizat, triaj-UPU, sala de operatie, terapie intensiva, recuperare. Abordarea este facuta intotdeauna in echipa, cu mentiunea ca membrii echipei se schimba in functie de momentul de abordare si evolutie a pacientului politraumatizat.[9] Masurile de investigare, monitorizare si tratament sunt cu atat mai ample si cresc in invazivitate, cu cat ne apropiem de abordul specializat in sala de operatie si reanimare. Interventia echipei medicale impusa de bilantul lezional complex si de situatia "de urgenta" se face de cele mai multe ori contracronometru, aici dovedindu-se utilitatea aplicarii cu strictete a protocoalelor de evaluare, diagnostic si de tratament. S-a dovedit ca omiterea oricarei trepte din protocol poate compromite evolutia ulterioara a pacientului.
Principiile de abordare specifice politraumatismelor sunt:
Implicarea unei echipe medicale experimentate (minimum 3 membri), fiecare cunoscandu-si clar rolul si tipul de interventie pe care trebuie sa-l efectueze
Identificarea si tratamentul imediat al leziunilor amenintatoare de viata
Ierarhizarea leziunilor in functie de impactul lor vital cu resuscitarea si stabilizarea functiilor vitale
Abordarea se face pe baza prezumtiei celei mai grave leziuni, cu respectarea ariilor vitale. Acestea trebuie rapid tratate, fara confirmarea paraclinica a diagnosticului (ventilatie, hemodinamica, coloana cervicala)
Leziunile trebuie tratate concomitent cu stabilirea diagnosticului si monitorizarea pacientului. Monitorizarea este continua, crescand rapid in invazivitate
Reevaluare continua, tinand cont ca aceste leziuni se pot modifica in dinamica.
Cuvintele cheie sunt: rapid, atent, ordonat.
Cel mai folosit si acceptat protocol de evaluare initiala si management al pacientului politraumatizat este Advanced Trauma Life Support (ATLS®) elaborat de catre American College of Surgeons. Avand la baza principiul "orele de aur ale socului", se considera ca leziunile cu impact vital trebuie abordate pe baza unui algoritm standard de diagnostic si tratament in primele ore-minute de la trauma acestea fiind incluse in ghidul ATLS[10].
Abordarea terapeutica standard a acestor pacienti este alcatuitǎ din urmǎtoarele etape succesive:
evaluarea primarǎ si resuscitarea cu stabilizarea functiilor vitale
evaluarea secundarǎ detailatǎ a tuturor leziunilor traumatice
initierea tratamentului definitiv al leziunilor (in general tratament chirurgical si de terapie intensivǎ)
evaluarea tertiarǎ (la 24 ore de la traumǎ pentru completarea definitivǎ a bilantului lezional)
Momentele-cheie de abord ale pacientului se deruleaza in teren (locul accidentului), triaj- UPU, sala de operatie, STI, sectia care este implicata in ingrijirea leziunilor cu evolutia cea mai lenta, reabilitare pana la reintegrarea in activitate. Protocoalele de evaluare primara abordate in teren se continua in spital pana la stabilizarea functiilor vitale, moment in care se incepe evaluarea secundara. Managementul definitiv (tertiar - actul anestezico-chirurgical) incepe in sala de operatie si este continuat apoi in terapie intensiva. Un bilant lezional complex, cu leziuni care au impact vital ce nu pot fi stabilizate, poate intrerupe evaluarea la nivel primar si poate orienta pacientul direct spre sala de operatie, unde se continua tratamentul initiat pentru stabilizarea pacientului si mentinerea functiilor vitale. Concomitent, se incepe interventia chirurgicala, care la acest tip de pacient (urgenta de gradul I), se rezuma la masuri menite sa contribuie la stabilizare (de ex. oprirea sangerarilor). Daca pacientul este stabilizat in etapa primara, el va continua a doua treapta a protocolului, evaluarea secundara, care prelungeste etapa preoperatorie cu un timp suficient pentru investigatii suplimentare, pe aparate si sisteme, necesare pentru definirea leziunilor acute traumatice si a patologiei asociate. Acestea sunt urgente de gradul II.
Momentul anestezico-chirurgical nu este izolat, el trebuie judecat si inteles in contextul pacientului politraumatizat, trebuie adaptat momentului de resuscitare, care incepe inca de la locul traumei si se continua intraoperator si in terapie intensiva.
Pacientul politraumatizat cu un ISS > 17 este un pacient critic, pentru care ansamblul de masuri ce presupun internarea in STI (monitorizare, terapie suportiva complexa) este absolut necesar pentru supravietuire. Nu trebuie neglijat ca acest pacient cu multiple disfunctii si cu instabilitate marcata va trebui supus actului anestezico-chirurgical in urgenta, ceea ce presupune prezenta tuturor factorilor agravanti ai acestei situatii: stomac plin, examen preanestezic sumar (comprimat de criza de timp impusa de gradul de urgenta sau lipsa de dialog cu un pacient aflat in coma) ceea ce explica saracia de date in ceea ce priveste patologia preexistenta si medicatia cronica aferenta. Desigur, nu se pune problema unei perioade de timp pentru premedicatie corespunzatoare. Managementul definitiv al acestor pacienti incepe inca din sala de operatie. Abordarea chirurgicala este de obicei interdisciplinara, cat mai precoce posibil, interventiile sunt esalonate in ordinea impactului lor vital, complexitatea si timpul necesar rezolvarii leziunilor nu sunt previzibile de la inceput. Conceptul modern urmareste ca intr-un singur timp anestezic sa se rezolve si sa se stabilizeze toate leziunile traumatice (early total care). Totusi, exista anumite categorii de pacienti la care aceasta atitudine este detrimentala (de exemplu, pacienti cu sangerare masiva ce au dezvoltat deja coagulopatia si la care se fac doar interventiile de oprire a hemoragiei, urmand a fi transferati cat mai repede in Terapie Intensiva pentru reechilibrare si resuscitare adecvata - conform principului "damage control"). Anestezia generala balansata trebuie adaptata cazului, asocierile farmacologice fiind mai putin importante decat sustinerea functiilor vitale si protectia antisoc. Resuscitarea si monitorizarea pacientului incepute inca din etapele anterioare, cresc in invazivitate si amploare in aceasta etapa.
Trebuie mentionat ca in contextul unei politraume, chiar daca interventia chirurgicala este minora, "anestezia generala este intotdeauna majora". Politraumatismul este una dintre situatiile in care mijloacele tehnice avansate, existente la ora actuala in terapiile intensive isi dovedesc pe deplin utilitatea: aparate de anestezie, ventilatoare performante, cell-saver, aparat de incalzire si perfuzie rapida ( LEVEL 1), incalzitoare externe (paturi cu aer cald).
Pacientul politraumatizat, prin complexitatea bilantului lezional (ISS > 17) cat si a raspunsului multisistemic consecutiv, necesita ingrijiri specifice pacientului critic, intrunind si din acest punct de vedere, criteriile valide internarii in sectia de terapie intensiva. Analizand mai in detaliu motivele pentru care trauma multipla are aceasta adresabilitate, pornim de la faptul ca acesti pacienti au nevoie de o monitorizare complexa, adesea invaziva.
4.1. Trauma multipla - entitati clinice critice
In contextul politraumatismului, se impune recunoasterea si rezolvarea unei ecuatii care are doi termeni importanti:
un prim termen reprezentat de totalitatea leziunilor produse de trauma la nivelul diverselor organe si sisteme
un al doilea termen, este reprezentat de efectele sistemice induse de trauma: soc, raspunsul inflamator sistemic (declansat imediat posttraumatic), tulburari ale echilibrului fluido-coagulant, la care se sumeaza efectele produse de circumstantele agravante caracteristice - hipotermie, acidoza
Exista cateva situatii particulare in bilantul lezional traumatic, care necesita inca de la sosirea in spital ingrijiri in terapia intensiva.
Pacientul cu trauma multipla, care in etapele primare a fost resuscitat, beneficiaza de intregul arsenal suportiv mentionat anterior. Ca o paranteza, trebuie insa subliniat, ca din pacate, resuscitarea in conditii de teren a pacientilor politraumatizati aflati in stop cardiorespirator are o rata mica de succes (< 6%), iar dintre acesti pacienti peste 80% raman cu sechele neurologice grave. Daca stopul cardiac este surprins in conditii de spital, succesul este > 50% si sechelele sunt mult mai mici. Sigur ca aceasta presupune ca pacientul politraumatizat sa fie monitorizat de la admisie, acest lucru facilitand recunoasterea rapida a tipului de oprire al inimii: fibrilatie ventriculara, asistolie, disociatie electromecanica. Cel mai frecvent stop cardiac la pacientul cu trauma este prin disociatie electromecanica, avand ca factori etiologici asocierea urmatoarelor situatii: hipotermia, diselectrolitemia, hipoxia, acidoza, hipovolemia, tamponada cardiaca, pneumotoraxul sufocant, embolia pulmonara.
Evaluarea primara si secundara in conditii de spital presupune monitorizarea hemodinamica, biochimica, hematologica, ceea ce va determina recunoasterea si tratarea precoce a tuturor cauzelor precipitante ale stopului cardiac, mentionate mai sus, care poate fi eventual prevenit.
Trauma craniana severa reprezinta prin ea insasi o situatie critica, deloc de neglijat atunci cand analizam si procentul de implicare a acestuia in bilantul lezional. Aceasta circumstanta va reprezenta o alta situatie in care pacientul este internat in terapie intensiva. Definita la un GCS ≤ 8, ea este responsabila de decesul a 30-50% dintre pacientii cu trauma multipla. Atunci cand se asociaza cu socul hemoragic, mortalitatea ajunge pana la 68%.
In trauma craniana, se descriu doua tipuri distincte de leziuni cerebrale, care schematic pot fi descrise astfel:
o producerea unui defect de membrana axonala, cu alterarea schimburilor ionice (Ca2+), cu depolarizare axonala consecutiva si anomalii ale transmiterii impulsului in reteaua neuronala, producandu-se in final disfunctie neuronala globala. Expresia clinica in acest tip de leziune va fi coma primara
o distructie nodala si leziune interna axonala, cu producerea unei degenerari axonale (acumulare intracelulara de Ca2+), ulterior cu sau fara regenerare axonala
Pentru a putea trata si evalua dezvoltarea leziunii secundare, care este responsabila in mare parte de sechelele postraumatice cerebrale, si care agraveaza prognosticul si creste mortalitatea in perioada de spitalizare, este absolut necesara monitorizarea invaziva a presiunii intracraniene (PIC), procedeu care trebuie introdus de rutina ("gold standard"). In functie de valoarea PIC, se adapteaza in general toate masurile terapeutice suportive, obiectivul principal fiind mentinerea acesteia sub 15 mmHg. Schematic, trauma multipla care are in bilantul lezional TCC sever, are urmatoarele principii terapeutice:
Intubatie precoce cu ventilatie mecanica (obligatoriu la GCS<8), cu mentinerea normoxiei, normocapniei
Repletie volemica si suport vasoconstrictor si inotrop pentru mentinerea: tensiunii arteriale mediii (TAM) peste 90 mmHg, presiunea de perfuzie cerebrala (PPC) peste 60-70 mmHg, normovolemie, hematocrit peste 30%
Analgosedare, relaxante neuromusculare
Mentinerea normotermiei
Mentinerea normala a osmolaritatii plasmatice, cu controlul valorilor Na+, glicemiei
Pozitionarea capului usor ridicata pana la 30s, fara torsiuni ale gatului pentru a favoriza drenajul venos
Interventie neurochirurgicala cand aceasta este indicata
Monitorizarea presiunii intracraniene (PIC)
Specific pentru trauma craniana este tratamentul prompt al edemului cerebral, care cuprinde cateva masuri-cheie:
aprofundarea analgo-sedarii
cresterea TAM pentru a mentine PPC > 60 mmHg (PPC=TAM-PIC)
terapie osmotica in primele 48 de ore, prin administrarea de bolusuri de manitol (0,25-1g/kgc)
drenajul LCR daca este posibil
alte masuri care se aplica individualizat sub o monitorizare stricta, pentru perioade scurte de timp: hipotermie moderata (34 - 35C), coma barbiturica, hiperventilatie
In ceea ce priveste traumatismul spinal, dupa evaluarea primara si secundara, orice fractura de coloana vertebrala, cu sau fara interesare medulara (chiar daca sectiunea este completa), are indicatie de stabilizare chirurgicala, cat mai precoce posibil. In lipsa acestei atitudini terapeutice, masurile de ingrijire si nursing sunt extrem de dificile. Nivelele inalte de trauma toracica (peste T3 -T4) necesita ingrijiri complexe, pornind chiar de la necesitatea instituirii suportului ventilator. Trebuie insa mentionat ca, desi exista multe controverse, se discuta si in contextul traumei medulare posibilitatea limitarii evolutiei leziunilor secundare (edemul si hemoragia centromedulara) prin instituirea masurilor terapeutice precoce, adaptate fiecarui caz in parte. In lipsa unei terapii adecvate, acestea se extind cateva nivele medulare (deasupra si dedesubtul nivelului de impact traumatic). Se readuce in discutie conform controversatului studiu NASCIS, corticoterapia initiata in primele 8 ore de la trauma spinala dupa urmatoarea schema: metilprednisolon 30 mg/kgc bolus administrat in o ora urmata de 5,4 mg/kgc/h in urmatoarele 24 de ore.[12]
Referindu-ne la componenta toracica a unui bilant lezional complex, exista leziuni specifice care fac din pacientul politraumatizat un pacient care necesita ingrijiri in terapie intensiva. Astfel:
4.1.4.1. Leziunile imediat letale
Leziunile imediat letale (ruptura de cord, ruptura de aorta / vena cava) ajung foarte rar la spital, decesul survenind de cele mai multe ori in teren. Atunci cand ruptura de cord sau de vase mari nu produce imediat decesul, pacientul fiind in soc hemoragic, ajunge direct in sala de operatie, unde concomitent cu evaluarea primara se instituie manevre complexe de stabilizare a functiilor vitale. Ulterior, acesti pacienti vor fi ingriji in terapie intensiva.
4.1.4.2. Leziunile rapid letale
Leziunile rapid letale (obstructia de cai aeriene, pneumotorax compresiv, hemotorax masiv, volet costal / torace moale, tamponada cardiaca, dilacerare de aorta / vase mari, ruptura traheobronsica) sunt de cele mai multe ori abordate in teren, in timpul evaluarii primare si secundare, pentru insuficienta respiratorie acuta. Daca aceste leziuni nu sunt stabilizate dupa manevrele chirurgicale adaptate fiecarei leziuni in parte si insuficienta respiratorie persista, ingrijirea se va face in terapie intensiva. Acest lucru se datoreaza in principal necesitatii suportului ventilator, initiat pe criterii largi, clasice (semne de insuficienta respiratorie: apnee mai mult de 2-3 minute, frecventa respiratorie sub 10/minut si peste35/minut, PaO2 55 mmHg si PaCO2 > 55 mmHg, pH < 7,2). Exista insa o serie de indicatii de ventilatie mecanica specifice politraumei:
a) GCS < 10 (incluzand ingestia concomitenta de alcool si droguri)
b) obstructie de cai aeriene
c) volet costal (anterior, peste 8 coaste), trei coaste cu TCC sau fractura de stern
d) contuzie pulmonara severa
e) oboseala muschilor respiratori
f) necesitatea sedarii sau analgeziei
g) traumatism toracic asociat cu boala pulmonara cronica / varsta inaintata
h) asocierea a trei sau mai multor leziuni traumatice
i) soc. [13]
O situatie particulara o reprezinta voletul costal, mai ales cel anterior (fractura a cel putin 3 coaste adiacente in doua sau mai multe locuri, ce creeaza un fragment toracic cu mobilitate paradoxala, segmentele implicate pierzand continuitatea cu restul cutiei toracice, compromitand mecanica ventilatorie). De cele mai multe ori, voletul costal este insotit de: contuzie pulmonara (care este frecvent cauza de ARDS primar- Acute Respiratory Distress Syndrome), hemotorax, pneumotorax. Pacientul are dureri mari in inspir, ceea ce limiteaza suplimentar miscarile respiratorii. Astfel, insuficienta respiratorie ce apare in contextul voletului costal are mai multe cauze:
dinamica toraco-pulmonara compromisa
alterari ale difuziunii alveolo - capilare
restrictie pulmonara
sunt intrapulmonar crescut.
Tratamentul consta in fixarea voletului prin mijloace externe sau prin fixare interna chirurgicala asociat cu ventilatie mecanica, cea din urma dovedindu-si superioritatea. Indicatiile pentru fixare sunt cazurile critice: mai mult de 3 coaste rupte concomitent cu TCC sau fractura de stern, mai mult de 8 coaste adiacente rupte, volet anterior, torace moale.
O alta situatie critica ce orienteaza pacientul cu trauma multipla din momentul evaluarii primare spre terapie intensiva o constituie tamponada cardiaca (de cele mai multe ori sunt suficienti 200 ml sange pentru a crea tabloul clinic, fara ca examenul radiologic sa aiba mare valoare diagnostica in aceasta situatie) 14,15] Elementele clinice trebuie rapid recunoscute si interpretate in contextul traumei. Astfel, triada lui Beck consta in recunoasterea zgomotelor cardiace asurzite, hipotensiune, jugulare turgescente, acest din urma semn putand lipsi daca pacientul este in soc hipovolemic. Pot fi prezente semnele Küssmaul (accentuarea distensiei venelor gatului in inspir, puls paradoxal), matitate cardiaca si traseul EKG microvoltat. Pacientul este in soc cu raspuns hipodinamic, determinat de scaderea functiei de pompa cardiaca, prin scaderea umplerii diastolice, limitata de lichidul pericardic. Pattern-ul hemodinamic al sindromului de debit cardiac mic este, in acest context, debitul cardiac scazut si presiunea in capilarul pulmonar blocata (PCWP) crescuta. [16] Tratamentul este complex, concomitent cu diagnosticul si tratamentul tuturor leziunilor traumatice toracice si extratoracice. Presupune efectuarea rapida a pericardiocentezei (ulterior in sala de operatie pericardiotomie, fereastra pericardica), concomitent cu umplere volemica si stabilizare hemodinamica. [17]
4.1.4.3. Leziuni cu potential letal
Leziuni cu potential letal (contuzia pulmonara, contuzia miocardica, ruptura/ hernia de diafragm, ruptura/perforatia de esofag). Contuzia pulmonara si contuzia miocardica sunt leziuni specifice, tratate in terapie intensiva, unde pacientii ajung de obicei dupa o evaluare primara si secundara complexa, prin care se stabilizeaza si se evalueaza suplimentar toate regiunile traumatizate.
Contuzia pulmonara este rezultatul aplicarii unei forte mecanice direct asupra plamanului, fiind o entitate postraumatica cu un diagnostic dificil. Morfologic, apar: edem alveolar, laceratii pulmonare, infiltrate sanguine, zone in care este afectata profund hematoza pulmonara.[18] Asocierea cea mai frecventa in context traumatic, asa cum am mentionat, este cu voletul costal. Clinic apare insuficienta respiratorie hipoxemica acuta, necontrolabila prin oxigenoterapie, expresie a colapsului alveolar, sunt intrapulmonar dreapta-stanga, cu dispnee, polipnee, cianoza, uneori hemoptizie, murmur vezicular diminuat. Imaginea radiologica si CT care pot fi normale initial, se modifica rapid (24-36 ore), apar infiltrate pulmonare extensive. In functie de severitatea contuziei pulmonare, evolutia spre ALI (Acute Lung Injury) sau ARDS variaza intre 10-40%. Diagnosticul diferential cu pneumonia de aspiratie este foarte greu de facut, mai ales la debut; cele doua entitati clinice pot coexista. [19,20]
Atitudinea terapeutica vizeaza atat leziunea pulmonara in sine, cat si factorii precipitanti si comorbiditatile.[21,22] Se tenteaza ori de cate ori este posibil ventilatie noninvaziva, sub controlul strict al parametrilor arteriali (PaO2 55-80 mmHg). Daca acest lucru nu este posibil, atunci se recurge la IOT si ventilatie mecanica, urmarindu-se mentinerea unui PEEP optim, FiO2 minim necesar, volum curent = 5-8 ml/kgc, presiunea de platou < 30 cmH2O. [23] In ultimii ani s-a impus utilizarea ventilatiei pulmonare protective in scopul de a reduce cat mai mult lezinile iatrogene induse de aceasta si anume a volutraumei si barotraumei (leziuni alveolare datorita folosirii unui volum curent si a unei presiuni de inspir prea mari). Pacientul trebuie in acest scop analgosedat si numai daca este necesar se folosesc relaxante neuromusculare. Antibioticele se utilizeaza numai in conditiile existentei unei infectii, ideal sustinuta bacteriologic, folosirea lor fiind conforma cu antibiograma. Utilizarea steroizilor este contraindicata.
Contuzia miocardica este mult mai frecventa decat sugereaza studiile existente pana acum. Aproximativ 60% din traumatismele toracice inchise sunt insotite de contuzii miocardice, care imbraca forme de gravitate variabile: de la forme asimptomatice pana la leziuni ischemice intinse, rupturi de cordaje, valve sau de cord.
Diagnosticul se bazeaza pe recunoasterea in context de traumatism toracic a modificarilor EKG (tahicardie sinusala fara alta cauza, alternanta tahi-bradicardie, extrasistole atriale, extrasistole ventriculare, fibrilatie atriala sau blocuri de ramura, unde T inversate, ST supradenivelat). Specifica insa pentru diagnostic este dozarea enzimelor cardiace: troponina, CK-MB.[24] Troponina, enzima cardiaca specifica, reflecta modificarile ischemice cardiace, mai ales atunci cand valorile sunt urmarite in dinamica (creste extrem de rapid - in 4 ore - si se mentine crescuta cateva zile). Troponina este markerul cel mai fidel al contuziei miocardice, inca din camera de garda. Analiza se va repeta din 4 in 4 ore, fiind mai fidela pentru leziunea ischemica cardiaca decat CK, CK-MB, respectiv raportul intre ele. Daca valoarea troponinei se asociaza cu modificari EKG in primele 12 ore, specificitatea pentru contuzie miocardica creste extrem de mult, aceasta combinatie fiind cel putin comparabila ca valoare cu datele furnizate de ecocardiografia transesofagiana.[25] Aceasta din urma este sugestiva pentru contuzie miocardica, cand pune in evidenta anomalii de contractie a peretilor, cu sau fara prezenta lichidului pericardic. Tratamentul leziunii este clasic, suportiv (monitorizare EKG continua, oxigenoterapie, analgezie, etc), cu accent pe preventia si tratarea tulburarilor de ritm. Prognosticul este mai bun ca in infarctul de miocard acut, fara anomalii functionale cardiace.
Ruptura diafragmatica este frecvent secundara unui traumatism toracic sau abdominal inchis, in urma carora rezulta o laceratie neregulata de dimensiuni suficient de mari pentru a permite hernierea continutului abdominal in torace. Semnele clinice pot apare imediat posttraumatic, dar frecvent sunt evidente la distanta de momentul traumatic. Simptomatologia este variabila, de obicei se remarca deteriorarea functiei respiratorii si cresterea presiunii intraabdominale. Clinic, apare dispnee (la pozitionare in decubit), durere toracica, lichid de lavaj peritoneal sau continut gastric pe pleurostoma. Aspectul radiologic evidentiaza hemidiafragmul ascensionat sau non-vizibil, infiltrate pulmonare dense bazale, hernierea stomacului (vizualizarea sondei naso-gastrice in torace), hernierea intestinului, ficatului in torace. Pentru confirmare se efectueaza examen CT torace inferior. Pe toata perioada necesara pentru diagnostic, se mentine sonda nazogastrica pentru decompresia stomacului. Interventia chirurgicala se efectueaza imediat la internare, laparatomia rezolvand concomitent si alte asocieri traumatice ale organelor abdominale. Manifestarea tardiva a rupturii diafragmatice va avea sanctiune chirurgicala, preferandu-se de data aceasta toracotomia. In postoperator, pacientul se ventileaza mecanic aproximativ 48 ore pentru a oferi protectie suturilor de diafragm.[26]
4.1.4.4. Leziunile toracice non-letale
Leziunile toracice non-letale (pneumotorax simplu, hemotorax simplu, fracturi costale, fractura de stern, fractura de clavicula, fractura de scapula, luxatia sterno-claviculara), se rezolva de obicei de catre chirurg, ortoped, pacientii fiind apoi ingrijiti in salonul de postoperator. Rar, cand fenomenele de insuficienta respiratorie nu sunt amendate de manevrele simple, clasice (pleurostome, fixarea externa sau interna a fracturilor), pacientul va fi ingrijit in terapie intensiva, unde preocuparea principala va fi stabilizarea functiilor vitale, plecand de la insuficienta ventilatorie. Concomitent, trebuie diagnosticate si tratate comorbiditatile care agraveaza tabloul clinic, fie cele traumatice (ex. contuzie pulmonara), fie bolile asociate (BPOC, astm bronsic).
Atitudinea terapeutica este nuantata de doua situatii distincte, trauma abdominala inchisa sau deschisa.
In trauma abdominala deschisa (penetranta), pacientul poate fi instabil hemodinamic, cu valori extrem de mici ale presiunii arteriale, de obicei fiind evidenta hemoragia externa, ceea ce necesita reechilibrare volemica, concomitent cu interventie chirurgicala hemostatica, inainte chiar de investigatii paraclinice diagnostice. Daca semnele de mai sus nu apar, pacientul poate fi supus unei evaluari secundare cat mai ample, cu continuarea investigatiilor paraclinice prin examen ecografic abdominal seriat. Evidentierea la acest examen a unei modificari traumatice intraabdominale poate impune de urgenta interventia chirurgicala; in caz contrar, pacientul se urmareste cel putin 48 ore. Rezultatul neconcludent in contextul unei simptomatologii incerte impune examen CT abdominal sau chiar examen laparoscopic.
In trauma abdominala inchisa (nepenetranta), existenta instabilitatii hemodinamice concomitente, care sugereaza prezenta unei sangerari intraabdominale (cel mai frecvent prin leziunea unui organ parenchimatos), impune laparotomia de urgenta (daca este posibil dupa examen ecografic sau CT de control). Prezenta semnelor de peritonita, care ridica suspiciunea lezarii unui organ cavitar, va orienta de asemenea catre interventia chirurgicala de urgenta.
Studii recente care abordeaza traumatismul abdominal in lumina noului concept de "damage control surgery", impun ca necesara efectuarea examenului CT abdominal cu contrast inca din momentul aplicarii algoritmului ATLS. [27,28] Extravazarea substantei de contrast impune fie interventia chirurgicala de urgenta pentru leziunea unui organ parenchimatos, fie chemoembolizare pe plexuri vasculare distruse (hematom retroperitoneal) cand leziunea nu are o sanctiune chirurgicala posibila (fracturi extinse de bazin). Toate acestea se efectueaza concomitent cu masurile de terapie de sustinere, care vizeaza in primul rand corectarea circumstantelor agravante posttraumatice: acidoza, hipotermia, coagulopatia de consum. In prezenta acestora, tratamentul chirurgical se va rezuma la stabilizare, hemostaza (conform principiilor de "damage control surgery"). Daca in urma evaluarii ATLS pacientul este stabil, poate fi rezolvat chirurgical definitiv per primam.
Analizand incidenta diferitelor leziuni traumatice in bilantul lezional complex al unei politraume, se observa ca imediat dupa TCC care are o frecventa de 65%, se situeaza traumatismul de bazin si de membre in procent de 61%. Modalitatea de abordare a acestora este dictata de evaluarea primara, care presupune un control riguros al membrului superior, inferior si al centurilor aferente, insotit intotdeauna de evaluare vasculara si neurologica, pentru excluderea eventualelor asocieri.
Daca radiografia de bazin atesta prezenta unei fracturi de bazin instabile, (ce poate presupune pierderi sanguine pana la 3-5 l prin leziunea de plexuri vasculare aferente, a caror sangerare este necontrolabila chirurgical), atitudinea terapeutica va consta in fixarea temporara a bazinului cu fixator extern. Aceasta permite evaluarea radiologica si ecografica a complexitatii leziunii si diagnosticarea eventualelor asocieri traumatice a organelor din micul bazin, a caror prezenta impune interventia chirurgicala de urgenta, concomitent cu fixarea externa a bazinului. Solutia chirurgicala definitiva urmeaza dupa saptamani. Fractura stabila permite un timp mai lung de investigare pentru CT, care poate evidentia prezenta sangerarii in micul bazin, care, daca este masiva, impune angiografie cu embolizarea vaselor interesate si subsecvent fixarea externa. [29]
Fractura oaselor lungi insotita de hemoragie externa, are ca prim gest oprirea sangerarii. In prezenta fracturii inchise de femur, care implica o pierdere de 1,5 l sange, se verifica perfuzia periferica, functia senzoriala/motorie, integritatea tesuturilor moi si, pe cat posibil, diagnosticarea cat mai precoce a unui sindrom de compartiment. Daca acest examen este negativ, solutia chirurgicala ortopedica este per primam definitiva. Asocierea fracturilor de oase lungi cu leziuni toracice bilaterale severe, cu soc hemoragic (cu trauma abdominala sau pelvina) sau cu sindrom de compartiment implica aplicarea principiilor "damage control orthopedics" (fasciotomii largi, hemostaza, decontaminare si stabilizare externa). Daca aceste interventii nu-si dovedesc eficienta, membrul afectat va trebui amputat.
Sindromul de compartiment periferic, prin impactul sau sistemic si implicatiile directe asupra morbiditatii si mortalitatii prin trauma, constituie o entitate particulara. El este reprezentat printr-un edem masiv al unei loji musculare sau a unui segment de membru care determina ischemie marcata. Efectuarea de urgenta a fasciotomiei si debridarilor largi evita interventii laborioase ulterioare si chiar amputarea segmentului respectiv. Repermeabilizarea tardiva a axului vascular poate duce ulterior la sindromul de reperfuzie ce precipita aparitia insuficientei multiple de organe (cea mai precoce si specifica fiind insuficienta renala).
complexa.
Pacientii cu trauma multipla beneficiaza de monitorizare neinvaziva clasica inca din teren (tensiune arteriala, alura ventriculara, EKG, temperatura, SpO2, diureza, frecventa respiratie), dar pe masura evolutiei cazului, monitorizarea se amplifica in functie de amploarea cazului, individualizat pentru fiecare caz in parte. De multe ori, monitorizarea presiunii venoase centrale si a presiunii arteriale invazive (cateterului venos central si a celui arterial) care se instituie ca manevre initiale, nu furnizeaza date suficiente pentru conducerea tratamentului. Astfel, devin necesare:
masurarea presiunii intracraniene, ca marker de evolutie a edemului cerebral in trauma cerebrala severa ;
montarea individualizata a cateterului Swan-Ganz pentru:
evaluarea profilelor hemodinamice in definirea formelor de soc
evaluarea functionalitatii cordului stang - inotropism alterat in contuzia miocardica sau insuficienta cardiaca hipodiastolica cu umplere deficitara a ventriculului stang in tamponada cardiaca, pneumomediastin sau pneumotorax compresiv
evaluarea rezistentelor pulmonare si periferice ca raspuns la terapie
In final, vom avea variabile de control atat pentru macrocirculatie (debit cardiac, SVO2, DO2, VO2, O2ER), cat mai ales pentru microcirculatie (deficit de baze, gaura anionica, lactat, gradient CO2 venos / arterial, CO2 / pH gastric intramucos), importante pentru evolutia temporala a pacientului politraumatizat si pentru prognostic.
Importanta acestei monitorizari complexe deriva din faptul ca la orice pacient critic si in cazul traumei multiple conducerea terapiei nespecifice suportive necesita elemente de fiziopatologie care sunt reflectate de parametrii mai sus mentionati. Cu alte cuvinte, nu numai mentinerea functiilor vitale este esentiala pentru prognosticul acestor pacienti, dar mai ales mentinerea homeostaziei la nivel periferic, tisular.
Obiectivele terapeutice sunt:
Realizarea acestor obiective terapeutice presupune ca sectia in care se ingrijesc astfel de pacienti sa poata aplica intregul arsenal de masuri nespecifice suportive (suport ventilator, vasopresor, inotrop, renal, metode alternative de nutritie, analgezie si sedare multimodala).
Asa cum s-a aratat mai sus, cunoasterea cat mai precoce si exacta a substratului lezional va impune sanctiune chirurgicala rapida (acesta reprezentand tratamentul etiologic). Trebuie subliniat impactul sistemic al traumei multiple. Importanta elementelor sistemice deriva nu numai din faptul ca ele pot avea acelasi potential letal ca oricare dintre leziunile traumatice primare, dar nerecunoscute si netratate la timp pot agrava evolutia acestora din urma, influentand direct morbiditatea si mortalitatea pacientilor politraumatizati. Acest al doilea termen de care vorbeam mai sus, reprezentat de marile sindroame fiziopatologice care insotesc trauma multipla, vor defini:
complexitatea cazului
gradul de urgenta, in functie de care se vor initia protocoalele de resuscitare, evaluare si tratament primar si secundar
ierarhia treptelor terapiei nespecifice, indicand prioritatile in care se vor derula masurile terapeutice pe intreaga perioada postraumatica.
Acest raspuns complex al organismului face ca trauma multipla sa fie considerata o boala multisistemica, iar pacientul politraumatizat un pacient critic. Vom descrie pe scurt cateva din aspectele specifice raspunsului sistemic in context traumatic.
Socul in trauma multipla este definit ca un sindrom multifactorial acut, caracterizat printr-o perfuzie tisulara deficitara, raportata la nevoile tisulare, tradusa printr-o discrepanta intre transportul de O2 (DO2) si consumul de O2 (VO2). Rezultatul final, in lipsa unei terapii eficace, va fi disfunctia severa a organelor vitale, cu evolutie pana la deces.
Desi derularea si evolutia socului este marcata de elementele periferice (tisulare/celulare), parametrii ca: TA, DC, PVC sunt utilizati pentru definirea diferitelor forme de soc, fiind mult mai accesibile si mai usor de monitorizat. Stabilizarea acestor elemente hemodinamice are drept scop tocmai mentinerea integritatii functionale periferice. Definirea profilului hemodinamic in soc este esentiala pentru deciziile terapeutice. Modificarile hemodinamice sunt extrem de variate la pacientii politraumatizati, ele fiind dictate si depinzand de leziunea traumatica primara, care induce aparitia fenomenelor de soc. Cu alte cuvinte, chiar daca formele de soc pot coexista in trauma (de exemplu soc hipovolemic, urmat imediat de soc septic), predomina intotdeauna una din reactiile de raspuns caracteristice socului, reactia hipo- sau hiperdinamica.
Socul traumatic are incidenta cea mai mare (73% in studiul nostru), situatie particulara in care recunoastem atat elemente de raspuns hipodinamic declansate de scaderea VSCE (mai putin evidenta ca in socul hemoragic), cat si elementele raspunsului hiperdinamic induse de leziunea tisulara-celulara traumatica, frecvent foarte extinsa. Aceasta din urma determina utilizarea deficitara la nivel celular - tisular a O2..
Reactia hipodinamica insoteste formele de soc in care debitul cardiac este scazut ca urmare a impactului traumatic primar asupra unuia din determinantii sai majori. In situatia unor leziuni traumatice ce determina pierderi masive de sange apare tabloul clinic de soc hemoragic. Socul cardiogen se produce prin alterarea contractilitatii miocardice prin contuzie miocardica sau in sindromul de DC mic din tamponada miocardica. Socul spinal apare cand leziunea medulara prin simpaticoliza produce o vasodilatatie enorma si consecutiv scaderea rezistentei periferice; astfel VSCE desi nemodificat ca valoare absoluta, este relativ scazut, prin discrepanta "dintre continut si continator".
Mai rar, poate exista un raspuns hiperdinamic, specific socului septic, in situatii cum ar fi:
solutii de continuitate tegumentara, cu patrunderea prin aceste plagi a unor germeni de virulenta extrema, inca din momentul traumatic
peritonita posttraumatica prin leziune primara enterala (leziune de organ cavitar digestiv)
Mentinerea unei discrepante intre DO2 si VO2, in lipsa unei interventii terapeutice precoce, sustinute si eficiente, duce la disfunctia severa a organelor vitale si deces. Este deja foarte bine cunoscut faptul ca hipovolemia neglijata va declansa un ciclu de autoagravare spre disfunctie severa de organe. Necorectarea volumului sanguin scazut in circumstante traumatice, va mentine un debit cardiac redus, ce presupune un DO2 sub nivelul minim necesar.[30] Aceasta alterare hemodinamica va declansa o serie de mecanisme compensatorii, care in prima faza au ca rezultat vasoconstrictie si perfuzie periferica inadecvata, in special in teritorii care nu au impact vital. Ca o consecinta a acestui flux capilar inadecvat, va apare ischemia tisulara. Impactul va fi in primul rand asupra unor organe cum sunt rinichiul si intestinul, consecinta imediata fiind eliberarea de endotoxine. Translocatia bacteriana postischemica duce rapid la soc septic si chiar la deces.
Tulburarile macrocirculatorii sunt imediat urmate de modificari importante la nivel microcirculator, cu ischemie tisulara si celulara, cu declansarea imediata a raspunsului inflamator, cu eliberare de mediatori (citokine, oxid nitric, etc) si edem tisular marcat, ceea ce agraveaza in cerc vicios tulburarile circulatorii deja instituite.
In cazul pacientului politraumatizat, scaderea aportului tisular periferic se poate datora mai multor cauze:
scaderea debitului cardiac prin unul sau mai multi determinanti majori (contuzie miocardica, hipovolemie, etc)
scaderea schimburilor alveolo-capilare - insuficienta pulmonara postraumatica (trauma toracica, contuzie pulmonara etc)
scaderea transportorului - scaderea concentratiei de hemoglobina (hemoragie acuta postraumatica)
Indiferent de mecanismul absolut sau relativ de scadere a volumuli sangvin circulant, daca aceasta nu depaseste 20% din valoarea anterioara traumei, mecanismele adaptative initiate si guvernate de baroreceptorii din atriul drept reusesc sa compenseze pierderea prin venoconstrictie si cresterea intoarcerii venoase.
Scaderea cu peste 20% declanseaza alte mecanisme de compensare ce au ca scop centralizarea circulatiei spre zonele de importanta vitala, cu sacrificarea teritoriilor nonvitale. Activarea baroreceptorilor sino-carotidieni, din arcul aortic, cu cresterea nivelului de catecolamine si raspunsul indus si receptorilor, cu repartitia lor teritoriala specifica (splanhnica si tegumentara), modificarea tonusului vasomotor in teritoriul mezenteric si tegumentar, sunt cateva din mecanismele ce intra in actiune. Aceste mecanisme de adaptare clasice, reactia simpato-adrenergica (eliberare de catecolamine), activarea sistemului renina-angiotensina-aldosteron, sistemul hipotalamo-hipofizo-corticosuprarenalian (cu eliberare de vasopresina si reactia ACTH-cortizolica) sunt de multe ori depasite in lipsa unei interventii terapeutice prompte.
O astfel de situatie ar putea apare prin nerecunoasterea si intarzierea terapiei in contextul hemoragiei masive, definite astfel:
pierderea intregului volum de sange in decurs de 24h (transfuzarea a 10 U de MER pentru un pacient de 70 kg)
pierderea a peste 50% din volumul de sange in 3h
rata de sangerare ≥ 150 ml/min
rata de sangerare ≥ 1,5 ml/kg/min pentru mai mult de 20 min
Managementul va avea ca principiu corectarea determinantilor majori alterati prin mecanism primar traumatic, dar nu se va pierde din vedere nici corectia variabilelor de care depinde transportul de O2. (modificat dupa [31])
Optimizarea debitului cardiac
Optimizarea presarcinii
o cum: cresterea presarcinii deficitare (soc hipovolemic)
o cu ce: cristaloizi, coloizi, ± sange (pe baza estimarii pierderilor sanguine)
Normalizarea postsarcinii (RSV)
o cum: refacerea RSV inadecvate
o cu ce: norepinefrina, dopamina, fenilefrina
Cresterea inotropismului cardiac
o cum: maximalizarea contractiliatii miocardice
o cu ce: selectarea agentului inotrop adecvat, normalizarea pH-ului si a electrolitilor: (K, Mg, Ca)
Frecventa cardiaca
Optimizarea variabilelor ce determina transportul de O2
hemoglobina si functia ventilatorie - gaze sanguine
Coagularea este conceputa la ora actuala ca un proces dinamic ce se desfasoara la nivelul celor doua suprafete celulare (trombocit si celula endoteliala purtatoare de factor tisular), fiind expresia echilibrului dinamic intre factori pro- si anticoagulanti. In acelasi timp, coagularea este intr-o interdeterminare permanenta cu fibrinoliza (factori pro- si antifibrinolitici), sistemul complement, sistemul kininoformator. In acest echilibru complex, un rol central, determinant am putea spune, il joaca sistemul inflamator.
In trauma, in multiplele situsuri de injurie exista tendinta spontana de a limita sangerarea la nivel microvascular dar asa cum s-a mentionat mai sus, functionand pe princpiul echilibrului dinamic, exista in permanenta tendinta de a distruge acumularile de trombi nou formati, care ar putea obstructiona vasele mici.[32]
Analizand mai in detaliu acest fenomen, trebuie subliniat ca tulburarile echilibrului fluido-coagulant sunt initiate inca din momentul injuriei. Distrugerile mari tisulare cu leziuni endoteliale subsecvente au drept consecinta eliberarea factorului tisular si expunerea matrixului subendotelial, cu activarea extensiva a cascadelor enzimatice ale coagularii. Nu trebuie uitat ca hemostaza este o interactiune intre vasele sanguine, elementele figurate si cascada enzimatica plasmatica. Astfel, imediat posttraumatic apare o vasoconstrictie mediata de o serie de factori cum ar fi reactia simpato-adrenergica, productia de TxA2. Acesta din urma amplifica agregarea trombocitara, declansata deja de distrugerea endoteliala. Activarea plachetelor sanguine consecutiv adeziunii si agregarii trombocitare are efecte procoagulante prin factorul V eliberat de acestea. Astfel, imediat dupa trauma, exista o tendinta procoagulanta care in anumite circumstante poata evolua spre tromboza masiva, in contextul existentei de leziuni traumatice multiple cu formrea de microtrombi intravasculari prin:
eliberarea de factor tisular, vasoconstrictie indusa de reactia simpatoadrenergica si TxA2, scaderea nivelului de anticoagulanti naturali si inhibitori ai fibrinolizei
declansarea celorlalte sisteme: inflamator, kininoformator, complement care favorizeaza trombogeneza.
Referindu-ne tot la acest moment posttraumatic imediat, trebuie sa subliniem ca politraumatismul este circumstanta clinica cea mai reprezentativa pentru modul in care se manifesta efectul cumulativ al factorilor de risc protrombotici:
existenta in bilantul lezional al urmatoarelor leziuni: coloana vertebrala, fracturile de bazin, sold, femur
varsta peste 40 ani
necesarul transfuzional, care la valori de peste 1,5ml/kgc prezinta o serie de elemente procoagulante
factori legati de amploarea si tipul interventiilor chirurgicale, calea de abord si pozitia pe masa de operatie
In evolutia pacientului cu trauma multipla exista mai multe momente protrombotice: cel posttraumatic imediat descris mai sus, in postoperatorul imediat si perioada tardiva de terapie intensiva, care tine pana la reluarea activitatii anterioare producerii traumei.
Perioada postoperatorie imediata se caracterizeaza prin declansarea reactiei de faza acuta indusa atat de interventia chirurgicala cat si de manevrele invazive necesare monitorizarii si tratamentului intensiv. Asistam la eliberarea unei pleiade de mediatori proinflamatori, cresterea fibrinogenului, activarea complexului FvW - FV, precum si la scaderea factorilor anticoagulanti, cum ar fi AT III sau PAI. Toate acestea definesc un status procoagulant.
In perioada tardiva posttraumatica pot fi luate in calcul:
imobilizarea prelungita
gradul de imobilizare
reducerea autonomiei la mers
durata spitalizarii
Preocuparea constanta pentru studiul si preventia acestei patologii deriva din faptul ca tromboembolismul pulmonar ramane cea mai frecventa cauza de deces intraspitalicesc care poate fi prevenit in mod eficient. Numeroase conferinte de consens ale ACCP (American College of Chest Physicians) care s-au desfasurat intre 1999-2005 au considerat pacientul politraumatizat in grupa de risc foarte inalt de tromboza. Desi s-a ajuns la concluzia ca LMWH (Low Molecular Weight Heparin) reprezinta cea mai eficienta si mai larg studiata metoda de profilaxie, totusi in aceasta grupa de risc exista recomandarea asocierii a doua sau mai multe metode profilactice.[33]
Indicatia pentru mijloacele alternative de profilaxie a trombozei sunt circumstante clinice particulare, care se constituie in criterii de excludere pentru utilizarea LMWH:
Hemoragie intracraniana franca: hematomul, hemoragia subarahnoidiana (nu: microhemoragiile locale, contuzia cerebrala, leziunea axonala difuza - sub monitorizare stricta CT)
Hemoragie incoercibila > 36 h de la traumatism
Coagulopatie sistemica
Trombocite serice < 100.000/mm3 sau scaderea brusca cu peste 40%
Necesitatea tratamentului anticoagulant
Insuficienta renala cronica (creatinina serica > 3 - 4 mg/dl)
Graviditatea
La aproximativ 75-80% dintre pacienti politraumatizati exista acest status hipercoagulant cu tendinte spre tromboza inca din primele momente dupa trauma, riscurile mentinandu-se inclusiv pe perioada de recuperare pana la reluarea activitatii anterioare momentului traumatic. Exista insa un procent de aproximativ 25% dintre cazuri, la care in perioada precoce posttraumatica (in primele 48 de ore) tabloul clinic este dominat de hemoragie. Gravitatea acestui tablou clinic deriva din faptul ca sangerarea este a doua cauza de deces precoce in trauma multipla (42%), dupa TCC sever si este prima cauza (45%) daca se includ si sangerarile difuze din contextul TCC. Cand vorbim de decesele in sala de operatie, sangerarea masiva este cauza majora de deces, avand un procent de aprox 80%. Trebuie precizat de la inceput ca in acest procent se incadreaza de fapt doua entitati distincte:
hemoragiile cu sanctiune chirurgicala: hemoragii prin ruptura de vase mari (25%), rupturi sau distructii de organe parenchimatoase si plexuri vasculare aferente (10%) sau sangerari la nivelul membrelor (9%); hemostaza chirurgicala trebuie abordata pe principiul "damage control surgery" - chirurgie de control si stabilizare primara a leziunilor, in contextul careia pe langa oprirea sangerarii se decontamineaza plagile, urmand ca gesturile definitive sa se faca intr-un timp ulterior
sangerarea difuza data de coagulopatia indusa de trauma; in momentul manifestarii clinice, fenomenul este foarte greu de stapanit, tratamentul fiind specific terapiei intensive
Aceste doua entitati pot coexista de cele mai multe ori, diagnosticul diferential fiind foarte greu de efectuat, dar important pentru ca tratamentul este total diferit.
Riscul de a dezvolta o coagulopatie se coreleaza cu severitatea traumei 34] Bilantul lezional este un factor de predictie pentru coagulopatie, incidenta acesteia crescand odata cu scorul ISS (Injury Severity Score). La ISS > 45, 2/3 din pacienti dezvolta dezechilibru hemostatic marcat. Mortalitatea la un ISS dat creste exponential in prezenta coagulopatiei posttraumatice.
Patogenia tulburarilor de coagulare este complexa si multifactoriala 35] Este legata in primul rand de trauma tisulara si consumul de factori de coagulare, care se produce in procesul de formare de trombi pentru a limita sangerarile in multiplele situsuri traumatice. In acelasi timp, este activata masiv fibrinoliza, pe principiile echilibrului dinamic in care functioneaza sistemul fluido-coagulant, organismul incercand sa limiteze formarea de trombi. Aceasta din urma poate deveni necontrolata, excesiva si extensiva, fiind denumita in literatura de specialitate "CID like" sau hiperfibrinoliza. In acelasi timp exista circumstante agravante in contextul traumei: hipotermie, acidoza si anemie, care amplifica in cerc vicios coagulopatia deja declansata. Concomitent, factorii iatrogeni, indispensabili terapiei pacientului critic, pot agrava aceasta tulburare a echilibrului fluido-coagulant, acestia fiind coagulopatia de dilutie si efectele secundare proprii solutiilor de repletie volemica. Problema majora semnalata de literatura de specialitate se refera la faptul ca aceasta coagulopatie este de multe ori ignorata si subestimata. Astfel, testele de laborator nu reproduc conditiile de temperatura si pH-ul existente in vivo, testele de coagulare modificandu-se inca din momentul recoltarii. In vitro nu se pot reproduce conditiile reale ale procesului de hemostaza, care implica prezenta a doua tipuri de celule - trombocitul si celula endoteliala purtatoare de factor tisular, pe suprafata carora se desfasoara intregul proces. TEG (trombelastograma) este o metoda care reflecta cel mai fidel ansamblul fenomenelor, dar nu este accesibila in cea mai mare parte a spitalelor din tara noastra.
In analiza factorilor agravanti ai coagulopatiei posttraumatice trebuie sa ne oprim asupra hipotermiei, care are un important efect sistemic la nivelul diferitelor organe cum ar fi cordul, ficatul, are impact asupra metabolismului celular, metabolizarii medicatiei administrate, fiind insotita si de grave tulburari de coagulare. Hipotermia scade numarul de trombocite prin sechestrarea splenica si hepatica a acestora, fenomen reversibil prin incalzirea prompta a pacientului. Hipotermia altereaza adezivitatea si agregarea plachetara prin inhibitia eliberarii de TxA2 precum si cinetica enzimelor implicate in cascada coagularii. Toate aceste modificari sunt reversibile prin incalzirea la 370 C.
S-a demonstrat ca exista o stransa corelare intre acidoza si tulburarea de coagulare prin influenta directa asupra generarii de trombina. Daca pH-ul scade de la 7.4 la 7, se observa o inhibare de pana la 70% a formarii de trombina. Desi acidoza este un factor agravant pentru coagulopatia in trauma, pana la un anumit nivel (7.10), ea este un marker al necesitatii resuscitarii microcirculatorii aditionale (resuscitare volemica). Efectele acidozei pe coagulare sunt insa, sub acest nivel, mult mai severe decat efectele hipotermiei, iar daca cele doua conditii se asociaza, riscul de coagulopatie creste exponential.
Aceste trei elemente - coagulopatie, hipotermie si acidoza se conditioneaza reciproc formand un triunghi patogenic denumit "triunghiul mortii". Oprirea hemoragiei nu se poate face decat prin corectarea concomitenta a acestor trei tulburari. Chiar daca fiecare dintre aceste trei elemente pot influenta prognosticul in trauma, asocierea lor va creste exponential mortalitatea si morbiditatea. Acesti trei parametri sunt influentati nu doar de trauma si sangerarea consecutiva, dar mai ales de hipoperfuzia tisulara si de durata ei.
Chiar daca resuscitarea volemica si microcirculatorie este un punct forte al terapiei, volumele mari de coloizi, cristaloizi si transfuzia masiva duc la hemodilutie cu accentuarea coagulopatiei in trauma. Dilutia indusa are impact pe nivelul de factori (deja scazuti prin pierdere si consum), cel mai vulnerabil fiind fibrinogenul. Concentratia lui scade < 1g/ml dupa inlocuirea a 143% din volumul plasmatic. S-a observat ca dupa administrarea a peste 12 unitati de masa eritrocitara se dubleaza atat PT cat si aPTT. In studiile lui Hipalla, se arata aparitia trombocitopeniei dilutionale in cazul transfuziei masive (1,5 x volumul sangvin pierdut). Doar 35-40% din trombocite raman in circulatie dupa inlocuirea unui volum de sange transfuzat. In plus, trombocitele isi pierd functionalitatea datorita ciclooxigenazei eliberate de hematiile transfuzate. Pe langa fenomenul dilutional, transfuzia masiva altereaza coagularea prin: acidoza, aport de potasiu, pierderea elasticitatii hematiilor, ischemie microcirculatorie, eliberarea de citokine de catre leucocitele transfuzate.
Principiile de tratament in hemoragia acuta din trauma trebuie sa aiba in vedere coexistenta celor doua entitati distincte: sangerarea chirurgicala si coagulopatia. [36] Ca principiu general, interventia chirurgicala hemostatica trebuie secondata de stabilizarea hemodinamica. Elementul central va fi restabilirea debitului cardiac prin ameliorarea presarcinii si optimizarea variabilelor ce determina transportul de oxigen, in special hemoglobina. Inlocuirea volumului sangvin pierdut si corectarea VSCE se face cu cristaloizi si coloizi in raport de 1/2, existand recomandarea utilizarii coloidului tip HAES (hidroxietil amidon) 130/0,4 (Voluven), demonstrat fiind faptul ca impactul sau pe coagulare este minim. Repletia volemica trebuie facuta concomitent cu incalzirea pacientului. Scopul final al resuscitarii va fi imbunatatirea microcirculatiei, cu ameliorarea acidozei lactice si a deficitului de baze.
Corectarea anemiei se face cu masa eritrocitara (MER) in cazul in care hematocritul este sub 21-24%. Trauma multipla este entitatea clinica in care se recomanda utilizarea metodelor de autotransfuzie intraoperatorie - cell saverul, salvarea sangelui autolog inlaturand nu numai riscurile infectioase si imunologice asociate transfuziei de sange dar reducand si necesarul tardiv de transfuzie datorita duratei de viata mai lunga a eritrocitelor retransfuzate.
Un element important este tratamentul cu substituenti ai factorilor de coagulare.[37] Corectarea deficitului de factori ai coagularii se face cu:
Plasma proaspata congelata (PPC) 10-15 ml/kgc, daca aPTT si PT se prelungesc de 1,5x
Masa trombocitara 1-2 U/ 10kgc la trombocite < 50,000
Crioprecipitat 1-2 U/ 10kgc, la fibrinogen < 1g/ml (atentie, nu are toti factorii de coagulare!)
Fibrinogen la scaderea nivelului plasmatic < 1g/ml (nu se mai utilizeaza la noi in tara)
Terapia hemostatica este cea mai controversata treapta terapeutica in contextul traumei multiple, in care exista sangerare masiva pe un teren protrombotic. S-au recomandat pentru efectele antifibrinolitice aprotinina (Trasylol, Gordox), analogi de lizina (acid epsilon aminocaproic - EACA, acid tranexanic). Dar asa cum arata Levi intr-o metaanaliza, efectul acestei medicatii este controversat si nejustificat, asa cum reiese din analiza mortalitatii, incidentei reinterventiilor pentru sangerare, necesarului transfuzional si a accidentelor coronariene dupa tratament. [38]
In ultimii ani se discuta despre efectele desmopresinei asupra factorului Von Willebrand - FvW (creste expresia lui pe suprafata celulei). Din acest motiv ea a fost introdusa si utilizata in unele protocoalele terapeutice pentru trauma multipla. [39]
Referindu-ne la noua generatie de agenti hemostatici, trebuie sa ne oprim asupra factorului VII activat si recombinat (Novoseven), care a facut obiectul a numeroase studii si este inca mult discutata oportunitatea introducerii sale in tratamentul coagulopatiei posttraumatice. A fost publicat recent un ghid de utilizare a Novoseven-ului in cazul sangerarii necontrolabile, ca ultima solutie terapeutica pentru pacientii cu sanse reale, dupa esecul tratamentului conventional.[40] Acest ghid se bazeaza pe studiile si recomandarile Grupului Israelian pentru sangerarea masiva din trauma multipla condus de Martinovitz. In 2006, Chiara publica o propunere de utilizare a F VII activat si recombinat in hemoragiile din trauma. [41]:
la pacienti la care nu este posibila hemostaza chirurgicala
sangerarea continua in panza si dupa interventie (fractura de bazin, leziune intraperitoneala, leziuni ale extremitatilor)
la pacienti care asociaza coagulopatie confirmata de testele de laborator si care necesita cantitati mari de masa eritrocitara (>8U MER)
Intotdeuna se va incepe obligatoriu cu tratamentul conventional (tratament de substitutie de factori de coagulare - PPC, crioprecipitat, masa trombocitara, corectarea acidozei si hipotermiei), dupa care se administreaza 90 unitati/kgc Novoseven. In conditiile in care sangerarea continua la 2 ore, se poate repeta o a doua doza, dupa care este obligatoriu controlul chirurgical. Exceptie fac cei la care sangerarea prin trauma apare pe fondul unei patologii anterioare, pentru care se administreaza terapie anticoagulanta. Nu se administreaza niciodata la cei cu acidoza metabolica severa, inainte de corectarea acesteia, sau la cei care au necesitat resuscitare cardio-respiratorie.
5.3.Concepte moderne in ingrijirea pacientului politraumatizat
Managementul pacientului politraumatizat a suferit modificari importante in ultimii ani, mai ales datorita interventiei terapeutice adecvate, chiar din etapa pre-spital, a dezvoltarii tehnicilor chirurgicale (in special osteosinteza fracturilor) si a masurilor avansate de terapie intensiva.
In prima parte a secolului 20, pacientii politraumatizati erau de regula tratati conservator, considerandu-se ca impactul traumei este mult prea sever ca pacientul sa poata suporta o interventie chirurgicala majora. S-a observat ca acesti pacienti aveau o rata foarte mare a mortalitatii, ca urmarea a complicatiilor datorate imobilizarii prelungite si a tractiunilor osoase necesare pentru reducerea fracturilor. Complicatiile frecvente erau cele de tip: pneumonie, tromboza venoasa profunda, atrofia musculara si leziuni de decubit 42,43]
Rapida dezvoltare a tehnicilor chirurgicale de fixare a fracturilor a dus la aplicarea acestora si la pacientul politraumatizat in perioada imediata posttraumatica, atitudine ce poarta denumirea de "early total care". Acesta s-a dovedit a avea impact favorabil asupra functiei pulmonare si complicatiilor postoperatorii. Johnson et al. a aratat ca intarzierea cu peste 24 ore a practicarii osteosintezei de femur duce la o crestere importanta a riscului de aparitie a sindromului de detresa respiratorie acuta. [44] Rezultatele studiului prospectiv efectuat de Bone et al. privind osteosinteza de femur precoce versus tardiva la pacientii cu trauma multipla au aratat o reducere semnificativa a riscului de aparitie a complicatiilor pulmonare (ARDS, embolia pulmonara, pneumonia) atunci cand interventia se practica in primele 24 ore dupa trauma.[45]
Atitudinea terapeutica de rezolvare per primam a tuturor leziunilor induse de trauma (early total care) se poate aplica la aproximativ 60% din politraumatizati. Totusi, pentru a putea suporta optim interventia chirurgicala ce poate fi uneori extensiva, acesti pacienti trebuie sa indeplineasca anumite conditii: sa fie stabili hemodinamic, sa nu necesite suport vasopresor sau inotrop, sa fie normoxemici, normocapnici, normotermici, valoarea lactatului <2 mmmol/, debit urinar orar>1 ml/kg/h. Totusi, in anii '90 s-a observat ca acesta atitudine terapeutica de rezolvare chirurgicala definitiva a tuturor leziunilor (in special cele ortopedice) nu are rezultatele scontate la o anumita categorie de pacienti politraumatizati - cei cu scor ISS mare, ce au in bilantul lezional fracturile osoase multiple asociat cu leziuni toraco-pulmonare severe, acest tip de pacient fiind considerat de catre Pape tip "borderline".[46,47] Practicarea osteosintezei intramedulare precoce la acestia duce la cresterea semnificativa a complicatiilor pulmonare, in special prin aparitia ARDS. Au fost astfel identificati cei trei factori de risc ce influenteaza prognosticul acestor pacienti: severitatea injuriilor induse de trauma (trauma multipla si socul asociat), prezenta traumei toracice si osteosinteza intramedulara de femur.
Avand la baza aceste observatii si alte studii clinice, atitudinea terapeutica s-a reorientat dinspre rezolvarea initiala completa a tuturor leziunilor (early total care), spre stabilizarea temporara a fracturilor si la aplicarea activa a masurilor de resuscitare hemodinamica urmata ulterior de rezolvarea definitiva a leziunilor, atunci cand pacientul este stabilizat.
5.4. SIRS (Sindromul de raspuns Inflamator Sistemic) la pacientul cu trauma multipla
Declansarea reactiilor sistemice posttraumatice si a intregului lant de cascade de mediatori este guvernata de raspunsul inflamator sistemic. Acesta este considerat elementul central care poate duce la disfunctia multipla de organe si deces. Trebuie subliniat ca si in cazul raspunsului inflamator exista un echilibru intre mediatorii proinflamatori si antiinflamatori. Mentinerea acestui echilibru face ca reactia inflamatorie sa fie benefica pana la un anumit moment. Ruperea acestui echilibru are consecinte grave la nivelul tuturor organelor si sistemelor, fiind implicate chiar si cele care nu sunt cuprinse in bilantul lezional traumatic. [51] Raspunsul hiperinflamator cu inflamatie necontrolata, dar si raspunsul hipoinflamator pot fi asociate cu prognostic fatal.
Activarea monocitelor, macrofagelor si neutrofilelor, cu excretia de citokine proinflamatorii influenteaza sistemul coagularii si complementului, ducand la disfunctie endoteliala cu afectarea permeabilitatii capilare, pierderea si mai mult a volumului intravascular si tulburari de perfuzie(vezi fig.1). Insuficienta microcirculatorie impreuna cu cea macrocirculatorie, agraveaza si mai mult hipoxia tisulara, contribuind la aparitia insuficientelor de organ.
Figura 1
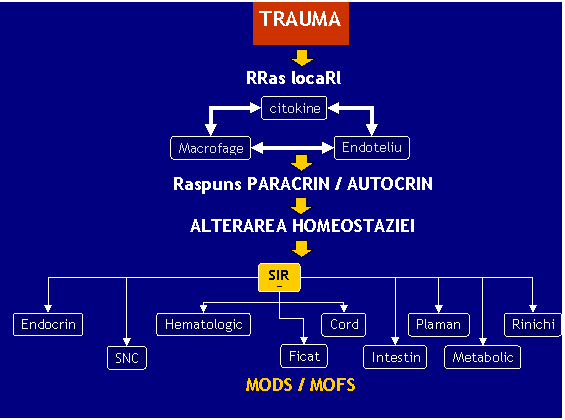
Reto Stocker, Eforie, iunie 2006
Simplificand foarte mult, in cele doua talere ale balantei exista:
pe de o parte o pleiada de mediatori, care prin reactia proinflamatorie imediata au impact asupra cascadelor sistemice (coagulare, fibrinoliza, kininoformare, complement), toate sub guvernarea reactiei neuro-endocrine de stres; acestea se autoagraveaza si duc la leziuni endoteliale secundare responsabile de MODS/MSOF,
pe de alta parte raspunsul compensator antiinflamator (CARS), care poate deveni dominant in zile, inducand imunosupresie si cresterea susceptibilitatii la infectie.
In conditiile create de traumatism, distrugerea tisulara cu injurie endoteliala extensiva, eliberare masiva de mediatori si leziuni de ischemie-reperfuzie, induce precoce raspunsul inflamator sistemic (MODS/MSOF primar); acest tip de raspuns este diferit de cel indus de sepsis, care apare tardiv in evolutie in contextul imunosupresiei (MODS/MSOF secundar)(vezi figura2).
Figura 2
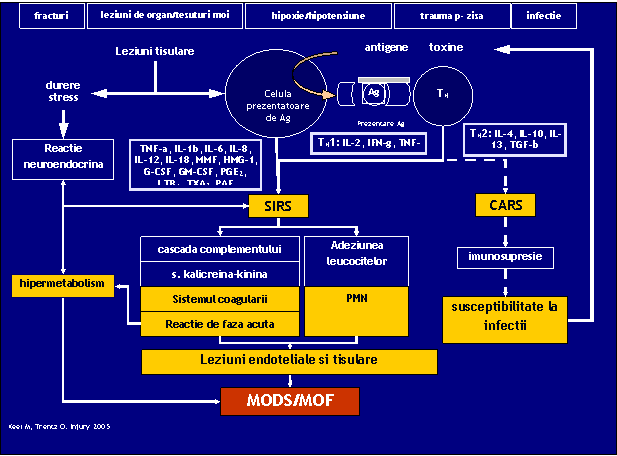
Reto Stocker, Eforie, iunie 2006
Pornind de la faptul ca organismul este supus la doua tipuri de agresiuni ce determina un raspuns de aparare, a aparut teoria "Two Hit Theory":
leziunea primara este legata de trauma propriu-zisa ("trauma load") cu distrugere tisulara locala si activarea concomitenta a raspunsului inflamator sistemic
leziunile secundare endogene ("antigenic load") si exogene ("interventional/surgical load"), joaca un rol decisiv in declansarea complicatiilor posttraumatice, influentand si gradul de severitate al acestora [52,53] Tipice pentru leziunile secundare endogene sunt: hipoxia prin sindrom de detresa respiratorie, episoadele de instabilitate cardio-circulatorie, acidoza metabolica, leziunile prin sindrom de ischemie-reperfuzie, necrozele tisulare, cateterele contaminate, infectia. Leziunile secundare exogene sunt reprezentate de: interventiile chirurgicale asociate cu distructii tisulare intinse, tratamentul chirurgical inadecvat sau tardiv, hipotermia, pierderile sangvine importante, transfuzia masiva de sange, aplicarea tardiva a masurilor de terapie intensiva, neglijarea terapeutica a unor leziuni, omisiunea unor leziuni.
5.5.Conceptul de "damage control"
Acest concept a fost descris initial in urma cu 20 ani, ca fiind o interventie chirurgicala abdominala rapida in scopul de a opri temporar sangerarea prin aplicarea de mese (packing) perihepatic in cazul pacientilor cu trauma hepatica severa, muribunzi datorita exangvinarii rapide. [48] Totodata, s-a observat ca aparitia coagulopatiei are impact sever asupra prognosticului acestor bolnavi [49]. Astfel, a fost propusa efectuarea unei laparotomii exploratorii rapide in scop hemostatic, urmate de masurile terapeutice de resuscitare si de combatere a coagulopatiei in Terapie Intensiva, cu revenirea in sala de operatie pentru rezolvarea definitiva a leziunilor atunci cand pacientul este stabilizat.
Datorita modificarii pattern-ului pacientilor traumatici, in sensul cresterii numarului de cazuri cu leziuni abdominale prin impuscare, s-a acumulat o experienta importanta in urma utilizarii acestei atitudini si astfel, Rotondo si colaboratorii au reusit definirea conceptelor fundamentale care stau la baza lui. Astfel, laparotomia initiala are ca scop principal controlul hemoragiei active si limitarea contaminarii gastrointestinale a cavitatii peritoneale, urmate de inchiderea temporara a cavitatii abdominale 50]
Intelegerea mecanismelor fiziopatologice la pacientul cu sangerare severa (exsangvinare) sta la baza conceptului de "damage control = minimizarea pierderilor" si are ca scop reducerea atat a mortalitatii primare cat si secundare la acesta categorie de pacienti.
Adaptarea practica a cunoasterii raspunsului la impactul sistemic indus de trauma si modularea masurilor care se impun in fata unui politraumatizat poate fi organizata sub forma unui algoritm, care urmeaza treptele clasice (vezi figura 3).
Figura 3
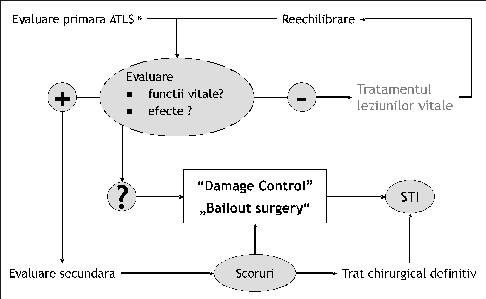
Reto Stocker, Eforie, iunie 2006
Prima treapta, ATLS - evaluarea primara, in contextul afectarii severe a functiilor vitale, impune masuri terapeutice agresive, imediate, concomitent cu evaluarea primara. Daca stabilizarea functiilor vitale nu este posibila cu metodele conventionale, se recurge la masuri chirurgicale precoce pe principiul "damage control surgery/ortopedics". O situatie speciala o reprezinta pacientul la care in timpul interventiei chirurgicale de rezolvare per primam a leziunilor (early total care), se descopera noi leziuni traumatice ce ar prelungi prea mult operatia sau hemostaza nu se poate realiza datorita aparitiei coagulopatiei. In aceste conditii se trece la abandonarea procedurii chirurgicale extensive, laborioase ("bail-out surgery") si se aplica conceptul de damage control cu finalizarea cat mai rapida a interventiei si transferul pacientului in Terapie Intensiva pentru stabilizarea si resucitarea adecvata.
Daca pacientul este stabilizat, se trece la evaluarea secundara pentru a obtine un diagnostic complet, avansat. Daca scorul de injurie este foarte mare si leziunile traumatice sunt instabile, cu posibilitatea evolutiei spre MODS, recurgem tot la principiile "damage control surgery". Dupa interventia chirurgicala de stabilizare, pacientul este ingrijit in terapie intensiva, ulterior fiind supus chirurgiei definitive. In contextul in care pacientul are leziuni stabile dupa evaluarea secundara, se recurge de la inceput la un tratament chirurgical definitiv.
Avand la baza conceptul de "damage control surgery" propus in anul 1993 de catre Rotondo, se subliniaza importanta abordarii in etape a tratamentului chirurgical. Se acorda prioritate refacerii homeostaziei pacientului prin interventie chirurgicala imediata de stabilizare: hemostaza si decontaminarea plagilor. In acest concept, rezolvarea definitiva a leziunilor suporta amanare. Principiile "damage control" se aplica in toate tipurile de chirurgie: abdominala, ortopedica, toracica.
Se disting patru faze terapeutice ale acestui concept (figura 4) ce se suprapun peste fazele de evolutie a raspunsului inflamator sistemic. Evolutia acestuia va fi implicata in deciziile terapeutice si amploarea acestora.
I. identificarea pacientiilor ce beneficiaza de "damage control surgery" - faza intiala de recunoastere
II. interventia chirurgicala de oprire a hemoragiei si de control a contaminarii - faza operatorie
III. tratament de stabilizare in STI cu refacerea parametrilor fiziologici si imunologici - faza de terapie intensiva
IV. reconstructie definitiva dupa reechilibrarea pacientului, cat mai precoce posibil - faza de reconstructie
Figura 4
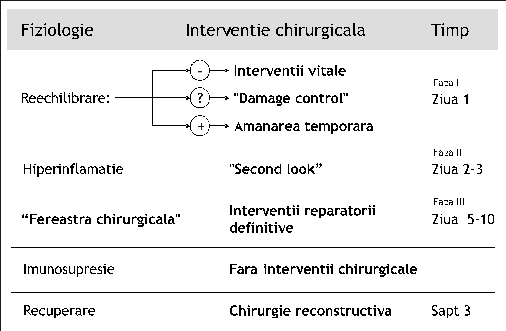
modificat dupa [54]
In ziua 1, in contextul raspunsului inflamator localizat este posibila interventia chirurgicala precoce. In ziua 2 si 3, care se caracterizeaza prin exacerbarea raspunsului inflamator, o interventie chirurgicala poate accentua raspunsul de faza acuta. Practic, nu se recomanda decat interventiile chirurgicale absolut necesare - second-look pentru o noua sangerare sau interventie pentru sindromul de compartiment abdominal.
Urmeaza apoi o asa-zisa fereastra chirurgicala intre ziua 5 si aproximativ 10, in care se fac interventii chirurgicale reparatorii. Acestea nu trebuie amanate foarte mult pentru a nu intra in perioada de imunosupresie, cand riscurile de infectii si complicatii sunt foarte mari.
Chirurgia reconstructiva se face in perioada de recuperare, dupa minimum 3 saptamani de la trauma.
Principiile "damage control" se aplica in toate tipurile de chirurgie: abdominala, ortopedica, toracica.
Faza I presupune recunoasterea tipului de pacient ce beneficiaza de aceasta abordare. Indicatiile principale pentru abordarea pacientului sunt:
coexistenta circumstantelor agravante pentru trauma: hipotermia, coagulopatia, acidoza
trauma severa cu pierdere masiva de sange la un pacient instabil sau cu insuficienta de organ posttraumatica (ex: la TCC sever cu fractura de femur sau gamba - nu se face osteosinteza cu tija, dar este obligatorie fixarea externa a focarelor de fractura instabile).
Faza a II-a permite efectuarea de interventii chirurgicale asupra leziunilor imediat amenintatoare de viata ("damage control"). Aceste interventii vor limita sangerarea si stabilizeaza pacientul care va fi internat in terapie intensiva.
controlul sangerarii se poate face initial doar prin aplicare de mese (in cazul unor leziuni extensive mesajul unor cavitati, ficatul in patru cadrane); autorii conceptului indica efectuarea controlului surselor de sangerare in maximum 10 minute de la incizie, indiferent de dificultatile locale
controlul surselor de contaminare a cavitatii abdominale si excizia tesutului necrozat; trebuie evitata inchiderea sub tensiune a peretelui abdominal; se indica folosirea unui perete abdominal artificial
leziunile toracice beneficiaza de toracotomie antero-laterala de urgenta, cu identificarea sursei de sangerare si hemostaza rapida (prin camplare uneori chiar a hilului, rezectie non-anatomica sau chiar mesajulcavitatii toracice in caz de sangerare difuza)
in cazul fracturilor de bazin ce asociaza frecvent sangerare importanta hematom retroperitoneal) se prefera reducerea si fixarea cu fixator extern de bazin in scopul opririi sangerarii. Totusi mai exista controverse privind atitudinea optima in acesta entitate, unii autori sustinand efecturea laparotomiei cu mesaj pelvin sau efectuarea angiografiei cu embolizarea sursei de sangerare
controlul fracturilor instabile cu fixatoare externe
Tot in primele 24 ore de la trauma, concomitent cu evaluarea secundara a politraumatizatului si cu initierea masurilor terapeutice de stabilizare se pot face interventiile chirurgicale amanate ("delayed primary surgery") asupra leziunilor neamenintatoare de viata. Acestea au ca scop reducerea leziunilor secundare endogene ("antigenic load") si pot include:
evacuare hematom subdural
decompresia maduvei spinarii si fixare in cazul fracturilor vertebrale instabile
fasciotomii in cazul sindromului de compartiment al membrelor
revascularizare membru ischiemiat
debridare si necretectomie a plagilor tegumentare, etc.
Si aceste interventii trebuie limitate in timp pentru a evita aparitia leziunilor secundare iatrogene ("surgery/inteventional load").
Faza a III-a este dominata de tratamentul de terapie intensiva ce continua stabilizarea pacientului atentia concentrandu-se asupra inlaturarii asa-numitei "triade letale": hipotermia, coagulopatia si acidoza. Obiectivele finale de resuscitare sunt urmatoarele:
stabilitate hemodinamica (ideal fara substante vasopresoare/inotrope)
normoxie, normocapnie
lactat seric sub 2 mmol/l in urmatoarele 12 ore
coagulare normala (normalizarea timpului de protrombina)
normotermie (temperatura centrala >35sC)
debit urinar orar peste 1 ml/kg/min
In acesta etapa apar fenomenele de hiperinflamatie (ziua 2-4 dupa trauma) in care pacientul este foarte susceptibil la dezvoltarea de leziuni secundare "second-hit" de aceea interventiile chirurgicale sunt limitate la maximum.
Leziunile cerebrale secundare prin cresterea presiunii intracraniene datorate edemului cerebral sau leziunilor de ischemie/reperfuzie pot fi limitate prin aplicare de diferite metode de neuroprotectie: optimizarea presiunii de perfuzie cerebrala prin cresterea presiunii arteriale medii si prin drenajul lichidului cefalorahidian (prin intermediul cateterului intraventricular), hiperventilatie usoara controlata, hipotermie moderata, iar in situatii extreme se poate aplica tehnica voletului dfecompresiv. [55]
Alimentatia entetrala precoce are ca scop reducerea incarcarii bacteriene patogene de la nivelul tractului intestinal si evita aparitia atrofiei mucoasei intestinale cu rol esential de bariera impotriva agresiunii bacteriene din flora digestiva.
Extrem de importanta in acesta etapa este monitorizarea presiunii intraabdominale, ca parametru de urmarire a sindromului de compartiment abdominal. Cresterea presiunii in compartimentul abdominal este o indicatie clara pentru relaparotomie - "second look". Metoda cea mai adecvata de inchidere temporara a peretelui abdominal in cazul prezentei sindromului de compartiment este cu ajutorul sistemului V.A.C® (Vacum Assisted Closure - inchiderea fasciala se face prin aplicarea unui sistem cu presiune negativa la nivelul marginlor plagii). [56] Sangerarea masiva sau continua poate exista concomitent cu coagulopatia posttraumatica, fiind necesar un diagnostic diferential extrem de rapid si corect, avand in vedere ca sanctiunea terapeutica este complet diferita in cele doua entitati.
In cazul pacientilor carora li s-au aplicat mese ("packing") intraabdominale in scop hemostatic necesita reinterventie chirurgicala "second look" in urmatoarele 24-72 ore, pentru inlaturarea acestora, a chegurilor sau colectiilor lichidiene, necrectomia tesuturilor devitalizate, montare jejunostomie de alimentatie si arareori interventii chirurgicale extensive.
Faza a IV-a este reprezentata de interventiile reparatorii definitive a leziunilor traumatice ale pacientului. Concomitent cu acestea, daca se anticipeaza IOT prelungita se va face traheotomia si jejunostomia pentru nutritia enterala. Acesta etapa se suprapune pe asa-numita fereastra de oportunitate "window of opportunity" (intre ziua 5-10 de la trauma) a raspunsului inflamator din trauma. In aceata etapa se pot practica: refacerea continuitatii tractului digestiv, conversia fixator extern cu osteosinteza interna a fracturilor, osteosinteza definitiva a leziunilor cu interesare articulara, acoperirea cu grefe de piele a leziunilor tegumentare sau suturile secundare, etc.
Ulterior, intre ziua 10 si saptamana 3-a de la trauma apare o perioada de imunosupresie ce contraindica efectuarea de interventiile chirurgicale definitive.
Dupa 3-4 saptamani de la trauma se pot practica interventii chirurgicale reconstructive secundare ca de exemplu: interventie de reconstructie ligamentara, montare de proteza articulara, reconstructii de nervi, acoperirea defectului osos in cazul practicarii anterioare a craniectomiei, etc.
6. Concluzii
Politraumatismul este o problema de sanatate publica subevaluata in tara noastra; este grevat de o mortalitate semnificativa, fiind prima cauza de deces la pacientii tineri. Trauma multipla are un impact direct asupra comunitatii, prin faptul ca este un eveniment ce survine de obicei neasteptat, in plina sanatate, intr-o perioada de productivitate maxima a individului.
Ingrijirea pacientilor presupune existenta unui sistem medical cu organizare specifica, care functioneaza in regim de urgenta. Sunt implicate cheltuieli importante directe, (spitalizare, recuperare, reinsertie sociala etc) si indirecte (pierderile materiale pe plan familial si social presupuse de pierderea unei vieti).
Evaluarea si tratamentul pacientului politraumatizat trebuie facute in echipa multidisciplinara: medicina de urgenta, ATI, chirurgie, ortopedie, neurochirurgie, imagistica etc.
Definirea politraumatismului este destul de dificila, fiind necesara includerea atat a elementelor din bilantul lezional (date anatomice), cat si a datelor functionale care reflecta impactul sistemic indus de leziunile traumatice. Scorul ISS este modalitatea cea mai complexa de definire a politraumatismului, prin multitudinea de date oferite de acesta. In acelasi timp, avem la indemana un sistem operational de comunicare si de evaluare, atat a circumstantei actuale cat si a evolutiei pacientului.
Atitudinea terapeutica este ghidata de protocoale; acestea scurteaza timpul de reactie si imbunatatesc procesul decizional.
Leziunile traumatice se pot asocia si agrava reciproc, cu deschiderea unor cercuri vicioase care determina un prognostic sever, frecvent catre deces. Trauma craniana severa, traumatismele toracice cu insuficienta ventilatorie sau instabilitate cardio-circulatorie severa, traumatismele abdominale, fracturile complexe de bazin, cu hemoragii greu controlabile chirurgical, sunt cateva entitati care indeplinessc criteriile unui pacient critic. In contextul pacientului cu trauma multipla, prezenta circumstantelor agravante (hipotermie, acidoza metabolica, coagulopatie posttraumatica), constituie o alta motivatie pentru internarea intr-o sectie de reanimare.
Politraumatismul trebuie privit ca o afectiune multisistemica, cu impact asupra tuturor organelor, chiar si a celor neimplicate direct in leziunea traumatica.
In acelasi timp, trauma declanseaza un raspuns sistemic guvernat de reactia neuroendocrina, reprezentat de inflamatia sistemica precoce ce apare din momentul distrugerii tesuturilor de catre trauma. Raspunsul inflamator sistemic va avea impact atat pe echilibrul fluido-coagulant, care deja este inclinat spre sangerare (coagulopatia posttraumatica), cat si asupra sistemului complement, sistemului kininoformator. Raspunsul compensator antiinflamator (CARS), amplificat la cateva zile dupa trauma, va scadea imunitatea si va creste susceptibilitatea la infectii.
"Damage control surgery" este un concept care adapteaza masurile terapeutice la severitatea leziunilor traumatice, respectand modificarile multisistemice induse de trauma putandu-se aplica in cazul managementului leziunilor traumatice abdominale, toracice, ale bazinului si membrelor, vasculare. Desi evidentele clinice de grad I lipsesc in cazul acestei abordari, totusi exista suficiente dovezi care sustin utilizarea aceastui concept mai ales in situatia asocierii de injurii traumatice severe, devenind modalitatea de abordare ce pare ca se adapteaza cel mai bine etapelor de evolutie a pacientului politraumatizat. [57]
Bibliografie:
NCHS Vital Statistics System.
Keel M, Trentz O. Pathophysiology of polytrauma. Injury 36, 691-709, 2005
Malone DL, Kuhls D, Napolitano LM: Back to basics: validation of the admission systemic inflammatory response syndrome score in predicting outcome in trauma. J Trauma 51:458, 2001
Trunkey DD: The trimodal distribution of death after injury. Scientific American 249 (2):28-53, 1983
Sauaia A, Moore FA, Moore EE,
Shackford SR, Mackersie RC, Holbrook TL, Davis JW, Hollingsworth-Fridlund P, Hoyt DB, Wolf PL: The epidemiology of traumatic death. A population-based analysis. Arch Surg 128:571-575, 1993
Rosch M, Klose T, Leidl R et al. Cost of acute hospitalisation in multiple trauma patients. Unfallcirurg 2000; 103:6332-9
Trunkey DD. What's wrong with trauma care? Bull Am Coll Surg 1990;75:10-5
Graham DJ, Adams JH, Gennarelli TA: Mechanisms of non penetrating head injury. Prog Clin Biol Res, 264:68,1998
ThoracicTrauma in Advanced Trauma Life Support
for Doctors ( editia 6)
Leavitt BJ, Meyer JA, Morton JR: Survival following nonpenetrating traumatic rupture of cardiac chambers. Ann Thorac Surg 44: 532- 535, 1987
Brathwaite CEM, Rodriguez A: Blunt traumatic cardiac rupture:a 5- years experience. Ann Surg 212: 701- 704, 1990
Kilpatrick ZM: On pericardiocentesis.Am J Cardiol 16:722,1965
Spodick DH: Acute cardiac tamponade, NEJM 2003; 349:684-690
Gattinoni L, Pelosi P, Suter PM: Acute respiratory distress syndrome caused by pulmonary and extrapulmonary disease. Different syndromes? Am J Respir Crit Care Med 158:3, 1998
Pelosi P, Gattinoni L: Acute respiratory distress syndrome of pulmonary and extrapulmonary origin: fancy or reality? Intensive Care Med 27:457, 2001
Steinberg KP, Hudson LD: Acute lung injury and acute respiratory distress syndrome. The clinical syndrome.Clin Chest Med 21: 401, 2000
Johson JA, Cogbill TH: Determinans of outcome after pulmonary contusion. J trauma 26:695-697, 1986
Cohn SM: Pulmonary contusion: Review of the clinical entity. J Trauma 1997; 42: 973-979
ARDSnet Investigators. Ventilation with lower tidal volumes as compared with traditional tidal volumes for acute lung injury and the acute respiratory distress syndrome. NEJM 351:327,2004
Norton MJ, Stanford GG: Early detection of myocardial contusion and its complications in patients with blunt trauma.Am J Surg 160: 577- 582, 1990
S. Geafar, I. Grintescu, D. Tulbure -Troponin I in Myocardial contusion, ESA Meeting, Vienna, 2000
Brasel KJ, Borgstrom DC: Predictors of outcome in blunt diaphragm rupture. J Trauma 41: 484, 1996
Rotondo MF, Schwab CW, McGonigal MD et al. 'Damage Control - an approach for improved survival in exsanguinating penetrating abdminal injury' J Trauma 1993;35:375-382
Chiara O, Cimbanassi S, Vesconi S: Critical bleeding in blunt trauma patients in Yearbook of Intensive Care and emergency Medicine ed. Vincent J- L, 2006:244-254
Ertel W, Eid K, Keel M et al. Therapeuthical strategies and outcome of polytraumatised patients with pelvic injuries - a six-year experience. Eur J Trauma 2000;6:14-7
Walley KR: Shock in Principles of Critical Care Third
Edition sub redactia Hall JB.,
Kaplan JA, Dunbar RW: Anesthesia for noncardiac surgery in patients with cardiac disease in Kaplan JA (ed): Cardiac Anesthesia. Grune & Stratton, Orlando, FL, 1979:377
Brohi K Acute traumatic coagulopathy. J Trauma 2003, 541:1127-1130
Hirsh J. Guidelines for Antitrombotic Therapy, Fifth Edition, 2005
MacLeod JBA Early coagulopahy predicts mortality in trauma. J Trauma
Brohi K Acute traumatic coagulopathy. J Trauma 2003, 541:1127-1130
Lawson JH, Murphy MP: Challenges for providing effective hemostasis in surgery and trauma. Semin Hematol 2004, 41:55-64
Levi M, Cromheecke ME, de Jonge E., et al. Pharmacological strategies to decrease excessive blood loss in cardiac surgery: a meta-analysis of clinically relevant endpoints. Lancet 1999;354:1940-7.
Rutledge R, Sheldon GF: Bleeding and coagulation problems in Moore EE, Mattox KL, Feliciano, eds.Trauma:891-908, 1991
Martinowitz U, Michaelson M: Guidelines for the use of recombinant activated factor VII (rFVIIa) in uncontrolled bleeding: a report by the Israeli Multidisciplinary rFVIIa Task Force. J Thromb Haemost 2005, 3:640-648
Chiara O, Cimbanassi S, Vesconi S: Critical bleeding in blunt trauma patients in Yearbook of Intensive Care and emergency Medicine ed. Vincent J- L, 2006:244-254
Renne J, et al. Fat macroglobulinemia caused by fractures or total hip replacement. J Bone Joint Surg 1978;66660-A:613-8
Reynolds MA et al. Is the timing of fracture fixation important for the patients with multiple trauma? Ann Surg 1995 (4):470-81.
Johnson KD et al. Incidence of adult respiratory distress syndrome in patients with multiple musculoskeletal injuries: effect of early stabilization of fractures. J Trauma 1985;25(5):375-84
Bone LB, Johnson KD et al. Early versus delayed stabilisation of femoral fractures: a preospective randomised study. J Bone Joint Surg 1989;71-A:336-40
Pape HC et al. Primary intramedullary femur fixation in multiple traumapatients with associated lung contusion - a cause of posttraumatic ARDS? J Trauma 1993;34(4)"540-8
Pape HC et al. Influences of different methods of intramedullary femoral nailing on lung function in patients with multiple trauma. J Trauma 1993; 35 (5):709-16
Feliciano DV, Mattox KL et al. Intra-abdominal packing for control of hepatic hemorrhage : a reprisal. J Trauma 1981;21:285-90
Stone HH, Strom PR et al. Management of the major coagulopathy with onset during laparotomy Ann Surg 983;197:532-5
Rotondo MF, Schwab CW, McGonigal MD et al. 'Damage Control - an approach for improved survival in exsanguinating penetrating abdminal injury. J Trauma 1993;35:375-382
Keel M, Trentz O. Pathophysiology of polytrauma. Injury 2005;36:691-709
Rotstein OD. Modeling the two-hit theory hypotesis for evaluating strategies to prevent organ injury after shock/resuscitation. J Trauma 2003;54(Suppl. 5):203-6
Dunham CM et al. Postraumatic multiple organ dysfunction syndrome - infection is an uncommon antecedent risk factor. Injury 1995;26:373-8
Keel M, Labler L, Trentz O. Damage control in severly injured patients. Eur J Trauma 2005;31:212-21
Rosenfeld JV. Damage control neurosurgery. Injury 2004;35;655-60
Miller PR et al. Prospective evaluation of vacum-assisted fascial closure after open abdomen. Planned ventral hernia rate is substantial reduced. Ann Surg 2004;239:608-16
Shapiro MB, Jenkins DH et al. Damage control: colective review. J Trauma 2000;49:969-78
|
Politica de confidentialitate |
| Copyright ©
2025 - Toate drepturile rezervate. Toate documentele au caracter informativ cu scop educational. |
Personaje din literatura |
| Baltagul caracterizarea personajelor |
| Caracterizare Alexandru Lapusneanul |
| Caracterizarea lui Gavilescu |
| Caracterizarea personajelor negative din basmul |
Tehnica si mecanica |
| Cuplaje - definitii. notatii. exemple. repere istorice. |
| Actionare macara |
| Reprezentarea si cotarea filetelor |
Geografie |
| Turismul pe terra |
| Vulcanii Și mediul |
| Padurile pe terra si industrializarea lemnului |
| Termeni si conditii |
| Contact |
| Creeaza si tu |