1. Generalitati
Datorita impactului extrem de negativ al depunerilor, in special a celor dure, asupra transferului termic prin tevile de otel carbon, au fost elaborate diverse modele de depunere a namolului pentru a aprecia gradul de murdarire al unor componente ale circuitului secundar functie de conditiile de operare ale acestuia. In acest context, Beal si Chen[121] au propus un model pe baza caruia au putut calcula dependenta masei depuse in timp in diferite zone si subzone ale circuitului secundar. Masele calculate pe baza vitezelor de depunere si reantrenare ale particulelor, depinzand in mare masura de conditiile termohidraulice din fiecare zona, au fost obtinute printr-o analiza tridimensionala a codului THIRST
Cunoscand faptul ca in decursul operarii centralelor nucleare de putere, procesele de coroziune care au loc la interfata aliaj feros/ apa fac ca diversi compusi ai fierului ca Fe(OH)2, Fe(OH)3, Fe3O4, etc. sa se acumuleze, pe suprafetele circuitelor confectionate din oteluri carbon, a aparut necesitatea indepartarii lor, fie partial prin descalare sau decrustare - in decursul functionarii instalatiilor-, fie la scoaterea lor din operare (de exemplu, decontaminarea finala).
La alegerea solutiilor de reactivi cu care se va face indepartarea partiala - denumita decrustare sau descalare - sau curatirea chimica a componentelor confectionate din aliaje feroase, trebuie sa se tina cont de urmatoarele cerinte:
- solutia aleasa trebuie sa fie capabila sa dizolve complet sau cel putin partial o parte din compusii prezenti in filmul depus, asa incat acesta sa poata fi complet sau, cel putin, partial indepartat;
- compozitia solutiei trebuie astfel formulata incat sa asigure un atac minim asupra metalului de baza;
- rezidiile chimice - substantele care iau nastere in urma reactiilor chimice de decrustare - nu trebuie sa cauzeze procese de coroziune in timpul exploatarii ulterioare a instalatiei, in caz ca spalarea ulterioara decrustarii nu le-a indepartat complet;
- solutia de spalare (decrustare) nu trebuie sa fie toxica sau exploziva si trebuie sa fie usor de manipulat [103].
In cazul centralelor nucleare PHWR, solutiile de spalare sau decrustare concepute pana in prezent, au continut:
unul sau un amestec de acizi organici ca: acid lactic, oxalic, citric, etc.
un agent de complexare ca: H-EDTA, Na4-EDTA, etc.
inhibitori adecvati, care sa micsoreze cat mai mult posibil atacul solutiei asupra metalului de baza, neacoperit.
Cea mai simpla reprezentare a reactiei de dizolvare a Fe3O4 in mediu acid (MDR- magnetite dissolution reaction) este urmatoarea [123]:
Fe3O4 + 8 H+ 2 Fe3+ + 4 H2O + Fe2+ (1)
In aceasta reactie nu sunt implicate procese redox, raportul intre ionii Fe3+/Fe2+ existenti in Fe3O4 fiind mentinut si in produsii de dizolvare. Pentru acest motiv, aceasta reactie este denumita "MDR stoichiometric". In prezenta agentilor reducatori, reactia MDR poate capata un caracter reducator:
Fe3O4 + 8 H+ + 2 e- 3 Fe2+ + 4 H2O (2)
In acest caz, fierul din Fe3O4 este eliberat in solutie doar sub forma ionilor Fe2+. Din reactia (2) rezulta faptul ca rolul principal al inhibitorilor de coroziune adaugati in solutiile de curatire acide consta in restrangerea atacului coroziv asupra metalului de baza [123].
Ecuatiile reactiilor (1) si (2) reprezinta cazuri particulare ale urmatoarei expresii generale a MDR:
Fe3O4 + 8 H+ + ne- (2-n)Fe3+ + (1+n)Fe2+ + 4H2O (3)
unde: 1<n<2. Cand "n" este 0 si respectiv 2, se revine la reactia (1) si respectiv (2) [123].
Este foarte important ca probele care urmeaza a fi curatate chimic in solutiile de descalare (decrustare) sa fie din acelasi metal cu cele care urmeaza a fi descalate in realitate din instalatie, deoarece mici diferente in compozitia chimica sau structura metalului pot conduce la diferente majore in performantele finale ale descalarii. Eventualele tratamente termice la care sunt supuse uneori componentele anterior introducerii lor in instalatie pot induce, chiar in cazul aceluiasi metal, diferente majore in ceea ce priveste dimensiunea grauntilor, orientarea acestora si stresurile reziduale. Suprafetele probelor trebuie curatite anterior decrustarii doar prin degresare, intrucat orice alt tip de curatire mai energic (ca de ex: sablarea, decaparea acida, etc) poate afecta capacitatea de descalare a solutiilor de curatare chimica si implicit reproductibilitatea experimentelor.
Solutiile de decrustare, aditivate sau nu cu inhibitori de coroziune, vor trebui sa indeplineasca urmatoarele conditii:
sa fie stabile chimic, astfel incat sa nu-si modifice caracteristicile fizico-chimice in decursul descalarii si
sa aiba acelasi pH final ca si solutia initiala.
In vederea selectarii rapide a unor inhibitori de coroziune cat mai eficienti, este recomandabila utilizarea metodelor electrochimice si cu precadere cea a polarizarii lineare. Eficienta curatirii chimice in absenta / prezenta inhibitorilor va putea fi evaluata rapid, utilizand urmatoarele doua procedee:
grafic - prin suprapunerea picurilor catodice corespunzatoare metalului testat, de exemplu, in solutii neinhibate sau inhibate cu diverse concentratii de inhibitori si
prin calcul, folosind ecuatiile (1) si (2) de mai jos, in care intra vitezele de coroziune calculate pe baza pantelor Tafel sau a rezistentelor de polarizare.
![]() (1) in care:
(1) in care:
(Vcor)o - viteza de coroziune a metalului masurata in solutia neinhibata si
(Vcor)i - viteza de coroziune a metalului masurata in solutia inhibata;
E - eficienta descalarii sau a inhibarii (in procente).
![]() (2) in
care:
(2) in
care:
(Rp)i - rezistenta de polarizare masurata in prezenta inhibitorului dupa timpul t;
(Rp)o -rezistenta de polarizare(Rp) masurata in absenta inhibitorului dupa acelasi timp.
Se stie ca produsii de coroziune iau nastere ca urmare a interactiei fierului rezultat din componentele metalice cu un fluid mai mult sau mai putin coroziv. Acest strat de produsi de coroziune se poate comporta ca un strat pasiv semiprotector sau complet protector. Fortele mecanice care pot cauza indepartarea straturilor superficiale de produsi de coroziune sunt, in principal, tensiunile mecanice exercitate asupra lor.
Metalele neacoperite rezista mai bine tensionarii mecanice decat compusii fragili cum sunt, de exemplu, filmele superficiale de produsi de coroziune [124].
In cazul unei film superficial aflat sub o tensiune de intindere sau compresiva, grosimea(h) la care el devine fragil sau apar fisuri prin el, este corelata cu energia superficiala de fracturare g, modulul lui Young (E) si cu forta aplicata t prin relatia (3)[125]:
![]() (3)
(3)
Fisurarea filmului se va produce cand tensiunea exercitata asupra lui va depasi limita sa de cedare. Tensiunile tangentiale cauzate de presiunea fluidului circulant sunt cu cateva ordine de marime mai mari decat cele axiale. Aceste forte care actioneaza asupra suprafetei este mai probabil sa indeparteze stratul de produsi de coroziune decat stresurile de forfecare ale peretilor. In cazul existentei unui suport mecanic al tevii, prezenta acestuia va afecta marimea tensiunii axiale. Tensiunea de forfecare a peretilor este un factor important in transportul reactantilor corozivi la suprafata metalului, insa fortele mecanice cele mai mari apar ca rezultat al fortelor tangentiale.
Filmele de produsi de coroziune formate pe tevi contin defecte spatiale neregulate. Metalul este, de asemenea, eterogen, constand din faze care contin graunti. In contextul lucrarii lui Ramachandran, un graunte este considerat o cristalita metalica cu dimensiunea de cca.20mm [124]. El a presupus ca procesul de coroziune implica numai dizolvarea fierului din grauntii superficiali aflati in contact direct cu fluidul. Din ecuatiile prezentate in lucrare, reiese faptul ca datorita cresterii modulului lui Young in pori, va avea loc ingrosarea stratului de produsi de coroziune, la care acesta va incepe sa se fisureze. In schimb, este posibil ca un strat mai gros de produsi de coroziune sa asigure un grad mai ridicat de protectie contra coroziunii prin scaderea vitezei de transport a speciilor reactive la suprafata metalului. S-a observat ca porozitatea unui strat de produsi de coroziune aflat in contact cu o solutie neinhibata va fi mai mare, deoarece el va include molecule de apa; in schimb, in cazul existentei unor inhibitori de coroziune in solutia respectiva, acestia vor determina scaderea porozitatii filmului superficial, care va conduce la cresterea modulului lui Young. Avand in vedere influenta nefasta a depunerilor atat asupra transferului termic prin peretii tevilor cat si asupra accentuarii coroziunii metalului de baza aflat sub ele, a devenit stringenta necesitatea indepartarii lor fie in decursul functionarii instalatiilor, fie la scoaterea din operare definitiva a aceastora.
2. Decrustari experimentale
2.1.Conditiile experimentale in care au fost executate decrustarile
Avand in vedere ca scopul curatirii chimice (descalarii) este de a indeparta partial sau total depunerile formate pe otelurile carbon din circuitul secundar al unei centrale nucleare, este necesar ca inainte de executarea acestei operatii sa se procedeze la filmarea (acoperirea cu filme de compusi superficiali) probelor respective. Aceasta filmare a fost executata in acele conditii de chimism ale apei si la parametrii de operare specifici circuitului secundar, adica: pH 9,7 ; (260 5)oC ; (5,5 0.1)MPa.
Aliajele supuse autoclavizarilor au fost cele trei tipuri de oteluri carbon, o atentie speciala acordandu-se otelului SA106gr.B, care s-a dovedit cel mai susceptibil la coroziune in conditiile de operare ale circuitului secundar. Probele din otel carbon au fost pregatite anterior autoclavizarilor conform procedurilor standard, dupa care au fost autoclavizate in conditiile susmentionate, simuland pe cele de operare ale circuitului secundar.
Avand in vedere ca desi inhibitorii asigura o oarecare protectie metalului de baza, neacoperit, ei contribuie destul de putin la incetinirea procesului de decrustare. Pornind de la aceste premize, in experimentele executate au fost utilizate atat solutii de decrustare neinhibate cat si aceeasi solutie de baza aditivata cu diversi inhibitori. Solutia propriu-zisa de decrustare neinhibata a continut: 0,4g/l acid citric, (0.1 0,3)g/l Na4-EDTA si o concentratie foarte mica de hidrazina, asa incat pH-ul final al solutiei sa nu depaseasca valoarea de 5,2; a fost impusa aceasta restrictie valorii maxime a pH-ului, intrucat in solutiile care au un pH mai mare, decrustarea nu mai este la fel de eficienta si deci, implicit, filmul superficial de produsi de coroziune nu se mai dizolva .
Au fost executate urmatoarele tipuri de teste:
- teste quasistatice de decrustare, efectuate intr-un balon prevazut cu refrigerent ascendent. Pentru executarea propriu-zisa a decrustarii probelor, solutia din balonul in care au fost imersate probele a fost mentinuta perioada de timp necesara la temperatura de 85oC, utilizand un incalzitor electric prevazut cu un agitator magnetic. Cantarind periodic si implicit inregistrand pierderile in greutate ale probelor dupa diferite perioade de expunere in solutia de decrustare, au fost obtinute datele gravimetrice necesare trasarii curbelor cinetice si, acolo unde a fost cazul, evaluarii eficientei inhibitorului;
- teste de decrustare in regim dinamic care au fost executate intr-o instalatie care opereaza in regim dinamic si in care, pe parcursul testelor, au fost mentinute constante temperatura, timpul si compozitia solutiilor de decrustare [126].
Derularea unui experiment in regim dinamic este urmatoarea: solutia de decrustare preparata este introdusa in rezervorul de stocare, unde este incalzita la temperatura de 85oC cu ajutorul a doua rezistente electrice. Solutia este apoi preluata din acest rezervor cu ajutorul unei pompe de recirculare si introdusa in sectiunea sau sectiunile de testare in care se afla suportii pe care sunt montate probele. Din timp in timp, pe parcursul decrustarii, instalatia a fost oprita si o parte din probe au fost demontate de pe suporti si cantarite in scopul evaluarii pierderilor in greutate functie de timp. Totodata, instalatia fiind prevazuta cu puncte de prelevare probe de solutie la iesirea din sectiunile de testare si la iesirea din coloana cu schimbatori de ioni, atunci cand instalatia a fost oprita pentru prelevarea probelor, au fost prelevate si solutii in scopul determinarii concentratiei ionilor de fier trecuti in solutie, utilizand metoda spectrofotometrica sau spectrometria de masa.
In solutiile de decrustare inhibate au fost introdusi diversi inhibitori de coroziune si anume: trietanolamina, trietilamina, propargilamina, etc. Dintre acestia, eficienta cea mai mare si respectiv cea mai ieftina s-a dovedit a fi trietanolamina. Pentru a selecta concentratia optima de inhibitor, aceasta a fost variata in domeniul [5.10-4M÷3.10-3M].
Avand in vedere complexitatea mai mare a testelor executate in instalatia de decrustare, inainte de demararea acestora, s-a procedat la determinarea prin metoda potentiodinamica a eficientei decrustarilor realizate in solutii similare de decrustare neinhibate si continand, respectiv, diverse concentratii din diferiti inhibitori.
Pentru realizarea acestor masuratori electrochimice, probele din otel carbon - atat filmate cat si neacoperite - au fost folosite ca electrozi de lucru in celula electrochimica aferenta lantului electrochimic Princeton Model 273 si respectiv 2273. Utilizand metoda potentiodinamica (PD), au putut fi determinati curentii si respectiv vitezele de coroziune din pante Tafel si din rezistentele de polarizare (Rp). Pentru realizarea masuratorilor electrochimice la temperatura de 85oC, solutia din celula electrochimica a fost incalzita pe un incalzitor electric prevazut cu agitare electromagnetica, iar dupa stabilizarea temperaturii solutiei, era demarat testul electrochimic propriu-zis.
Asa cum s-a aratat deja, valorile vitezelor de coroziune si/ sau ale rezistentelor de polarizare aferente sistemelor electrod/ solutie de descalare aditivata sau nu cu inhibitor, calculate la sfarsitul fiecarui test, au fost utilizate ulterior la calculul eficientei protectiei asigurate de diversi inhibitori utilizand ecuatiile (1) si (2).
Exceptand masuratorile electrochimice mentionate anterior, utilizate pentru selectarea solutiilor de decrustare si a inhibitorilor adecvati a fi folositi in ele, probele decrustate au fost supuse si altor tipuri de masuratori electrochimice si anume:
variatia lui Ecor functie de timp executata in solutii de decrustare neinhibate sau continand diverse concentratii de inhibitori si
masuratori de impedanta electrochimica (EIS) pe probe filmate si respectiv decrustate diferite perioade de timp, necesare pentru a determina caracteristicile electrochimice ale filmelor initiale sau remanente.
Toate aceste tipuri de masuratori au fost executate atat la temperatura camerei cat si la (80 5)oC, functie de scopul final al testului. Testele electrochimice executate pentru aprecierea eficientei solutiilor de decrustare neinhibate sau continand diversi inhibitori, au fost efectuate in solutiile respective de decrustare. In schimb, in masuratorile de impedanta a fost folosita o solutie de acid boric si borat de sodiu, intrucat aceasta nu altera integritatea si caracteristicile atat ale probelor propriu-zise, neacoperite cat si pe ale celor filmate. In scopul aprecierii gradului de porozitate si compactare a filmelor superficiale, masuratorile de impedanta au fost efectuate dupa mentinerea probelor in solutia de acid boric si borat de sodiu (codificata electrolit), timp de: 0.5; 4; 8 si 24 ore.
Pentru determinarea grosimii si uniformitatii filmelor superficiale de compusi formati initial sau remanenti pe suprafetele cupoanelor din otel carbon, a fost utilizata microscopia metalografica, iar compozitia filmelor superficiale formate post-autoclavizare si respectiv ramase dupa decrustare, a fost evaluata prin difractie de raze X.
Utilizand determinarile gravimetrice, s-a putut determina masa filmului dizolvat si/ sau a metalului neacoperit din probele martor, trecut in solutia de decrustare, dupa diferite perioade. Reprezentand grafic aceste date functie de timpul cat a durat decrustarea probelor, au putut fi trasate curbele si respectiv au fost determinate ecuatiile cinetice corespunzatoare fiecarui sistem tip otel/tip solutie de decrustare / perioada de decrustare.
In paralel cu aceste evaluari cinetice, s-a determinat spectrofotometric concentratia ionilor de fier trecuti in solutie dupa diferite perioade de decrustare, in diverse variante de solutii neinhibate sau aditivate cu inhibitori.
Cinetica decrustarii otelurilor carbon in regim static si dinamic
Pentru a evalua cinetica decrustarii probelor de otel carbon, in regim quasistatic sau dinamic in solutiile de decrustare specifice, in fiecare test de acest tip au fost introduse ambele categorii de probe: filmate si respectiv neacoperite. Probele neacoperite au fost folosite ca probe-martor, ele utilizandu-se pentru estimarea atacului solutiei de decrustare asupra metalului de baza, neacoperit, in perioada respectiva de decrustare. Dupa diferite perioade de decrustare, probele destinate determinarilor cinetice au fost scoase, clatite in apa, acetona, uscate si cantarite. Pe baza determinarilor gravimetrice, au fost trasate curbele cinetice aferente pierderilor in greutate inregistrate post-decrustare functie de timp, caracteristice atat diferitelor tipuri de probe cat si diverselor solutii.
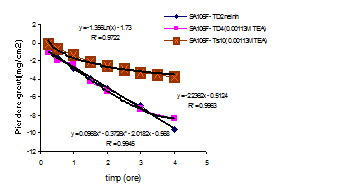
Fig.1[126] Cinetica descalarii otelului SA106 filmat in solutie de descalare neinhibata (TD2) si in solutie continand 0.00113M TEA (TD4) in regim dinamic si respectiv static (Ts10)
Pentru exemplificare, in figura 1[126] sunt prezentate curbele cinetice corespunzatoare decrustarii in regim dinamic a otelului SA106 filmat, atat intr-o solutie clasica neinhibata (TD2) cat si aditivata cu 1,13 10-3M TEA (TD4) comparativ cu curba pierderilor in greutate inregistrate pe acelasi tip de otel post-descalare, in regim static, in prezenta aceleasi concentratii de inhibitor (Ts10). aceasta figura, se desprind urmatoarele remarci:
in cazul descalarii dinamice, pierderile in greutate au fost mai mari, practic duble, comparativ cu descalarea executata in regim static in solutia similara si
in timp ce pierderile in greutate inregistrate dupa descalarea statica tind spre un palier dupa cca.2,5 ore, in cazul descalarilor dinamice, ele tind spre pierderi in greutate tot mai mari pe masura cresterii perioadei de decrustare. Aceasta ultima remarca ne indreptateste sa presupunem ca in urma executarii descalarilor dinamice o perioada de minim doua ore, intregul film superficial este indepartat, dupa care incepe sa aiba loc dizolvarea metalului neacoperit in solutia respectiva de decrustare.
S-a observat, de asemenea, ca adaugarea unor concentratii mici de trietanolamina (TEA) cuprinse intre 5.10-4 si 1,13.10-3M in solutiile utilizate in descalarile executate in regim static, n-a condus la modificarea marcanta a curbelor pierderilor in greutate comparativ cu cele aferente sistemului otel carbon filmat/ solutie de descalare neinhibata.
Comparand pozitia curbelor pierderilor in greutate in cazul sistemelor otel carbon SA106 neacoperit/ solutie de descalare neinhibata si respectiv continand 5.10-4M TEA, inregistrate in regim static si respectiv dinamic, se observa ca dupa 0,5h, au fost inregistrate pierderi in greutate mai mici in regim static decat in regim dinamic, aceasta diferenta crescand foarte mult dupa 1,5 ore (fig.2[126]).
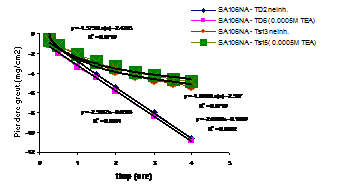
Fig.2[126] Curbele aferente otelului carbon neacoperit descalat in regim dinamic(TD2 si TD6) si respectiv static, in solutii neinhibate(Ts13) si continand 5.10-4M TEA (Ts15)
De asemenea, in timp ce curbele descalarii in regim static tind spre valori practic constante dupa 2,5ore, cele corespunzatoare descalarii in regim dinamic sunt drepte descrescatoare, care tind spre pierderi in greutate tot mai mari pe masura derularii descalarii Fig.3[126].
Comparand in fig. 4[126] cele doua regimuri de descalare, utilizand de aceasta data o solutie aditivata cu 1,13.10-3M TEA, se confirma observatiile facute in cazul solutiei neinhibate.
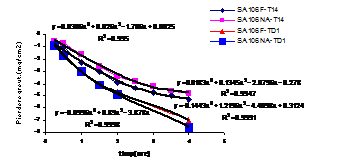
Fig.3[126] Cinetica descalarii otelului carbon filmat si respectiv neacoperit in solutii de descalare neinhibate continand 0,1g/l Na4EDTA in regim static (T14) si dinamic (TD1)
In plus, se pot remarca urmatoarele:
- curbele pierderilor in greutate corespunzatoare descalarii in regim static a ambelor oteluri - filmate si respectiv neacoperite - sunt paralele, foarte apropiate si corespund unor pierderi in greutate mult mai mici decat cele aferente testelor executate pe probe similare in regim dinamic;
- in cazul utilizarii regimului dinamic, curbele corespunzatoare celor doua tipuri de suprafete sunt apropiate, tinzand continuu spre pierderi in greutate din ce in ce mai mari cu cresterea perioadei de descalare.
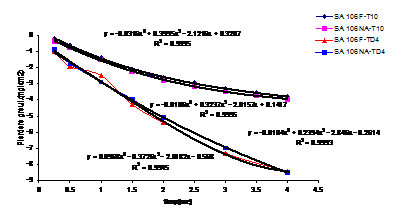
Fig.4[126] Cinetica descalarii otelului carbon filmat si respectiv neacoperit in solutii de descalare aditivate cu 1,13 10-3M TEA in regim static (T10) si respectiv dinamic (TD4)
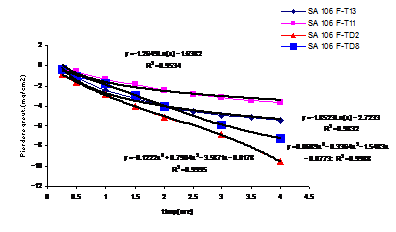
Fig.5[ Cinetica descalarii otelului SA106 filmat in solutii neinhibate in regim static (T13) si respectiv dinamic (TD2) si in regimuri similare in solutii aditivate cu 0,0083 M TEA (T11 si TD8)
In figura 5[126] este prezentata influenta adausului concentratiei maxime de inhibitor(3 10-3M) asupra pierderilor in greutate inregistrate pe probele de otel carbon filmate, descalate atat in regim static cat si dinamic. Din aceasta figura remarcam urmatoarele:
- lucrand in regimuri identice de agitare sau curgere, se observa ca in cazul descalarilor executate in solutii aditivate cu inhibitor, se obtin pierderi in greutate mai mici decat cele inregistrate in testele in solutii neinhibate;
- pierderile in greutate inregistrate in solutii identice, sub regimuri diferite de agitare, variaza astfel: pierderile in greutate inregistrate in regim dinamic sunt mai mari decat cele consemnate in regim static.
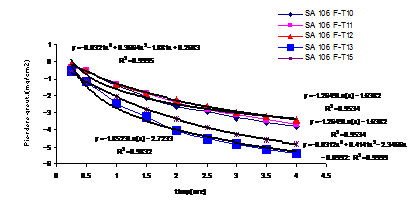
Fig.6[126] Cinetica descalarii otelului carbon filmat in regim static, in solutie neinhibata (T13 ) si respectiv aditivata cu urmatoarele concentratii de TEA: 0.0005 M (T15), 0.00113 M (T10), 0.0045 M (T11), 0.0083 M (T12)
Curbele cinetice ale pierderilor in greutate inregistrate in urma descalarilor executate in regim static, efectuate in solutie de descalare neinhibata si respectiv aditivata cu concentratii crescatoare de TEA, cuprinse intre 5.10-4M si 8,3.10-3M (fig.6[126]), releva urmatoarele aspecte:
- pierderile in greutate cele mai mari au fost obtinute in solutia neinhibata;
- cu cresterea concentratiei de TEA, pierderile in greutate inregistrate dupa perioade similare de timp au fost din ce in ce mai mici, astfel incat curba corespunzatoare celor mai mici pierderi in greutate a fost cea inregistrata in testul in care s-a utilizat solutia de decrustare care a continut cea mai mare concentratie de TEA.
Curbele pierderilor in greutate inregistrate in urma descalarii in regim dinamic in solutiile neinhibate si respectiv aditivate cu concentratii crescatoare de TEA sunt prezentate in figura 7. [126]
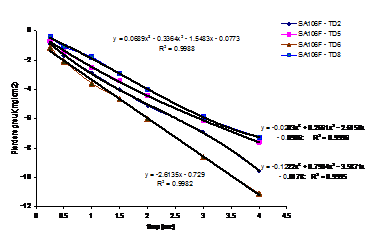
Fig.7[126] Cinetica descalarii otelului carbon filmat in regim dinamic in solutie neinhibata (TD2) si aditivata cu urmatoarele concentratii de TEA: 0.0005 M (TD6), 0.00113 M (TD5), 0.003 M (TD8)
Curbele din aceasta figura au aceeasi tendinta generala remarcata si in cazul testelor executate in regim static. Principala diferenta consta in faptul ca in cazul regimului dinamic, curbele au o tendinta continua spre pierderi in greutate din ce in ce mai mari cu cresterea perioadei de descalare.
In fig.8[126] este reflectata influenta regimului de curgere asupra pierderilor in greutate inregistrate in decursul descalarilor probelor filmate, descalari efectuate in solutii neinhibate. In cazul descalarii executate in regim quasistatic, variatia concentratiei Na4EDTA nu a atras dupa sine o variatie semnificativa a curbelor cinetice. In schimb, trecerea de la regimul static la cel dinamic a condus la schimbarea tipului ecuatiei care fiteaza curba: logaritmica - in cazul regimului quasistatic - si polinomiala de ordinul 3, puternic descrescatoare, in cazul regimului dinamic.
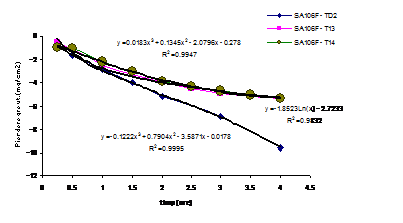
Fig.8[126] Cinetica descalarii in regim static a otelului carbon in solutii neinhibate continand 0,1 si respectiv 0,3g/l Na4EDTA(T13,T14) si respectiv in regim dinamic, in solutie neinhibata continand 0,3g/l Na4EDTA (TD2)
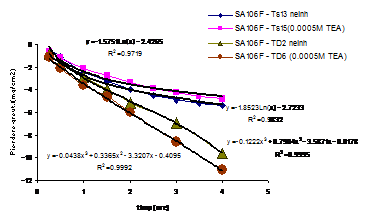
Fig.9[126] Cinetica descalarii otelului carbon filmat in regim static(Ts13) si dinamic (TD2), in solutii de descalare neinhibate si in regimuri similare in solutii continand 0,0005M TEA (Ts15,TD6)
Din fig.9[126], in care sunt prezentate comparativ curbele cinetice corespunzatoare descalarii otelului filmat in ambele regimuri: static si dinamic, in solutie neinhibata si respectiv continand concentratia minima de TEA - 5.10-4M -, remarcam urmatoarele:
- curbele corespunzatoare pierderilor in greutate inregistrate ca urmare a utilizarii regimului static de descalare se prezinta grupate in zona pierderilor celor mai mici in greutate, carora le corespund descalarile executate in prezenta inhibitorului. In cazul regimului dinamic, toate curbele manifesta o tendinta marcanta spre valori mai mari ale pierderilor in greutate;
- cele doua curbe corespunzatoare descalarii in regim dinamic sunt situate sub cele corespunzatoare descalarii in regim static, avand o tendinta pronuntata de crestere continua a pierderilor in greutate. Acest fapt este demonstrat si de ecuatiile corespunzatoare curbelor trasate in regim dinamic care sunt polinomiale, spre deosebire de cele aferente regimului static, care sunt logaritmice.
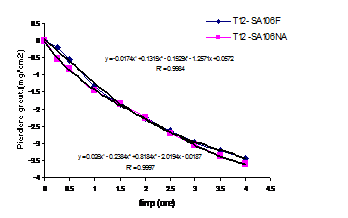
Fig.10[126]Cinetica decrustarii in regim static a otelului carbon filmat si respectiv neacoperit in solutia continand 0.0083M TEA
In cazul utilizarii unei concentratii mai mari de inhibitor - 10-3M TEA - pH-ul solutiei de descalare se modifica puternic, devenind egal cu 7,56. In aceasta situatie, capacitatea de descalare in regim static a ambelor tipuri de probe - filmate si neacoperite - devine comparabila, fapt dovedit de ecuatiile si alura curbelor din fig.10[126].
Desi cele doua curbe sunt foarte apropiate, totusi curba aferenta probelor neacoperite este situata deasupra celei corespunzatoare probelor filmate, corespunzand, deci, unor pierderi ceva mai mari in greutate. Deci, in prezenta acestor concentratii mai mari de inhibitor, actiunea de protectie a metalului de baza datorata prezentei inhibitorului a devenit dominanta, in detrimentul decrustarii.
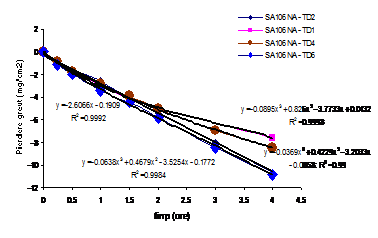
Fig.11[126] Cinetica descalarii in regim dinamic a otelului carbon neacoperit in solutii de descalare neinhibate (TD1, TD2) si in prezenta a (5x10-4)M TEA (TD6) si respectiv (1.13x10-3 )M TEA (TD4)
Cinetica descalarii in regim dinamic a otelului carbon neacoperit in solutii neinhibate continand doua concentratii diferite de Na4EDTA si avand implicit pH-uri initiale diferite si respectiv in prezenta unor concentratii crescatoare de TEA (fig.11[126]), a prezentat urmatoarele caracteristici:
- prezenta unei concentratii minime de inhibitor - 5.10-4M TEA - nu a avut un efect sesizabil asupra cineticii descalarii otelului carbon neacoperit comparativ cu solutia neinhibata; in consecinta, curbele corespunzatoare acestor situatii sunt foarte apropiate si au aceeasi tendinta de crestere usoara a pierderilor in greutate cu marirea perioadei de descalare;
- curba corespunzatoare descalarii in solutia continand concentratia maxima de TEA este plasata pe grafic deasupra celorlalte doua, corespunzand, deci, unor pierderi in greutate mai mici.
In fig.12[126] sunt prezentate curbele omoloage celor din figura 11, dar, corespunzand, de aceasta data, otelului SA106 filmat. Prezenta unui film superficial pe probe atrage dupa sine departajarea curbelor, chiar si in prezenta concentratiei minime de TEA.
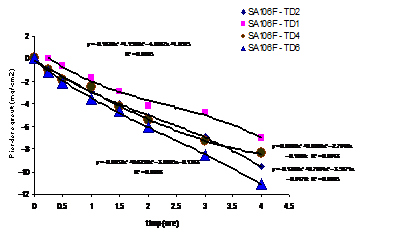
Fig.12[126] Cinetica descalarii otelului carbon filmat in regim dinamic in solutii neinhibate (TD1, TD2) si respectiv in solutii continand
5x10-4 M TEA (TD6) si 1.13x10-3M TEA (TD4)
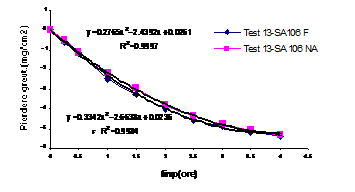
Fig.13[126] Cinetica descalarii otelului carbon filmat si respectiv neacoperit in solutii de descalare neinhibate continand 0.1g/l Na4EDTA
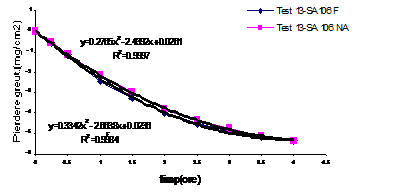
Fig.14[126] Cinetica descalarii otelului carbon filmat si neacoperit
in solutii de descalare neinhibate continand 0.2g/l Na4EDTA
Comparand amplasarea curbelor in cazul testelor executate in regim static in solutii neinhibate continand concentratii diferite de Na4EDTA (figurile 13,14)[126], remarcam urmatoarele:
- prezenta unei concentratii de Na4EDTA egala cu 0,2g/l estompeaza diferentele dintre probele filmate si cele neacoperite;
- dupa perioade egale de decrustare, in solutia continand 0,2g/l Na4EDTA, se inregistreaza pierderi in greutate mai mari decat in cealalte solutii care contin 0,1g/l Na4EDTA.
Analizand comparativ valorile cantitatilor de produsi de coroziune total formati si in special ai celor aderenti cu cele pe baza carora au fost trasate curbele cinetice aferente decrustarilor in regim static si dinamic, remarcam ca, in general, in decursul unei decrustari de o ora in regim static si respectiv 45 minute in regim dinamic, aproape tot filmul superficial de produsi aderenti a fost indepartat. Rezulta ca ulterior are loc un atac asupra metalului de baza, care este dizolvat cu atat mai usor cu cat solutia de decrustare a continut o concentratie mai mica de inhibitor.
Examinarea prin difractie de raze X a probelor din otel carbon autoclavizate a aratat ca filmul depus este format in principal din magnetita(Fe3O4) depusa pe suport feritic( -Fe); magnetita reprezinta cca. 88% din filmul superficial, restul revenind unor cantitati foarte mici de -FeOOH, -FeOOH, Fe(OH)2 si Fe2O3. Dupa o ora de decrustare in regim static, s-a constatat ca pe otelul carbon a ramas cca.55% magnetita.
Micrografia filmului format post-autoclavizare pe otelul carbon demonstreaza ca acesta este continuu si relativ uniform, grosimea lui fiind cuprinsa intre 3 si 8 m(fig.15[126]).
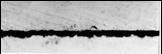
Fig.15[ Aspectul in sectiune al filmului de oxid format
post-autoclavizare pe otelul carbon SA106 gr.B(x 500)
Dupa decrustarea probelor in regim static timp de o ora si cu atat mai mult dupa doua ore, se constata subtierea puternica a filmului initial (fig.16[126]). Aplicand decrustarea dinamica timp de o ora, in ambele tipuri de solutii -neinhibata sau inhibata-, filmul initial este indepartat complet.
|
|
Fig.16[126]Aspectul in sectiune al filmului remanent pe suprafata otelului carbon autoclavizat dupa decrustare in regim dinamic timp de o ora (a) si respectiv doua ore (b) (x 500) |
3.2.Utilizarea metodelor electrochimice pentru caracterizarea filmelor superficiale initiale si remanente post-decrustare
Metodele electrochimice folosite pentru caracterizarea filmelor superficiale initiale si remanente post-decrustare, au fost urmatoarele:
. variatia potentialului de coroziune in circuit deschis (Ecor) in timp;
. metoda potentiodinamica si
. metoda impedantei electrochimice (EIS).
Primele doua metode, au fost aplicate in solutii de decrustare neinhibate sau aditivate cu diferite concentratii de inhibitor, iar determinarile EIS au fost facute in solutia de acid boric si tetraborat de sodiu.
3.2.a. Rezultatele masuratorilor variatiei potentialului de coroziune in timp
Pentru a monitora indepartarea in timp, in regim quasistatic a filmelor superficiale de pe otelul carbon SA106gr.B pe parcursul procesului de decrustare, s-a inregistrat variatia potentialului de coroziune (Ecor) in timp in cazul unor sisteme reprezentative proba filmata/ solutii de decrustare neinhibata si respectiv aditivata cu diverse concentratii de inhibitor (TEA).
|
|
|
|
|
d) |
|
Fig.17 a, b, c, d [126] Variatia potentialului de coroziune in circuit deschis in cazul sistemelor otel carbon filmat/urmatoarele solutii de decrustare: (a) neinhibata si respectiv (b,c,d) solutii aditivate cu urmatoarele concentratii de TEA: (b)5·10-4 M; (c) 1,13·10-3 M si (d) 3·10-3 M. |
|
Testele au fost executate la temperatura de 85oC, perioade de timp de maxim doua ore, pe o plita incalzita electric si prevazuta cu agitator electromagnetic pentru agitarea solutiei. Curbele Ecor/timp prezentate in figura 17a,b,c,d[126] au fost trasate in urmatoarele solutii: solutie neinhibata (fig.17a) si respectiv solutii aditivate cu urmatoarele concentratii de trietanolamina: 0,0005M (fig.17b), 0,00113M (fig.17c) si 0,003M (fig.17d).
Curba Ecor /timp din fig.17(a) corespunzatoare sistemului otel filmat/ solutie de decrustare neinhibata prezinta variatia cea mai mare de potential si anume intre valoarea initiala de (-199)mV si valoarea (-753)mV stabilita pe palier. Deplasarea cea mai abrupta de potential spre domeniul catodic s-a produs in primele 10 minute, ceea ce inseamna ca procesul de dizolvare al filmului superficial a avut loc preponderent in aceasta perioada. In final, s-a stabilit un echilibru la interfata, fapt confirmat de stabilirea unui palier al potentialului la (-753)mV.
Adausul unei concentratii foarte mici de TEA - 5.10-4M - a modificat atat valoarea potentialului initial, la care a inceput procesul de decrustare cat si valoarea palierului la care el s-a stabilizat in final(fig.17b). In cazul celorlalte doua curbe - corespunzatoare solutiilor aditivate cu 0.00113M si respectiv 0.003M TEA (fig.17c si 17d) - se constata ca variatia cea mai mare a potentialului de coroziune (Ecor) s-a produs in decursul primei ore. De aici rezulta ca procesul de decrustare a decurs mai lent in prezenta acestor inhibitori.
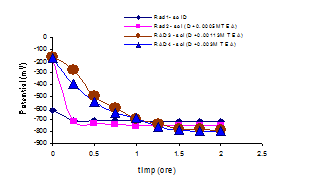
Fig.18[126] Curbele Ecor/timp aferente sistemelor otel carbon filmat/ urmatoarele solutii de decrustare: neinhibata (Rad1) si respectiv aditivata cu: 0.0005M TEA(Rad2 ), 0.00113M TEA(Rad3 ) si 0.003M TEA(Rad4)
Pentru o comparare mai sugestiva a acestor curbe, in fig.18[126] ele sunt prezentate suprapuse. Avand in vedere valorile palierelor de potential stabilite in final, care, sunt situate toate in domeniul catodic, rezulta ca procesul de decrustare a avut ca rezultat final indepartarea completa a filmelor superficiale. Deci, mecanismul de actiune al inhibitorilor consta in adsorbtia acestora pe filmele preexistente urmata de dizolvarea complecsilor formati. Cu alte cuvinte, inhibitorii nu franeaza procesul de dizolvare al filmelor, ci contribuie la o uniformizare a dizolvarii acestora concomitent cu protejarea metalului de baza.
3.2.b.Folosirea metodei potentiodinamice la evaluarea vitezelor de decrustare in diverse tipuri de solutii
Dupa cum se stie, metoda potentiodinamica poate fi folosita pentru:
- evaluarea vitezelor de coroziune ale electrozilor de lucru si
- compararea pe cale grafica a eficientei diversilor inhibitori de coroziune sau a diferitelor concentratii din acelasi inhibitor.
Valorile principalelor caracteristici electrochimice determinate din curbele potentiodinamice(PD) sunt prezentate in tabelul 1.
Examinand valorile incluse in tabelul 1[126] si pozitia celor patru curbe din figura 19[126], remarcam urmatoarele:
viteza cea mai mare de decrustare a fost inregistrata in solutiile de decrustare neinhibate, iar cea mai mica in solutia aditivata cu concentratia cea mai mare de inhibitor;
valoarea rezistentei de polarizare a fost minima in solutia de decrustare neinhibata si maxima in solutia aditivata cu concentratia maxima de inhibitor;
ramurile catodice si anodice ale picurilor fiind paralele, indica faptul ca TEA este un inhibitor mixt care, dupa adsorbtie, actioneaza asupra ambelor tipuri de procese catodice si anodice.
Tabelul nr.1[126] Parametrii electrochimici aferenti diverselor sisteme otel carbon filmat/ diferite solutii de decrustare
|
Cod |
Parametrii electrochimici determinati din curbele PD |
Sistemul studiat |
||||
|
E(I=O) [mV] |
ba [V[V/dec] |
bc [V/dec] |
Vcor [mpy] |
Rp W |
||
PD5 |
OLC F / SB |
|||||
|
PD6 |
OLC F/(SB + 1,13·10-3M TEA) |
|||||
|
PD7 |
OLC F/(SB + 5·10-4M TEA) |
|||||
|
PD8 |
OLCF/(SB + 3·10-3M TEA) |
|||||
Legenda: SB - solutia de baza de descalare, neinhibata
|
|
Fig.19[126] Curbele potentiodinamice aferente sistemelor otel carbon filmat/urmatoarele solutii de decrustare: solutie neinhibata (PD5) si continand urmatoarele concentratii de TEA: 0.0005M (PD71), 0.00113M (PD6) si 0.003M (PD83) |
3.2.c. Utilizarea metodei spectroscopiei impedantei electrochimice la caracterizarea filmelor superficiale
Filmele formate pe probele din otel carbon autoclavizate in conditiile specifice de operare ale circuitului secundar s-au dovedit a fi relativ aderente si compacte, fapt ilustrat prin suprapunerea aproape integrala a curbelor Bode si ale unghiurilor de faza corespunzatoare expunerii lor in electrolit (solutie de acid boric si borax) anterior masurarii impedantei, perioade de timp cuprinse intre 0,5 si 24h (fig.20[126]).
Examinand curbele din aceasta figura, se remarca faptul ca simultan cu cresterea perioadei de mentinere in solutie a probelor anterior executarii masuratorilor EIS, s-a constatat o usoara deviere a curbelor Nyquist spre valori ale rezistentei de polarizare(Rp) mai mici. De aici rezulta faptul ca filmul superficial format pe otelul carbon post-autoclavizare avand o oarecare porozitate, permite schimbul de ioni la interfata proba/ electrolit, urmat ulterior de derularea unor procese electrochimice. In schimb, filmul remanent pe acelasi tip de otel, dupa prima ora de decrustare in regim static, are un caracter protector mai slab fata de materialul de baza, fapt evidentiat atat prin deplasarea unghiurilor de faza spre valori mai mici de (-30)0, cat si prin aparitia unei intreruperi in curbele Bode corespunzatoare expunerii probei in solutie timp de 24 ore(fig.21[126]).
Masuratorile prin difractie de raze X au confirmat rezultatele susmentionate, aratand ca in urma primei ore de decrustare in regim static pe proba a ramas doar cca.55% magnetita.
|
|
Fig.20[126] Curbele Bode (a), ale unghiurilor de faza (b) si Nyquist (c) aferente urmatoarelor perioade de mentinere in electrolit a otelului carbon filmat: 0,5h( ); 4h (x); 8h (+) si 24h ( |
|
|
|
|
|
Faptul ca stratul de magnetita s-a subtiat este evidentiat si de masuratorile effectuate prin microscopie metalografica executate pe filmele remanente de pe probele autoclavizate, decrustate o ora si respectiv doua ore in regim static, cu care ocazie s-a observat ca grosimea stratului superficial a ajuns, in final, la cca.2μm, oxidul devenind neuniform.
Morfologia suprafetei probei evidentiaza diferente remarcabile intre marginile si centrul aceleiasi probe, dizolvarea oxidului fiind mult mai puternica la marginea probei.
|
|
Fig.21[126] Curbele Bode(a) si ale unghiurilor de faza(b) inregistrate dupa 0,5h de mentinere in electrolit a otelului carbon filmat ( ), decrustat static (x) si respectiv dinamic ( timp de o ora |
|
|
Oxidul nu a fost indepartat complet nici dupa doua ore de decrustare in regim static, dar zonele in care a aparut metalul de baza au devenit tot mai extinse. Asa se explica faptul ca stratul de oxid a devenit neuniform, discontinuu, cu zone in care lipsea complet oxidul si altele in care grosimea stratului era sub 1μm. Deci, aplicand un ciclu, respectiv doua cicluri de decrustare de cate o ora in regim dinamic otelului carbon filmat, s-a observat scaderea marcanta a grosimii filmului superficial, reflectata in scaderea impedantei si a caracterului protector al filmului fata de metalul de baza.
Curbele Bode si ale unghiurilor de faza din fig.22[126] sustin faptul ca filmul remanent pe proba de otel carbon decrustata dinamic timp de doua ore, este foarte subtire, poros si lipsit de aderenta. De aceea, in decursul expunerii ulterioare a probelor decrustate in solutia de electrolit perioade mai indelungate de 0,5h, ionii din electrolit au reusit sa patrunda prin filmul foarte subtire, contribuind la scindarea legaturilor interionice si interatomice.
Comparand curbele din figurile 20 22[126] aferente impedantelor filmelor existente initial si respectiv celor remanente dupa o ora si respectiv doua ore de decrustare, s-a constatat ca doar filmul format initial si-a pastrat caracteristicile pe parcursul expunerii probelor timp de 24 ore in electrolit. In cazul probelor decrustate o ora, valoarea impedantei Z a scazut la 2,75W.cm2, iar in cazul celor decrustate doua ore, aceasta a atins 2,1W.cm2.
|
|
Fig.22[126] Compararea curbelor Bode (a) si ale unghiurilor de faza (b) aferente otelului carbon filmat, decrustat in regim dinamic timp de doua ore si expus ulterior in electrolit urmatorii timpi: 0,5h ( ); 4h (x) si 24h ( anterior executarii masuratorilor EIS |
|
|
Deci, compusii superficiali depusi pe otelurile carbon in urma autoclavizarii in conditiile de operare specifice circuitului secundar, formeaza un film relativ aderent si protector fata de metalul de baza, fapt demonstrat si de curbele unghiurilor de faza din figura 20[126]. In schimb, filmul remanent pe acelasi otel carbon dupa aplicarea unui ciclu de decrustare de o ora in regim static are o impedanta mult mai mica comparativ cu filmul initial si un unghi de faza egal cu cca.(-30)o comparativ cu(-70)o, valoarea corespunzatoare filmului initial.
Comparand calitatea filmelor superficiale remanente pe probele de otel carbon filmate supuse unei decrustari de o ora si respectiv doua ore in regim dinamic, s-au remarcat urmatoarele:
- filmul ramas pe proba dupa o ora de decrustare in regim dinamic este mai subtire si poros decat cel remanent in urma decrustarii statice, fapt demonstrat de scaderea valorilor unghiurilor de faza cu perioada de expunere in solutie a probelor;
- fenomenul este si mai evident in cazul probelor supuse timp de doua ore decrustarii in regim dinamic, cand impedanta filmului superficial remanent post-decrustare pe proba mentinuta 24h in electrolitul din celula, a atins valoarea de 2,1Wcm2;
- s-a observat ca valorile unghiurilor de faza corespunzatoare filmelor initiale n-au variat sensibil cu perioada de mentinere a probelor autoclavizate in electrolit. In schimb, filmelor remanente post-decrustarea statica si dinamica le-au corespuns unghiuri de faza mai mici, care au virat spre valori si mai mici prin cresterea perioadei de mentinere a probelor in electrolit.
Prin decrustarea dinamica se realizeaza, asa cum era de asteptat, indepartarea mult mai rapida si profunda a filmului superficial, fapt confirmat atat micrografic(figura 16[126]), cat si prin valorile impedantei si ale unghiurilor de faza mult mai mari in cazul filmului initial comparativ cu cele ale filmelor remanente dupa o ora si respectiv dupa doua ore de aplicare a decrustarii.
Masuratorile EIS realizate pe filmele de pe probele autoclavizate supuse unei decrustari de cate o ora si respectiv doua ore in regim static sau dinamic, mentinute in electrolitul din celula diferite perioade de timp - cuprinse intre 0.5 ore si 24 ore- anterior masuratorilor de impedanta, au relevat urmatoarele aspecte:
- utilizarea a doua cicluri de decrustare a cate 0.5 ore fiecare in locul unuia singur conduce la o indepartare mai profunda, aproape totala a filmului initial existent pe probe;
- regimul dinamic de decrustare aplicat perioade identice cu cel static, asigura o indepartare mai profunda a filmului prezent pe probe;
- caracterul protector al filmelor rezultate in urma decrustarilor, indiferent daca au fost statice sau dinamice, scade drastic cu scaderea grosimii filmelor, fiind mult mai redus comparativ cu cel al filmului initial.
3.3.Variatia concentratiei fierului existent in solutiile prelevate post-decrustare
Determinarea concentratiilor ionilor de fier din solutiile prelevate post-decrustare a fost efectuata prin metoda spectrofotometrica.
Dupa executarea decrustarilor in regim dinamic, s-a ajuns la concluzia ca in solutiile neinhibate prelevate dupa diferite perioade de timp, indiferent de concentratia Na4EDTA, au fost inregistrate concentratii crescatoare de ioni de fier pe masura cresterii perioadei de decrustare pana la 2 ore; in intervalul 2-4ore, concentratia ionilor de fier a ramas practic neschimbata (fig.23[126]).
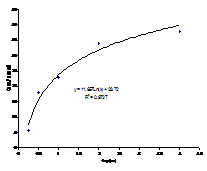
Fig.23[126] Variatia concentratiei ionilor de fier eliberati in solutia de decrustare neinhibata, in regim dinamic, dupa aplicarea decrustarii
diferite perioade de timp
Aceasta constatare ne-a condus la concluzia ca ionii de fier aparuti in solutie in primele doua ore au provenit din dizolvarea filmului superficial in solutie. Faptul ca in urmatoarele ore nu s-a constatat o crestere a concentratiei fierului din solutie se datoreste, probabil, faptului ca solutia s-a saturat in ioni de fier, ceea ce a facut ca la interfata proba/ solutie sa se stabileasca un echilibru dinamic dizolvare metal de baza/ redepunere ioni din solutie.
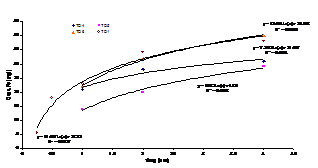
Fig.24[126] Variatia concentratiilor ionilor de fier in urmatoarele solutii:
solutie neinhibata (TD1) si respectiv aditivata cu urmatoarele concentratii de TEA: 0.0005M (TD6), 0.00113M (TD4) si 0.0015M (TD5)
Introducerea unor concentratii din ce in ce mai mari de TEA in solutia de decrustare a avut ca efect micsorarea concentratiei ionilor de fier eliberati in solutie pe parcursul decrustarii (figura 24[126]).
Mecanismele propuse in literatura de specialitate au presupus ca trietanolamina (TEA) se adsoarbe pe filmul superficial stabilizandu-l. In acest fel, ea faciliteaza ulterior fie o dizolvare mai redusa a acestuia, fie micsorarea accesului ionilor din solutie la metalul de baza si invers, ceea ce va conduce la scaderea ponderii reactiei de dizolvare a metalului de baza. In vederea selectarii unui inhibitor de coroziune cat mai eficient, trebuie cunoscuta mai intai relatia dintre structura acestuia si mecanismul lui de actiune.
Conform unor mecanisme propuse in literatura de specialitate, TEA se adsoarbe pe filmul superficial stabilizandu-l, permitand ulterior fie o dizolvare mai redusa a acestuia, fie micsorand accesul ionilor din solutie la metalul de baza si invers, ceea ce va conduce la scaderea ponderii reactiei de dizolvare a metalului de baza. In vederea selectarii unui inhibitor de coroziune cat mai eficient, trebuie cunoscuta mai intai relatia dintre structura acestuia si mecanismul lui de actiune. Pentru intelegerea mecanismului de actiune al inhibitorilor, trebuie tinut cont de faptul ca prima etapa in cadrul acestuia il constituie adsorbtia lor pe suprafata de interes. Stiind ca adsorbtia inhibitorilor este facilitata de prezenta heteroatomilor din molecula inhibitorilor, rezulta ca se vor adsorbi mai usor inhibitorii care contin in molecula lor: N, O, P, S, triple sau duble legaturi, inele aromatice, etc[31,43, 127, 128]. In general, eficienta unui inhibitor este cu atat mai mare cu cat aria legaturii de coordinatie formate este mai mare; deci, aceasta eficienta va creste in ordinea : O<N<S<P [129].
De asemenea, s-a aratat ca adsorbtia mai depinde si de alte caracteristici fizico-chimice ale inhibitorilor ca: tipul de grupari functionale, factorii sterici, aromaticitatea, densitatea de electroni a atomilor donori, caracterul orbitalilor p ai electronilor donati, etc.[130]. Folosirea inhibitorilor de coroziune este una dintre cele mai practice metode de prevenire si respectiv protectie contra coroziunii, in special in cazul utilizarii lor in medii acide. Se stie ca solutiile acide sunt larg utilizate atat in energetica clasica cat si nucleara, cele mai importante domenii de aplicatie fiind decaparea acida si decrustarea (descalarea) acida a componentelor executate din aliaje feroase. Rolul inhibitorilor consta, in principal, in reducerea atacului coroziv al solutiilor asupra metalului neacoperit. Majoritatea inhibitorilor folositi in medii acide sunt compusi organici care contin N, S si O. Compusii organici care contin N- ca de exemplu aminele si compusii lor heterociclici - s-au bucurat de o atentie deosebita din partea multor cercetatori. In acest context s-a stabilit ca eficienta inhibitorilor tip compusi organici heterociclici care contin azot in molecula a crescut concomitent cu cresterea accesibilitatii speciilor chimice din solutie la atomii electronegativi din molecula. Inlocuirea unui atom de azot cu un atom mai electronegativ - ca de exemplu cel de oxigen - a condus la obtinerea unei eficiente a inhibarii foarte inalte chiar la concentratii foarte coborate.
Datele din literatura si cele experimentale obtinute de noi au pledat pentru ipoteza conform careia o prima etapa in cadrul mecanismului de actiune al majoritatii inhibitorilor este adsorbtia lor pe suprafata metalului. In acest context, este necesar ca inhibitorii care se chemisorb pe suprafata metalului, sa posede o inalta energie de adsorbtie pe acesta si sa formeze, in consecinta, un film-bariera compact. Selectarea inhibitorilor trebuie sa se faca pe baza proprietatilor lor fizice dictate de sistemul in care vor fi folositi, dintre care cele mai importante sunt: starea de agregare, valoarea punctelor de fierbere, topire, inghetare, etc., stabilitatea in timp pe domeniul de temperatura in care vor fi folositi, compatibilitatea cu alti aditivi din sistem, solubilitatea in sistemul in care vor fi utilizati, etc. Aceste caracteristici fizice vor constitui baza calitativa a testelor de acceptanta.
Urmatoarea etapa in evaluarea inhibitorilor consta in imaginarea de experimente in care sa fie simulate cat mai real conditiile din instalatiile in care ei vor fi folositi. Variabilele care trebuie luate in considerare in acest caz sunt: temperatura, presiunea, influenta vitezei de curgere a fluidului asupra proprietatilor metalelor imersate in el si chimia mediului coroziv in care vor fi utilizati inhibitorii.
Alegerea unui inhibitor adecvat depinde nu numai de tipul si structura inhibitorului, ci si de caracteristicile sistemului metal/ mediu, adica de proprietatile electrolitului si starea suprafetei metalului de protejat. De aceea, inhibitorii desemnati pentru aplicare intr-un anumit sistem metal/ mediu pot sa nu fie la fel de eficienti in alt mediu. Pornind de la aceasta constatare, trebuie gasiti factorii care influenteaza performantele diversilor inhibitori in diferite medii. De aici a aparut necesitatea gasirii unor metode adecvate cu ajutorul carora sa se stabileasca rapid eficienta inhibitorilor si, in masura in care este posibil, mecanismele lor de actiune.
Se stie ca mecanismele de actiune ale inhibitorilor sunt strans corelate cu structurile moleculare ale acestora. Existenta unor tehnici avansate de investigare a structurii inhibitorilor ca: spectroscopia electronilor Auger (AES), spectroscopia fotoelectronilor si razelor X (XPS), spectroscopia in infrarosu (IRS) si Raman ca si spectroscopia de masa a ionilor secundari (SIMS), a permis stabilirea cu mare exactitate a structurii acestora, fapt care a constituit prima etapa in elucidarea mecanismelor de actiune ale inhibitorilor[131]. Cand un inhibitor se adsoarbe pe o suprafata metalica, se formeaza o legatura coordinativa prin transferul partial al electronilor de la inhibitor la metal prin intermediul unui atom polar al inhibitorului. Taria legaturii realizata prin adsorbtie reprezinta o masura a polarizabilitatii mai mari sau mai mici a metalului. Prin similitudine cu sistemul format dintr-un acid si o baza, acizii tari prefera pentru coordinatie bazele tari, iar acizii slabi pe cele slabe. Un inhibitor care actioneaza intr-un mediu acid respecta in mare masura principiile susmentionate[133].
Pentru a corela eficienta inhibarii cu structura electronica a diferitelor clase de compusi organici, au fost utilizate calcule de chimie cuantica, care au demonstrat ca eficienta inhibarii creste cu cresterea sumei orbitalilor moleculari cel mai deplin ocupati(HOMO) si a celor cel mai putin ocupati(LOMO)[132]. Eficienta inhibitorilor este influentata si de alti parametri structurali ca: aria moleculei, greutatea moleculara si configuratia moleculei influenteaza. Recent, a fost creat un nou domeniu interdisciplinar care coreleaza structura calitativa si cantitativa a inhibitorului cu activitatea acestuia, domeniu numit QSAR ('quantitative structure - activity relationship')[134-135]. Analiza relationala QSAR a aratat ca numarul gruparilor (>NH) are o mare influenta asupra inhibarii coroziunii metalelor, dar numai in regiunea pasiva. In schimb, probabilitatea formarii de legaturi de hidrogen este posibil sa creasca cu numarul radicalilor (>NH).
In regiunea activa, legaturile de hidrogen se formeaza intre amine si produsii de coroziune intermediari, ca de exemplu compusul adsorbit [Fe(OH)ads]. Adsorbtia inhibitorilor datorita crearii unor legaturi de hidrogen cu [Fe(OH)ads] va aduce o mica contributie la inhibarea coroziunii. Suprafata metalului in regiunea pasiva fiind net diferita, va rezulta o aderenta net diferita pe filmul superficial comparativ cu cea pe substratul metalic. In aceasta regiune, straturile de amine suprapuse peste oxizi si legate de ei prin legaturi de hidrogen, vor fi compacte, formand astfel un scut protector eficient in calea atacului corodentilor asupra substratului metalic. In lumina teoriei QSAR, un inhibitor tip amina eficient va trebui sa contina o molecula mare care sa fie solubila in apa, un numar cat mai mare de atomi donori de azot si cat mai multe grupari (>NH). In general, exista doua mecanisme principale de adsorbtie ale aminelor: prin chemisorbtie pe suprafata metalului si prin formarea unor legaturi de hidrogen cu filmul superficial pasiv.
|
Politica de confidentialitate |
| Copyright ©
2025 - Toate drepturile rezervate. Toate documentele au caracter informativ cu scop educational. |
Personaje din literatura |
| Baltagul caracterizarea personajelor |
| Caracterizare Alexandru Lapusneanul |
| Caracterizarea lui Gavilescu |
| Caracterizarea personajelor negative din basmul |
Tehnica si mecanica |
| Cuplaje - definitii. notatii. exemple. repere istorice. |
| Actionare macara |
| Reprezentarea si cotarea filetelor |
Geografie |
| Turismul pe terra |
| Vulcanii Și mediul |
| Padurile pe terra si industrializarea lemnului |
| Termeni si conditii |
| Contact |
| Creeaza si tu |